Лекции / Лекция 38-3 Окисление метилбензола
.doc
Раздел VI. ПРОЦЕССЫ ОКИСЛЕНИЯ
Лекция 38-3 Окисление метилбензолов
1. Теоретические основы окисления метилбензолов
2. Технология окисления п-ксилола (получение синтеза терефталевой кислоты)
1. Теоретические основы окисления метилбензолов
Окислением метил- и диметилбензолов получают имеющие научно-практическое значение следующие ароматические карбоновые кислоты: бензойную (бензолмонокарбоновую) (С6Н5-СООН) и терефталевую (НООСС6Н4СООН).
Синтез ароматических карбоновых кислот наиболее привлекательно (т.е. технологично и экономично) получать окислением метилбензолов.
Для синтеза ароматических кислот более всего подходят метильные производные бензола, радикально-цепное окисление, которых протекает через стадии образования первичного гидропероксида и далее спирта и альдегида.
ArСН3 + О2 → ArСН2ООН → ArСНО + О2 →ArСООН
Окисление метилбензолов проводят в жидкой фазе.
Окисление метилбензолов в среде исходных веществ
Окисление осуществляют кислородом воздуха под давлением, необходимым для поддержания реакционной среды в жидком состоянии. Реактором может служить барботажная колонна, т.к. ароматические кислоты стабильны к дальнейшему окислению.
Толуол окисляется в бензойную кислоту при относительно мягких условиях: температура 100÷150ºС и небольшое давление.
На рис. 1. приведена кривая зависимости накопления продуктов окисления толуола.
Видно, что концентрация альдегида проходит через максимум. Установлено, что при 50÷60 %-ной конверсии толуола наблюдается торможение его окисления и чем выше температура, тем больше степень превращения, при которой начинается это торможение. Оно связано, по-видимому, с уменьшением концентраций углеводорода, а также с влиянием образующихся продуктов. Все эти факторы в совокупности определяют оптимальную степень конверсии исходного сырья жидкофазного метода окисления толуола.
-
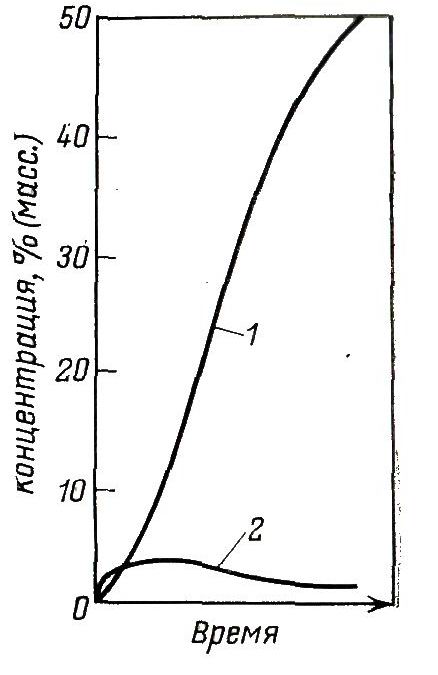
Рис. 1 Зависимость накопления продуктов окисления толуола от степени конверсии: 1 – бензойная кислота, 2- бензальдегид
Ксилолы и вообще полиметилбензолы окисляются молекулярным кислородом в присутствии солевых катализаторов лишь до монокарбоновой кислоты, если температура процесса ≤ 150ºС:
![]()
Обычные параметры окисления метилбензолов: катализатор в виде раствора в углеводороде в количестве 0,05÷0,20 %, нафтенат кобальта или соль кобальта , которая образуется при окислении, температура 120÷200°С, иногда давление от 0,2 до 1,0÷2,0 МПа. Выход ароматических кислот при этих условиях достигает 90÷97% масс.
Только при более жестких условиях по температуре (260÷280 °С) и давлению (≈7 МПа) можно окислить и вторую метильную группу, но выход соответствующей дикарбоновой кислоты составит всего 40÷60 % масс.
Окисление ди- и полиметилбензолов в среде исходных веществ до ароматических ди- и поликарбоновых кислот является многостадийным. Поэтому разработка одностадийных методов стала актуальной задачей.
Одностадийное окисление ксилолов в растворе уксусной кислоты.
Было разработано несколько вариантов одностадийного синтеза дикарбоновых ароматических кислот, общей чертой которых является использование уксусной кислоты в качестве растворителя. Наиболее широкое применение нашел вариант окисления на кобальтовом или кобальтмарганцевом катализаторе с промотирующей добавкой бромидов, особенно NaBr.
Изучение закономерностей окисления ксилолов в присутствии ме-таллобромидных катализаторов показало, что процесс проходит через два резко разграниченных этапа (рис. 2., кривые 2 и 3).
-
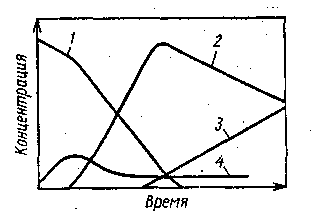
Рис. 117. 'Зависимость накопления продуктов окисления ксилолов с кобальт-бромидным катализатором от степени конверсии:
1 - ксилолы; 2- толуиловые кислоты; 3 - фталевые кислоты; 4 – альдегиды.
Вначале окисляется только одна метильная группа и лишь после исчерпания ксилола начинается окисление второй метильной группы с получением ароматической дикарбоновой кислоты, причем вторая стадия протекает медленнее первой. Кривая 4 накопления альдегидов имеет максимум вскоре после начала реакции, а затем концентрация альдегидов снижается, не увеличиваясь и на втором этапе окисления. Таким образом, процесс идет в соответствии со схемой:
![]()
![]()
Предполагаемый механизм действия бромидного промотора:
![]()
![]()
![]() и т.д.
и т.д.
2. Технология окисления п-ксилола (получение синтеза терефталевой кислоты)
Известны промышленные варианты многостадийного синтеза терефталевой кислоты.
Однако за последнее время они вытесняются более прогрессивным и экономичным одностадийным методом. В этом случае окисление соответствующих ксилолов проводят воздухом в растворе уксусной кислоты при 125÷275°С (лучше при 150°С) и давлении до 4 МПа. Реактором служит барботажная колонна или аппарат с мешалкой. Тепло реакции отводят за счет испарения воды и уксусной кислоты, которые концентрируют, удаляют воду, а кислоту в реактор. Далее кислоту и катализатор отделяют от реакционной массы и снова подают на окисление (предварительно удалив из уксусной кислоты воду, так как она замедляет реакцию).
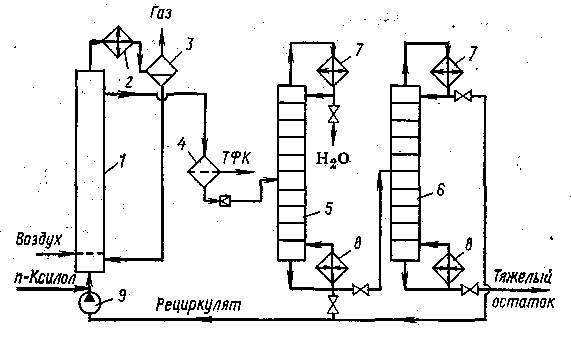
На рис. 3. изображена схема одностадийного способа получения терефталевой кислоты окислением n-ксилола. В реактор 1 подают n-ксилол, воздух, рециркулирующую уксусную кислоту и катализатор (потери двух последних компонентов восполняют, подавая свежий раствор катализатора в уксусной кислоте, что на схеме не изображено). Реакционное тепло отводят за счет испарения уксусной кислоты и воды, пары которых конденсируются в холодильнике 2. Конденсат отделяют от газовой фазы в сепараторе 3 и возвращают в реактор.
|
Рис. 3. Технологическая схема одностадийного синтеза терефталевой кислоты: 1- реактор; 2 - холодильник; 3 - сепаратор; 4 - центрифуга; 5 - ректификационная колонна; 6 - колонна регенерации уксусной кислоты; 7 - дефлегматоры; 8 - кипятильники; 9-насос |
Реакционная масса представляет собой суспензию терефталевой кислоты в растворителе. Эту суспензию фильтруют в центрифуге (или на фильтре) 4, на которой терефталевую кислоту промывают свежей уксусной кислотой и направляют на очистку. От фильтрата отгоняют воду в ректификационной колонне 5; из куба колонны уксусная кислота с растворенным в ней катализатором возвращается в реактор 1. В кислоте при многократной циркуляции накапливаются смолистые примеси, поэтому часть кислоты отводят в колонну 6 для регенерации. Уксусная кислота отгоняется от тяжелого остатка и возвращается в цикл. Остаток сжигают или регенерируют из него кобальт.
Полученную терефталевую кислоту специально очищают от n - карбоксибензальдегида (при двухстадийном синтезе очистка достигается при получении и кристаллизации эфира). Для этого применяют способ гидрирования в водной суспензии при относительно высоких температуре и давлении, когда примеси переводятся в более растворимые соединения (оксикислоты) и переходят в воду.
Используются и другие методы очистки, например, переводом ТФК этерификацией в диметилтерефталат и перекристаллизацией последнего.
Возможен, наконец, прямой синтез достаточно чистой, не требующей специальной очистки, ТФК в присутствии кобальтмарганецбромидного катализатора при оптимальных параметрах процесса.
ArСН3 + О2 → ArСН2ООН → →ArСНО + О2 →ArСООН
Рис. 1 Зависимость накопления продуктов окисления толуола от степени конверсии: 1 – бензойная кислота, 2- бензальдегид |
Рис. 2. 'Зависимость накопления продуктов окисления ксилолов с кобальт-бро-мидным катализатором от степени конверсии: 1 - ксилолы; 2- толуиловые кислоты; 3 - фталевые кислоты; 4 – альдегиды. |
и т.д.
|
Рис. 3. Технологическая схема одностадийного синтеза терефталевой кислоты: 1- реактор; 2 - холодильник; 3 - сепаратор; 4 - центрифуга; 5 - ректификационная колонна; 6 - колонна регенерации уксусной кислоты; 7 - дефлегматоры; 8 - кипятильники; 9-насос |