
- •Теоретические основы дегидрирования парафинов.
- •Принципиальная технологическая схема дегидрирования парафинов. Аппаратура.
- •Теоретические основы дегидрирования парафинов
- •1.1 Двухстадийное дегидрирование парафинов. Химия и технология.
- •2. Принципиальная технологическая схема дегидрирования парафинов. Аппаратура.
ЛЕКЦИЯ № 26-1
Тема: Химия и технология дегидрирование парафинов и олефинов.
Теоретические основы дегидрирования парафинов.
Принципиальная технологическая схема дегидрирования парафинов. Аппаратура.
Теоретические основы дегидрирования парафинов
Химию и технологию процессов дегидрирования парафиновых углеводородов изучается в основном применительно к бутану, изопентану, изопентанам (изоамиленам), так как на их основе получаются наиболее важные в научном и практическом отношении мономеры - 1,3-бутадиен (дивинил) и 2-метил-1,3-бутадиен (изопрен). Они являются исходным сырьем для получения различных ценных для народного хозяйства синтетических каучуков и пластмасс.
Дегидрирование бутана и изопентана осуществляют двумя способами:
1) как двухстадийный (первая стадия-дегидрирование парафинов в олефин, вторая- дегидрирование или окислительное дегидрирование олефина в диен;
2) одностадийное дегидрирование парафина в диен.
1.1 Двухстадийное дегидрирование парафинов. Химия и технология.
В термодинамическом отношении дегидрирование парафинов более благоприятно, чем дегидрирование олефинов и аллилароматических углеводородов. Поэтому при режимной температуре около 6000С дегидрирование парафинов ведут практически при атмосферном давлении, т.е. без применения вакуума или разбавителей в виде инертных газов или водяного пара.
Дегидрирование парафинов С4-С5 приводит к образовании смеси изомерных олефинов. Например, из бутана получают 1-бутен и цис-, транс-2-бутен
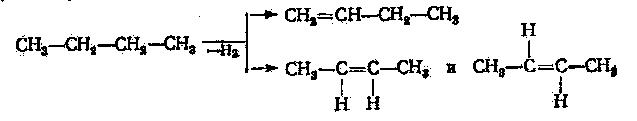
(1.1)
(1.2)
В небольшом количестве образуется соответствующие диены (т.к. условия реакции термодинамически неблагоприятны для их образования). Побочно также протекают реакции расщепления, изомеризации и коксообразования. Значительная часть кокса образуется за счет диенового синтеза части диенов с последующей дегидроконденсацией полученных ароматических соединений, а также разложения углеводородов, например, олефинов на углерод и водород. В общем виде процессы дегидрирования парафинов можно изобразить следующей схемой:
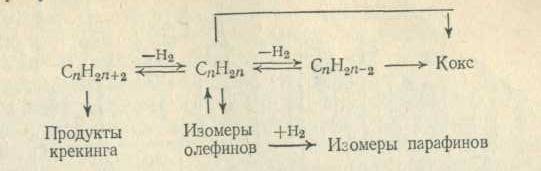
(1.3)
СnH2n C + nH2 (1.4)
Наиболее активными и селективными катализаторами дегидрирования парафинов являются оксидные алюмохромовые катализаторы на основе A12O3, содержащие 10-40% Cr2O3 и 2-10% оксидов щелочных металлов (Na2O, BeO); последние служат для нейтрализации кислотных центров A12O3, вызывающих крекинг и изомеризацию углеводородов. Эти катализаторы очень чувствительна к влаге, поэтому ее содержание в исходной фракции парафина должна быть не более 1мг/м3.
Алюмохромовые
катализаторы активны к дегидрированию
бутана и изопентана при 500-650![]() С.
Оптимальной считают 560-590
С
при дегидрировании бутана и 530-560
С
при дегидрировании более реакционно-способного
изопентана. Повышение температуры
процесса выше указанной ведет к
усиленному развитию побочных реакций
(имеющих более высокую энергию активации).
Селективность процесса падает также
при повышении степени конверсии
исходного парафина (главным образом
из-за замедления дегидрирования
приближении к равновесию - время для
протекания вторичных процессов
увеличивается), поэтому ее ограничивают
величиной 40-45%. При этих условиях
селективность процесса по бутиленам
составляет около 75% (плюс 6-7% по бутадиену),
а по изоамиленам - около 70% (плюс 4-5% по
изопрену). В указанных условиях
катализаторы всё же довольно быстро
закоксовываются. С них периодически
выжигают кокс (регенерируют) при
600-650
С
воздухом.
С.
Оптимальной считают 560-590
С
при дегидрировании бутана и 530-560
С
при дегидрировании более реакционно-способного
изопентана. Повышение температуры
процесса выше указанной ведет к
усиленному развитию побочных реакций
(имеющих более высокую энергию активации).
Селективность процесса падает также
при повышении степени конверсии
исходного парафина (главным образом
из-за замедления дегидрирования
приближении к равновесию - время для
протекания вторичных процессов
увеличивается), поэтому ее ограничивают
величиной 40-45%. При этих условиях
селективность процесса по бутиленам
составляет около 75% (плюс 6-7% по бутадиену),
а по изоамиленам - около 70% (плюс 4-5% по
изопрену). В указанных условиях
катализаторы всё же довольно быстро
закоксовываются. С них периодически
выжигают кокс (регенерируют) при
600-650
С
воздухом.
