
- •Раздел 5. Химия и технология дегидрирования и гидрирования
- •Процессы дегидрирования и гидрирования. Классификация реакций дегидрирования и гидрирования
- •Теоретические основы реакций гидрирования и дегидрирования
- •Катализаторы реакций гидрирования и дегидрирования
- •Механизм и кинетика гидрирования и дегидрирования
Раздел 5. Химия и технология дегидрирования и гидрирования
Лекция 24. Химия реакций дегидрирования и гидрирования
Процессы дегидрирования и гидрирования. Классификация реакций дегидрирования и гидрирования
Теоретические основы реакций гидрирования и дегидрирования.
Катализаторы реакций гидрирования и дегидрирования.
Механизм и кинетика гидрирования и дегидрирования.
Процессы дегидрирования и гидрирования. Классификация реакций дегидрирования и гидрирования
Под дегидрированием понимают химические процессы, связанные с отщеплением атомов водорода от органического соединения.
Гидрирование (или гидрогенизация) заключается в превращениях органических соединений под действием молекулярного водорода. В ряде случаев гидрирование приводит к восстановлению кислородсодержащих веществ, а дегидрирование - к их окислению.
Дегидрированием получают мономеров для производства синтетического каучука и пластических масс (бутадиен-1,3, изопрен, стирол), альдегиды и кетоны (формальдегид, ацетон, метилэтилкетон). Реакциями гидрирования синтезируют циклогексан и его производные, многие амины (анилин, гексаметилендиамин), спирты (н-пропанол, н-бутанол и высшие). Процессы гидрирования применяют также при гидрогенизации жиров и получении искусственного жидкого топлива (гидрокрекинг, риформинг, гидрогенизация угля). Часто реакции гидрирования и дегидрирования являются этапами многостадийных синтезов ценных органических соединений - мономеров, ПАВ, растворителей и т. д.
Классификация реакций дегидрирования
Наиболее типичные реакции дегидрирования можно классифицировать по виду связей между атомами, от которых отщепляется водород (С-С-, С-О-, С-N-дегидрирование).
При С-С-дегидрировании парафинов образуются соединения с двойной углерод-углеродной связью, а при дальнейшем развитии реакции — диены:
![]()
Боковые цепи ароматических соединений также могут дегидрироваться с образованием веществ типа стирола:
![]()
Дегидрирование по С-О-связи характерно для первичных и вторичных спиртов, с образованием альдегидов и кетонов:
![]()
Дегидрирование по С—N-связи является отщепление водорода от первичных аминов, протекающее с образованием нитрилов:
![]()
Процесс дегидроциклизации, когда из парафинов путем замыкания цикла и дегидрирования получаются ароматические углеводороды:
![]()
Дегидроконденсация - приводит к образованию ди- и полиядерных соединений:
![]()
Иной вид дегидроконденсации наблюдается при синтезе аминов и нитрилов из углеводородов и аммиака, когда образуются новые С-N-связи:
![]()
Реакции окисления, например, синтез карбонильных соединений из спиртов, синтез нитрилов из углеводородов и аммиака, синтез нитрилов из аминов:
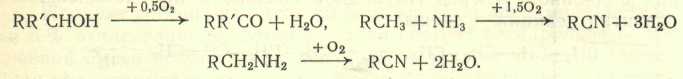
Окислительное дегидрировании при недостатке кислорода, когда одновременно происходят и окисление, и дегидрирование:
![]()
Окислительное дегидрировании при избытке кислорода:
![]()
Классификация реакций гидрирования
Реакции гидрирования (или гидрогенизации) можно разделить на три группы:
присоединение водорода по ненасыщенным связям;
действие водорода, сопровождающееся отщеплением воды или других веществ, не содержащих углерода;
реакции с водородом, сопровождающиеся расщеплением углерод-углеродных связей (деструктивное гидрирование).
Реакции первой группы ведут с присоединением водорода по связям С ≡ С, С=С, Сар—Сар, по С=О-связи альдегидов и кетонов, по C=N- и C≡N-связям азотсодержащих соединений и т. д.:

Вторая группа процессов гидрирования соответствует восстановлению органических соединений. К ним принадлежит гидрирование карбоновых кислот в спирты, спиртов - в углеводороды, амидов кислот и нитросоединений - в амины и т. д.:
![]()
При этом может отщепляться не только вода, но хлорид водорода, аммиак, сероводород:
![]()
Третья группа реакций гидрирования - с расщеплением углерод-углеродных связей - деструктивного гидрирования, или гидрогенолиза. К ним способны углеводороды с открытой цепью, нафтены, ароматические соединения с боковой цепью:
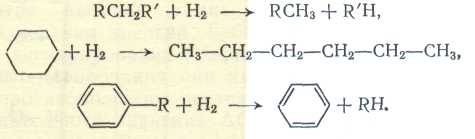
Эти реакции, следовательно, противоположны процессам дегид-роконденсации и дегидроциклизадии. Нередко к третьей группе относят и упомянутые выше процессы гидрирования с выделением воды и особенно H2S и NH3, когда происходит деструкция молекулы по С-S- или по С-N-связям.
