
- •Содержание
- •Введение
- •1. Технологические свойства азотной кислоты
- •2. Сырье для производства азотной кислоты
- •3. Общая схема азотнокислотного производства
- •4. Прямой синтез концентрированной азотной кислоты
- •4.1 Физико-химические основы и принципиальная схема процесса прямого синтеза
- •4.2 Технологическая схема производства концентрированной азотной кислоты прямым синтезом
- •4.3 Расходные коэффициенты в процессах производства концентрированной азотной кислоты
- •Заключение
- •Список используемой литературы
Министерство науки и высшего образования Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
высшего образования
«Уфимский государственный нефтяной технический университет»
Кафедра «Общая химическая технология»
Реферат
По дисциплине «Химическая технология органических веществ»
на тему:
«Производство азотной кислоты»
Студент гр. БТС-20 А. Б. Шкурина
Принял:
канд. техн. наук, доцент А. А. Исламутдинова
Стерлитамак – 2020
Содержание
Введение………………………………………………………………….….……3
1. Технологические свойства азотной кислоты……………………….…….....4
2. Сырье для производства азотной кислоты…………………………….…….6
3. Общая схема азотнокислотного производства……………….…………..…..7
4. Прямой синтез концентрированной азотной кислоты………..…………..….9
4.1 Физико-химические основы и принципиальная схема процесса прямого синтеза…………………………………………………….…………..…9
4.2 Технологическая схема производства концентрированной азотной кислоты прямым синтезом………………………………………………..…….11
4.3 Расходные коэффициенты в процессах производства концентрированной азотной кислоты…………………………………..……..14
Заключение……………………………………………………………………….15
Список литературы……………………………………………………..………..16
Введение
Азотная кислота - одна из важнейших минеральных кислот. По объему производства в химической промышленности она занимает второе место после серной кислоты. Азотная кислота широко применяется для производства многих продуктов, используемых в промышленности и сельском хозяйстве:
около 40% ее расходуется на получение сложных и азотных минеральных удобрений;
азотная кислота используется для производства
синтетических красителей,
взрывчатых веществ,
нитролаков,
пластических масс,
лекарственных синтетических веществ и др.;
железо хорошо растворяется в разбавленной азотной кислоте. Концентрационная азотная кислота образует на поверхности железа тонкий, но плотный слой нерастворимого в концентрированной кислоте оксида, защищающего металл от дальнейшего разъедания. Эта способность железа пассивироваться используется для защиты его от коррозии.
Концентрированную азотную кислоту (особенно с добавлением 10% H2SO4) перевозят обычно в стальных цистернах. Многие органические вещества (в частности животные и растительные ткани) при действии HNO3 разрушаются, а некоторые из них от соприкосновения с очень концентрированной кислотой могут воспламеняться. В лабораторной практике обычно применяется азотная кислота, содержащая около 65% HNO3 (пл.1,40). В промышленности применяют два сорта азотной кислоты: разбавленную с содержанием 50-60% HNO3 и концентрированную, содержащую 96-98% HNO3.
1. Технологические свойства азотной кислоты
Безводная азотная кислота (моногидрат HNO3) представляет бесцветную жидкость с температурой кристаллизации -41,6°С, температурой кипения - 82,6°С и плотностью - 1,513 г/м3. Смешивается с водой во всех отношениях, образуя при этом индивидуальные соединения - гидраты состава HN03-H20 и НЖ>з-ЗН20, которые дают три эвтектики (рис.1).
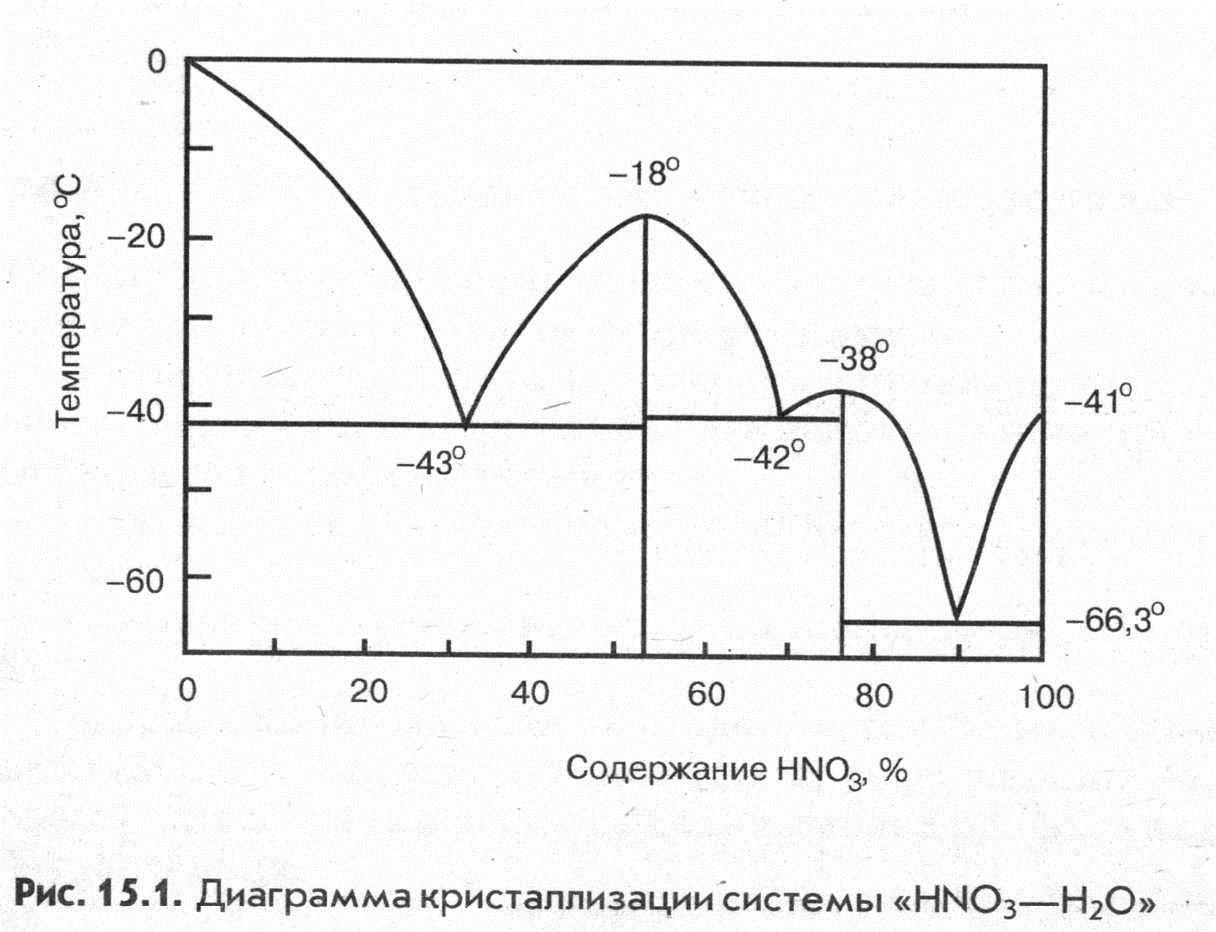
Рис. 1. Диаграмма кристаллизации системы “HNO3 - H2O”
Температура кипения водных растворов азотной кислоты зависит от их концентрации. С увеличением концентрации температура кипения возрастает, достигая максимума 120,7°С при азеотропном составе кислоты 68,4% (мае), после чего снижается (рис. 2). Это имеет существенное значение для концентрирования азотной кислоты.
Безводная азотная кислота малоустойчива термически и разлагается уже при хранении по уравнению:
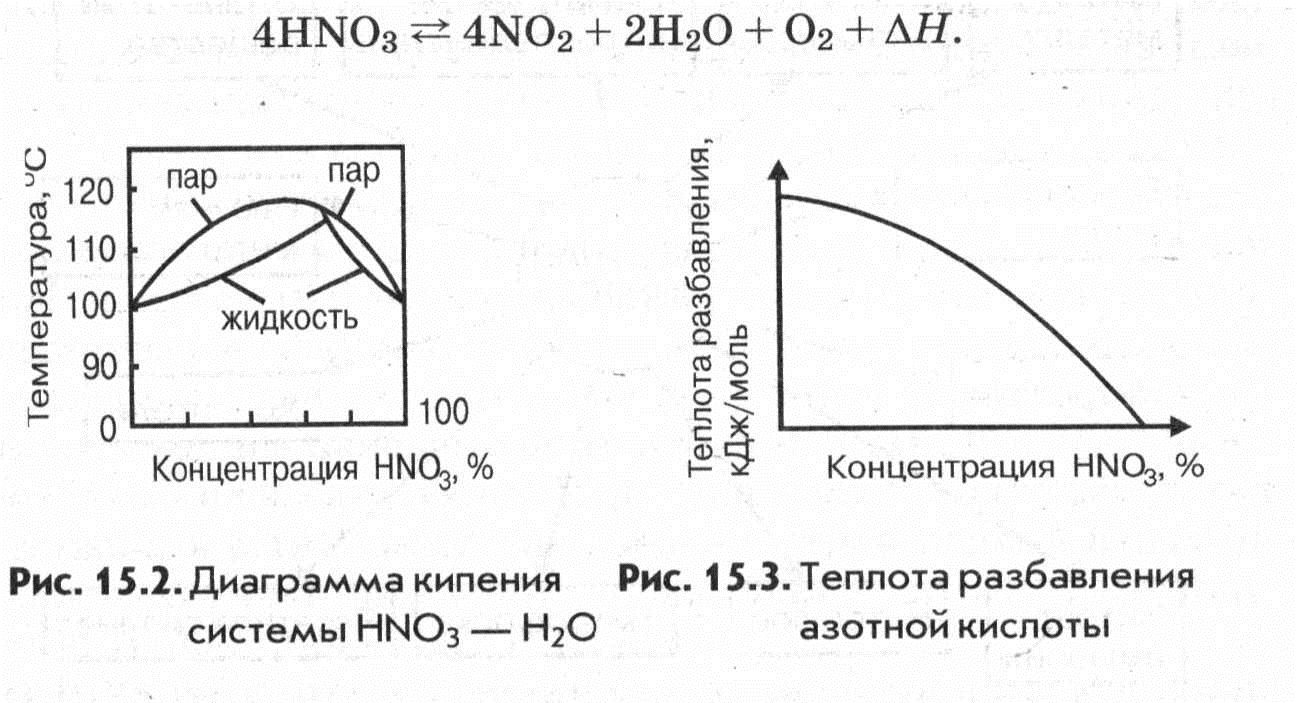
Рис. 2. Диаграмма кипения системы “HNO3 - H2O”
Скорость разложения возрастает с повышением концентрации; для 99% -ной кислоты температурный градиент составляет всего 5°С.
При нагревании процесс ускоряется и протекает по уравнению:
![]()
Выделяющийся оксид азота (IV) растворяется в кислоте и окрашивает ее в желтооранжевый цвет. Для удаления оксида из кислоты в технологическом процессе ее производства предусмотрена операция «отбелки» кислоты.
При растворении оксида азота (IV) в кислоте образуется соединение составаHN03-N02 (нитроолеум), являющийся промежуточным продуктом в прямом синтезе азотной кислоты.
Азотная кислота корродирует и растворяет все металлы кроме золота, платины, титана, тантала, родия и иридия, однако в концентрированном виде пассивирует железо и его сплавы.
