
- •Определение и общая характеристика фотосинтеза, значение фотосинтеза
- •Пигменты фотосинтезирующих растений, их физиологическая роль.
- •Сущность фотофизического этапа. Фотохимический этап. Циклический и нециклический транспорт электронов.
- •Компоненты этц хлоропластов. Фотосистемы I и II.
- •Нециклический транспорт электронов при фотосинтезе. Псевдоциклический транспорт электронов при фотосинтезе. Последовательность переносчиков электронов и физиологическое значение.
- •Циклический транспорт электронов вокруг фотосистемы 1 и 2. Последовательность переносчиков электронов и физиологическое значение.
- •Биохимический этап – цикл Кальвина. С3 путь (Цикл Кальвина)
- •Факторы, определяющие интенсивность фотосинтеза.
- •Общее представление о путях дыхательного обмена и их взаимосвязь с другими обменными процессами.
- •Общее представление о гликолитическом пути дыхания. Его биологическая роль.
- •Гликолиз: химизм, био роль. Особенности гликолиза у растений.
- •2 Стадия:
- •Окислительное декарбоксилирование пировиноградной кислоты
- •Дыхательная цепь переноса электронов, также электрон-транспортная цепь
- •Пентозофосфатный путь
- •Подробнее:
- •Глиоксилатный путь
- •Антиоксидатные системы растительной клетки
- •Дыхательный коэффициент и его изменения в зависимости от дыхательного материала. Общее представление об окислении белков, углеводов, липидов.
- •Влияние внешних и внутренних факторов на интенсивность дыхания.
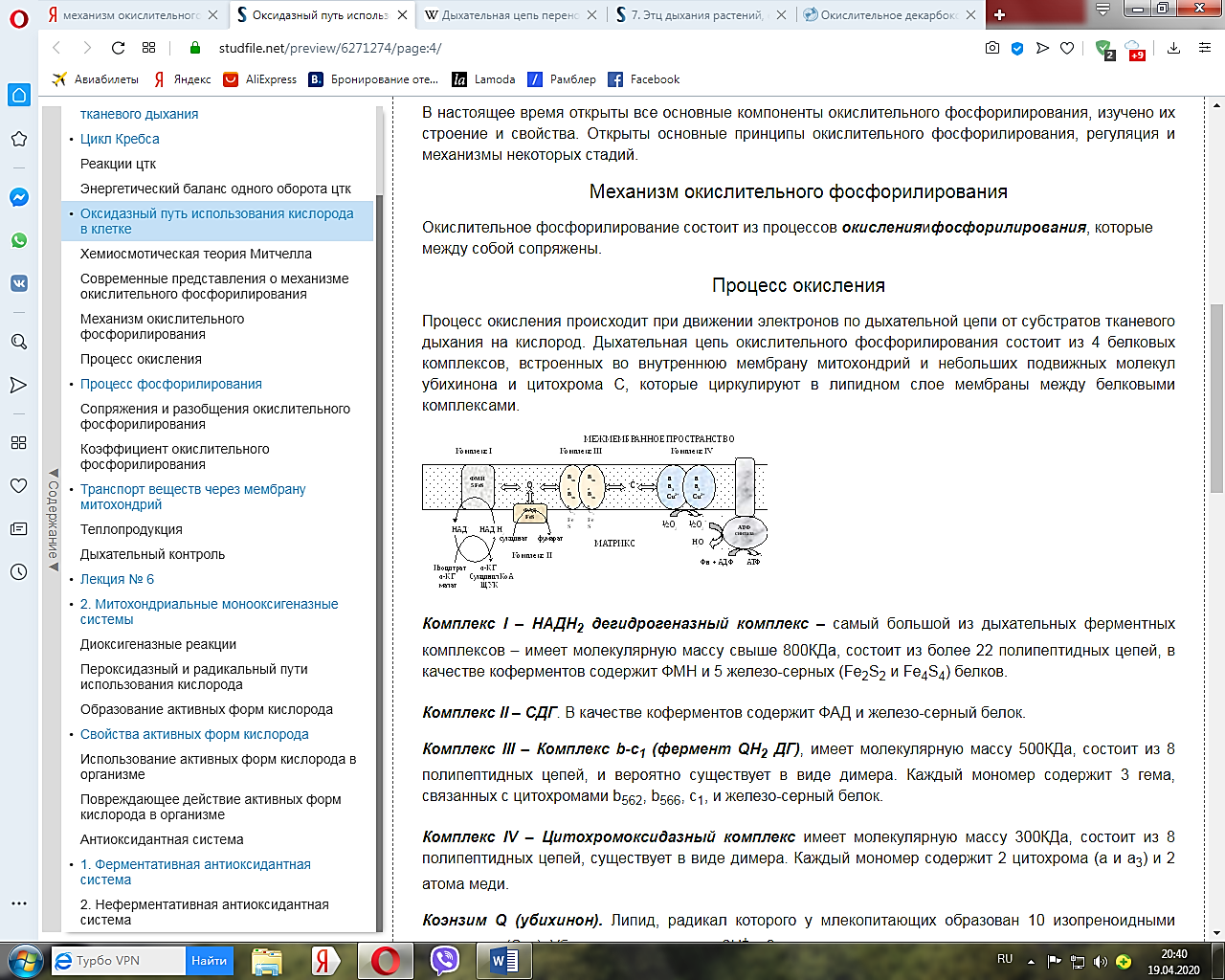
Дыхательная цепь переноса электронов, также электрон-транспортная цепь
— система трансмембранных белков и переносчиков электронов, необходимых для поддержания энергетического баланса. ЭТЦ поддерживает баланс за счёт переноса электронов и протонов из НАД∙Н и ФАДН2 в акцептор электронов.
В случае аэробного дыхания акцептором может быть молекулярный кислород (О2).
В случае анаэробного дыхания акцептором могут быть NO3−, NO2−, Fe3+, фумарат, диметилсульфоксид, сера, SO42−, CO2 и т. д.
ЭТЦ локализована на внутренней мембране митохондрий и состоит из:
4-х мультибелковых компонентов:
ФМН(флавинмононуклеоитд)-кофермент дегидрогеназы
ФАД(флавинадениндинуклеотид) – кофермент сукцинатдегидрогезы и железосерные белки
цитохромы b и c, FeSR(железосерный белок Риске)
цитохромы а и а3
2
 -х
небольших компонентов Q(убихинон) и
С(цитохрома с)
-х
небольших компонентов Q(убихинон) и
С(цитохрома с)
Переносчики расположены по обеим сторонам внутренней мембраны митохондрий и пересекают ее. Они расположены в порядке уменьшения сродства к электрону, то есть по своему окислительно-восстановительному потенциалу, где у акцептора самое сильное сродство к электрону. Цепь начинается с НАДН, имеющего потенциал –0,32 В, и кончается, например, кислородом с потенциалом +0,82 В.
На внутренней стороне мембраны, расположенной к матриксу митохондрии, два протона и два электрона от НАДН переходят на флавинмононуклеотид и железосерные белки. Флавинмононуклеотид, получив протоны, восстанавливается и переносит их на внешнюю сторону мембраны, где отдает протоны в межмембранное пространство. Железосерные белки, находящиеся внутри мембраны, передают электроны от НАДН окисленному убихинону Q. Он, присоединив еще два протона, диффундирует в мембране к цитохромам. Цитохром b560 отдает два электрона убихинону, который, присоединив еще два протона из матрикса, передает два электрона цитохрому b556 и два электрона цитохрому c1, а протоны выходят в межмембранное пространство. На наружной стороне мембраны цитохром с, получив два электрона от цитохрома c1, передает их цитохрому а, который переносит их через мембрану на цитохром а3. Цитохром а3, связывая кислород, отдает ему электроны. Кислород присоединяет два протона с образованием воды.
Транспорт электрона на всём протяжении цепи протекает самопроизвольно с выделением энергии. Выделение энергии в межмембранное пространство при переносе электронов происходит ступенчато, в виде протона (H+). Протоны из межмембранного пространства попадают в протонную помпу, где наводят протонный потенциал. Протонный потенциал преобразуется АТФ-синтазой в энергию химических связей АТФ. В результате прохождения двух электронов по цепи образуется 3 молекулы АТФ.
Сопряжённая работа ЭТЦ и АТФ-синтазы носит название окислительного фосфорилирования.
О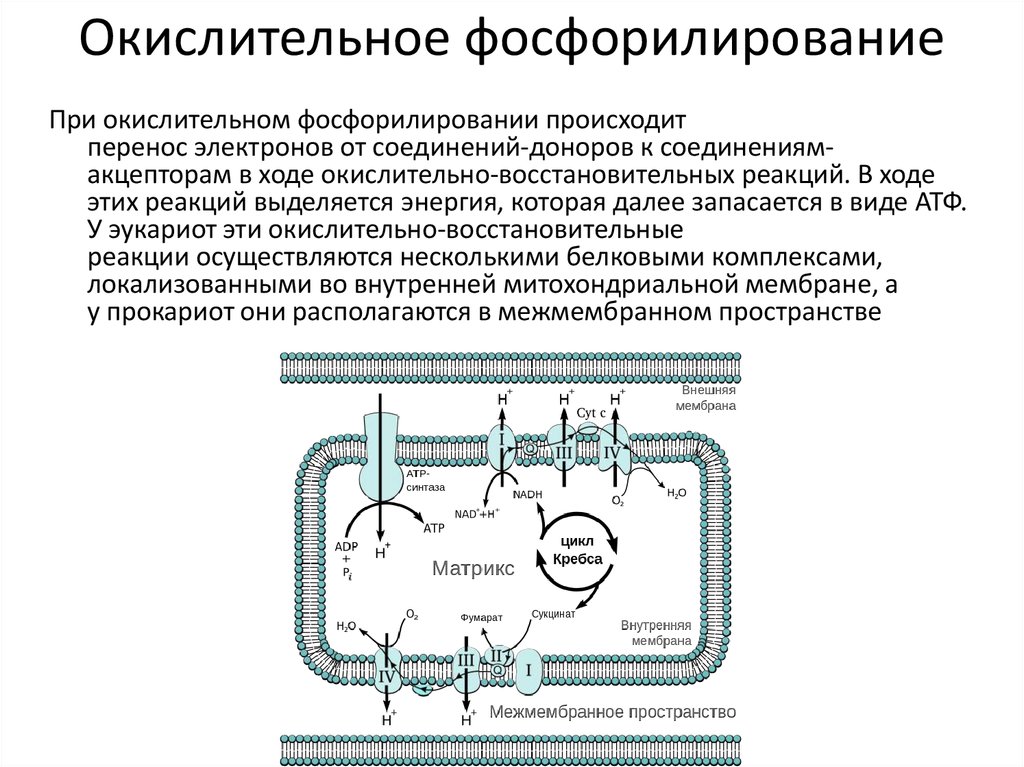 кислительное
фосфорилирование состоит из процессов
окисления и фосфорилирования, которые
между собой сопряжены:
кислительное
фосфорилирование состоит из процессов
окисления и фосфорилирования, которые
между собой сопряжены:
Процесс окисления: происходит при движении электронов по дыхательной цепи. Компоненты дыхательной цепи располагаются в мембране в порядке повышения их редокс-потенциала. При переходе е- от комплекса с низким редокс-потенциалом к комплексу с более высоким редокс-потенциалом происходит выделение свободной энергии. При окислении 1 НАДН2 выделяется 220 кДж/моль свободной энергии. I, III и IV комплексы дыхательной цепи используют 65-70% этой свободной энергии для переноса Н+ из матрикса митохондрий в межмембранное пространство, 30-35% свободной энергии рассеивается в виде тепла.
При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов(в матриксе рН выше, чем в цитозоле). Так как каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность потенциалов, внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который в типичной клетке составляет около 60+160=220 мВ. Образовавшийся на внутренней мембране митохондрий электрохимический потенциал используется для:
фосфорилирования АДФ в АТФ
транспорта веществ через мембрану митохондрий
теплопродукцию
Процесс фосфорилирования: осуществляется АТФ-синтетазой, которая потребляет 40-45% свободной энергии, выделившейся при окислении. Это нтегральный белок внутренней мембраны митохондрий, она состоит из 2 белковых комплексов:
Гидрофобный комплекс F0: погружён в мембрану и служит основанием, которое фиксирует АТФ-синтазу в мембране. Он состоит из нескольких субъединиц, образующих канал, по которому протоны переносятся в матрикс.
Комплекс F1: выступает в митохондриальный матрикс. Он состоит из 9 субъединиц (3α, 3β, γ, δ, ε). Субъединицы α и β уложены попарно, образуя «головку»; между а- и β-субъединицами располагаются 3 активных центра, в которых происходит синтез АТФ; γ, δ, ε – субъединицы связывают комплекс F1, с F0.
Электрохимический потенциал внутренней мембраны заставляет Н+ двигаться из межмебранного пространства по каналу АТФ-синтазы в матрикс митохондрий. При каждом переносе протонов через канал F0 энергия электрохимического потенциала расходуется на поворот стержня, в результате которого циклически изменяется конформация а- и β-субъединиц и все 3 активных центра, образованных парам α- и β-субъединиц, катализируют очередную фазу цикла:
связывание АДФ и Н3РО4
образование фосфоангидридной связи АТФ
освобождение конечного продукта АТФ
Х емиосмотическая
теория Митчелла:
Для объяснения
механизма окислительного фосфорилирования
в 1961 году Митчеллом была предложена
хемиосмотическая теория, которая
включала 4 независимых постулата,
касавшиеся функции митохондрий:
емиосмотическая
теория Митчелла:
Для объяснения
механизма окислительного фосфорилирования
в 1961 году Митчеллом была предложена
хемиосмотическая теория, которая
включала 4 независимых постулата,
касавшиеся функции митохондрий:
Внутренняя мембрана митохондрий непроницаема для всех ионов
Она содержит ряд белков-переносчиков, осуществляющих транспорт необходимых метаболитов и неорганических ионов
При прохождении электронов по дыхательной цепи внутренней мембраны происходит перемещение Н+ из матрикса в межмембранное пространство
При достаточно большом протонном градиенте протоны начинают «течь» через АТФ-синтетазу, что сопровождается синтезом АТФ.
