
- •1. Определение и общая характеристика фотосинтеза, значение фотосинтеза
- •2. Пигменты фотосинтезирующих растений, их физиологическая роль
- •6. Биохимический этап – цикл Кальвина
- •8. Факторы, определяющие интенсивность фотосинтеза.
- •10. Общее представление о гликолитическом пути дыхания. Его биологическая роль
- •11. Гликолиз: химизм, биологическая роль
- •2 Стадия:
- •12. Окислительное декарбоксилирование и цикл Кребса: химизм и биологическая роль
- •13. Этц: компоненты, локализация. Механизм окислительного фосфорилирования. Хемиосмотическая теория Митчелла
- •14. Пентозофосфатный путь окисления и его роль
- •2) Рекомбинацию сахаров для регенерации исходного субстрата:
- •15. Глиоксилатный цикл
- •16. Дыхательный коэффициент и его изменения в зависимости от дыхательного материала. Общее представление об окислении белков, углеводов, липидов.
- •17. Влияние внешних и внутренних факторов на интенсивность дыхания
1. Определение и общая характеристика фотосинтеза, значение фотосинтеза
Фотосинтез - процесс образования органического вещества из углекислого газа и воды на свету при участии фотосинтетических пигментов. Реализуется высшим растениями, красными и бурыми водорослями, цианобактерии, пурпурными бактериями.
У высших растений органом фотосинтеза является лист. Углекислый газ, который необходим для процесса, поступает в лист через устьица. К верхней стороне листа прилегает палисадная (мезофилла) ткань, клетки которой богаты хлоропластами. В процессе фотосинтеза происходит превращение вещества и энергии.
С общей точки зрения. Фотосинтез - процесс образования органического вещества из неорганического при помощи световой энергии.
С энергетической точки зрения. Фотосинтез - процесс поэтапной стабилизации внешней неустойчивой энергии квантов света во внутреннюю устойчивую энергию химических связей органических веществ через промежуточные формы энергии (энергия электронов хлорофилла, энергия дельта-рН, энергия макроэргических связей АТФ и НАДФ*Н2, Ковалентные связи химических веществ).
С биохимическое точки зрения. Фотосинтез - окислительно-восстановительные процесс превращения устойчивы молекул неорганических веществ в молекулы органических веществ - углеводов.
Значение фотосинтеза:
Накопление органической массы.
Обеспечение постоянства содержания СО2 в воздухе (0,03). Превышение до десятых приводит к ухудшение самочувствия. Связывание СО2 в ходе фотосинтеза компенсирует его выделение за счет:
Дыхание
Брожение
Горение
Вулканическая активность
Производственная деятельность человека
Препятствие развитию парникового эффекта.
Накопление кислорода в атмосфере (21%).
Формирование озонового экрана (защита от УФ-излучения).
2. Пигменты фотосинтезирующих растений, их физиологическая роль
Хлорофилл.
Наиболее важный в фотосинтезе пигмент. В настоящее время выделяют около 10 хлорофиллов. У высших растений А и В, у диатомовый водорослей С, наиболее важным является А.
Это сложный эфир дикарбоновой кислоты - хлорофиллина и 2 остатков спиртов (фитол и метанол). В центре молекулы атом магния, соединенный 4 атомами азота пиррольных группировок. Пиррольные группировки являются хромофорными группами хлорофилла, благодаря которым он поглощает свет.
Молекула полярная. Порфириновое ядро гидрофильное, а фитольный хвост - гидрофобный. Также порфириновое ядро связано с белком. (Порфириновое ядро — это плоское образование в молекуле хлорофилла, образованное четырьмя пиррольными кольцами, соединёнными между собой метиновыми мостиками, с атомом магния в центре.)
Способность к ОВР в молекуле обусловлена азотом пиррольных группировок, который может окисляться и восстанавливаться.
Хлорофилл поглощает максимум света в красной и синей части спектра. Растворы обладают флюоресценцией и фосфоресценцией. Собственное излучение - красное.
Каротиноды.
В настоящее время известно около 600 пигментов. Имеют желтый, оранжевый и красный цвет. Вырабатываются водорослями, бактериями, грибами и высшими растениями. Располагаются в хромопластах и хлоропластах, а антоцианы - в клеточном соке. Делятся на 3 группы:
⁃ Каротины - обычно имеют оранжевый цвет. Пример - альфа-каротин. Состоят (как и ксантофиллы) из 8 остатков изопрена, соединенных двойными связями.
⁃ Ксантофиллы - желтые пигменты, находятся в листьях.
⁃ Каротиноидные кислоты.
При разделении пигментов по Крауссу в верхнем бензиновом слое будут хлорофиллы и каротин, а в нижнем спиртовом - ксантофиллы.
Поглощают максимум света в синей и фиолетовой частях спектра. Не способны к флуоресценции.
Главная функция - вспомогательные элементы в поглощении света, также защищают молекулы хлорофилла от окисления и участвуют в фототропизме.
Фикобилины.
Пигменты красных и сине-зеленых водорослей. Молекулы состоят из 4 пиррольных колец. Они являются хромофорными группами белков фикобилин-протеинов. Проводят часть спектра к хлорофиллу, которую он не может уловить (присутствует на глубине). Делятся на 3 группы:
⁃ Фикоэритрины - белки красного цвета
⁃ Фикоцианины - сине-голубые
⁃ Аллофикоцианины - синие
Фикобилины имеют максимум поглощения в желтой и зеленой частях спектра. Около 90% поглощенной энергии передают на хлорофилл А и запускается фотосинтез. Группа фикобилинов - фикохромы - являются рецепторами красного и дальнего красного цвета, участвуют в процессах регуляции развития растений.
Обладают флуоресценцией. (красный или оранжевый)
3. Сущность фотофизического этапа. Фотохимический этап. Циклический и нециклический транспорт электронов.
Фотофизический этап - самый важный, начинается с поглощения квантов света электронами, входящими в состав пигментов. В первую очередь, доп энергию квантов света поглощает подвижные пи-электроны в молекуле хлорофилла (делокализованные пи-электроны двойной связи и неспаренные электроны атомов кислорода и азота в порфириновом ядре). Именно поэтому молекулы хлорофилла имеют 2 основные линии поглощения. Из возбужденного первого состояния молекула хлорофилла возвращается в основное состояние, при этом потеря энергии может проходить путем выделения энергии в виде света (всегда испускается красное длинноволновое излучение - флуоресценция), в виде тепла, путем переноса энергии на другую молекулу пигмента, путем затрачивания энергии на фотохимические процессы. В любом из этих случаев молекула пигмента дезактивируется и переходит на основной энергетический уровень. Энергия, испускаемая в виде флуоресценции или в виде теплоты, не может быть использована. Энергия переноса и энергия, тратящаяся на химические реакции, - то, что нужно для фотосинтеза. Для фотосинтеза установлено, что хлорофилл имеет 2 функции: поглощение и передача энергии. Основная часть молекул хлорофилла включается в светособирающий комплекс, т. е. поглощает кванты света и переносит энергию возбуждения на особые молекулы, которые непосредственно участвуют в фотохимическом процессе. Энергия квантов света улавливается от 200 до 400 молекулами хлорофилла (антенны-хлорофиллы) и стекается резонансным путем к одной особой молекуле хлорофиллу-ловушке, входящей в реакционный центр. Кроме антенны хлорофиллов в светособирающие комплексы также входят растительные пигменты каротиноиды и фикобилины.
Фотохимический этап - комплекс ОВР, в результате которых идёт дальнейшая трансформация энергии с образованием энергии макроэргических связей АТФ. Для нормального протекания фотосинтеза необходимы 2 фотосистемы: фотосистема 1 и фотосистема 2. Обе включают светособирающие комплексы и реакционные центры. Хлорофилл-ловушка фотосистемы 1 поглощает свет с длиной 700 нм, а 2–680 нм.
Выделяют 2 типа фосфосинтеических фосфорилирований: цикическое и нециклическое.
Особенности нециклического (Z-схема):
участие в двух фотосистемах,
нециклический транспорт электронов от воды к НАДФ,
образование двух энергетических эквивалентов - АТФ и НАДФН2 (используются в темновой фазе фотосинтеза),
фотоокисление воды и выделение кислорода.
Схема: электрон фотосистемы Р700 переходит на более высокий энергетический уровень. В возбужденном состоянии молекула легко отдаёт электрон в электрон-транспортную цепь и остаётся сама в виде положительно заряженного иона. С фотосистемы на переносчик Z, от него на феридоксин, от него - на НАДФ. Таким образом, работа 2-ой фотосистемы начинается с поглощения квантов света. Энергия стекается к хлорофиллу-ловушке Р680, затем электрон передается переносчику Коэнзим-Q, затем - на пластохинон (для его вос-ия также нужны протоны). Затем электрон передается на цитохромы, ненужные протоны Н+ выбрасываются, конечным переносчик - пластоцианин, и электроны передаются на фотосистему 1. Для восстановления в хлорофилл-ловушку Р680 электрон поступает из воды, при этом происходит её фотоокисление и выделение кислорода.
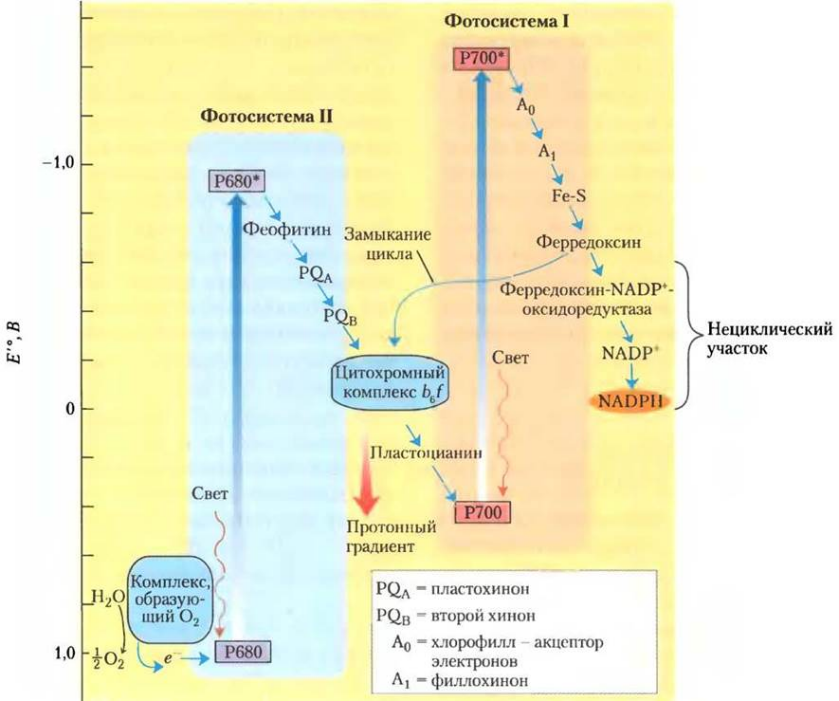
Циклическое фосфорилирование:
Особенности:
Циклический транспорт электронов
Участие только 1 фотосистемы
Энергия запасается только в виде АТФ
Начинается также как и нециклическое, но на уровне феридоксина через цитохромы ток электронов возвращается обратно к молекуле хлорофилла Р700. При переносе создаётся разность потенциалов, там, где она достаточна синтезируется АТФ.
Синтез АТФ:
Синтез АТФ объясняет хемиосмотическая теория Митчелла: её суть заключается в том, что пластохинон, присоединив 2 электрон от хлорофилла-ловушки фотосистемы 1 Р680, присоединяет 2 протона из стромы хлоропласта и переносит через мембрану во внутритилакоидное пространство. Протоны накапливаются внутри тилакоида и в результате фотоокисления воды. Благодаря неравномерному распределению протонов по обе стороны мембраны, создаётся разность химических потенциалов протонов и возникает электрохимический мембранный потенциал ионов водорода. Его энергия используется для обратного транспорта протонов из внутритилакоидного пространства в строму хлоропласта по особым каналам. С обратным транспортом протонов сопряжено фосфорилирование АДФ.
Спряжение обратного транспорта протонов и фосфорилирование АДФ обеспечивает Н+ АТФ-синтетазы, расположенной в тилакоидные мембранах и состоящая из 2 частей: каталитической (водорастворимой, обращенной к строме хлоропласта) и мембранной части (Ф0). По протонному каналу Водород возвращается в старому хлоропласта, АДФ и фосфат соединяются друг с другомв каталитической части фермента (Ф1-атф-синтетазы).
Таким образом, 2 протона, перемещаясь по градиенту концентрации электрохимического потенциала, по протонному каналу Ф0, соедияняется с фосфатом, образуя воду. Потеря кислорода активирует фосфатную группу, и она присоединяется к АДФ с образованием АТФ.
Фермент Н+АТФ-синтаза активна пока транспортируются протоны. При возвращении второму хлоропласты 2 протонов синтезируется 1 молекула АТФ.
4. Компоненты ЭТЦ хлоропластов. Фотосистемы 1 и 2.
Электрон-транспортная цепь (ЭТЦ) хлоропластов высших растений состоит из двух фотосистем (ФС I и ФС II), цитохромного комплекса (цитохром b6/f), пула хинонов, пластоцианина, светособирающих антенн и некоторых стромальных белков.
ЭТЦ хлоропластов включает ряд переносчиков: цитохромы, железосерные белки, хиноны, флавиновые ферменты и пиридиннуклеотиды. Одновременно с электронами некоторые переносчики транспортируют через тилакоидную мембрану протоны. В процессе транспорта молекула, отдающая электрон или протон, окисляется, а молекула, присоединяющая электрон или протон, восстанавливается. К таким специфическим переносчикам электронов относятся циклические тетрапирролы (хлорофиллы реакционных центров, феофетин), марганецсодержащий кластер, осуществляющий окисление воды, некоторые аминокислотные остатки белков (тирозин в ФСII) и медьсодержащий белок пластоцианин.
Цитохромы: цитохромы группы b (цитохром b559 и цитохром b563 или цитохром b6) и цитохром группы с (цитохром f). Цитохромы b6, а также цитохром f входят в состав цитохромного b6f-комплекса и участвуют в окислении пластохинолов и восстановлении пластоцианина; цитохром b559 связан с комплексом ФСII.
Железосерные белки. В молекулах этих белков 2 или 4 атома железа связаны с таким же числом атомов неорганической серы или серы в цистеине, образуя при этом железосерный центр белка. В ЭТЦ хлоропластов входят 3 железосерных центра, содержащих железосерные кластеры Fx, FA и FB и 2 белка – ферредоксин и центр Риске. Железосерные кластеры Fx, FA и FB и ферредоксин участвуют в восстановлении НАДФ+ в ФСI. Центр Риске находится в цитохромном b6 f-комплексе и осуществляет окисление пластохинолов.
Хиноны: бензохиноны (пластохиноны) и нафтохиноны (филлохинон) включены в ЭТЦ фотосинтеза. Филлохинон – переносчик электронов в ФСI, участвует в переносе электронов от первичного акцептора электронов к железосерному кластеру FX. Пластохиноны осуществляют транспорт электронов от ФСII к цитохром-b6f-комплексу; также могут передавать электроны от ФСI к цитохром- b6f комплексу. В липидном бислое соединяют белковые комплексы и могут одновременно с двумя электронами переносить через мембрану два протона из стромы хлоропласта в люмен.
Флавинсодержащий переносчик электронов ЭТЦ хлоропластов. Фермент ферредоксин-НАДФ-оксидоредуктаза содержит в качестве редокс-кофактора ФАД. Восстанавливает НАДФ+ в ФСI. Электроны для восстановления получает от восстановленного ферредоксина.
Пластоцианин – водорастворимый белок, содержащий один атом меди. Осуществляет перенос электронов по одноэлектронному типу, причем атом меди изменяет свою валентность (Сu+ ↔ Сu2+). Пластоцианин – переносчик электронов от цитохрома f из цитохром-b6f-комплекса к П700 из ФСI.
Марганецсодержащий кластер. Располагается в комплексе ФСII и образует систему окисления воды. Кластер включает четыре атома марганца, валентность которых меняется в ходе индуцируемых светом ОВР. Марганецсодержащий кластер окисляет воду с образованием молекулярного кислорода.
Электроны от марганецсодержащего кластера передаются на П680 через промежуточный переносчик электронов – остаток тирозина белка D1 ФСII.
Тетрапиррольные переносчики электронов – уникальные компоненты ЭТЦ хлоропластов. Они являются первичными донорами и первичными акцепторами электронов в реакционных центрах ФСI и ФСII. ОВР циклических тетрапирролов сопровождаются образованием заряженных радикалов.
ФОТОСИСТЕМА — совокупность светофокусирующих (антенных) молекул пигментов, фотохимического реакционного центра и переносчиков электрона. ФС I расположена в тилакоидах стромы, а ФС II – только в тилакоидах гран.
ФСI состоит из светофокусирующих пигментов и реакционного центра I. Хлорофилл-ловушка ФСI осуществляет поглощение света длинной волны 700 нм.
ФСII состоит из светофокусирующих пигментов и реакционного центр II. Свет поглощается с длиной волны в 680 нм.
Поглощение света этими фотосистемами происходит раздельно и нормальное протекание фотосинтеза требует их одновременного участия.
ФСI и ФСII работают синхронно и непрерывно (но при этом фотосистема I может функционировать отдельно).
ОВР в ФСI индуцируются светом. Фотохимическое разделение зарядов в реакционном центре ФСI приводит к формированию сильного восстановителя, способного через цепь переносчиков электронов осуществить восстановление НАДФ+. Таким образом, при участии ФСI синтезируется НАДФ∙Н+ – источник электронов для последующих реакций восстановления углерода в хлоропластах. Кроме того, ФСI может осуществлять циклический транспорт электронов, сопряженный с синтезом АТФ, обеспечивая дополнительный синтез АТФ в хлоропластах.
После возбуждения квантом света он восстанавливает первичный акцептор, a тот — вторичный (филлохинон), после чего электрон передаётся на ферредоксин, который и восстанавливает НАДФ с помощью фермента ферредоксин-НАДФ-редуктазы.
Белок пластоцианин, восстановленный в b6f-комплексе, транспортируется к реакционному центру ФСI со стороны внутритилакоидного пространства и передаёт электрон на окисленный П700.
Комплекс ФСII осуществляет окисление воды и восстановление пластохинонов. ОВР в комплексе инициируются светом. В ходе первичных фотохимических реакций в реакционном центре ФСII образуется сильный окислитель П680, который способен вызвать цепь ОВР, приводящих в итоге к окислению воды. Система окисления воды ФСII поставляет электроны в ЭТЦ хлоропластов, которые через ряд промежуточных переносчиков (пластохиноны, цитохром b6 f-комплекс и пластоцианин), попадают в ФСI и используются на восстановление НАДФ.
5. Фотосинтетическое фосфорилирование. Механизм сопряжения электронного транспорта с формированием трансмембранного градиента электрохимического потенциала. Структурно-функциональная организация и механизм работы АТФ-синтетазного комплекса.
ФОТОСИНТЕТИЧЕСКОЕ ФОСФОРИЛИРОВАНИЕ – процесс преобразования энергии света в энергию АТФ. Соответственно двум типам потока электронов различают циклическое и нециклическое фотофосфорилирование.
МЕХАНИЗМ СОПРЯЖЕНИЯ ЭЛЕКТРОННОГО ТРАНСПОРТА С ФОРМИРОВАНИЕМ ТРАНСМЕМБРАННОГО ГРАДИЕНТА ЭЛЕКТРОХИМИЧЕСКОГО ПОТЕНЦИАЛА
Важнейшим интермедиатом в реакциях превращения энергии в биологических системах является градиент электрохимического потенциала.
Механизм сопряжения электронного транспорта с генерацией электрохимического потенциала рассматривается в рамках хемиосмотической теории Митчелла. Ее суть заключается в том, что пластохинон, присоединяет два электрона от П680, затем присоединяет еще два протона из стромы хлоропласта и переносит их через мембрану в внутритилакоидное пространство. Протоны накапливаются внутри тилакоида и в результате фотоокисления воды. В результате активного переноса протонов из стромы во внутритилакоидное пространство на мембране создается электрохимический потенциал ионов водорода, имеющий две составляющие химическую (концентрационную), возникающую в результате неравномерного распределения протонов по обе стороны мембраны, и электрическую, обусловленную возникновением противоположного заряда на поверхности мембран (благодаря накоплению протонов с внутренней стороны мембраны).
СТРУКТУРНО-ФУНКЦИОНАЛЬНАЯ ОРГАНИЗАЦИЯ И МЕХАНИЗМ РАБОТЫ АТФ-СИНТЕТАЗНОГО КОМПЛЕКСА
Сопряжение диффузии протонов через мембрану осуществляется макромолекулярным ферментным комплексом, называемым АТФ-синтазой или сопрягающим фактором. Этот комплекс состоит из двух частей: мембранной части, выступающей с наружной стороны мембраны (здесь располагается каталитический центр фермента), и части, погруженной в мембрану. Мембранная часть и формирует в мембране протонный канал, по которому ионы водорода попадают к фактору сопряжения F1. Белок F1 представляет собой белковый комплекс, состоящий из мембраны, при этом он сохраняет способность катализировать гидролиз АТФ. Изолированный F1 не способен синтезировать АТФ. Способность синтезировать АТФ – это свойство единого комплекса, встроенного в мембрану. Связано это с тем, что работа АТФ-синтазы при синтезе АТФ сопряжена с переносом через нее протонов. Направленный транспорт протонов возможен только в том случае, если АТФ-синтаза встроена в мембрану.
Существуют две гипотезы относительно механизма фосфорилирования (прямой и косвенный механизмы). Согласно первой гипотезе (прямой механизм), фосфатная группа и АДФ связываются с ферментом в активном участке комплекса F1. Два протона перемещаются через канал по градиенту концентрации и соединяются с кислородом фосфата, образуя воду. Согласно второй гипотезе (косвенный механизм), АДФ и неорганический фосфор соединяются в активном центре фермента спонтанно. Однако образовавшаяся АТФ прочно связана с ферментом, и для ее освобождения требуется энергия. Энергия доставляется протонами, которые, связываясь с ферментом, изменяют его конформацию, после чего АТФ высвобождается.
