
Обмен веществ
.pdf
4)Альфа-КГ окисляется с присоединением КоА. Дальше идёт декарбоксилирование и дегидрирование с образованием активной формы янтарной кислоты (сукцинил-КоА). Образование 3 АТФ в АЭРОБНЫХ условиях. Фермент - альфа-кетоглутарат-дегидрогеназа (Альфа-КГ-дегидрогеназный комплекс) Коферменты - НАДФ, КоА, ТДФ, липоевая кислота. 5)Реакция субстратного фосфорилирования, идет с участием ГДФ и Н3РО4, отщепляется КоА, образуется ГТФ, который превратится в АТФ. Получается янтарная кислота (сукцинат). Фермент - сукцинат-тиокиназа.
6)Образуется 2 АТФ в АЭРОБНЫХ условиях. Она окисляется путем дегидрирования в фумаровую кислоту (фумарат). Фермент - сукцинат-дегидрогеназа ФАД-зависимая. 7)Из фумарата образуется дикарбоновая кислота - яблочная (малат). Фермент - фумарат-гидратаза.
8)Окисление малата дегидрирование. Образуется 3 АТФ в АЭРОБНЫХ условиях, продукт реакции - щавелево-уксусная кислота (оксалоацетат). Молекула ЩУК снова может вовлекаться молекулу ацетил-КоА в новый цикл. Фермент - малат-дегидрогеназа.
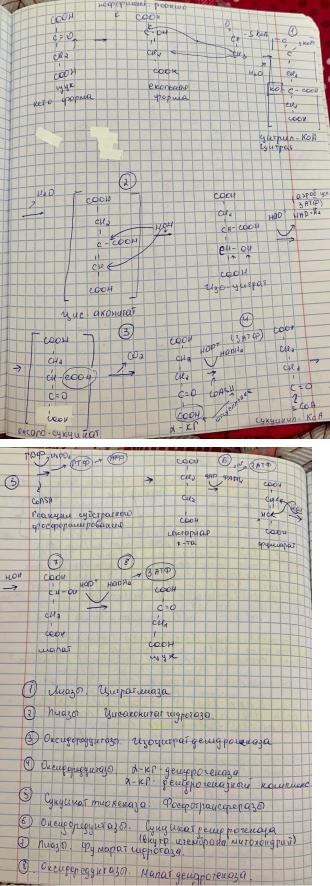

Биохимические функции ЦТК
1. Водород-донорная функция - в реакциях ЦТК происходит окисление субстратов путем дегидрирования и атомы водорода с участием НАД и ФАД передаются в дыхательную цепь.
2. Энергетическая функция - в ЦТК есть реакция субстратного фосфорилирования, в котором образуется ГТФ и АТФ; ЦТК совместно с окислительным фосфорилированием (работой дыхательной цепи и
АТФ-синтазой) в 1 обороте цикла приводит к образованию: 3 стадия в АЭРОБНЫХ условиях даёт 3 АТФ, 4 стадия - в аэр. 3 АТФ, 5 стадия субстратное фосфорилирование не зависит от условий, образуется ГТФ, которая может превратиться в 1 АТФ, 6 стадия - в аэр. 2 АТФ, 8 стадия - в аэр. 3 АТФ. Таким образом, суммарная энергетическая эффективность 1 оборота ЦТК = 12 АТФ.
Реакции ЦТК обратимы, но на самом деле в физиологических условиях эти реакции протекают только как окислительные, в обратную сторону не идут. Но у некоторых бактерий ЦТК может быть восстановительным (т.е. в обратную сторону). В анаэробных условиях ЦТК начинает замедляться, энергетическая эффективность субстратного фосфорилирования снижается. В анаэробных условиях будут накапливаться.
3. Интегративная - на уровне ЦТК может происходить переключение на другие виды обмена. Альфа-КГ, сукцинил-КоА, ЩУК может переключаться на обмен углеводов, липидов и АК.
3. Система окислительного фосфорилирования
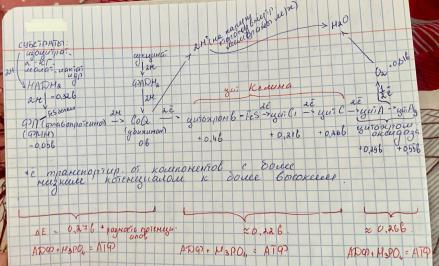
Все её компоненты погружены во внутреннюю мембрану митохондрий. В неё входит дыхательная цепь и АТФ-синтаза.
Дыхательная цепь
Это электрон-транспортная цепь (ЭТЦ), где компоненты встроены во внутреннюю мембрану митохондрий.
Характеристика компонентов:
В ДЦ атомы Н2 передаются НАД-дегидрогеназами (изоцитрат-дегидрогеназой, альфа-КГ-дегидрогеназой, малат-дегидрогеназой, лактат-дегидрогеназой и тд) и НАД-дегидрогеназами (сукцинат-дегидрогеназой). НАДН2 передаёт атомы водорода флавопротеину. Флавопротеин содержит в качестве кофермента ФМН и тесно связан с железо-серо-содержащим белком.
Железо-серо-содержащие белки находятся на 2 участках дыхательной цепи, содержат ионы железа, благодаря чему и могут принимать электроны.
КоэнзимQ (убихинон) принимает атомы водорода от флавопротеина и от ФАДН2. На уровне убихинннона атомы водорода разделяются на катионы водорода и электроны. Катионы перекачиваются на наружную сторону внутренней мембраны м/х (в межмембранное пространство).
Электроны передаются цитохромам Келина (в, с1, с) - гемопротеины, в центре - ионы железа. Цитохромоксидаза - фермент, у которого в активном центре есть ионы железа и ионы меди. Она принимает электроны от цитохромов Кейлина и сбрасывает их на молекулу О2, который восстанавливается до воды.
Результат работы ДЦ - создание на внутренней мембране митохондрий трансмембранного потенциала (за счет электронов на внутренней стороне мембраны создаётся отрицательный заряд, а за счет перекачки катионов водорода на наружной стороне мембраны создаётся положительный заряд, тем самым образуется трансмембранный электрохимический потенциал).
На внутренней стороне мембраны находятся грибовидные тела - молекулы АТФ-синтазы. Ножка фермента погружена во внутреннюю мембрану митохондрий, в ножке находится ионный канал для катионов водорода. Таким образом этот фермент называют Н+-АТФ-синтаза. Шляпка обращена в матрикс митохондрии, в ней находится активный центр фермента (здесь идёт синтез АТФ из АДФ и фосфата).
Работа дыхательной цепи приводит к поляризации мембраны (возникновению трансмембранного потенциала), что приводит к активации АТФ-синтаза за счет изменения ее конформации, и АТФ-синтаза в шляпке синтезирует АТФ.
В идеальных условиях если ДЦ функционирует от НАДН2, то АТФ-синтаза срабатывает 3 раза. Если цепь идёт от ФАДН2 - 2 АТФ.
Одновременно в ножке АТФ-синтазы открывается канал для катионов водорода. И избыток катионов Н+ перетекает обратно в матрикс. Это приводит к разрядке внутренней мембраны митохондрий (исчезает трансмембранный потенциал). Как только потенциал исчезает, АТФ-синтаза снижает активность, перестает синтезировать АТФ до того момента, пока ДЦ снова не создаст трансмембранный потенциал. Этот механизм называется
ОКИСЛИТЕЛЬНЫМ ФОСФОЛИРИРОВАНИЕМ.
Таким образом, ДЦ создаёт условия для окислительного фосфорилирования (синтеза АТФ). В САМОЙ ДЦ АТФ НЕ СИНТЕЗИРУЕТСЯ.
Сопряжение окисления и фосфолирирования характеризуется коэффициентом фосфолирирования. Р/О - отношение потребленных атомов фосфора для синтеза АТФ к числу потребленных атомов О2 в дыхательной цепи.
Видеале, если ДЦ работает от НАДН2, то Р/О=3. Если ДЦ от ФАДН2, то Р/О=2.
Вреальности окисление и фосфорилирование не всегда сопрягаются. От НАДН2 Р/О=2,5 От ФАД-Н2 Р/О=1,5.
Причиной отличия является разобщение процесса окисления и фосфолирирования даже в физиологических условиях (например, ЭТЦ функционирует, транспорт электронов идет, а синтез АТФ - нет).
При патологических состояниях возможно усиление разобщения окисления и фосфолирирования, тем самым снижается выход АТФ, а энергия трансмембранного потенциала может рассеиваться в виде тепла.
Транспорт АТФ из митохондрий в цитозоль осуществляется ферментативно, с помощью АТФ-транслоказы, которая переносит их в обмен на АДФ (АТФ переносит в цитозоль, а АДФ - в м/х).
2. Микросомальное окисление (монооксигеназная система)
Располагается в мемранах ЭПР. Это электрон-транспортная цепь (ЭТЦ), главным компонентом которой является цитохром Р450.
1 стадия - присоединение субстрата (образование фермент-субстратного комплекса)
2)Восстановление двойного фермент-субстратного комплекса первым электроном.
3)Образование тройного фермент-субстратного комплекса (присоединение кислорода)
4)Восстановление тройного комплекса вторым электроном
5)Атом кислорода встраивается в субстрат, при этом у субстрата образуется гидроксогруппа, а второй атом кислорода образует молекулу воды.

Биологические функции микросомального окисления:
1. Обезвреживание ксенобиотиков (чужеродных веществ) и собственных (эндогенных) некоторых субстратов. Вещества, которые окисляется данной системой - гидрофобные. Микросомальная система, гидроксилируя данные субстраты, делает их более гидрофильными, чтобы их вывести.
Данная система чаще всего является 1 стадией обезвреживания ксенобиотиков (иногда одной её работы недостаточно, и протекает вторая стадия - конъюгация). Продукты монооксигеназной системы конъюгируются с различными кислотами (глюкуроновая, серная кислота), становятся полностью гидрофильными и выводятся с мочой.
Микросомальные системы содержатся в печени, стенках ЖКТ, коже и легких.
2. В микросомальной системе происходит заключительная стадия биосинтеза холестерина (приобретает гидроксо-группу).
!!!!!!Перекисное окисление липидов (образование активных форм кислорода, Перекисное окисление липидов, Антиоксидантные системы (ферменты антиоксиданты и небелковые вещества-антиоксиданты - витамины) - разобрать)
Короткие пути окисления - разобрать.
Обмен углеводов
Экзогенный распад (переваривание в ЖКТ)
Начинается в ротовой полости путем гидролиза с помощью фермента альфа-амилаза слюны. Крахмал амилазой слюны расщепляется до декстринов.
В желудке переваривание углеводов не протекает. Идёт в кишечнике. Здесь работают ферменты двух групп:
1. Поджелудочной железы (панкреатические) - альфа-амилаза панкреатическая расщепляет альфа-1,4-гликозидные связи, но её недостаточно, поэтому работают также альфа-1,6-гликозидазы. Результат работы этих ферментов - дисахариды (Мальтоза и изомальтоза).
2. Кишечника - работают с дисахаридами. расщепляются до моносахаридов. Крахмал - до глюкозы.

Катаболизм глюкозы
В АЭРОБНЫХ условиях состоит из 3 этапов: 1 этап - до ПВК. Протекает в цитозоле.
2 этап - ПВК превращается в ацетил-КоА. Окислительное Декарбоксилирование ПВК, затем она включается в цикл Кребса (ЦТК), которые протекает в м\х.
3 этап - Окислительное фосфорилирование. Протекает на внутренней мембране м/х.
2 и 3 этап - см. Предыдущую лекцию.
1 этап.
Аэробный гликолиз
Расщепление глюкозы в АЭРОБНЫХ условиях происходит дихотомическим путем - дихотомический распад глюкозы.
Реакции протекают в цитозоле.
1. Фосфорилирование. Образуется глюкоза-6-фосфат. Глюкокиназа(только глюкозу)/гексокиназа(все углеводы) Узкое место гликолиза.
2. Изомеризация (обратимая) - образуется фруктоза-6-фосфат. Глюкоза-6-фосфат-изомераза
3. Фосфорилирование (необратимая) - с затратой АТФ(донор фосфатной группы). Образуется фруктоза-1,6-дифосфат. Фосфофруктокиназа. Узкое место гликолиза.
4. Распад углеродного скелета (обратимая) - образуется глицеральдегид-3-фосфат (ГАФ) и диоксиацетон-фосфат (ДОАФ) - 6-углеродный скелет расщепляется на 2 триозы, которые могут изомеризоваться друг в друга. Фруктоза-1,6-дифосфат-С-С-лиаза (альдолаза).
5. Изомеризация диоксиацетон-фосфата в глицеральдегид-3-фосфат (обратимая). Триозофосфат-изомераза.
6. Окисление глицеральдегид-3-фосфата (обратимая) - НАД+ → НАДН2, атомы водорода которого уходят в дыхательную цепь (цитозольный НАДН2 сначала передаёт атомы челночному механизму, а тот уже - митохондриальному НАД, образуется митохондриальный НАДН2, который передаёт атомы водорода в дыхательную цепь) → в результате выделяется 3 АТФ х 2. Образующиеся вещество - 1,3-дифосфоглицерат (1,3-дифосфоглицериновая кислота). Глицеральдегид-3-фосфат-дегидрогеназа.
7. Субстратное фосфорилирование (обратимая). 2 АДФ → 2 АТФ. Образуется 3-фосфоглицерат (3-фосфоглицериновая кислота). Фосфоглицераткиназа.
8. Изомеризация (обратимая). Образуется 2-фосфоглицерат. Фосфоглицератмутаза. 9. Дегидратация (обратимая). Образуется фосфоэнолпируват (ФЭП). Эноилгидратаза. 10. Субстратное фосфорилирование (необратимая). 2 АДФ → 2 АТФ. Образуется ПВК.
Пируваткиназа. После этой реакции пируват превращается в ацетил-КоА и вовлекается в цикл Кребса. Узкое место гликолиза
*фермент
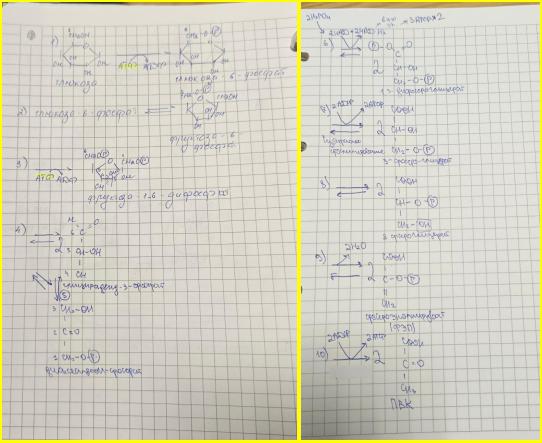
Теоретически ожидаемая энергетическая эффективность всех реакций: 1)-1 АТФ 3)-1 АТФ
6)+6 АТФ (2х3 АТФ)
7)+2 АТФ (2х1 АТФ)
10)+2 АТФ Суммарно: + 8 АТФ (в аэробных условиях).
Энергетическая эффективность окисления 1 молекулы глюкозы в аэробных условиях:

Анаэробный гликолиз
Ванаэробных условиях не функционирует дыхательная цепь. Протекает окисление глюкозы до ПВК (10 реакций - см. выше) + 11 реакция - превращение ПВК в молочную кислоту (гидрирование). Реакция обратима. Лактатдегидрогеназа (ЛДГ).
Ванаэробных условиях идёт прямая реакция, а обратная - в аэробных.
Теоретически ожидаемая энергетическая эффективность: 1)-1 АТФ 3)-1 АТФ 7)+2 АТФ 10)+2 АТФ
Суммарно: +2 АТФ.
Анаэробный путь окисления глюкозы является эволюционно более древним. Эти эволюционно-древние пути называются брожением.
Спиртовое брожение
суммарное уравнение:

До ПВК это те же 10 реакций гликолиза. После ПВК - 11 и 12 реакции:
11. Декарбоксилирование ПВК до ацетальдегида. Пируватдекарбоксилаза 12. Гидрирование - восстановление альдегида в этиловый спирт. Реакция обратима, в
обратном направлении присутствует у человека (превращение этилового спирта в ацетальдегид, который затем при помощи альдегид-дегидрогеназы превращается в уксусную кислоту → ацетил-КоА). Алкогольдегидрогеназа
В клетках человека Спиртовое брожение не протекает, протекает у бактерий и дрожжей. Энергетическая эффективность: 2 АТФ, как и у анаэробного гликолиза.
Молочнокислое брожение
Окисление глюкозы до молочной кислоты (см. Анаэробный гликолиз). Энергетическая эффективность: 2 АТФ.
Молочнокислое брожение протекает у бактерий.
Глюконеогенез
Глюконеогенез - синтез глюкозы из веществ неуглеводной природы (из глицерина, аминокислот, лактата). Процесс обратный гликолизу. Идёт в противоположную ему сторону, но за счет того, что в гликолизе есть необратимые реакции, существуют обходные пути глюконеогенеза (соответствуют узким местам гликолиза):
- ПВК → ФЭП - этому превращению соответствует 1 обходной путь глюконеогенеза. Идёт реакция Карбоксилирование ПВК с образованием ЩУК, затрачивается АТФ. Фермент - пируваткарбоксилаза. Реакция протекает в митохондриях. Дальше протекает малатный челночный механизм (в митохондриях ЩУК превращается сначала в малат -
