
1 семестр ФИБС / Химия Яльмяшева / Билеты / 66-68
.docx66. Диаграмма плавкости бинарной системы с образованием химических соединений.
Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.
Диаграммы плавкости – частный вид диаграмм состояния.
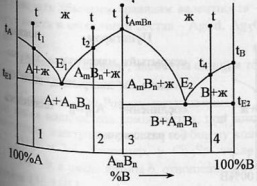
Устойчивое, плавящееся без разложения хим.соединение АmВn проявляется на диаграмме в виде max. Чем круче мах, тем устойчивее хим.соединение.
Систему А-В можно представить как бы состоящей из 2 простейших эвтектических диаграмм, где роль одного из компонентов играет устойчивое хим.соединение АmВn .
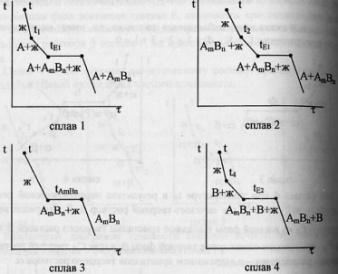
Кривые охлаждения четырех сплавов.
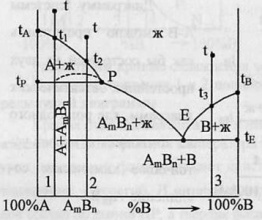
Хим. соединение АmВn разлагается ниже t пл. Имеются 2 точки нонвариантного равновесия - Р и Е.Пунктиром показан “скрытый” мах – так выглядела бы диаграмма, если бы хим.соединение АmВn плавилось без разложения.
Кривые охлаждения 3 сплавов-1,2,3.
Кривая охлаждения сплава1:первоначально при t1 выпадают кристаллы компонента А, жидкая фаза меняет свой состав в интервале t1-tP по линии t1Р; при достижении жидкой фазой состава Р получает развитие перитектическая реакция, в результате чего жидкая фаза исчезает.
Для сплава2 при tP по перитектической реакции исчезают кристаллы компонента А, далее в интервале tP-tЕ из жидкой фазы выпадают кристаллы АmВn ,а при достижении жидкой фазы состава Е происходит кристаллизация эвтектики АmВn +В.На кривой охлаждения сплава 2 наблюдается 2 площади- при tP и tЕ .
На кривой охлаждения сплава3 наблюдаются перегиб при t3 – начало выделения кристаллов компонента В и площадка при tЕ - кристаллизация эвтектики В+АmВn.
67. Адсорбция и абсорбция. Хемосорбция.
Процесс сорбции представляет собой поглощение одной средой — жидкостью или твердым телом других окружающих сред — веществ, газов или других жидкостей. То вещество, которое поглощает окружающую среду — сорбент. Вещество, газ, или жидкость, которые поглощаются сорбентом, называют сорбатом или сорбтивом.
Явление сорбции подразделяют в зависимости от механизма поглощения одних сред другими на адсорбцию, абсорбцию, хемосорбцию и капиллярную конденсацию.
Адсорбция и абсорбция различаются по тому, каким образом одно вещество распределяется в другом. При абсорбции поглощение и распределение вещества происходит по всему объему жидкого абсорбента. При адсорбции твердый, жидкий или газообразный сорбат скапливается на поверхности раздела фаз адсорбента (на поверхности твердого вещества или жидкости).
Выделяют физическую адсорбцию, при которой скопление веществ на поверхности адсорбента происходит вследствие неспецифических межмолекулярных сил, не зависящих от природы веществ.
Хемосорбция (или химическая адсорбция) — это сорбционные процессы, при которых происходят химические превращения между сорбентом и поглощаемым веществом.
Адсорбция растворенных в жидкости веществ на поверхности твердого сорбента происходит по причине разности межмолекулярных сил на поверхности раздела фаз. При адсорбции выделяют два вида взаимодействия между молекулами:
молекулы растворенного вещества взаимодействуют с молекулами или атомами поверхности адсорбента;
молекулы растворенного вещества взаимодействуют с водой в процессе гидратации.
Конечная сила удержания вещества на поверхности адсорбента складывается из разности указанных выше сил межмолекулярного взаимодействия. При повышении энергии гидратации молекул растворенного вещества ослабляется адсорбция вещества из раствора, поскольку в этом случае молекулы растворенного вещества испытывают более сильное противодействие.
Абсорбция играет важную роль в обмене веществ, в частности в газообмене с окружающей седой. В качестве сорбента выступает жидкая фаза, в которой происходит растворение газов, либо между двумя несмешивающимися жидкостями происходит перераспределение вещества. Абсорбционное равновесие характеризуется константой распределения, где С1 и С2 соответствуют константе вещества в абсорбенте и в окружающей среде.

Адсорбция: в отличие от абсорбции адсорбция связана с поглощением вещества на поверхности раздела контактирующих фаз. При адсорбции различают адсорбент – вещество, на поверхности которого протекает адсорбция и адсорбат – компонент, который концентрируется на поверхности адсорбента. Адсорбция бывает:
Физическая – обусловлена силами межмолекулярного взаимодействия и образования Н связей (Э = 4-40 кДж/моль). Благодаря незначительной энергии физическая адсорбция всегда обратима и сопровождается экзотермичностью.
Химическая – не обратима, связана с химическим взаимодействием адсорбента и адсорбата (Эсв = 400 кДж/моль).
На практике чаще всего используют для поглощения газов, паров, растворимых веществ – твердые адсорбенты (сажа, активированный уголь, аморфный SiO2, Al2O3 и т д). количественно адсорбция характеризуется удельной адсорбцией Г – равновесное количество поглощаемого вещества на единицу поверхности или массы твердого адсорбента
Г = n/m [ммоль/Гадс][мэкв/Гадс][мг/Гадс]
Адсорбция – чисто поверхностный процесс – молекулы сорбируемого вещества покрывают поверхность адсорбента мономолекулярным слоем. Сорбция протекает на активных центрах сорбента: выступах, впадинах, капиллярах, трещинах, ребрах, углах – для кристаллических сорбентов.
Хемосорбция может протекать при температурах выше и ниже критической температуры адсорбируемого газа. От физической адсорбции ее отличает прежде всего зависимость от химической природы адсорбента и адсорбата. Теплоты хемосорбции близки к теплотам химических реакций. Хемосорбированные вещества удалить с поверхности сорбента значительно труднее, чем при физической адсорбции, причем десорбция может сопровождаться химическими реакциями. Например, при термической десорбции кислорода с угля (кислород хемосорбируется на угле очень прочно) вместо кислорода выделяется смесь CO и CO2. При хемосорбции количество адсорбируемого вещества также уменьшается с повышением температуры, но обычно количество хемосорбированного вещества больше, чем при физической адсорбции. Скорость процесса хемосорбции существенно зависит от температуры- растет по экспоненте с повышением температуры. Энергия активации хемосорбции достигает несколько 10-ов ккал/моль.
Хемосорбция нередко протекает сравнительно медленно. Со скоростью, определяемой наличием активационного барьера (отсюда название «активационная адсорбция»). При хемосорбции молекулы или атомы адсорбента обмениваются электронами, образуя поверхностное химическое соединение. В этом случае действуют гораздо большие (валентные) силы, чем Ван-дер-ваальсовские.
Очень часто для одного и того же вещества, но в различных интервалах температур можно наблюдать оба типа адсорбции.
При низких температурах наблюдается физическая адсорбция, при высоких – хемосорбция. Оба процесса разделены промежуточной областью, которая характеризуется увеличением количества адсорбированного вещества.
Сорбцией (от латинского sorbeo – поглощаю, втягиваю) называют любой процесс поглощения одного вещества (сорбтива) другим (сорбентом), независимо от механизма поглощения.
В зависимости от механизма сорбции различают адсорбцию, абсорбцию, хемосорбцию и капилярную конденсацию.
Адсорбция это процесс, происходящий на границе раздела фаз. Он затрагиваетолько поверхностные слои, взаимодействующих фаз, и не распространяется на глубинные слои этих фаз.
Адсорбцией называют явление накопления одного вещества на поверхности другого. В общем случае, адсорбцией называют изменение концентрации вещества на границе раздела фаз.
Абсорбция, в отличии от адсорбции, это процесс захватывающий не только поверхность раздела фаз, но распространяющийся на весь объём сорбента.
Примером процесса абсорбции является растворение газов в жидкости.
Хемосорбцией называется поглощение одного вещества другим, сопровождающееся их химическим взаимодействием.
Капиллярная конденсация — сжижение пара в капиллярах, щелях или порах в твердых телах.
Явление конденсации отлично от физической адсорбции.
Таким образом, сорбционные процессы различны по их механизму. Однако, любой сорбционный процесс начинается с адсорбции на границе соприкасающихся фаз, которые могут быть жидкими, газообразными или твёрдыми.
Типы адсорбции
Адсорбция на границе жидкость-газ
Адсорбция на границе твёрдое тело-газ
Адсорбция на границе твердое тело-жидкость
Адсорбированные молекулы взаимодействуют с молекулами или атомами
поверхности и снижают как свободную поверхностную энергию Гиббса
конденсированной фазы, так и суммарную энергию системы.
Поэтому адсорбция – самопроизвольный процесс, происходящий с выделением тепла.
Количественные характеристики адсорбции
Избыточная гиббсовская адсорбция (Г ) – избыток адсорбата в
поверхностном слое по сравнению с его количеством в объемефазы, отнесенный к единице площади поверхности (моль/м2)
характеризует адсорбцию на жидкой поверхности
Абсолютная адсорбция ( ɑ ) – количество адсорбата на единице
массы адсорбента (моль/г) используется для характеристики адсорбции на
твердой поверхности
Изотерма адсорбции — зависимость количества адсорбированного вещества (величины адсорбции) от парциального давления этого вещества в газовой фазе (или концентрации раствора) при постоянной температуре
Различают шесть основных типов изотерм адсорбции
Тип I характерен для микропористых твёрдых тел с относительно малой долей внешней поверхности.
Тип II указывает на полимолекулярную адсорбцию на непористых или макропористых адсорбентах.
Тип III характерен для непористых сорбентов с малой энергией взаимодействия адсорбент-адсорбат.
Типы IV и V аналогичны типам II и III, но для пористых адсорбентов.
Изотермы типа VI характерны для непористых адсорбентов с однородной поверхностью.
Два предельных случая адсорбции: адсорбция химическая или хемосорбция и физическая или физадсорбция.
Физическая адсорбция Взаимодействие адсорбента и адсорбата за счет сил Вандер-Ваальса и водородных связей (мало специфична).
Химическая адсорбция Взаимодействие адсорбента и адсорбата за счет образования химических связей (строго специфична)
Сорбция – процесс поглощения одного вещества поверхностью или всем объемом другого вещества. Поглощаемое вещество – сорбат, поглотитель – сорбент (часто твердое тело).
Поглощение может происходить только поверхностью (адсорбция) или всем объемом (абсорбция).
Физическая адсорбция – адсорбат и адсорбент связаны лишь слабыми силами межмолекулярного взаимодействия.
Хемосорбция – процесс, при котором поглощаемое вещество химически взаимодействуют с поглотителем.
В результате проявления сил химической связи на поверхности адсорбента образуется новое химическое соединение.
В научной и производственной практике наибольшее значение имеет адсорбция (нежели абсорбция).
Адсорбционная
способность
адсорбента определяется по удельной
площади поверхности

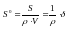

 степень дисперсности
адсорбента.
степень дисперсности
адсорбента.
Адсорбционная способность тем выше, чем меньше размеры частиц, на которые раздроблен адсорбент.
68. Агрегатные состояния вещества. Стеклообразное и жидкокристаллическое состояния вещества.
Многие вещества могут, в зависимости от внешних условий (температура, давление), находиться в трех агрегатных состояниях – твердом, жидком и газообразном.
Простейшее определение:
газы не имеют постоянных объема и формы при постоянной температуре; жидкости имеют постоянный объем, но форма зависит от сосуда;
твердые вещества имеют постоянную форму и объем.
Наиболее проста теория (и математическое описание) газового состояния. При “нормальных условиях” (0о С или 273,15 К и 1 атм. или 101325 Па) большинство газов вполне удовлетворительно описываются уравнением состояния идеального газа (уравнение Менделеева-Клапейрона):
pv = nRT
Идеальный газ состоит из частиц (молекул), представляющих собой абсолютно твердые упругие шарики бесконечно малого размера, взаимодействием между которыми (кроме редких упругих столкновений) можно пренебречь. Для многих приблизительных расчетов и решения учебных задач используется следствие из закона Авогадро – при н.у. 1 моль газа (6,022. 1023 молекул) занимает объем, равный 22, 4 л.
Для реальных газов используют уравнения состояния с поправками, учитывающими собственный размер молекул и взаимодействие между ними. Во многих случаях достаточно приближенного уравнения Ван-дер-Ваальса:
(p +a/V2 )(V - b) = RT
a/V2 – поправка, учитывающая взаимное притяжение молекул (“внутреннее давление”)
b – поправка, учитывающая собственный объем молекул и их взаимное отталкивание.
Теория жидкостей разработана гораздо хуже, чем газов, поскольку свойства жидкостей зависят от геометрии и полярности взаимно близко расположенных молекул. Кроме того, отсутствие определенной структуры жидкостей затрудняет их формализованное описание – в большинстве учебников жидкостям уделено гораздо меньше места, чем газам и твердым кристаллическим веществам.
Между жидкостями и газами нет резкой границы – она полностью исчезает в критических точках. Для каждого газа известна температура, выше которой он не может быть жидким ни при каком давлении; при этой критической температуре исчезает граница (мениск) между жидкостью и ее насыщенным паром. Существование критической температуры (“температуры абсолютного кипения”) установил Д.И.Менделеев в 1860 г.
Твердые кристаллические вещества обладают упорядоченной структурой с повторяющимися элементами, что позволяет исследовать их методом дифракции рентгеновских лучей (метод рентгеноструктурного анализа, используется с 1912 г.). Твердые вещества плавятся при фиксированной температуре. Они достаточно подробно описаны в рекомендованных учебниках.
Стеклообразное состояние – твердое аморфное состояние вещества, которое получается в результате глубокого переохлаждения жидкости. Это состояние неравновесно, однако, стекла могут существовать длительное время. Размягчение стекла происходит в некотором диапазоне температур – интервале стеклования, границы которого зависят от скорости охлаждения. С увеличением скорости охлаждения жидкости или пара возрастает вероятность получения данного вещества в стеклообразном состоянии. Стекла текут, хотя и очень медленно.
В-ва в С.с.-стекла-отличаются от веществ в кристаллич. состоянии рядом характерных особенностей, в частности изотропностью, постепенностью затвердевания и размягчения. Мн. стекла характеризуются высокой прозрачностью в видимой части спектра.
Жидкокристаллическое состояние – промежуточное между кристаллическим и жидкостью. Жидкие кристаллы обладают одновременно текучестью и анизотропией (оптической, электрической, магнитной). Иногда это состояние называют мезоморфным (мезофазой) – из-за отсутствия дальнего порядка.
Жидкий кристалл – это специфическое агрегатное состояние вещества, в котором оно проявляет одновременно свойства кристалла и жидкости.
Некоторые органические вещества, обладающие сложными молекулами, кроме трех названных состояний, могут образовывать четвертое агрегатное состояние — жидкокристаллическое. Это состояние осуществляется при плавлении кристаллов некоторых веществ. При их плавлении образуется жидкокристаллическая фаза, отличающаяся от обычных жидкостей. Эта фаза существует в интервале от температуры плавления кристалла до некоторой более высокой температуры, при нагреве до которой жидкий кристалл переходит в обычную жидкость.
Подобно обычной жидкости, жидкий кристалл обладает текучестью и принимает форму сосуда, в который он помещен. Этим он отличается от известных всем кристаллов.
Однако, несмотря на это свойство, объединяющее его с жидкостью, он обладает свойством, характерным для кристаллов. Это — упорядочение в пространстве молекул, образующих кристалл. Правда, это упорядочение не такое полное, как в обычных кристаллах, но, тем не менее, оно существенно влияет на свойства жидких кристаллов, чем и отличает их от обычных жидкостей.
Неполное пространственное упорядочение молекул, образующих жидкий кристалл, проявляется в том, что в жидких кристаллах нет полного порядка в пространственном расположении центров тяжести молекул, хотя частичный порядок может быть. Это означает, что у них нет жесткой кристаллической решетки. Поэтому жидкие кристаллы, подобно обычным жидкостям, обладают свойством текучести.
Обязательным свойством жидких кристаллов, сближающим их с обычными кристаллами, является наличие порядка» пространственной ориентации молекул. Такой порядок в ориентации может проявляться, например, в том, что все длинные оси молекул в жидкокристаллическом образце ориентированы одинаково. Эти молекулы должны обладать вытянутой формой. Кроме простейшего названного упорядочения осей молекул, в жидком кристалле может осуществляться более сложный ориентационный порядок молекул.
