
- •61. Сущность термографического анализа. Основные принципы построения диаграммы плавкости бинарных систем.
- •1. Принцип непрерывности.
- •2. Принцип соответствия.
- •62. Диаграмма состояния однокомпонентной системы на примере воды.
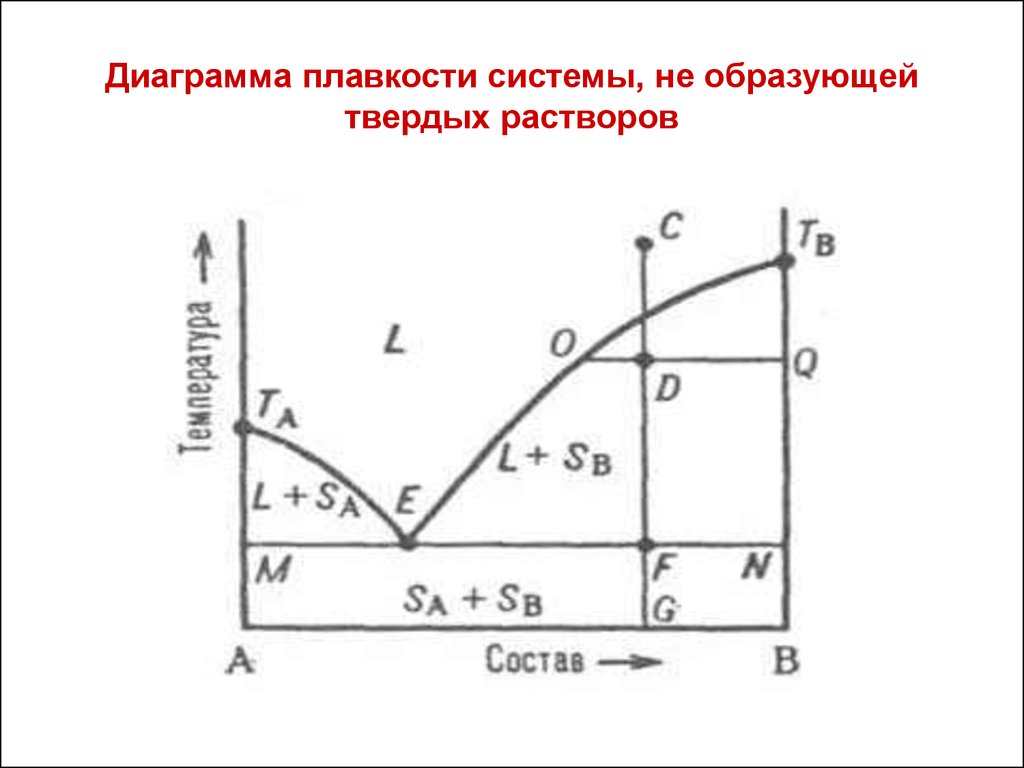
- •63.Эвтектическая диаграмма плавкости (без образования твердых растворов).
- •64. Диаграмма плавкости непрерывных твердых растворов. Правило рычага.
- •65. Диаграмма плавкости бинарной системы с ограниченными твердыми растворами.
64. Диаграмма плавкости непрерывных твердых растворов. Правило рычага.
Пример. Cu-Ni, Fe-Ni, Bi-Sb, Ag-Au, FeO-MnO и др.

Все
кривые охлаждения сплавов не имеют
площадок, а лишь 2 перегиба. Линии
 линия
ликвидуса,
линия
ликвидуса,  солидуса.
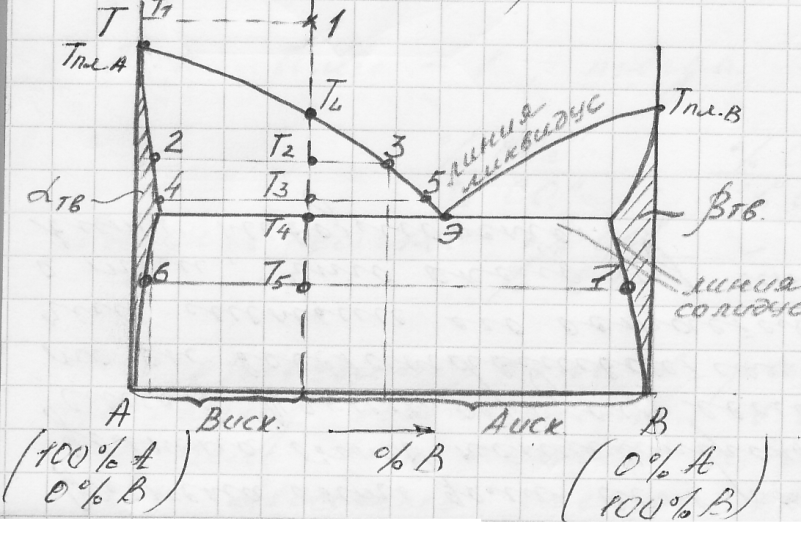
Во всем интервале составов в твердом
состоянии присутствуют смешанные
кристаллы – твердый раствор α.
солидуса.
Во всем интервале составов в твердом
состоянии присутствуют смешанные
кристаллы – твердый раствор α.

Рассмотрим ход кристаллизации сплава состава 5, взятого при t. В интервале t-t’ никаких фазовых превращений не наблюдается, t меняется монотонно. При достижении t’ из жидкого сплава начинают кристаллизоваться кристаллы α состава N, т.е. первые порции тв. фазы обогащены более тугоплавким компонентом. В равновесии находятся твердые и жидкие фазы различного состава, отсюда и отсутствие площадок на кривых охлаждения.
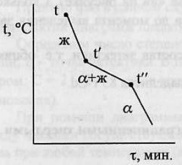
При понижении от t’ до t” состав твердой фазы меняется по линии nt”, а состав жидкой фазы – по линии t’m.
Состав твердой фазы в процессе кристаллизации непрерывно меняется, состав слитка по сечению будет неоднородным: периферийные зоны слитка, кристаллизующиеся в первую очередь, будут более тугоплавкими, а центральные - более легкоплавкими. Это явление носит название ликвация. Ликвацию устраняют, проводя так называемый отжиг, при котором слиток нагревают до t, близкой к t солидуса, и выдерживают при этой t длительное время.
Эта система моновариантна (С=К-Ф+1=2-2+1=1), поэтому любой произвольно выбранной t соответствуют вполне определенные составы жидкого расплава и смешанных кристаллов: состав жидкой фазы находят на линии ликвидуса, а состав твердой - на линии солидуса.
При помощи диаграммы плавкости можно определить соотношение между массами сосуществующих при равновесии фаз для сплава данного состава при любой температуре (правило рычага).
Для данного случая правило рычага можно записать:
 z
– cостав твердой фазы, х – состав жидкой
фазы.
z
– cостав твердой фазы, х – состав жидкой
фазы.

65. Диаграмма плавкости бинарной системы с ограниченными твердыми растворами.
Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.
Диаграммы плавкости – частный вид диаграмм состояния.
Для данных систем характерны полная взаимная растворимость компонентов в жидком состоянии и ограниченная - в твердом. Если твердые растворы образуют эвтектику, то точка нонвариантного равновесия Е лежит ниже t плавления чистых компонентов,если же перитектику,то нонвариантная точка P лежит между t плавления чистых компонентов.
Пример. Cu-Ag,Pb-Sn; Hg-Cd.
Рассмотрим первый случай.
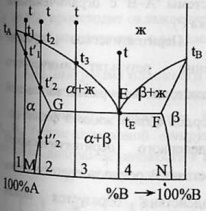
Система А-В с ограниченная твёрдыми растворами- с эвтектикой. В системе имеется 2 твердых раствора: α - р-р компонентов В в А и β- р-р компонента А в В.
Max растворимость В в А при t эвтектики tЕ отвечает точке G, а при комнатной t – точке M.
Линия GM характеризует уменьшение растворимости В в А по мере понижения t от эвтектич-й до комнат-й.Линия FN-снижение растворимости А в В при понижении t от tЕ до комнат-й.
Кривые охлаждения 4 сплавов:1,2,3,4.

На кривой охлаждения сплава 1 имеются 2 перегиба, отвечающих началу и концу выделения кристаллов твёрдого р-ра α.
На кривой охлаждения сплава 2 дополнительно наблюдается слабо выраженный перегиб при t”2,отвечающий частичному распаду в твёрдом состоянии кристаллов α с выделением кристаллов тв. р-ра β. Кривая охлаждения сплава 3: при t3 из жидкой фазы выделяются кристаллы тв. р-ра α, жидкая фаза при понижении от t3 до tЕ меняет свой состав по линии t3Е,т.е.обогащается компонентом В.Как только жидкая фаза достигнет состава Е, начинается кристаллизация эвтектики - мех. смеси 2 тв.фаз-тв.р-ра α состава G и тв.р-ра β состава F,на кривой охлаждения наблюдается площадка.
Сплав 4 точно отвечает эвтектич.составу,кривая охлаждения его подобна кривой охлаждения чистого компонента.
Система А-В с ограничен.тв.р-рами- с перитектикой(т.Р).
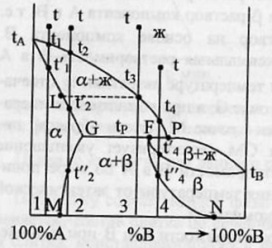
Перитектическое превращение-результат химического взаимодействия ранее выпавшей тв.фазы с жидкой фазой определенного (перитектического) состава.
В результате этого взаимодействия образуется новая тв.фаза. Кривые охлаждения 4 сплавов-1,2,3,4. Кривые охлаждения 1 и 2 полностью похожи на эвтектические.

Кривая охлаждения 3: в интервале t от t до t3 идет охлаждение жидкой фазы, и t изменяется монотонно. При t3 из жидкой фазы выпадают кристаллы тв.р-ра α, на кривой охлаждения – перегиб. В интервале t3-tP жидкая фаза меняет свой состав по линии t3Е,а тв.фаза по линии LG. Как только жидкая фаза достигнет состава P (перитектического), получает развитие перитектическая реакция. В результате этой реакции исчезает жидкая фаза и ниже tP наблюдается смесь 2 тв.фаз-тв.р-ров α и β.На кривой охлаждения наблюдается площадка, т.к. имеет место нонвариантное превращение:С=К-Ф+1=2-3+1=0.
Для сплава 4 при tP в результате перитектической реакции исчезает тв.р-ра α. В интервале tP –t’4 из жид.фазы выпадают кристаллы тв.р-ра β. От t’4 до t”4 происходит охлаждение тв.фазы β, а при t”4 тв.р-р β частично распадается-с выделением кристаллов тв.р-ра α.
