методичка по Общей фармакологии
.pdfЧерез слезные железы выводятся антибиотики и сульфаниламиды, что находит практическое применение в офтальмологии.
При грудном вскармливании необходимо учитывать выделение лекарственных средств молочными железами.
Молоко имеет слабокислую реакцию (рН 6,5-7,0), поэтому эпителий молочных желез более проницаем для лекарств основного характера.
Они могут накапливаться в молоке.
Соотношение концентраций в молоке и плазме для антибиотика со свойствами основания - эритромицина равно 7, а для антибиотика кислого характера - бензилпенициллина - только 0,2.
Проникновение лекарственных средств в молоко зависит также от их концентрации в плазме и степени связывания с белками.
Основной тип транспорта через эпителий молочных желез - простая диффузия.
Молоко представляет собой жировую эмульсию, поэтому растворимые в липидах лекарственные средства концентрируются в жировой фракции.
Прием многих лекарственных средств противопоказан при грудном вскармливании из-за опасности токсического действия на ребенка.
Кроме того, лекарства даже в малой концентрации в молоке могут вызывать у детей аллергические реакции.
ФАРМАКОДИНАМИКА
Фармакодинамика состоит из первичной и вторичной фармакологических реакций.
Первичная фармакологическая реакция - взаимодействие лекарственного средства с циторецептором.
Оно необходимо для развития вторичной фармакологической реакции, которая проявляется в виде изменений метаболизма и функций клеток.
Одна и та же первичная фармакологическая реакция может приводить к различным вторичным изменениям.
Например, активация α-адренорецепторов норэпинефрином вызывает расширение зрачков и сужение сосудов.
В основе одной и той же вторичной фармакологической реакции могут лежать различные первичные механизмы.
Так, спазм бронхов возникает при активации м-холинорецепторов ацетилхолином или H1-рецепторов гистамином.
ВЗАИМОДЕЙСТВИЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ С ЦИТОРЕЦЕПТОРАМИ
Циторецепторы (от греч. kytos - сосуд, клетка; лат. recipere - получать) - биомакромолекулы, генетически детерминированные для взаимодействия с биологически активными веществами, включая лекарственные средства.
Циторецепторы сформировались в процессе эволюции для взаимодействия с эндогенными лигандами: нейромедиаторами, гормонами, факторами роста, аутокоидами.
Большинство лекарственных средств взаимодействует с циторецепторами.
Нерецепторным механизмом действия обладают осмотические мочегонные средства, кровезаменители, комплексообразователи.
Циторецепторы имеют химическое строение липопротеинов, гликопротеинов, металлопротеинов, нуклеопротеинов.
Взаимодействие циторецепторов с ксенобиотиками возможно благодаря сходству стереохимической композиции лекарственных средств и биологически активных веществ организма.
Концепцию циторецепторов предложили Пауль Эрлих и Джон Ленгли в начале ХХ в. П. Эрлих считал, что функции рецепторов выполняют молекулярные боковые цепи клеточной протоплазмы, способные воспринимать питательные вещества и токсины.
Боковые цепи, циркулирующие в крови, образуют антитоксины (антитела).
Рецепторами являются также «крайние образования» чувствительных клеток.
Они превращают физическую или химическую энергию раздражения в возбуждение чувствительных нервов.
Дж. Ленгли установил, что яд кураре устраняет сокращение скелетных мышц, вызываемое никотином, но не изменяет возбуждающий эффект электрического тока.
Развитие радионуклидных методов в 1970-е годы позволило визуализировать циторецепторы и создать модели для их изучения.
Всовременной практике для идентификации циторецепторов используют методы молекулярной генетики и компьютерное моделирование.
Вструктуре циторецепторов присутствуют домен для связывания лигандов и эффекторный домен.
Активные (ортостерические) центры циторецепторов образованы функциональными группами аминокислот, фосфатидов, нуклеотидов, сахаров.
Лекарственные средства устанавливают с циторецепторами непрочные физикохимические связи: вандерваальсовы, ионные, водородные, дипольные по принципу комплементарности (активные группы лекарственного средства взаимодействуют с соответствующими группами активного центра циторецептора).
Необратимые ковалентные связи образуют лишь немногие вещества: фосфорорганические соединения, тяжелые металлы, цитостатики.
Все они токсичны.
По отношению к циторецепторам лекарственные средства обладают аффинитетом) (от лат. affinis - родственный) и внутренней активностью.
Аффинитет (сродство) рассматривают как способность образовывать комплекс с циторецептором.
Внутренняя активность направлена на создание активной стереоконформации рецептора, приводящей к появлению клеточного ответа.
В зависимости от выраженности аффинитета и наличия внутренней активности различают две группы лекарственных средств.
► Агонисты (от греч. agonistes - соперник, agonia - борьба), или миметики (от греч. mimeomai - подражать), - лекарственные средства с умеренным аффинитетом и высокой внутренней активностью.
Полные агонисты вызывают максимально возможный клеточный ответ, частичные (парциальные) агонисты - менее выраженную клеточную реакцию.
► Антагонисты (от греч. antagonisma - соперничество, anti - против, agonia -
борьба), или блокаторы, - лекарственные средства с высоким аффинитетом, но лишенные внутренней активности.
Они экранируют циторецепторы от действия эндогенных лигандов, усиливают эффекты других, неблокированных циторецепторов.
Лекарственные средства, блокирующие активные центры циторецепторов, являются конкурентными антагонистами.
Возможно сочетание в фармакодинамике одного лекарственного средства свойств агониста и антагониста.
Агонисты-антагонисты активируют одни циторецепторы и блокируют другие.
Эндобиотики являются только агонистами, ксенобиотики могут как активировать, так и блокировать циторецепторы.
Циторецепторы активируются в начальный момент взаимодействия с лекарственными средствами.
Для агонистов характерна высокая константа диссоциации комплекса лекарствоциторецептор.
Комплекс агониста с циторецептором неустойчив, и после диссоциации молекула лекарственного средства может повторно активировать циторецепторы.
Антагонисты обладают высоким аффинитетом и более продолжительно связываются с циторецепторами.
В первый момент взаимодействия они могут активировать циторецепторы, после чего наступает длительный период блокирования.
Лекарственные средства присоединяются также к аллостерическим центрам циторецепторов, что модифицирует структуру активного центра и изменяет его реакцию на лекарства или эндогенные лиганды.
В зависимости от направленности этих изменений, аллостерические центры могут быть позитивными и негативными.
Пример позитивного аллостерического центра - бензодиазепиновый рецептор, повышающий аффинитет ГАМКА-рецептора к гамма-аминомасляной кислоте (ГАМК).
Негативный аллостерический центр - участок связывания пикротоксина на ГАМКА- рецепторе, уменьшающий эффекты ГАМК.
На мембране одной и той же клетки могут присутствовать более 20 типов циторецепторов с различным функциональным значением.
Клеточный ответ на активацию различных циторецепторов является алгебраической суммой вызываемых ими независимых реакций.
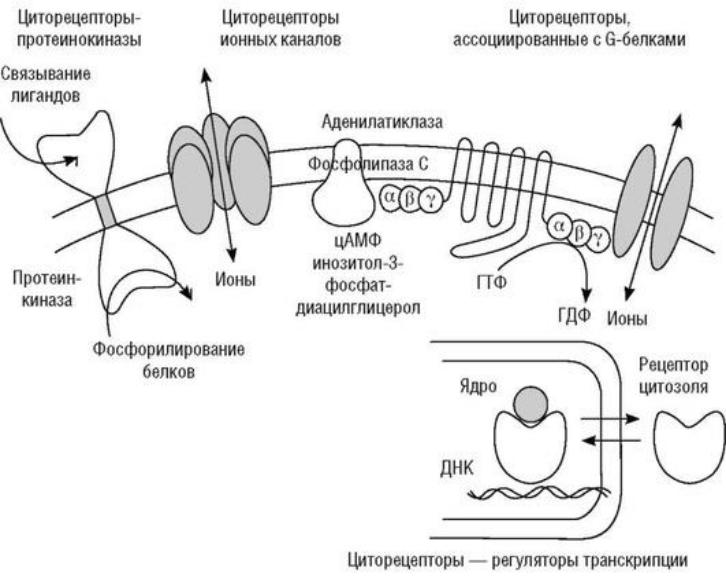
Функционирует четыре основных типа циторецепторов (рис. 5.1):
►рецепторы, ассоциированные с ионными каналами;
►рецепторы-протеинкиназы;
►рецепторы, ассоциированные с G-белками;
►рецепторы - регуляторы транскрипции.
Рис. 5.1. Циторецепторы: цАМФ - циклический аденозинмонофосфат; ГТФ - гуанозин-3-фосфат; ГДФ - гуанозиндифосфат; ДНК - дизоксирибонуклеиновая кислота
Циторецепторы ионных каналов получили название ионотропных, цито- рецепторы-протеинкиназы и ассоциированные с G-белками являются метаботропными.
Циторецепторы, ассоциированные с ионными каналами
Циторецепторы, расположенные в воротах ионных каналов, увеличивают проницаемость мембран для Na+, K+, Ca2+ и Cl-.
При действии лигандов на такие рецепторы возникает мгновенный клеточный ответ в виде деполяризации или гиперполяризации мембран.
►Рецепторы, вызывающие деполяризацию мембран и активацию функций клеток (увеличивают проницаемость для Na+, K+ и Ca2+): н-холинорецепторы, некоторые рецепторы глутаминовой кислоты, 5-НТ3-рецепторы, пуриновые рецепторы Р2Х.
►Рецепторы, вызывающие гиперполяризацию и торможение функций клеток (увеличивают проницаемость для Cl-): ГАМКА-рецепторы и рецепторы глицина.
Циторецепторы-протеинкиназы
Циторецепторы-протеинкиназы связаны с плазматической мембраной клеток.
Они имеют внеклеточный домен для взаимодействия с лигандами и внутриклеточный каталитический домен - протеинкиназу.
Оба домена соединены внутримембранной аминокислотной цепью.
Рецепторы-протеинкиназы фосфорилируют белки клеток: киназы, регуляторные и структурные белки.
Чаще всего фосфат присоединяется к остаткам тирозина белков-мишеней.
Примеры циторецепторов-протеинкиназ: рецепторы инсулина, цитокинов, эпидермального и тромбоцитарного факторов роста.
Циторецепторы, ассоциированные с G-белками
Это группа интегральных мембранных белков с характерной вторичной структурой: семь трансмембранных доменов соединены тремя внеклеточными и тремя внутриклеточными петлями.
N-конец рецептора расположен на внеклеточной поверхности мембраны, C-конец - на внутриклеточной поверхности.
Внеклеточные петли выполняют регуляторную функцию - отвечают за распознавание и связывание лигандов.
G-белки передают информацию от внеклеточного регуляторного домена к эффекторной системе, используя энергию гуанозинтрифосфата (ГТФ).
G-белки имеют строение тримеров и состоят из α-, β- и γ-субъединиц.
Когда α-субъединица связывается с молекулой ГТФ, G-тример диссоциирует на βγсубъединицу и комплекс α-ГТФ.
Диссоциированные субъединицы активируют или ингибируют эффекторные системы клеток.
Эффекторные системы представлены аденилатциклазой, фосфолипазами A2, C и D, белками ионных каналов, транспортными белками.
При активации ферментов образуются внутриклеточные биологически активные вещества - вторичные мессенджеры (от англ. messenger - вестник, посредник).
Они запускают каскад биохимических и функциональных изменений в клетке.
Аденилатциклаза превращает аденозинтрифосфат (АТФ) во вторичный мессенджер - циклический аденозинмонофосфат (цАМФ).
Рецепторы, ассоциированные с аденилатциклазой, могут ее активировать (Rs) или ингибировать (Ri).
При активации циторецепторов количество внутриклеточного цАМФ примерно в 100 раз превышает количество агониста, что обеспечивает мощный фармакологический ответ («эффект домино»).
Аденилатциклазу активируют:
►β-адренорецепторы;
►D-рецепторы 1-го и 5-го типа;
►5-НТ-рецепторы 4, 5, 7-го типа;
►Н2-рецепторы;
►пуриновые А2-рецепторы (рецепторы аденозина);
►V2-рецепторы (рецепторы вазопрессина).
Примеры рецепторов-ингибиторов:
►α2-адренорецепторы;
►D2-рецепторы;
►5-НТ-рецепторы 1-го и 5-го типа;
►м-холинорецепторы 2-го и 4-го типа;
►пуриновые рецепторы A1 и Р2Y12;
►опиоидные рецепторы.
Фосфолипаза С катализирует гидролиз фосфатидилинозитолдифосфата.
Этот минорный фосфолипид клеточных мембран представляет собой эфир шестиатомного спирта инозитола с диацилглицеролом (ДАГ), имеющим два остатка жирных кислот (одна из них - арахидоновая кислота).
Продукты реакции - вторичные мессенджеры инозитол-3-фосфат (ИФ3) и ДАГ.
Одна молекула ИФ3 способствует выделению 20 ионов кальция из ЭПР.
В гладких мышцах ионы кальция связываются с кальмодулином, затем комплекс Са2+-кальмодулин активирует киназу легких цепей миозина.
Фосфорилированные легкие цепи миозина связываются с актином с образованием актомиозина и последующим сокращением гладких мышц.
Протеинкиназу С и Са2+-кальмодулинзависимую протеинкиназу II активирует ДАГ.
Протеинкиназа С, фосфорилируя ферменты, белки ионных каналов и транспортные системы, стимулирует рост и деление клеток, выделение нейромедиаторов и гормонов.
С фосфолипазой С связаны следующие рецепторы:
►α1-адренорецепторы;
►5-НТ2-рецепторы;
►м-холинорецепторы 1-го и 3-го типа;
►Н1-рецепторы;
►V1-рецепторы;
►АТ1-рецепторы;
►рецепторы окситоцина;
►CCK-рецепторы (рецепторы холецистокинина).
Фосфолипаза А2 участвует в гидролизе фосфатидилхолина с высвобождением арахидоновой кислоты - субстрата для синтеза простагландинов, тромбоксанов, простациклина, лейкотриенов.
Фосфолипаза D отщепляет от фосфатидилхолина фосфатидную кислоту.
Эта кислота мобилизует ионы кальция из ЭПР, затем превращается в ДАГ.
Циторецепторы - регуляторы транскрипции
Циторецепторы - регуляторы транскрипции взаимодействуют с тиреоидными, стероидными гормонами, витамином D и ретиноидами.
Транспортные белки плазмы передают лиганды клеточным белкам, затем комплексы поступают в ядро.
Функции таких рецепторов - активация или ингибирование транскрипции генов.
Известны и другие типы циторецепторов.
Например, рецепторы предсердного натрийуретического пептида, ассоциированные с гуанилатциклазой, повышают продукцию вторичного мессенджера - циклического гуанозинмонофосфата (цГМФ).
Рецепторную функцию выполняют также мембраносвязанные и растворимые ферменты:
-дигидрофолатредуктаза,
-ацетилхолинэстераза,
-моноаминоксидаза (МАО),
-циклооксигеназа (ЦОГ),
-Na+,К+-зависимая аденозинтрифосфатаза (АТФаза).
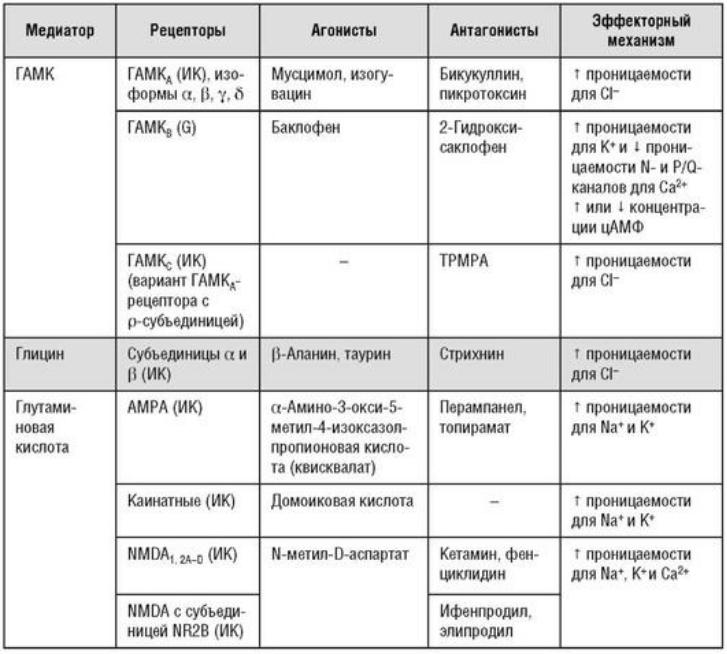
Основные циторецепторы, их агонисты, антагонисты и механизмы функционирования представлены в табл. 5.1.
Таблица 5.1. Циторецепторы