
методичка по Общей фармакологии
.pdfЭЛИМИНАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ. БИОТРАНСФОРМАЦИЯ.
Элиминация (от лат. elimino, eliminatum - выносить за порог, удалять) - удаление лекарственных средств из организма в результате биотрансформации и экскреции.
Лекарственные средства элиминируются только из центральной камеры.
Лекарства, находящиеся в периферической камере, предварительно транспортируются в центральную камеру и только потом подвергаются элиминации.
Лекарственные средства элиминируются из плазмы согласно экспоненциальной кинетике первого порядка: выводится постоянная доля вещества за единицу времени.
Элиминацию лекарственных средств характеризуют рядом фармакокинетических параметров:
►константа скорости элиминации - доля лекарственного средства, удаляемая за единицу времени (измеряется в процентах);
►период полуэлиминации - время, за которое концентрация лекарственного средства в плазме уменьшается наполовину (Т1/2);
►клиренс (от англ. clearance - очищение) - объем жидких сред организма, освобождающихся от лекарственного средства в результате биотрансформации и экскреции (измеряют в мл/мин на килограмм массы тела).
Различают печеночный (метаболический, желчный) и почечный клиренс.
Метаболический клиренс зависит от состояния ферментных систем печени и интенсивности печеночного кровотока.
Для элиминации местного анестетика лидокаина с быстрым метаболизмом в печени основное значение имеет печеночный кровоток, для элиминации антипсихотических средств группы фенотиазина - активность ферментных систем детоксикации.
При повторном применении лекарственных средств в биофазе циторецепторов создается равновесное состояние, когда количество поступающего вещества равно количеству элиминируемого.
При равновесном состоянии концентрация лекарственного средства колеблется в небольших пределах, а фармакологические эффекты проявляются в полной мере.
Обычно равновесное состояние наступает через 3-5 периодов полуэлиминации.
Биотрансформация лекарственных средств
Биотрансформация представляет собой метаболические превращения лекарственных средств.
В большинстве реакций образуются метаболиты, более полярные, чем исходные лекарственные средства.
Полярные метаболиты хуже растворяются в липидах, но обладают хорошей растворимостью в воде, а значит, в меньшей мере подвергаются энтерогепатической циркуляции (выведению с желчью в кишечник и повторному всасыванию в кровь) и реабсорбции в почечных канальцах.
Без биотрансформации одна терапевтическая доза снотворного средства фенобарбитала могла бы находиться в организме 100 лет.
Эндобиотики подвергаются превращениям под влиянием специфических ферментов, осуществляющих метаболизм их эндогенных аналогов.
Ксенобиотики используют для метаболизма ферменты с малой субстратной специфичностью, например, окисляются при участии цитохрома Р450.
Предшественник цитохрома Р450 появился у бактерий в протерозое примерно 1,5 млрд лет назад.
После расхождения путей эволюции растений и животных около 1,2 млрд лет назад у животных появились изоферменты 3 и 4 цитохрома Р450 для обезвреживания токсических веществ растений.
Выход живых существ из моря на сушу в девоне около 400 млн лет назад сопровождался возникновением большого числа новых видов растений, часть которых образовывала неизвестные ранее токсические продукты.
У животных для безопасного питания этими растениями сформировались изоферменты цитохрома Р450 1 и 2.
Биотрансформация ксенобиотиков происходит в печени (90-95%), слизистой оболочке тонкой кишки, почках, легких, надпочечниках, коже, крови.

Наиболее изучены процессы биотрансформации на мембранах гладкого эндоплазматического ретикулума (ЭПР) печени.
При гомогенизации и ультрацентрифугировании клеток канальцы ЭПР разрываются и превращаются в функционально активные фрагменты - микросомы.
Реакции биотрансформации протекают также в ядре, цитозоле, митохондриях, на плазматической мембране.
Процессы биотрансформации разделяют на две фазы.
В реакциях первой фазы - метаболической трансформации -
лекарственные средства подвергаются окислению, восстановлению или гидролизу.
В их молекулы включаются полярные группы кислого (гидроксил, карбонил, оксогруппа, карбоксил, тиоловая группа) и основного (аминогруппа) характера.
Большинство лекарственных средств преобразуется в неактивные метаболиты, но также могут появляться активные и токсические производные (табл. 3.1).
Таблица 3.1. Активные метаболиты лекарственных средств
Лекарственное средство |
Активный метаболит |
Прокаинамид |
N-ацетилпрокаинамид |
Пропранолол |
Гидроксипропранолол |
Хлордиазепоксид |
Деметилхлордиазепоксид, нордазепам, |
|
оксазепам |
Диазепам |
Нордазепам,оксазепам |
Имипрамин |
Дезипрамин |
Амитриптилин |
Нортриптилин |
Теофиллин |
Кофеин |
Кодеин |
Морфин |
Ацетилсалициловая кислота |
Салициловая кислота |
Фенилбутазон |
Оксифенилбутазон |
Метилдопа |
Метилнорэпинефрин |
Спиронолактон |
Канренон |
В редких случаях изменяется характер фармакологической активности.
Благодаря этому явлению был открыт один из первых антидепрессантов - ипрониазид.
Изначально ипрониазид использовали как противотуберкулезное средство, но потом обнаружили, что он оказывает тимоаналептическое действие (улучшает настроение) при депрессии.
В реакции деалкилирования ипрониазид превращается в изониазид, используемый только как противотуберкулезное средство.
Во второй фазе - реакциях конъюгации - к лекарственным средствам присоединяются ковалентной связью полярные фрагменты с образованием неактивных продуктов.
Для активации полярных фрагментов необходима затрата энергии.
Реакции метаболической трансформации
Окисление
ВЭПР функционируют дыхательные цепи, зависимые от никотинамидадениндинуклеотидфосфата (НАДФ) и никотинамидадениндинуклеотида (НАД).
ВНАДФ-зависимой системе терминальным переносчиком электронов служит цитохром Р-50 - мембраносвязанный липофильный фермент группы многоцелевых монооксигеназ.
Монооксигеназы включают кислород в окисляемые субстраты.
Цитохром P450 имеет строение гемопротеина: состоит из глобулярного белка и железопротопорфиринового комплекса (атом железа в степени окисления +3, порфириновый макроцикл, осевые лиганды).
Буква Р в названии - первая буква слова «пигмент», число 450 означает, что восстановленный, связанный с оксидом углерода цитохром наиболее активно поглощает излучение с длиной волны 450 нм.
Цитохром Р450 глубоко погружен в липидный бислой мембраны ЭПР и функционирует совместно с НАДФ-зависимой цитохром P450-редуктазой.
Соотношение количества молекул цитохрома Р450 и редуктазы составляет 10:1.
Активные центры этих ферментов ориентированы на цитоплазматическую поверхность ЭПР.
Цикл окисления лекарственных средств при участии цитохрома Р450 состоит из следующих реакций (рис. 3.1):
►окисленный цитохром Р450 соединяется с лекарственным средством;
►цитохром восстанавливается электроном НАДФН, реакцию катализирует цитохром Р450-редуктаза;
►восстановленный цитохром связывается с молекулярным (триплетным) кислородом;
►кислород активируется электроном НАДФН, триплетный кислород становится синглетным;
►на финальном этапе один атом кислорода включается в молекулу окисляемого лекарственного средства, второй - в молекулу воды;
►цитохром Р450 регенерирует в исходную окисленную форму.
НАД-зависимая дыхательная цепь включает цитохром b5, НАДН-цитохром Ь5- редуктазу и стероил-КоА-десатуразу (коэнзим А).
Гемсодержащий фермент цитохром b5 состоит из глобулярного цитозольного домена, связанного с редуктазой, и короткой спирализованной гидрофобной цепи, погруженной в мембрану ЭПР.
Электроны от НАДН переносятся редуктазой на окисленный атом железа цитохрома b5.
Стероил-КоА-десатураза катализирует образование двойных связей в жирных кислотах.
Суперсемейство цитохромов Р450 поражает своими почти неограниченными метаболическими возможностями.
Оно включает более 1000 клонированных вариантов, способных катализировать около 60 типов ферментативных реакций с тысячами субстратов как эндогенных (стероиды, жирные кислоты, простагландины, лейкотриены, цитокины, биогенные амины), так и ксенобиотиков.
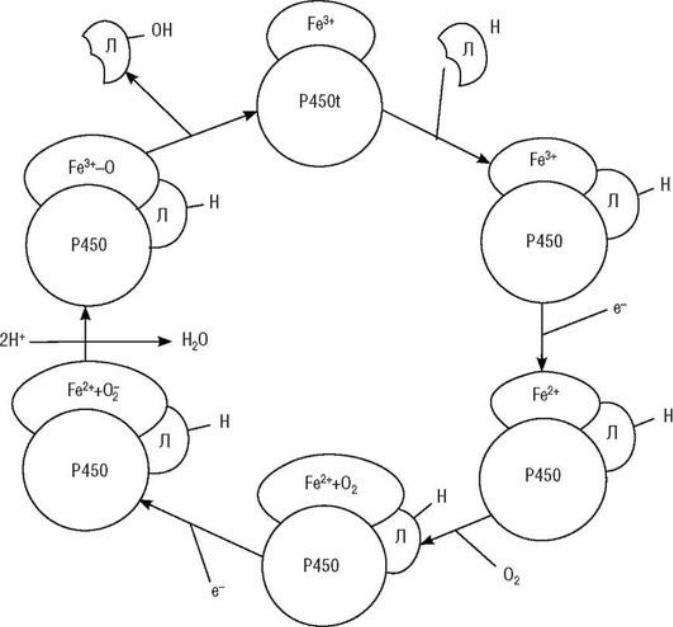
Рис. 3.1. Механизм окисления лекарственных средств при участии цитохрома Р450 В клетках человека обнаружено 18 семейств цитохрома Р450, разделенных на 44 подсемейства.
Названия изоферментов цитохрома Р450 обозначают символом CYP, первая цифра означает семейство, затем следует латинская буква, указывающая подсемейство, последняя цифра соответствует конкретному полипептиду.
В молекулах изоферментов одного семейства идентичны более 40% аминокислот, в молекулах одного подсемейства - более 55%.
Метод фенотипирования позволяет установить субстратную специфичность изоферментов цитохрома Р450 по соотношению концентраций неизмененного вещества и его метаболитов в крови.
Методом генотипирования с помощью полимеразной цепной реакции изоферменты идентифицируют по их генам, так как каждый изофермент кодируется одним из 53 генов, локализованных в разных локусах хромосом.
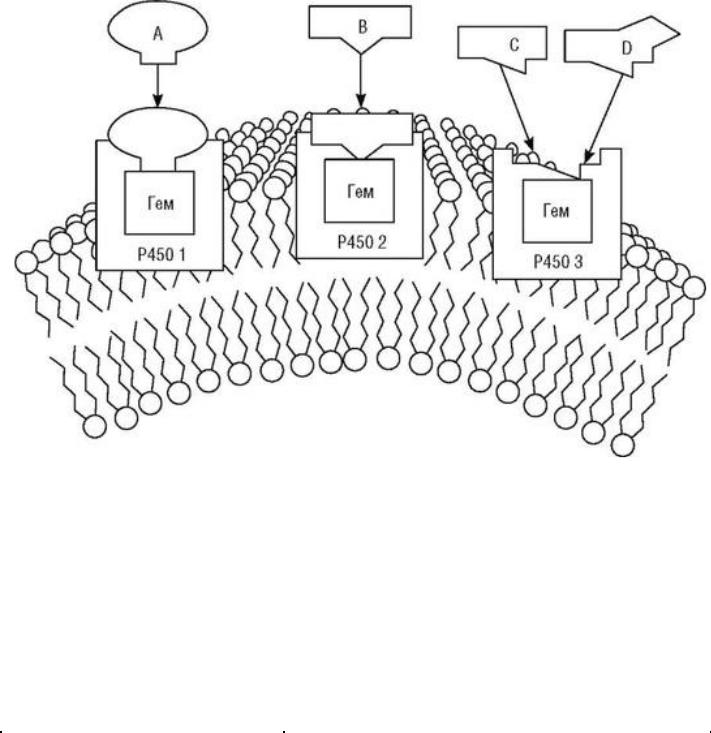
Большинство реакций катализируют изоферменты цитохрома Р450 семейств 1, 2 и 3 (рис. 3.2, табл. 3.2).
Рис. 3.2. Изоферменты цитохрома Р450
Таблица 3.2. Участие изоферментов |
цитохрома Р450 в метаболизме |
||
лекарственных средств |
|
|
|
Изофермент |
|
Доля в метаболизме, % |
|
CYP3A4 |
|
40 |
|
CYP2D6 |
|
20 |
|
CYP2C9 |
|
18 |
|
CYP1A2 |
|
12 |
|
CYP2C19 |
|
10 |
|
Реакции окисления, катализируемые цитохромом Р450, могут расщепляться с образованием свободных радикалов кислорода и токсических промежуточных продуктов (эпоксидов, N-, S-оксидов, альдегидов).
Свободные радикалы и активные интермедиаты, инициируя перекисное окисление мембранных липидов, вызывают некроз клеток, мутации, тератогенный и эмбриотоксический эффекты, способствуют появлению неоантигенов, провоцируют канцерогенез и ускоряют старение.
По этой причине не существует абсолютно безвредных ксенобиотиков.
Токсические продукты биотрансформации обезвреживаются конъюгацией с восстановленным глутатионом и ковалентным связыванием с альбуминами.
Повреждение молекулы альбумина неопасно, так как этот белок синтезируется в печени в количестве 10-16 г в день и присутствует в высоких концентрациях в ЭПР.
Ксенобиотики в процессе окисления могут разрушать цитохром Р450.
Такие вещества получили название «суицидные субстраты».
Свойствами суицидных субстратов обладают четыреххлористый углерод, галотан и парацетамол, преобразуемые цитохромом Р450 в свободные радикалы.
Эффект этих веществ можно рассматривать не только как токсический, но и как протективный: под их влиянием элиминируются молекулы цитохрома Р450, генерирующие реакционноспособные метаболиты.
Восстановление.
Восстанавливаются альдегиды, кетоны и карбоновые кислоты.
Ароматические соединения, содержащие нитрогруппу, подвергаются в анаэробных условиях нитроредукции.
Промежуточные продукты этой реакции - нитрозо-и гидроксиламиносоединения. В печени функционируют микросомальная и цитоплазматическая нитроредуктазы, в кишечнике - бактериальная нитроредуктаза.
Лекарственные средства с азогруппой восстанавливаются в первичные амины в микросомах печени и кишечной микрофлорой; например, сульфасалазин, применяемый для лечения язвенного колита, ферментом микрофлоры кишечника расщепляется по азосвязи с образованием сульфапиридина и 5-аминосалициловой кислоты.
Гидролиз.
Гидролиз необходим для биотрансформации лекарственных средств, имеющих строение сложных эфиров и замещенных амидов.
Реакции гидролиза протекают в цитозоле и ЭПР гепатоцитов и эпителия кишечника, а также в крови при участии эстераз и амидаз.
При гидролизе молекулы лекарственных средств распадаются на фрагменты, которые могут (чаще только один из фрагментов) проявлять фармакологическую активность.
В медицинской практике применяют пролекарства, активируемые гидролазами.
Блокаторы АТ1-рецепторов ангиотензина II олмесартана медоксомил и азилсартана медоксомил в кишечнике гидролизуются с образованием соответственно олмесартана и азилсартана.
Антикоагулянт непрямого действия дабигатрана этексилат при участии карбоксиэстераз плазмы и печени гидролизуется в активный дабигатран.
Реакции конъюгации
Из всех реакций конъюгации наибольшее значение имеет глюкуронирование - присоединение активированной уридиндифосфатом (УДФ) глюкуроновой кислоты к алифатическим, ароматическим спиртам, карбоновым кислотам, веществам с аминогруппой и сульфгидрильной группой.
Глюкуронирование катализирует УДФ-глюкуронилтрансфераза.
Этот фермент функционирует в ЭПР и цитозоле клеток печени, почек, кишечника, кожи.
Семейство глюкуронилтрансфераз включает более 20 изоферментов.
O-, N- и S-глюкурониды хорошо растворяются в воде и экскретируются с мочой и желчью.
После экскреции с желчью глюкурониды под влиянием β-глюкуронидазы кишечных бактерий превращаются в исходные липофильные вещества, затем всасываются в кровь, что дает начало энтерогепатической циркуляции.
В энтерогепатическую циркуляцию вовлекаются стероидные гормоны, дигоксин, хлорамфеникол.
Сульфатирование - перенос неорганического сульфата с З'-фосфоаденозил- 5'-фосфосульфата на гидроксильную группу алифатических спиртов и фенолов при участии цитозольного фермента сульфотрансферазы.
Некоторые лекарственные средства в малых дозах образуют сульфоконъюгаты, в больших дозах - глюкурониды.
При ацетилировании ацетилрадикал переносится с коэнзима А (КоА) на молекулы аминов, гидразинов, сульфаниламидов.
Реакцию катализирует ацетилтрансфераза цитозоля клеток.
Ацетилированные метаболиты плохо растворяются в воде и медленно элиминируются.
Метилирование - перенос метила с S-аденозилметионина на лекарственное средство при участии метилтрансферазы.
Это единственная реакция конъюгации, в которой не образуются полярные метаболиты.
В реакциях конъюгации могут образовываться токсические метаболиты: N- сульфоэфиры, N-ацетоксиариламины.
Они алкилируют ДНК и вызывают мутагенез и канцерогенез.
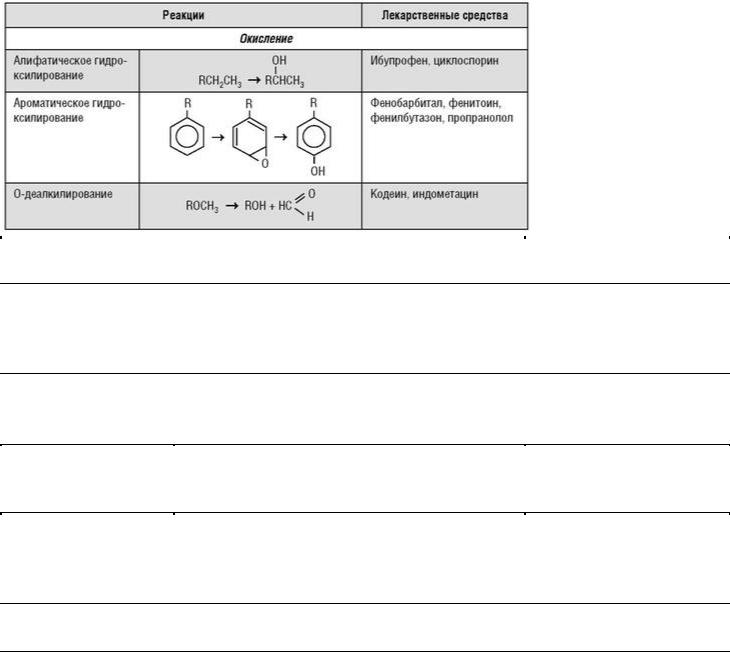
Примеры реакций биотрансформации ксенобиотиков приведены в табл. З.З.
Таблица 3.3. Реакции биотрансформации ксенобиотиков
Реакции |
|
|
|
Лекарственные |
|
|
|
|
|
средства |
|
N- |
|
RNHCH3 -» RNH2 + HCf |
|
Морфин, |
кодеин, |
деалкилирование |
|
|
|
диазепам, |
имипрамин, |
|
|
|
|
теофиллин, |
|
|
|
|
|
эритромицин |
|
Окислительное |
|
2RCH2 3 x2NHH2-» NH3 + HCf |
|
Норэпинефрин, |
|
дезаминирование |
|
H |
|
эпинефрин, диазепам |
|
Восстановление |
|
|
|
|
|
Восстановление |
|
ООН Il I R1CR2-»? R1CHR2 |
|
Варфарин |
|
|
|
|
|||
альдегидов, |
|
|
|
|
|
кетонов, кислот |
|
|
|
|
|
Нитроредукция |
|
RNO2-»? RNH2 |
|
Нитразепам, |
|
|
|
|
|
хлорамфеникол, |
|
|
|
|
|
нитрофураны, |
|
|
|
|
|
метронидазол |
|
Азоредукция |
|
R1N = NR2-» R1NH2 + R2NH2 |
|
Сульфасалазин |
|
Гидролиз |
|
|
|
|
|
Гидролиз эфиров |
|
О Il |
|
Ацетилсалициловая |
|
|
|
||||
|
|
R1COR2-»? R1COOH + R2OH |
|
кислота, |
прокаин, |
|
|
|
|
суксаметония йодид |
|
