
Болезни / 17_TELA
.docx17. ТЭЛА. Классификация. Этиология. Факторы, категории риска. Патогенез. Клиника. Принципы диагностики и лечения.
Тромбоэмболия легочной артерии (ТЭЛА) – острое, часто рецидивирующее состояние, связанное с эмболией ветвей легочной артерии различного калибра тромботическими массами. Сопровождается повышением давления в легочной артерии, нарушением газообмена и перегрузкой правых отделов сердца.
Тромбоэмболия лёгочной артерии (ТЭЛА) — это окклюзия просвета основного ствола или ветвей легочной артерии тромботическими массами, сформировавшимися в венах большого круга или полостях правого сердца, переносимыми в малый круг кровообращения с током крови.
Классификация ТЭЛА:
Массивная ТЭЛА – эмболическое поражение легочного ствола и главных легочных артерий (окклюзия более половины артериального русла) – обструкция более 50% сосудистого русла легочной артерии;
Субмассивная ТЭЛА – окклюзия нескольких долевых или многих сегментарных легочных артерий (30-50% артериального русла) – окклюзия менее 50% объема сосудистого русла легочной артерии;
Немассивная ТЭЛА – тромбоэмболия мелких ветвей легочной артерии – окклюзия менее 25% объема сосудистого русла легочной артерии.
Классификация по локализации:
Уровень эмболической окклюзии:
сегментарные артерии,
долевые и промежуточные артерии,
главные ЛА и главный легочный ствол.
Сторона поражения:
левая,
правая,
двусторонняя ТЭЛА.
Варианты течения ТЭЛА по Теодори:
молниеносное (синкопильное) течение – от нескольких минут до 30 минут;
острое (быстрое) течение – от нескольких часов до нескольких дней (максимально 3-5);
подострое (замедленное) течение – от одной до нескольких недель;
хроническое рецидивирующее течение.
Клиническая классификация и начальная стратификация риска (ESC):
высокий риск – имеется наличие шока или артериальной гипотонии на фоне подтвержденной или подозреваемой ТЭЛА;
невысокий риск – нет шока и артериальной гипотонии на фоне подтвержденной или подозреваемой ТЭЛА.
Этиология:
Из лекции: тромбоз глубоких вен нижних конечностей; гиподинамия (работа и перелеты – ведет к тромбозу глубоких вен нижних конечностей); использование КОК (например, у человека есть тромбофилия, а в КОК есть прогестерон, который обладает способностью свертывания и повышения риска тромбоза).
В зависимости от выявдяемых факторов риска и потенциальных причин ТЭЛА, выделяют формы:
первичная – есть наследственные предрасполагающие факторы;
вторичная – есть приобретенные предрасполагающие факторы;
идиопатическая – нет выявляемых предрасполагающих факторов.
Основной причиной возникновения ТЭЛА является тромбоз любой локализации, который чаще образуется в бассейне нижней полой вены: подколенно-бедренный или илиокавальный сегмент, дистальные отделы глубоких вен, большая и малая подкожные вены бедра. Также источником тромба может быть правое предсердие, при наличии эндокардита, мерцательной аритмии, дилатации и бассейн верхней полой вены, чаще при постановке венозных катетеров.
К наследственным факторам относят генетически-обусловленное нарушение системы гемостаза: лейденская мутация (мутация V фактора свертывания), мутация гена протромбина, недостаточность протеина S и C, недостаточность антитромбина III.
Факторы риска:
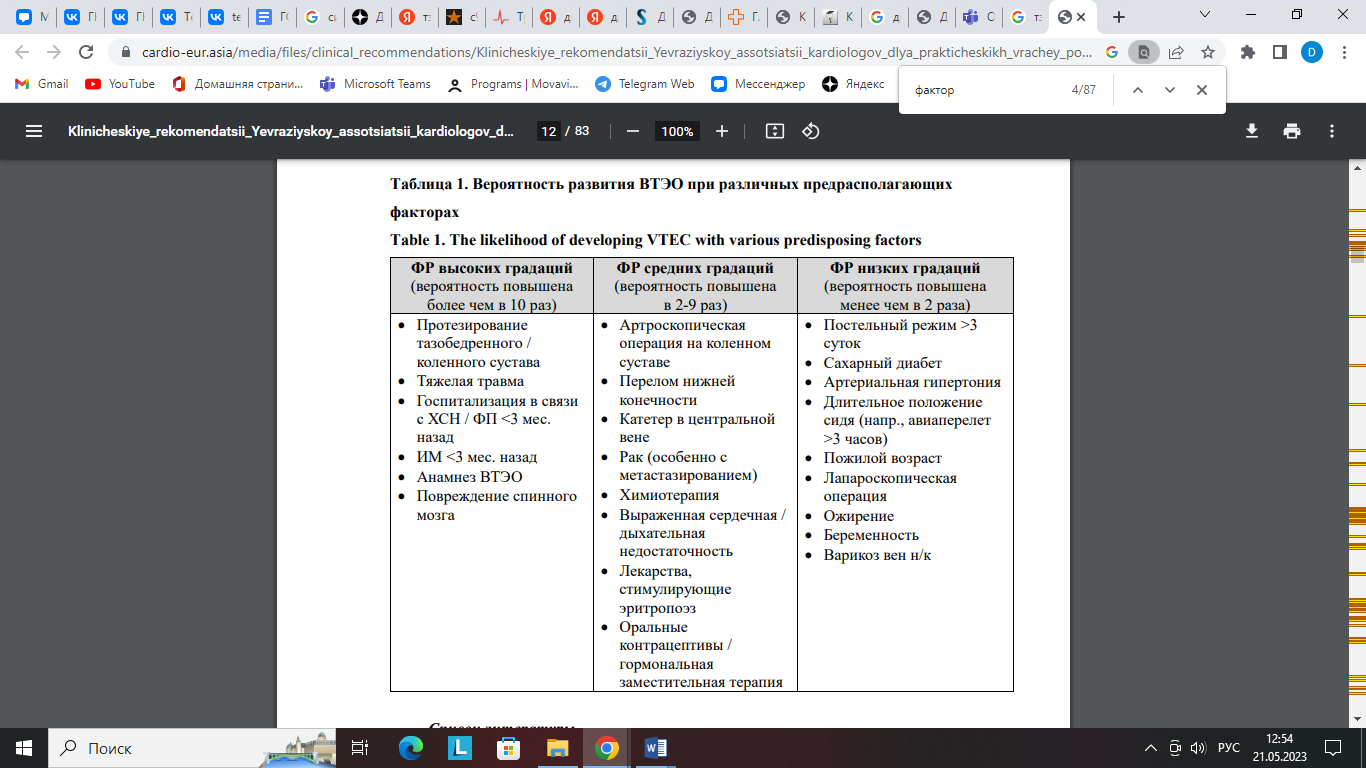
Категории риска:
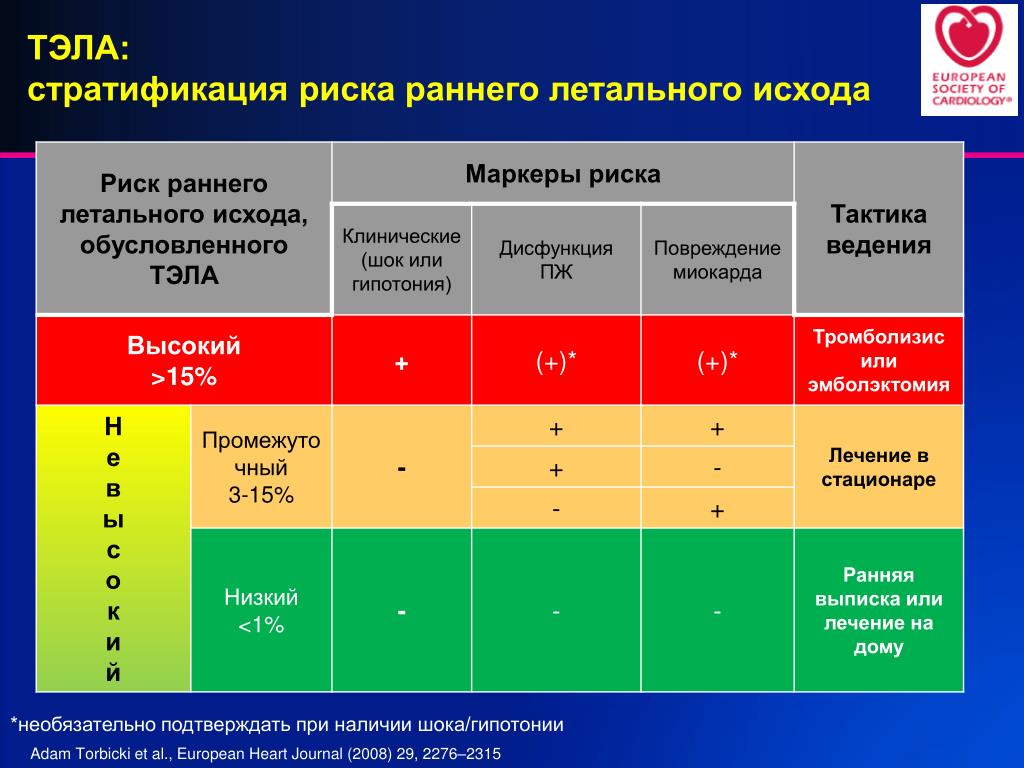
Патогенез:
Образование тромбоза любой локализации определяется триадой Вирхова:
Повреждение эндотелия – при его повреждении выделяются факторы свертывания и угнетается выработка фибринолитических веществ;
Изменение скорости кровообращения – в участках с замедленным кровотоком тромбы образуются чаще;
Изменение реологических свойств крови – изменение состава крови, дисбаланс свертывающей и противосвёртывающей систем способствуют адгезии и агрегации тромбоцитов и запускают дальнейший каскад реакций коагуляционного гемостаза.
Тромботическая окклюзия более 30-50% артериального русла легких ведет к повышению сосудистого сопротивления и увеличению нагрузки на правый желудочек. При очень массивной или множественной ТЭЛА сосудистое сопротивление в легочной системе возрастает до уровня, который не может быть преодолен силой сокращения ПЖ, что ведет к перегрузке и дилатации правых отделов сердца и, как следствие, остановке кровообращения и внезапной смерти при сохранной электрической активности сердца.
В менее тяжелых случаях кровоток в МКК сохраняется, но резко уменьшается объем крови, притекающей к ЛЖ, что ведет к снижению сердечного выброса и развитию обструктивного шока. Также нарушение функции желудочков усугубляет снижение коронарной перфузии вследствие снижения давления в аорте.
Развитию шока препятствует активация симпато-адреналовой системы, вызывающая увеличение сердечного выброса и вазоконстрикцию, что сопровождается повышением системного АД и давления в ЛА. При этом среднее давление в ЛА, которое способен создать тонкостенный ПЖ, не превышает 40 мм рт.ст.
Дыхательная недостаточность при ТЭЛА является следствием гемодинамических нарушений:
при снижении сердечного выброса уменьшается протекающей через легкие крови, а значит и количество кислорода, которое она способна принять;
в легких появляются зоны сниженного кровотока и зоны переполненного капиллярного русла, снабжаемые открытыми сосудами, что приводит к вентиляционно-перфузионным нарушениям и гипоксии.
ТЭ мелких ветвей ЛА не вызывает серьезного нарушения гемодинамики, но вследствие прекращения кровотока в легочных капиллярах нарушается микроциркуляция в капиллярном русле бронхиальных артерий, что ведет к развитию геморрагического инфаркта. Влияние геморрагического инфаркта на газообмен обычно невелико, за исключением пациентов, страдающих сердечно-легочными заболеваниями.

Клиника:
Клинические проявления крайне неспецифичны и вариабельны. Может быть полное отсутствие симптомов, немая эмболия, а может иметь место и быстро развивающееся состояние острой сердечно-легочной недостаточности, которое в течение нескольких минут может привести к смерти.
В 90% случаев: внезапно появившееся одышка, боль за грудиной, гипотензия и потеря сознания. В ряде случаев с первых часов появляется лихорадка, связанная с выбросом в кровь БАВ.
Диспноэ – внезапная одышка без наличия других причин, зачастую становится основным и единственным клиническим проявлением ТЭЛА. Одышка инспираторного характера, не сопровождается изменением аускультативно картины в легких, не усиливается в горизонтальном положении тела (нет ортопноэ).
Синкопе (обморок) – указывает на тяжелые гемодинамические нарушения.
Боль в груди – частый симптом ТЭЛА, который связан с раздражением плевры ввиду дистальной эмболизации и инфарктом легкого. В большинстве случаев это острая кинжальная боль, но может иметь и типичный ангинозный вид ввиду острой ПЖ недостаточности.
Эмболия основного легочного ствола артерии характеризуется раздирающими загрудинными болями. При инфаркте легкого отмечаются острые, резкие боли в грудной клетке, усиливающиеся при дыхании и кашле.
В результате эмболии ЛА развивается легочное сердце:
набухание шейных вен, повышение ЦВД;
патологическая пульсация в эпигастральной области и во 2 межреберье слева от грудины;
расширение правой границы сердца;
акцент и раздвоение 2 тона над ЛА;
болезненное набухание печени и положительный симптом Плеша (увеличение набухания шейных вен при надавливании на печень).
Есть смысл проводить синдромальную диагностику:
Кардиальный синдром:
острая недостаточность кровообращения;
обструктивный шок;
синдром острого легочного сердца;
кардиальная боль;
тахикардия.
Синдром ОДН:
одышка;
цианоз в сочетании с бледностью кожных покровов;
кашель, иногда с мокротой;
кровохарканье ?;
ослабленное дыхание на стороне поражения при аускультации.
Церебральный синдром:
потеря сознания или эйфория;
гемиплегия (паралич половины тела);
судороги (вследствие гипоксии).
Абдоминальный синдром:
боль в различных отделах живота;
икота, тошнота, рвота;
парез кишечника, нарушение стула.
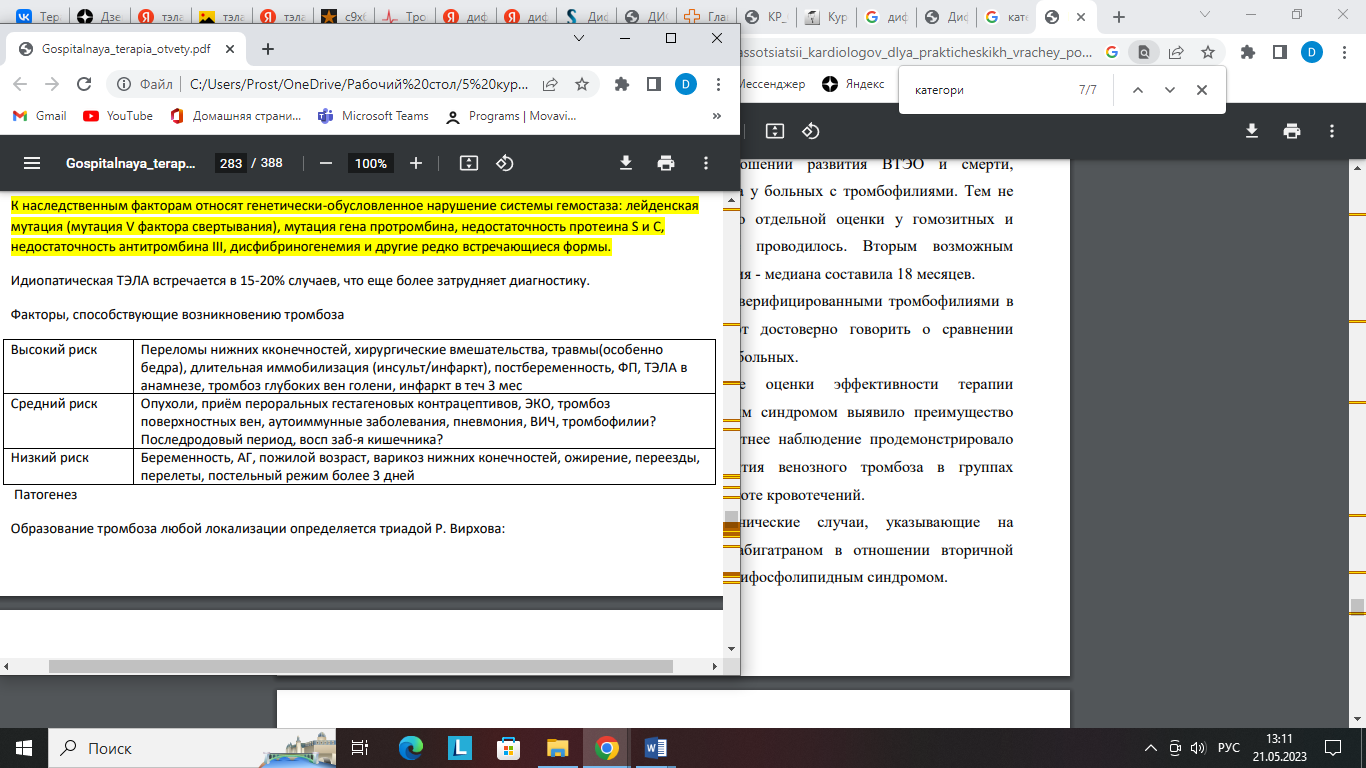
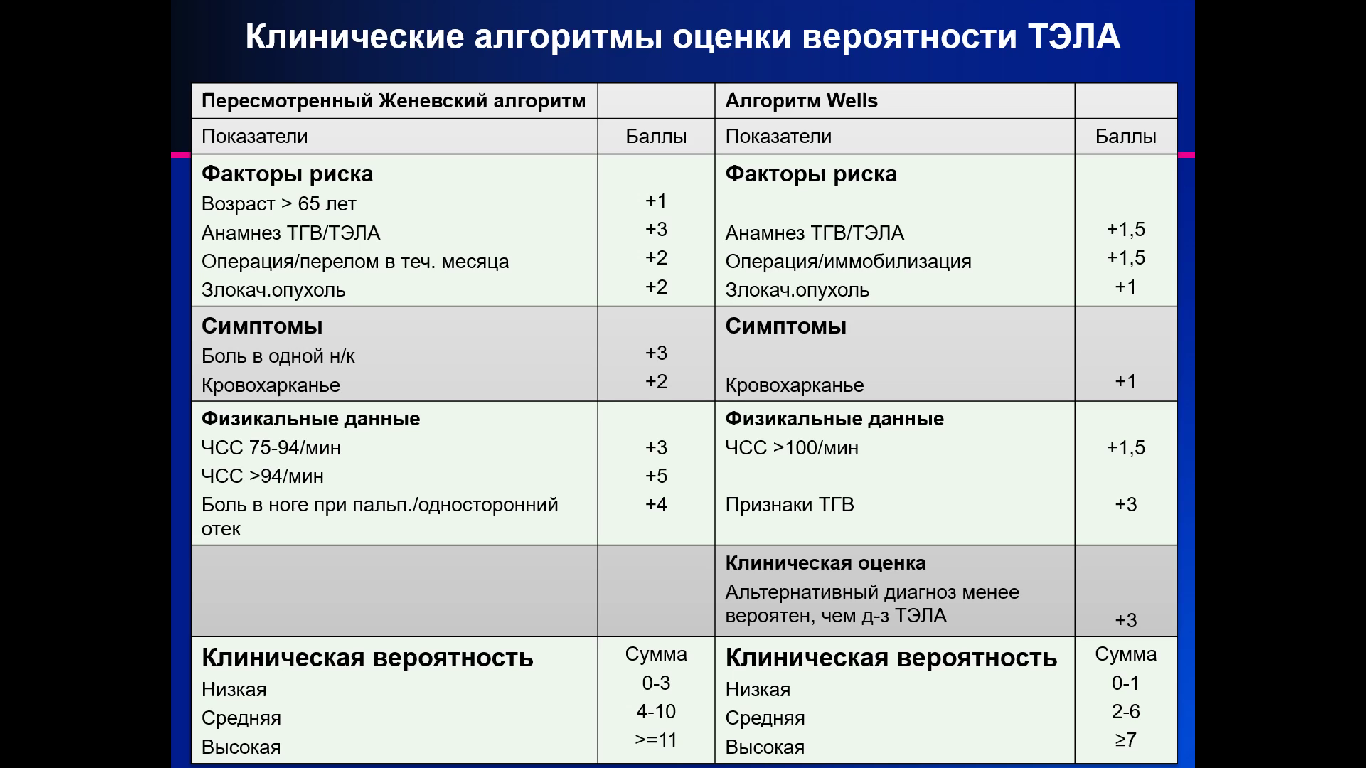
Оценка клинической вероятности: несмотря на невысокую чувствительность и специфичность отдельных симптомов, признаков и результатов обследования, их сочетание позволяет классифицировать пациентов с подозрением на ТЭЛА на категории по клинической вероятности. Для этого используют алгоритм Wells и шкала Geneva, позволяющие стратифицировать пациентов на группы риска по трехуровневой шкале (низкий, промежуточных и высокий риски) или с помощью двухуровневой шкал по вероятности наличия легочной эмболии.

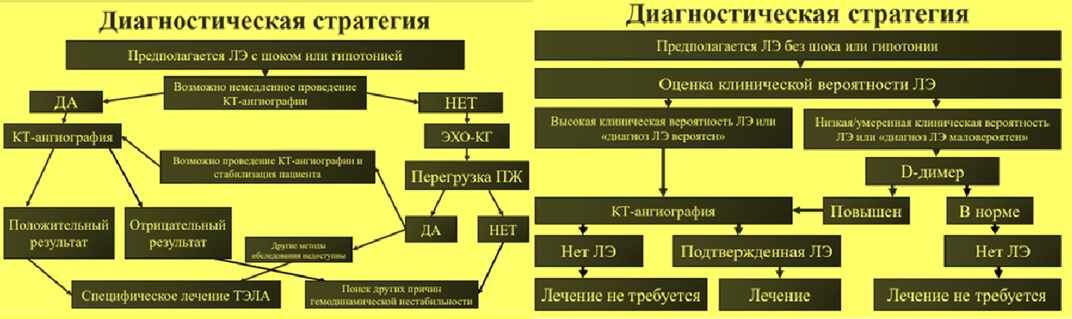
Принципы диагностики:
Измерение D-димера:
Плазменный D-димер – это продукт распада фибрина, волокна, образующиеся в процессе фибринолиза при расщеплении фибринового сгустка плазмы. Концентрация Д-димера в плазме увеличивается при наличии острого тромба, вследствие спонтанной активности коагуляции и фибринолиза.
Но содержание фибрина повышается и при воспалении, инфекционных заболеваниях, беременности, опухолях и тд.
Нормальное значение Д-димера – менее 0,5 мкг/мл.
ЭКГ:
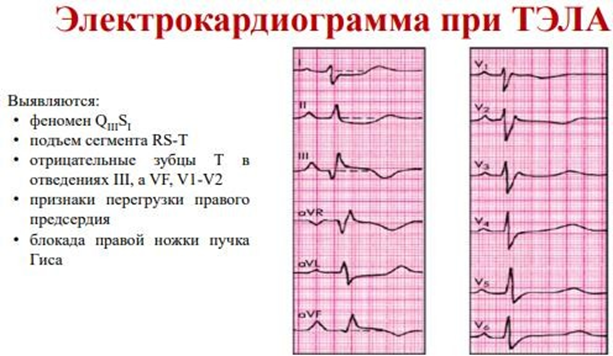
Изменения ЭКГ неспецифичны и выявляются в 70-80% случаев, чаще при ТЭЛА высокого риска, но их отсутсвие не позволяет отклонить диагноз. ЭКГ-признаки острого легочного сердца:
симптом QIIISI: появление патологического зубца Q в III отведении и глубокого зубца S в I отведении;
подъем сегмента RS-T в отведениях III, aVF, V1, V2 и дисконрдантное снижение сегмента RS-T в отведениях I, aVL, V5, V6;
появление отрицательных зубцов Т в отведениях V1-V3;
появление высоких (более 2 мм) заостренных зубцов Р в III и aVF отведениях (p-pelmonale);
блокада правой ножки пучка Гиса.
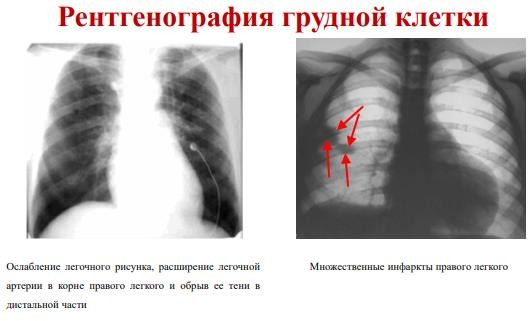
Рентгенография грудной клетки:
Признаки также неспецифичны, в большинстве случаев рентгенография грудной клетки позволяет заподозрить ТЭЛА и исключить другие патологии (пневмония, рак легких, перикардит, пневмоторакс).
Наиболее часто определяются: ателектаз части легкого, плевральный выпот, инфильтрация легочной ткани, высокое стояние купола диафрагмы на стороне поражения.
Классическими признаками инфаркта легкого являются наличие затемнения клиновидной формы, верхушка которого направлена к корю легкого, а основание к плевре (бугорок Хэмптона) или уменьшение выраженности сосудистого легочного рисунка в зоне тромбоэмболии (симптом Вестермарка). Также отмечается: расширение центральной ЛА с резким ее обрывом, так называемые «обрубленные корни», увеличение размеров сердца (особенно его правых отделов), признаки отека легких.
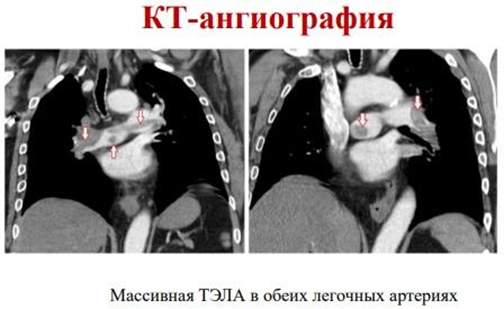
КТ-ангиография:
Один из основных методов диагностики ТЭЛА. В периферическую вену вводят контраст, затем выполняют КТ органов грудной клетки. Признаками ТЭЛА являются: дефект наполнения сосуда (полный или частичный), обеднение сосудистого рисунка в сегменте эмболии, инфаркт легкого, ателектазы.
Вентиляционно-перфузионная сцинтиграфия:
В/в вводят макроаггрегированные альбуминовые частица, меченые технецием-99, которые оседают в мелких легочных капиллярах и позволяют оценить перфузию легких на клеточном уровне. При окклюзии ветвей ЛА периферическое капиллярное русло не получает меченых частиц, в соответствующем легочном поле визуализируется «холодное поле». Далее проводят вентиляционную стадию, для которой используются различные изотопы (ксенон-133, аэрозоли, меченные технецием-99). Цель – увеличение специфичности теста путем выявления зон гиповентиляции и неэмболической причины гипоперфузии. При локальной бронхиальной обструкции области снижения активности при перфузионной фазе будут соответствовать зонам пониженной активности вентиляционной сцинтиграфии, что обусловлено рефлекторной вазоконстрикцией.
В случае ТЭЛА напротив гипоперфузионных областях сохраняется нормальная вентиляция, что и называется вентиляционно-перфузионным несоответствием.
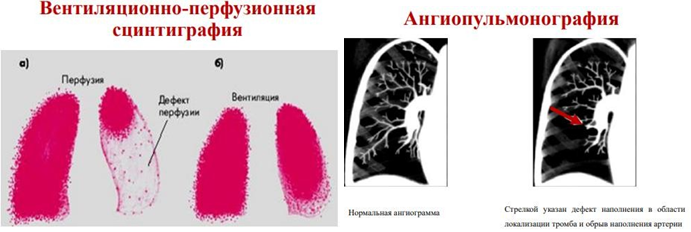
Ангиопульмоногрфия:
Селективная ангиопульмонография – рентгенологический метод исследования сосудов легких и легочного кровотока, при котором контрастный препарат вводится с помощью катетеров непосредственно в сосудистое русло легких, «золотой стандарт» диагностики ТЭЛА.
Для введения рентгеноконтрасного вещества в ствол ЛА и ее ветви производят чрескожную катетеризацию бедренной вены и проводят катетер через правое сердце. Метод инвазивный, что ограничивает его применение особенно у пациентов с высоким риском.
Прямые признаки ТЭЛА: изображение тромба, внутрисосудистые дефекты наполнения, полная обструкция сосуда с резким расширением проксимальнее закупорки и отсутствием изображения дистальных участков.
Косвенные признаки: олигемия – уменьшение перфузии в периферических отделах легких вследствие обтурации, удлинение артериальной фазы кровотока или стаз вследствие повышенного периферического сопротивления, асимметрия заполнения сосудов.
ЭХО-КГ:
Позволяет выявить признаки острого легочного сердца и повышения давления в ЛА, оценить гемодинамические нарушения.
ЭХО-КГ критерии, характерные для ТЭЛА: расширение и гипокинез ПЖ, непосредственная визуализация тромбоэмбола, расширение проксимальной части ЛА, увеличение скорости трикуспидальной регургитации, аномальное движение межжелудочковой перегородки, расширение НПВ и ее коллабирование на вдохе менее 50%.

Венозная компрессионная ультрасонография:
Наличие прокисмальных тромбов у пациентов с подозрением на ТЭЛА является показанием для начала антикоагуляционной терапии без дальнейшего обследования.
Единственным критерием, подтверждающим наличие тромба в венах нижних конечностей, является неполная компрессия вены, которая указывает на наличие тромба. Диагностика затруднена при обследовании пациентов, страдающих ожирением или имеющих нестандартную анатомию венозной системы.
Принципы лечения:
Задачи лечения:
восстановление легочного кровотока; нормализация гемодинамики, устранения дыхательных и сердечно-сосудистых расстройств; предотвращение рецидива заболевания.
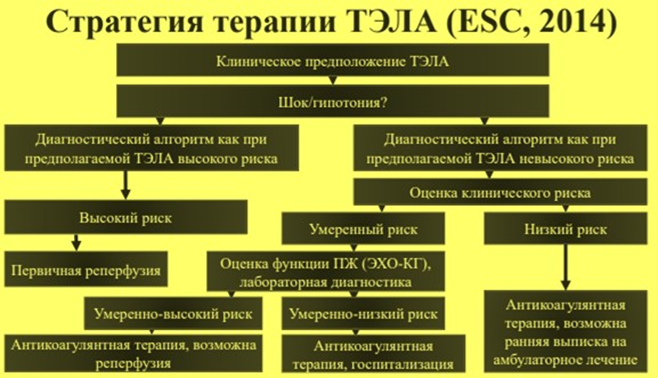
Антикоагулянтная терапия:
должна быть начата немедленно: в острую фазу назначаются на первые 5-10 дней парентеральные антикоагулянты (нефракционированный гепарин (НФГ), низкомолекулярные гепарины (НМГ), фондапаринукс). Далее к паренетральному введению добавляем антагонисты витамина К или новый оральный антикоагулянт (НОАК) – Дабигатран, Эдоксабан. Если вместо них использовать Ривароксабан или Апиксабан, то их следует назначить немедленно или через 1-2 лня терапии НФГ, НМГ или фондапаринуксом. Лечение в острую фазу будет состоять их высокой дозы перорального антикоагулянта в течение первых 3 недель (для ривароксабана), либо первых 7 дней (для апиксабана).
Стандартная продолжительность терапии не менее 3 месяцев.
Классификация прямых антикоагулянтов:
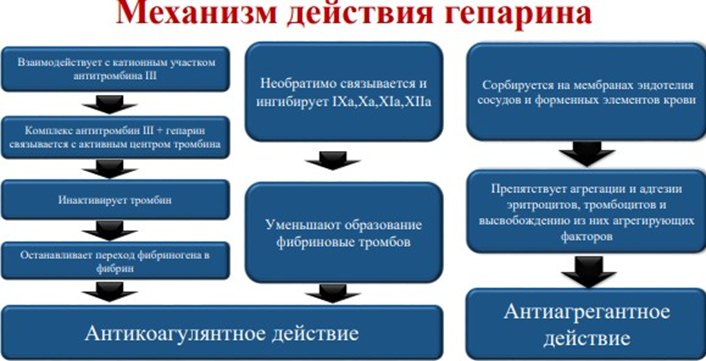
Гепарин (НФГ и НМГ):
НФГ применяется под контролем АЧТВ (21,1-36,5 секунд). На фоне приема препарата АЧТВ должно быть в 1,5-2 раза больше. Но большое увеличение = склонность к кровотечению, следовательно дозировку необходимо скорректировать.
НМГ имеют более предсказуемый и дозозависимый эффект, меньшее количество побочек, больший период полувыведения, что делает возможным назначать препарат 1-2 раза в сутки, в отличие от НФГ (6 раз в сутки). Контроля АЧТВ не требует.

Непрямой антикоагулянт – Варфарин. Механизм действия:
Ингибитор витамина К: препятстсвует превращению неактивного (восстановленного) К-эпоксида в активный витамин К-гидрохинон, ингибируя ферменты эпоксидредуктазу и DT-диафоразу;
Блокирует выработка К-зависимых факторов свертывания: 2, 7, 9 и 10;
Замедляется процесс свертывания;
МНО – дополнительный способ представления результатов протромбинового теста. Целевое значение при приеме препарата – 2,0-3,0;
Во время добавления варфарина к парентеральному введению прямых антикоагулянтов следует контролировать МНО и применять двойную антикоагулянтную терапию до тех пор, пока МНО не стане от 2 до 3, в течение минимум 2 дней подряд.
Раннее восстановление проходимости ЛА ведет к адекватному снижению напряжения и давления в ЛА и нормализации функции ПЖ.
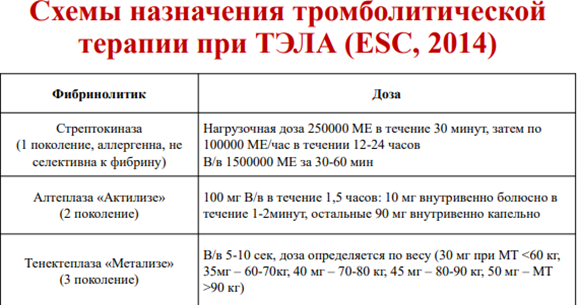
Альтеплаза:
золотой стандарт тромболитической терапии;
является фибрин-селективным препаратом, обладает способностью растворять устойчивые к лизису тромбы и не вызывает резкого снижения плазминогена;
в отличие от препаратов 1 поколения не обладает аллергенными свойствами, на введение препараты не вырабатываются АТ, можно использовать повторно.
Тромболитическая терапия:
Абсолютные противопоказания:
перенесенный геморрагический инсульт или нарушение мозгового кровообращения;
ишемический инсульт в последние 6 месяцев до;
повреждение ЦНС или ее новообразования, или артериовенозные мальформации№
недавняя серьезная травма/хирургическое вмешательство/травма головы;
ЖКК (в течение последнего месяца);
геморрагический диатез;
расслоение аорты.
Относительные противопоказания:
ТИА в предыдущие 6 месяцев;
наличие плохо контролируемого АД;
тяжелые заболевания печени;
инфекционный эндокардит;
травматичная или длительная (более 10 минут) СЛР;
для стрептокиназы – введение стрептокиназы, в том числе модифицированной, более 5 суток назад или известная аллергия на нее;
беременность;
обострение ЯБ;
прием антагонистов витамина К.
Чрескожная катетерная эндартерэктомия и фрагментация тромба:
Цель – удаление тромбов из главных ЛА для восстановления функции ПЖ.
У тех, кто с абсолютными противопоказаниями к трмболизису интервенционная терапия включает варианты:
фрагментация тромба баллонным катетером;
реолитическая тромбэктомия гидродинамическими катетерами;
аспирационная тромбэктомия аспирационными катетерами;
ротационная тромбэктомия
Хирургическая эмболэктомия:
Она может быть использована у больных с острым эпизодом ТЭЛА, ассоциированным с гипотензией: которым противопоказан тромболизис; у которых тромболизис или катетерная эмболэктомия оказалась неэффективными; у которых имеется шок, угражающий наступлением смерти еще до наступления эффекта от терапии.
Кава-фильтры (венозные фильтры) устанавливают обычно в инфраренальном отделе нижней полой вены, если тромб обнаруживается в почечных венах, может быть показано супраренольное размещение. Показаны пациента, у котоырх есть абсолютные противопоказания к антикогулянтам и пациентам с подтверждённой легочной эмболией, несмотря на приме препаратов. Венозные фильтры могут обеспечить длительную защиту от ТЭЛА, но есть вероятность возникновения осложнений (поздний рецидив, посттромботический синдром).
Гемодинамическая и дыхательная поддержка:
Острая недостаточность ПЖ, ведущая к низкому сердечному выбросу, ведущая причина смерти. Поэтому необходимо поддерживающее лечение и ТЭЛА, и острой правожелудочковой недостаточности.
Норэпинефрин улучшает функцию ПЖ путем прямого инотропного эффекта и увеличивает коронарную перфузию посредством стимуляции периферических альфа-адренорецепторов и повышения системного АД.
Добутамин повышает сердечный выброс, сердечный индекс, улучшает транспорт кислорода и оксигенацию тканей, не влияя на ЧСС и системное АД. Но повышение СИ выше физиологических значений, может усугубить вентиляционно-перфузионное несоответствие.
Эпинефрин сочетает в себе и свойства добутамина, и норэпинефрина без системного вазодилатирующих эффектов. Полезно при сочетании ТЭЛА + шок.
Вазодилататоры снижают давление и сосудистое сопротивление в МКК. Но они недостаточно селективны к легочной сосудистой системе при в/в введении. Лучше назначить ингаляционно, так как ингаляции оксида азота позволяют улучшить гемодинамику и газообмен.

