
Кузина ОХТ полимеров
.pdf
препятственно. При отрицательном значении dB растворимость затруднена и может происходить разделение на фазы. При dB = 0 устанавливается равновесие, и молярная доля растворенного вещества соответствует насыщению раствора.
С позиций термодинамики dB равно сумме двух величин, имеющих вполне определенный физический смысл:
dB |
|
Ht |
St |
(10) |
|
|
|
RT |
|
R |
|
Первый член уравнения |
Ht |
соответствует теплоте, поглощенной |
|||
системой при переносе одного моля В из своей фазы в раствор. Второй член уравнения характеризует соответствующее изменение энтропии системы.
Если вещество В является полимером, содержащим r повторяющихся
звеньев, то растворяющую силу для полимера dp |
можно представить |
следующим образом: |
|
dP r dm |
(11) |
где dm – растворяющая сила, отнесенная к повторяющемуся звену. В свою очередь,
dP |
m ms , |
(12) |
|
RT |
|
где m , ms – химические потенциалы |
повторяющегося звена |
|
соответственно в собственной фазе (полимере) и в растворе.
Следует отметить, что dm характеризует растворяющую силу только определенного растворителя по отношению к определенному полимеру (его повторяющемуся звену). Для данного полимера другого типа значение dm может меняться. Например, оно уменьшается при переходе от аморфного к кристаллическому состоянию полимера. При снижении молекулярной массы полимера dm повышается. Необходимо отметить, что в уравнении не учтено влияние концевых групп полимера, которым при достаточно больших молекулярных массах можно пренебречь.
21
1.3 Растворители
Растворители – это соединения, которые при комнатной температуре и атмосферном давлении обычно представляют собой жидкости, способные растворять другие вещества, не изменяя их химическую структуру.
Растворитель должен обладать постоянными физическими характеристиками согласно спецификации производителя и должен быть:
-прозрачными и бесцветными;
-летучим, не оставлять осадок;
-устойчивым к химическим веществам в течение долгого времени;
-нейтральным;
-со слабым или приятным запахом;
-без содержания воды;
-с низкой токсичностью;
-биологически разлагаемым;
-недорогим.
Применяемые растворители в основном классифицируются по химической природе (таблица 4):
Наряду с индивидуальными растворителями используют и смесевые растворители, составы некоторых из них приведены в таблице
1.3.1 Физические и химические свойства растворителей
Плотность и коэффициент преломления. Величины этих показателей в определенной степени определяют чистоту растворителя.
Плотность растворителей обычно измеряют при 20 ºС и сравнивают с плотностью воды, измеренной при 4 ºС (относительная плотность d420).
У большинства органических растворителей значение плотности меньше, чем у воды, за исключением галогенированных углеводородов. Плотности большинства органических растворителей уменьшаются с увеличением температуры.
Относительная плотность сложных эфиров и гликолевых эфиров одного гомологического ряда уменьшаются с увеличением молекулярной массы, тогда как аналогичные показатели для кетонов и спиртов увеличиваются.
22
Таблица 4 - Классификация основных органических растворителей, применяемых в лакокрасочной промышленности
Классы |
Группы |
Подгруппы |
|
|
органических |
органических |
органических |
Примеры растворителей |
|
растворителей |
растворителей |
растворителей |
|
|
|
|
|
|
|
|
Алифатические |
– |
Пентан, гексан, гептан |
|
|
|
|
|
|
|
Ациклические |
– |
Циклопентан, циклогексан |
|
|
|
|
|
|
Углеводороды |
Ароматические |
– |
Толуол, бензол, ксилол, тетралин |
|
|
|
|
|
|
|
Нефтяные |
– |
Уайт-спирит, сольвент, нефрас, петролейный эфир |
|
|
|
|
|
|
|
Терпеновые |
– |
Скипидар, пинен |
|
|
|
|
|
|
Кетоны |
Алифатические |
– |
Ацетон, метилэтилкетон, спирт диацетоновый |
|
|
|
|
||
Циклические |
– |
Циклогексанон, метилциклогексанон |
||
|
||||
|
|
|
|
|
|
|
Алифатические |
|
|
|
|
эфиры одноатом- |
Диэтиловый эфир |
|
|
|
ных спиртов |
|
|
|
Простые |
|
|
|
Эфиры |
Алифатические |
|
||
|
эфиры двухатом- |
Метилцеллозольв, этилцеллозольв, бутилцеллозольв |
||
|
|
|||
|
|
ных спиртов |
|
|
|
|
|
|
|
|
|
Циклические |
Тетрагидрофуран, 1,4 -диоксан |
|
|
|
|
|
|
|
Сложные |
– |
Этилацетат, бутилацетат, пропилацетат |
|
|
|
|
|
23
Продолжение таблицы 4
Классы |
Группы |
Подгруппы |
|
|
органических |
органических |
органических |
Примеры растворителей |
|
растворителей |
растворителей |
растворителей |
|
|
|
|
|
|
|
|
|
Одноатомные |
Этиловый спирт, бутиловый спирт, изопропиловый |
|
|
Алифатические |
спирт |
||
|
|
|||
Спирты |
|
|
|
|
|
Двухатомные |
Этиленгликоль, пропиленгиколь, диэтиленгликоль |
||
|
|
|
|
|
|
Циклические |
– |
Циклогексанол, бензиловый спирт |
|
|
|
|
|
|
Галогенсодер- |
Хлорсодержащие |
– |
Хлороформ, четыреххлористый углерод, |
|
тетрахлорэтилен |
||||
жащие |
|
|
||
|
|
|
||
Фторсодержащие |
– |
Хладон-113 |
||
|
||||
|
|
|
|
|
|
Азотсодержащие |
– |
Диметилформамид |
|
|
|
|
|
|
Прочие |
Фурановые |
– |
Фурфурол |
|
|
|
|
|
|
|
Серусодержащие |
– |
Диметилсульфоксид |
|
|
|
|
|
24
Таблица 5 – Состав некоторых смесевых растворителей
Наименование |
Состав растворителя |
||
растворителя |
|
|
|
Компоненты |
Содержание, % (масс.) |
||
|
|
|
|
|
Бутилацетат |
10,0 |
|
|
|
|
|
|
Этилцеллозольв |
8,0 |
|
|
|
|
|
Растворитель 646 |
Ацетон |
7,0 |
|
|
|
||
Бутиловый спирт |
15,0 |
||
|
|||
|
|
|
|
|
Этиловый спирт |
10,0 |
|
|
|
|
|
|
Толуол |
50,0 |
|
|
|
|
|
|
Бутилацетат |
29,8 |
|
|
|
|
|
Растворитель 647 |
Этилацетат |
21,2 |
|
|
|
||
Бутиловый спирт |
7,7 |
||
|
|||
|
|
|
|
|
Толуол |
41,3 |
|
|
|
|
|
|
Бутилацетат |
50,0 |
|
|
|
|
|
Растворитель 648 |
Бутиловый спирт |
10,0 |
|
|
|
||
Этиловый спирт |
20,0 |
||
|
|||
|
|
|
|
|
Толуол |
20,0 |
|
|
|
|
|
|
Бутилацетат |
12,0 |
|
|
|
|
|
Растворитель Р-4 |
Ацетон |
26,0 |
|
|
|
|
|
|
Толуол |
62,0 |
|
|
|
|
|
|
Бутилацетат |
10,0 |
|
|
|
|
|
Растворитель Р-5 |
Ацетон |
50,0 |
|
|
|
|
|
|
Ксилол |
40,0 |
|
|
|
|
|
Коэффициент преломления nD измеряется при помощи рефрактометра с лампой, содержащей пары натрия (линия натрия D 598,0 и 589,6 нм). С увеличением температуры коэффициент преломления растворителей уменьшается.
Величина коэффициента преломления сильно зависит от углеводородного звена вещества. Алифатические эфиры, кетоны и спирты имеют значения коэффициентов преломления о 1,32 до 1,42. В гомологических рядах коэффициент преломления увеличивается с повышением длины углеводородной цепи и снижается с уменьшением степени разветвленности углеводорода. Наличие циклоалифатических и ароматических соединений увеличивает коэффициент преломления из-за влияния функциональных групп.
25
Вязкость и поверхностное натяжение. В гомологических рядах растворителей вязкость повышается с увеличением молекулярной массы, например в ряду метанол (0,61 мПа·с), этанол (1,19 мПа·с), н-пропанол (2,26 мПа·с), н – бутанол (3,0 мПа·с) и гексанол (4,3 мПа·с). Растворители, содержащие гидроксильные группы, имеют более высокую вязкость из-за образования водородных связей. Вязкость уменьшается с увеличением температуры.
Влияние растворителей на вязкость лакокрасочных материалов зависит
восновном от двух факторов:
-вязкости самого растворителя;
-взаимодействия между пленкообразователем и растворителем, а также между разными компонентами смесевого растворителя.
Вязкость растворов полимеров в целом зависит от объемного содержания компонентов. Поэтому при сравнении вязкости растворов, содержащих разные растворители, необходимо, чтобы их объемное содержание было одинаковым. Однако, поскольку известны объемы только чистых компонентов, а растворы полимеров в большинстве случаев неидеальные, то полученные при таком подходе данные будут не совсем точные. Так, если в случае сложных эфиров установлена связь между вязкостью растворов акриловых полимеров и вязкостью чистого растворителя, то эта зависимость не применима для всех растворителей, особенно для тех, которые способны взаимодействовать с полимером.
Поверхностное натяжение растворителя связано с энергией когезии. Приведенное ниже соотношение применяется как для полярных, так и для неполярных растворителей:
|
|
|
|
a |
(13) |
|
2,1 K |
|
0 |
|
, |
||
|
3 |
V |
|
|
||
где – параметр растворимости, (Дж/см3)1/2;0 – поверхностное натяжение, мН/м;
V – молярный объем, см3/моль;
K и a – константы, зависящие от вещества (K ~3,6 и a ~ 0,56)
Величина поверхностного натяжения растворителей в лакокрасочном материале влияет на скорость испарения, на образование покрытий, а также на смачивание окрашиваемых поверхностей, пигментов и наполнителей.
Испарение и летучесть. Температура кипения растворителя
26
определяется как температура, при которой давление насыщенного пара жидкости достигает значения 101,3 к Па. Тепловая энергия расходуется на испарение жидкости и извлекается из окружающей среды, приводя к ее охлаждению. Знание температур кипения растворителей для специалистов важно при проведении процессов перегонки и экстракции.
Всоответствии с температурой кипения растворители классифицируют следующим образом:
- низкокипящие – температура кипения < 100 ºС; - среднекипящие - температура кипения 100 – 150 ºС; - высококипящие – температура кипения > 150 ºС.
Влакокрасочной промышленности важным является знание значений летучести растворителей, которые меньше величин температур кипения. Не существует прямой зависимости между летучестью и температурой кипения растворителей. Обычно летучесть уменьшается с увеличением температуры кипения растворителей, принадлежащих одному гомологическому ряду. Растворители, которые способны к образованию водородных связей (спирты, амины, вода) менее летучи, чем другие растворители с такой же температурой кипения. Это связано с тем, что энергия сначала тратится на разрушение водородных связей, и лишь потом на процесс парообразования.
Скорость испарения растворителей зависит от следующих факторов: - давления насыщенного пара при температуре процесса; - удельной теплоемкости; - энтальпии парообразования;
- степени ассоциации молекул; - скорости подачи тепла; - поверхностного натяжения; - молекулярной массы;
- атмосферной турбулентности; - влажности воздуха.
Теоретически прогнозировать скорости испарения растворителей невозможно, поскольку все вышеперечисленные факторы взаимосвязаны.
На практике время испарения растворителя определяют экспериментально при одинаковых условиях внешней среды и сравнивают эту величину с данными для диэтилового эфира (в некоторых странах для бутилацетата).
Относительную летучесть (по диэтиловому эфиру) рассчитывают по следующей формуле:
27
Е (диэтиловый эфир) = t1 (испытуемый растворитель) / t2 (диэтиловый эфир), (14)
где t1 – продолжительность испарения испытуемого растворителя, с; t2 – продолжительность испарения диэтилового эфира, с.
Получаемые значения относительной летучести в Германии называют индексами испарения (или числами испарения) и соотносят с данными для диэтилового эфира (индекс испарения = 1).
На основе индексов испарения растворители классифицируют на
четыре группы: |
|
|
1. |
Сильнолетучие растворители |
– < 10. |
2. |
Умереннолетучие растворители |
– 10 – 35. |
3. |
Слаболетучие растворители |
– 35 – 50. |
4. |
Очень слаболетучие растворители |
– > 50. |
Относительную летучесть (по бутилацетату) рассчитывают по формуле:
Е (бутилацетат) = t90 (бутилацетат) / t90 (испытуемый растворитель), |
(15) |
где t90 – время, за которое 90 % испытуемого растворителя по сравнению с 90 % бутилацетата испаряется в данном типе приборе при жестко контролируемых условиях.
За основу классификации растворителей в США принимается число
летучести бутилацетата (=1): |
|
||
Класс 1: Быстроиспаряющиеся растворители |
> 3,0. |
||
Класс 2: Умеренноиспаряющиеся растворители |
0,8 – 3,0. |
||
Класс 3: Медленно испаряющиеся растворители |
< 0,8. |
||
Таблица 6 – Относительная летучесть некоторых растворителей |
|||
|
|
|
|
|
Относительная лету- |
|
Относительная |
Растворитель |
честь (по диэтиловому |
|
летучесть (по бутил- |
|
эфиру =1) |
|
ацетату = 1) |
|
|
|
|
Толуол |
6,1 |
|
2,0 |
|
|
|
|
Ксилол |
13,5 |
|
0,76 |
|
|
|
|
Этанол |
8,3 |
|
2,4 |
|
|
|
|
Ацетон |
2,0 |
|
5,6 |
|
|
|
|
28
Продолжение таблицы 6
|
Относительная лету- |
Относительная |
Растворитель |
честь (по диэтиловому |
летучесть (по бутил- |
|
эфиру =1) |
ацетату = 1) |
|
|
|
Изопропиловый спирт |
11,0 |
1,5 |
|
|
|
Бутанол |
33,0 |
0,47 |
|
|
|
Изобутанол |
25,0 |
0,85 |
|
|
|
Этилацетат |
3,0 |
4,2 |
|
|
|
Бутилацетат |
12,0 |
1,0 |
|
|
|
Этилгликоль |
43,0 |
0,38 |
|
|
|
Этилдигликоль |
1200 |
0,017 |
|
|
|
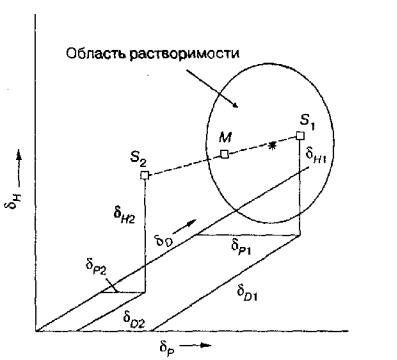
Летучесть растворителей из полимерной пленки зависит от разницы между параметрами растворимости растворителя и полимера. Полимеры занимают определенную область на диаграмме парамет ров растворимости с координатами δD, δP и δH (см. рисунок 3).
Рисунок 3 – Диа грамма параметра растворимости
Растворители, у которых параметры лежат близко к центру области растворимости поли мера, сильно взаимодействуют с полимером, поэтому они медленно испаряются из высушиваемой пленки и могут удерживаться внутри её. Растворители, которые слабо взаимодействуют с полимером,
29

расположены на границе области растворимости полимера (т.е. в переходной области между растворителями и нерастворителями) и, следовательно, более легко испаряются из полимерной пленки.
Качество образующейся пленки (её сплошность, глянец, декоративный вид и т.п.) во многом зависит от скорости улетучивания растворителя при пленкообразовании. Слишком быстрое испарение растворителя может привести к сильному охлаждению пленки и вследствие этого – к её помутнению за счет конденсации на поверхности влаги из окружающей среды. Кроме того, в этом случае могут образовываться пористые пленки, а также пленки с более высокими напряжениями, поскольку при большой скорости удаления растворителя не успевают пройти релаксационные процессы. Пористые пленки могут образовываться и при слишком медленном улетучивании растворителя (например, при формировании пленок из термореактивных пленкообразователей).
Для обеспечения нормальных условий пленкообразования наиболее целесообразным оказывается введение в пленкообразующую систему одновременно нескольких растворителей, отличающихся по своей летучести и температуре кипения.
Плотность пара. Плотность пара – это масса растворителя на кубический метр воздуха (кг/м3), который находится в равновесии с жидкостью при 101,3 кПа. Плотность пара соотносится с содержанием растворителя в атмосфере при насыщении и зависит от температуры. Относительная плотность ds соотносится с плотностью воздуха и может быть рассчитана по формуле:
dS |
M S , |
(16) |
|
M Air |
|
где MS – молекулярная масса растворителя;
M Air – молекулярная масса воздуха (28,95 г/моль).
В идеальном случае относительная плотность пара не зависит от температуры. Ниже приведены относительные плотности пара некоторых растворителей:
Толуол |
3,18 |
Ксилол |
3,67 |
Этанол |
1,59 |
Бутанол |
2,56 |
30
