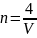идз / ИДЗ3 Андреева
.docxМИНОБРНАУКИ РОССИИ Санкт-Петербургский государственный электротехнический университет «ЛЭТИ» им. В.И. Ульянова (Ленина) Кафедра микро- и наноэлектроники |
||||||
отчет по индивидуальному домашнему заданию № 3 по дисциплине «Методы анализа структур электроники и микросистемной техники» Тема: «Рентгеновская фотоэлектронная спектроскопия»
|
||||||
|
||||||
Санкт-Петербург 2025 |
МОДЕЛИРОВАНИЕ СПЕКТРА
Исследуемый
образец – Mn2O4Ti.
В таблице 1 приведём значения энергии
связи
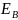 электронов, содержащихся в исследуемом
образце.
электронов, содержащихся в исследуемом
образце.
Таблица 1 – Энергии связи электронов для различных оболочек атомов, входящих в состав образца, эВ
Z |
М, г/моль |
Элемент |
Оболочка |
||||||||
1s1/2 |
2s1/2 |
2p1/2 |
2p3/2 |
3s1/2 |
3p1/2 |
3p3/2 |
3d3/2 |
3d5/2 |
|||
25 |
54,938 |
Mn |
6539 |
769 |
652 |
641 |
84 |
49 |
4 |
||
8 |
16 |
O |
532 |
24 |
7 |
– |
– |
– |
– |
– |
|
22 |
47,9 |
Ti |
4965 |
564 |
461 |
455 |
59 |
34 |
3 |
||
В качестве источника излучения возьмём мишень Mg:
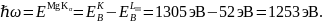
В таблице 2 приведём значения энергии фотоэлектронов.
Таблица 2 – Кинетические энергии фотоэлектронов, эВ
Элемент |
Оболочка |
|||||||||
1s1/2 |
2s1/2 |
2p1/2 |
2p3/2 |
3s1/2 |
3p1/2 |
3p3/2 |
3d3/2 |
3d5/2 |
||
Mn |
– |
484 |
601 |
612 |
1169 |
1204 |
1249 |
|||
O |
721 |
1229 |
1246 |
– |
– |
– |
– |
- |
||
Ti |
– |
689 |
792 |
798 |
1194 |
1219 |
1250 |
|||
Пример расчёта для фотоэлектрона на уровне 2s1/2 атома Mn:
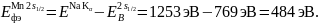
На рисунке 1 изобразим качественный обзорный РФЭ-спектр исследуемого образца.
Из-за ограничений по разрешению энергетического спектра (10 эВ) некоторые спектральные линии будут сливаться в одну детектируемую спектрометром линию – в данном случае это: Ti2p1/2-линия и Ti2p3/2-линия, Mn3d-линия, O2p-линия, и Ti3d-линия.
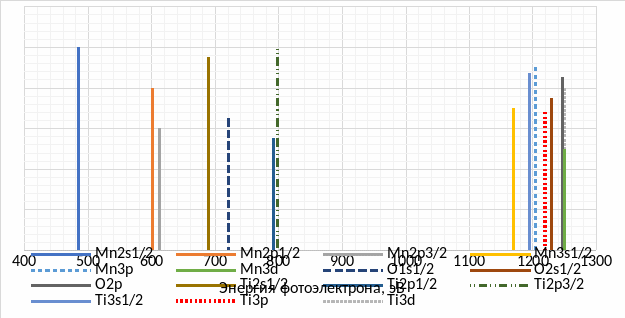
Рисунок 1 – Качественный рентгеновский спектр
Для всех значений энергий фотоэлектронов проведём расчет сечения фотоионизации, используя соотношение (1). Данные приведём в таблице 3.
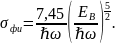 (1)
(1)
Таблица 3 – Сечение фотоионизации, Å2
Элемент |
Оболочка |
|||||||||||||
1s1/2 |
2s1/2 |
2p1/2 |
2p3/2 |
3s1/2 |
3p1/2 |
3p3/2 |
3d3/2 |
3d5/2 |
||||||
Mn |
– |
0,00175 |
0,00116 |
0,00111 |
6,9⋅10-6 |
1,8⋅10-6 |
3,4⋅10-9 |
|||||||
O |
0,0007 |
3⋅10-7 |
1,4⋅10-8 |
– |
– |
– |
– |
– |
||||||
Ti |
– |
0,00081 |
0,00049 |
0,00047 |
2,9⋅10-6 |
7,2⋅10-7 |
1,7⋅10-9 |
|||||||
Пример расчёта для уровня 2s1/2 атома Mn:
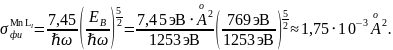
Для того, чтобы найти количество формульных единиц в единице объёма, необходимо найти объём ячейки. В нашем случае решётка имеет тетрагональную сингонию, как видно на рисунке 2, соответственно объём можем найти по формуле (2).
|
(2) |
где 𝑎 = 6,17 Å,
c = 8,564 Å.
Число формульных единиц на одну ячейку равно 4. Тогда концентрация формульных единиц в единице объёма будет определяться выражением (3).
|
(3) |
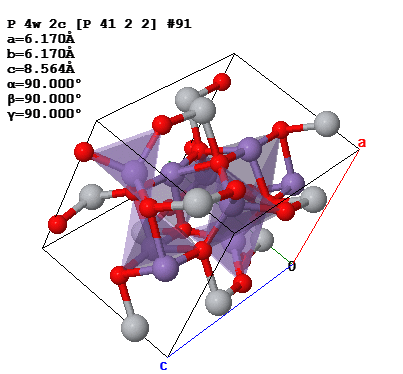
Рисунок 2 – Элементарная ячейка Ti2O4Ti
Произведём расчёт:
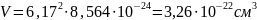
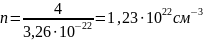
Количество атомов элемента в единице объёма можно найти как произведение количества формульных единиц в единице объёма на количество атомов элемента в одной формульной единице. Произведём расчёт для каждого элемента.
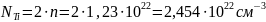
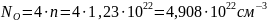
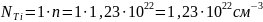
Проведем расчет интенсивности спектральных линий, используя соотношение (4). Расчет представим в таблице 4. Спектр представим на рисунке 3, причём изобразим только самые интенсивные линии для каждого из элементов соединения.
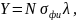 (4)
(4)
Длину свободного пробега найдём по универсальной кривой, где энергии сопоставим энергиям фотоэлектрона, представленным в таблице 2.
Таблица 4 – Расчет интенсивности
|
N,см-3 |
σфи, Å^2 |
Ефэ, эВ |
λ, Å |
Y |
Yнорм |
Mn2s1/2 |
2,45⋅1022 |
1,75⋅10-3 |
484 |
10 |
4,31⋅10-4 |
0,739 |
O1s1/2 |
4,91⋅1022 |
6,98⋅10-4 |
721 |
17 |
5,83⋅10-4 |
1 |
Ti2s1/2 |
1,23⋅1022 |
8,08⋅10-4 |
689 |
16,5 |
1,64⋅10-4 |
0,281 |
Пример расчёта для Mn2s1/2:
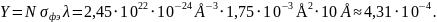
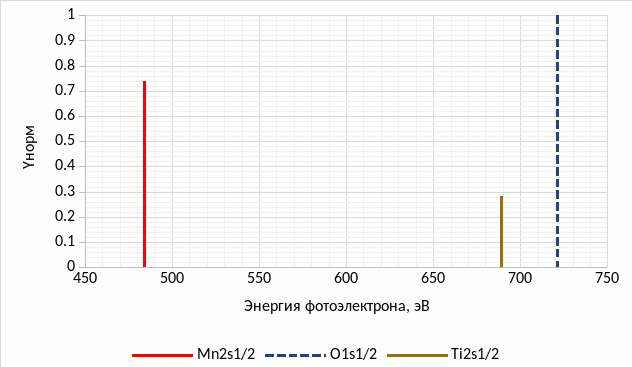
Рисунок 3 – Нормированный спектр