
ЛБ 1
.pdf
Министерство науки и высшего образования Российской Федерации
федеральное государственное автономное образовательное учреждение высшего образования
«НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
Инженерная школа природных ресурсов Направление подготовки Химическая технология Отделение химической инженерии
ОТЧЕТ
по лабораторной работе № 1
Название работы
ВЫЧИСЛЕНИЕ ФИЗИКО-ХИМИЧЕСКИХ ПОКАЗАТЕЛЕЙ ПРИРОДНОГОГАЗА
Вариант 1
Студент
Группа ФИО Подпись Дата
2Д12 |
Ткач Е.А. |
|
11.02.2025 |
|
|
Чижова А.В. |
|
|
|
|
Змеева Е.С. |
|
|
|
Руководитель |
|
|
|
|
Должность |
ФИО |
Ученая степень, звание |
Подпись |
Дата |
доцент ОХИ, |
Бешагина Е.В. |
к.т.н. |
|
|
ИШПР |
|
|
|
|
Томск – 2025 г.
Цель работы: рассчитать высшую и низшую теплоту сгорания газа, относительную плотность и число Воббе, используя хроматографию природного газа.
Теоретические сведения
Хроматография – физический метод разделения, в котором разделяемые компоненты распределены между двумя фазами, одна из которых является неподвижной (стационарная или неподвижная фаза), в то время как другая (подвижная фаза) движется в определенном направлении.
Неподвижная жидкая фаза - это фаза, определяющая селективные взаимодействия между компонентами пробы и твердым носителем, т.е. определяет последовательность выхода из колонки и отношение времен удерживания максимумов их зон, а также характер размывания хроматографических зон. В качестве неподвижной фазы в газовой хроматографии применяют твердый адсорбент, или жидкость, нанесенная в виде тонкой пленки на адсорбционно-инертный твердый носитель. Эффективность хроматографического разделения во многом зависит от выбора неподвижной фазы. Правильный выбор неподвижной фазы в свою очередь зависит от природы анализируемого вещества. При выборе стационарной фазы следует учитывать, что неполярные вещества лучше разделяются на неполярных фазах. В капиллярных колонках неподвижная жидкая фаза наносится в виде тонкой пленки на внутренние стенки капилляра. При этом сама трубка остается по существу “полой”. В насадочных применяют жидкость нанесенную в виде тонкой пленки на адсорбционно-инертный твердый носитель. К неполярным сорбентам относят активированный уголь. Силикагель, молекулярные сита, оксид алюминия применяют как полярные адсорбенты. Полисорбы, порапаки подразделяются на сорбенты средней полярности и неполярные. Сильное влияние на качество разделения оказывают водородные связи, которые возникают между анализируемым веществом и жидкой фазой.
В качестве подвижной фазы используют газ-носитель. Природа газа носителя оказывает влияние на работу детектора и характеристики колонки. Помимо обеспечения высокой чувствительности детектора, газ носитель должен быть инертным по отношению к разделяемым веществам и сорбенту, иметь небольшую вязкость для поддержания минимального перепада давления в колонке, быть взрывобезопасным и достаточно дешевым. На практике нашли применение азот, водород, гелий, аргон, углекислый газ, воздух.
Характерными особенностями любых хроматографических методов являются следующие:
•высокая разрешающая способность процесса разделения;
•мягкие условия разделения.
Основные задачи:
• разделение многокомпонентных по составу смесейна индивидуальные компоненты;
•концентрирование веществ из их очень разбавленных растворов;
•очистка технических продуктов, доведение этих продуктов до заданной степени химической чистоты, получение чистых химических реактивов;
•проверка вещества на однородность, на чистоту;
•контроль различных производств методами хроматографии.
В основу классификаций хроматографических методов положены принципы, учитывающие следующие различные особенности процесса разделения:
•различия в агрегатном состоянии фаз используемой хроматографической системы (Таб.1);
•различия в характере взаимодействий разделяемых веществ с неподвижной фазой (Табл.2);
•экспериментальные различия в способах проведения процесса хроматографического разделения (Табл.3).
|
|
|
|
Таблица 1 |
Варианты хроматографии, различающиеся по агрегатному состоянию фаз |
||||
Подвижная фаза |
Неподвижная фаза |
|
Название варианта |
|
|
|
|
|
|
|
|
общее |
|
частное |
газ |
абсорбент |
газовая |
|
газо-абсорбционная |
|
жидкость |
|
|
газо-жидкостная |
жидкость |
абсорбент |
жидкостная |
|
жидкостно- |
|
|
|
|
абсорбционная |
|
жидкость |
|
|
жидкостно- |
|
|
|
|
жидкостная |
газ или пар в |
абсорбент |
флюидная |
|
флюидно- |
сверхкритическом |
|
|
|
абсорбционная |
состоянии |
жидкость |
|
|
флюидно- |
|
|
|
|
жидкостная |
Таблица 2
Варианты хроматографии, различающиеся по характеру взаимодействий разделяемых соединений с неподвижной фазой
Механизм процесса разделения |
Название процесса |
|
|
по размеру молекул |
ситовая хроматография |
за счет физической адсорбции |
молекулярная хроматография |
за счет растворения |
распределительная хроматография |
за счет ионного обмена |
ионообменная хроматография |
за счет образования водородной связи, проявления |
хемосорбционная хроматография |
химического сродства и другое |
|
за счет образования координационных связей |
лигандообменная хроматография |
разделяемых органических молекул с катионами |
|
металлов в привитых на поверхности адсорбента |
|
группах (лигандах) |
|
за счет образования прочного комплекса только |
аффинная хроматография |
одним из разделяемых компонентов с привитой |
|
специфической группой неподвижной фазы |
|
|
|
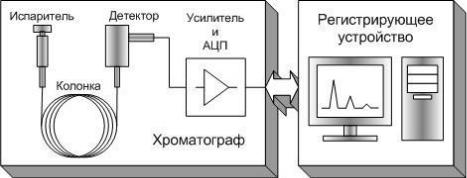
Таблица 3
Варианты хроматографии, различающиеся по способу проведения процесса разделения
Способ проведения процесса разделения |
Название варианта |
|
|
В цилиндрическом слое сорбента |
колоночная хроматография |
в слое сорбента на плоской поверхности |
хроматография в тонких слоях |
в пленке жидкости, содержащейся в полоске |
хроматография на бумаге |
бумаги |
|
в пленке жидкости или тонком слое адсорбента, |
капиллярная хроматография |
размещенном на внутренней стенке капилляра |
|
в полях электрических, магнитных, |
хроматография в полях сил |
центробежных и других сил |
|
Принципиальная схема газового хроматографа
Газовый хроматограф представляет собой прибор, использующий принцип хроматографии в системах газ-адсорбент или газ-жидкость. В аппаратурном оформлении это совокупность нескольких самостоятельных, параллельно функционирующих систем: источник газа-носителя и блок подготовки газов, испаритель, термостат колонок и сами хроматографические колонки, детектор, система регистрации и обработки данных. Типичная блок-схема газового хроматографа изображена на рисунке 1.
Рис. 1 Принципиальная схема газового хроматографа:
Устройство ввода (рис. 1) подает в поток газа-носителя определенное количество анализируемой смеси в газообразном состоянии непосредственно перед колонкой. В хроматографической колонке осуществляется разделение смеси на отдельные составляющие компоненты за счет процессов сорбции и десорбции веществ на неподвижной фазе. При этом слабо сорбируемые вещества, будут переноситься подвижной фазой по колонке с большей скоростью и наоборот. Из колонки разделенные компоненты смеси попадают в детектор.
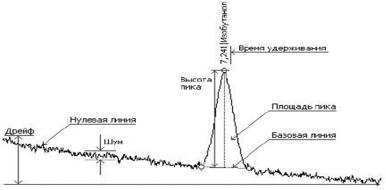
Детектор регистрирует присутствие веществ, отличающихся по физическим или физико-химическим свойствам от газа-носителя, и преобразует возникающие изменения в электрический сигнал. Далее происходит усиление и аналого-цифровое преобразование полученного сигнала. Регистрирующий прибор (компьютер или самописец) строит график зависимости сигнала детектора от времени, называемый хроматограммой (Рис.2).
Рис. 2 Типичная дифференциальная хроматограмма индивидуального вещества и несорбируемого газа
Прохождение в детекторе газа-носителя без пробы на хроматограмме отражается фоновым сигналом детектора, который называется нулевой линией. Нулевая линия имеет высокочастотные колебания – шум. Изменение сигнала нулевой линии детектора во времени называется дрейфом. При прохождении через детектор анализируемого компонента происходит отклонение уровня сигнала детектора от нулевой линии. Это отклонение отображается на хроматограмме в виде пика.
Исходными экспериментальными данными, с помощью которых выполняется качественный газохроматографический анализ, являются элюционные характеристики: время удерживания, объем удерживания и соответствующий им отрезок на хроматограмме - расстояние удерживания.
Время удерживания (tR) - это время, прошедшее от момента ввода пробы до выхода максимума концентрации определяемого компонента. Время удерживания – качественная характеристика анализируемого компонента, площадь и высота – количественные характеристики.
Площадь – область, ограниченная профилем пика и базовой линией. Высота – расстояние от вершины пика до базовой линии.
Расстояние удерживания (lR) — это расстояние на хроматограмме от момента ввода пробы до выхода пика определяемого компонента.
Удерживаемый объем (VR) — это объем газа-носителя (в см3), прошедший через хроматографическую колонку от момента ввода пробы до момента выхода максимальной концентрации определяемого вещества, измеренный при давлении и температуре на выходе из колонки.
Объемная скорость газа-носителя - объем газа-носителя, протекающего за единицу времени через пенный расходомер, т.е. на выходе из колонки и при температуре колонки.
Исходные данные
Исходные данные для расчета согласно варианту 1 приведены в таблице 4.
|
|
|
Таблица 4. Исходные данные |
|
|
|
|
Название |
|
Концентрация |
|
|
|
|
|
|
1016,1 |
|
1016,2 |
|
|
|
|
Кислород |
0,04082 |
|
0,03166 |
|
|
|
|
Азот |
2,210 |
|
2,149 |
|
|
|
|
Диоксид углерода |
2,578 |
|
2,568 |
|
|
|
|
Этан |
4,878 |
|
4,834 |
|
|
|
|
Пропан |
6,778 |
|
6,838 |
|
|
|
|
и-Бутан |
1,878 |
|
1,962 |
|
|
|
|
н-Бутан |
2,723 |
|
2,934 |
|
|
|
|
нео-Пентан |
0,005073 |
|
0,005422 |
|
|
|
|
и-Пентан |
0,8168 |
|
0,9658 |
|
|
|
|
н-Пентан |
0,6333 |
|
0,7990 |
|
|
|
|
Циклопентан |
0,04075 |
|
0,06037 |
|
|
|
|
2,2-диметилбутан |
0,0002583 |
|
0,0002643 |
|
|
|
|
2,3-диметилбутан+изогексан |
0,08653 |
|
0,1267 |
|
|
|
|
н-гексан |
0,07808 |
|
0,1595 |
|
|
|
|
Бензол + циклогексан |
0,01520 |
|
0,03239 |
|
|
|
|
2-метилгексан |
0,003039 |
|
0,005506 |
|
|
|
|
3-метилгексан |
0,03908 |
|
0,08891 |
|
|
|
|
н-Гептан |
0,001322 |
|
0,004887 |
|
|
|
|
Метилциклогексан |
0,007929 |
|
0,02231 |
|
|
|
|
Толуол |
0,002663 |
|
0,008038 |
|
|
|
|
2-метилгептан |
0,002917 |
|
0,01171 |
|
|
|
|
Анализ природного газа проводился на хроматографе Хроматек 5000, при следующих параметрах: температура сгорания 25 ; температура измерения 20 ; давление
101,325 кПа.
Вычисление физико-химических показателей природного газа
1. Вычисление теплоты сгорания
Для значения объемной теплоты сгорания требуется поправка, учитывающая отличие объема моля реального газа от объема моля идеального газа. Она требуется также при вычислении значений плотности, относительной плотности и числа Воббе. Такие поправки на объем, обусловленные неидеальностью газа, вводят с помощью коэффициента сжимаемости Zmix.

Коэффициент сжимаемости Zmix для стандартных условий измерений, рассчитывают по следующей формуле:
|
2 |
|
|
|
|
( 2, 2) = 1 − [∑ ( ∙ √ ) ] ,
=1
где суммирование проводят по всем N компонентам смеси. Значения так называемого коэффициента суммирования √ приведены в таблице 5, для трех стандартных условий измерений, представляющих общий интерес, для всех компонентов природного газа и имитатора природного газа, рассматриваемых в ГОСТ 31369–2008 Вычисление теплоты сгорания, плотности, относительной плотности и числа Воббе на основе компонентного состава.
Таблица 5. Результаты расчета коэффициента сжимаемости
|
Средняя |
Коэффициент |
|
|
|
|
Коэффициент |
|
Название |
молярная доля |
|
|
|
|
|
|
сжимаемости, Zmix |
суммирования,√ |
|
|
|
|
||||
|
√ * xj |
|||||||
|
компонента, xj |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кислород |
0,0003624 |
0,0265 |
|
|
9,6036E-06 |
0,99914095 |
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Азот |
0,0217950 |
0,0173 |
|
|
0,00037705 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Диоксид углерода |
0,0257300 |
0,0728 |
|
|
0,00187314 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Этан |
0,0485600 |
0,0894 |
|
|
0,00434126 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Пропан |
0,0680800 |
0,1288 |
|
|
0,0087687 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
и-Бутан |
0,0192000 |
0,2005 |
|
|
0,0038496 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
н-Бутан |
0,0282850 |
0,1783 |
|
|
0,00504322 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
нео-Пентан |
0,0000525 |
0,2025 |
|
|
1,0626E-05 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
и-Пентан |
0,0089130 |
0,2168 |
|
|
0,00193234 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
н-Пентан |
0,0071615 |
0,2345 |
|
|
0,00167937 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Циклопентан |
0,0005056 |
0,2236 |
|
|
0,00011305 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
2, 2 диметилбутан |
0,0000026 |
0,255 |
|
|
6,6632E-07 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
2, 3 диметилбутан + изогексан |
0,0010662 |
0,5289 |
|
|
0,00056389 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
н-Гексан |
0,0011879 |
0,2846 |
|
|
0,00033808 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Бензол + циклогексан |
0,0002380 |
0,5376 |
|
|
0,00012792 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
2-метилгексан |
0,0000427 |
0,272 |
|
|
1,1621E-05 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
3-метилгексан |
0,0006400 |
0,2683 |
|
|
0,0001717 |
|
||
|
|
|
|
|
|
|||
н-Гептан |
0,0000310 |
0,3521 |
|
|
1,0931E-05 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Метилциклогексан |
0,0001512 |
0,3256 |
|
|
4,9229E-05 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
Толуол |
0,0000535 |
0,3286 |
|
|
1,7582E-05 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
2-метилгептан |
0,0000731 |
0,272 |
|
|
1,9893E-05 |
|
||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
Сумма |
|
|
|
|
0,02930948 |
|
||
|
|
|
|
|
|
|
|
|
Значение молярной теплоты сгорания идеального газа, определяемое исходя из значений молярной доли компонентов смеси известного состава, при температуре t1 вычисляют по формуле:

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
̅0 |
( ) |
|
|
̅̅̅0 |
( )], |
|
|
|
|
|||
|
|
|
|
|
|
= ∑[ ∙ |
|
|
|
|
|
||||||
|
|
|
|
|
|
1 |
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
=1 |
|
|
|
|
|
|
|
|
|
где |
̅0 |
( 1) |
— значение идеальной теплоты сгорания смеси (высшей или низшей); |
|
|||||||||||||
|
|
||||||||||||||||
— молярная доля j-го компонента; |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
̅̅̅0 |
( ) — значение идеальной теплоты сгорания j-го компонента (высшей или низшей). |
||||||||||||||||
|
|||||||||||||||||
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Значения молярной теплоты сгорания компонентов природных газов при |
||||||||||||||||
температуре измерения 20 и результаты расчетов приведены в таблице 6. |
|
||||||||||||||||
|
|
|
|
|
|
|
|
Таблица 6 – Расчет молярной теплоты сгорания |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
Молярная теплота |
|
|
|
|
|
|
Идеальная теплота сгорания |
|||||
Название |
|
Средняя молярная |
сгорания компонента, |
|
|
|
xj*Hj |
|
смеси, кДж/моль |
||||||||
|
доля компонента, xj |
|
кДж/моль |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
Высшая |
|
Низшая |
|
|
Высшая |
Низшая |
Высшая |
|
Низшая |
|||
Кислород |
|
|
0,0003624 |
|
- |
|
- |
|
|
|
0 |
|
0 |
|
|
|
|
Азот |
|
|
|
0,021795 |
|
- |
|
- |
|
|
|
0 |
|
0 |
|
|
|
Диоксид углерода |
|
0,02573 |
|
- |
|
- |
|
|
|
0 |
|
0 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Этан |
|
|
|
0,04856 |
1561,41 |
|
1428,74 |
|
|
|
75,82 |
|
69,38 |
|
|
|
|
Пропан |
|
|
|
0,06808 |
2220,13 |
|
2043,23 |
|
|
151,15 |
|
139,10 |
|
|
|
||
и-Бутан |
|
|
|
0,0192 |
2869,38 |
|
2648,26 |
|
|
|
55,09 |
|
50,85 |
|
|
|
|
н-Бутан |
|
|
|
0,028285 |
2878,57 |
|
2657,45 |
|
|
|
81,42 |
|
75,17 |
|
|
|
|
нео-Пентан |
|
|
0,000052475 |
3516,01 |
|
3250,67 |
|
|
|
0,18 |
|
0,17 |
|
|
|
||
и-Пентан |
|
|
0,008913 |
3530,24 |
|
3264,89 |
|
|
|
31,47 |
|
29,10 |
|
|
|
||
н-Пентан |
|
|
0,0071615 |
3537,17 |
|
3271,83 |
|
|
|
25,33 |
|
23,43 |
|
|
|
||
Циклопентан |
|
|
0,0005056 |
3320,88 |
|
3099,76 |
|
|
|
1,68 |
|
1,57 |
|
|
|
||
2, 2 диметилбутан |
|
0,000002613 |
4179,15 |
|
3869,59 |
|
|
|
0,01 |
|
0,01 |
449,9634621 |
|
407,9957892 |
|||
2, 3 диметилбутан + |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
изогексан (2- |
|
|
|
8375,88 |
|
7756,75 |
|
|
|
8,93 |
|
8,27 |
|
|
|
||
метилпентан) |
|
|
0,00106615 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
н-Гексан |
|
|
0,0011879 |
4196,58 |
|
3887,01 |
|
|
|
4,99 |
|
4,62 |
|
|
|
||
Бензол + |
|
|
|
37256,62 |
|
6858,61 |
|
|
|
8,87 |
|
1,63 |
|
|
|
||
циклогексан |
|
|
0,00023795 |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
2-метилгексан |
|
0,000042725 |
4608,32 |
|
4387,20 |
|
|
|
0,20 |
|
0,19 |
|
|
|
|||
3-метилгексан |
|
0,00063995 |
5264,98 |
|
4911,19 |
|
|
|
3,37 |
|
3,14 |
|
|
|
|||
н-Гептан |
|
|
0,000031045 |
4855,29 |
|
4501,49 |
|
|
|
0,15 |
|
0,14 |
|
|
|
||
Метилциклогексан |
|
0,000151195 |
4602,35 |
|
4292,78 |
|
|
|
0,70 |
|
0,65 |
|
|
|
|||
Толуол |
|
|
|
0,000053505 |
3948,84 |
|
3771,95 |
|
|
|
0,21 |
|
0,20 |
|
|
|
|
2-метилгептан |
|
0,000073135 |
5567,86 |
|
5212,14 |
|
|
|
0,41 |
|
0,38 |
|
|
|
|||
Значение теплоты сгорания идеального газа, рассчитанное на основе значений объемной доли компонентов, для температуры сгорания t1, смеси известного состава, измеренных при температуре t2 и давлении р2, вычисляют по формуле:
̃0[ 1, ( 2, 2)] = ̅0( 1) ∙ ∙2 2
Где R – универсальная газовая постоянная;
Т2 = (t2 + 273,15) – абсолютная.
Тогда идеальная высшая объемная теплота сгорания смеси:
449,9634621 |
101,325 |
|
= 18,706 |
|
8,314 293,15 |
||||
|
|
|||

Идеальная низшая объемная теплота сгорания смеси:
407,9957892 |
101,325 |
|
= 16,96 |
|
8,314 293,15 |
||||
|
|
|||
Значение объемной теплоты сгорания газа для температуры сгорания смеси известного состава, объемная доля компонентов которой измерена при температуре t2 и давлении р2, вычисляют по формуле:
̃ |
̃0 |
[1, (2, 2)] |
|||
|
|
||||
[1, (2, 2)] = |
|
|
|
|
|
|
|
( |
, ) |
||
|
|
|
|
2 |
2 |
Где Zmix – коэффициент сжимаемости смеси при стандартных условиях измерений. Тогда идеальная высшая объемная теплота сгорания смеси:
0,9991409518,706 = 18,722
Идеальная низшая объемная теплота сгорания смеси:
0,9991409516,96 = 16,974
2. Вычисление плотности, относительной плотности и числа Воббе
Согласно представленному стандарту относительную плотность реального газа вычисляют по формуле:
( , ) = 0 ∙ ( , )( , )
Где ( , ) - относительная плотность реального газа;
( , ) - коэффициент сжимаемости газа.
( , )- коэффициент сжимаемости сухого воздуха стандартного состава; Относительная плотность идеального газа не зависит от выбора стандартного
состояния, и ее вычисляют по формуле:
0 = ∑ ∙
=1
Где 0- относительная плотность идеального газа;- молярная масса j-го компонента;
- молярная масса сухого воздуха стандартного состава.
В разделе В.3 (приложение В) соответствующего стандарта приведен состав стандартного воздуха; рассчитанное значение Mair равно 28,9626 кг·кмоль-1.
Коэффициент сжимаемости ( , ) вычисляют по формуле, с использованием значений коэффициентов суммирования √b, приведенных для индивидуальных чистых веществ в таблице 2 (раздел 10) данного стандарта. Коэффициент сжимаемости ( , ) приведен в разделе В.3 (приложение В):
