
пример выполнения ИЗ-1
.pdfТитульный лист материалов по дисциплине
|
Организация |
научно-исследовательской |
ДИСЦИПЛИНА |
деятельности (ОНИД) |
|
|
|
|
|
(полное наименование дисциплины без сокращений) |
|
ИНСТИТУТ |
ИТХТ имени М.В. Ломоносова |
|
КАФЕДРА |
|
|
Физической химии им. Я.К. Сыркина |
||
|
|
|
|
полное наименование кафедры |
|
ВИД |
9. Дополнительно |
|
УЧЕБНОГО |
|
|
|
|
|
МАТЕРИАЛА |
(в соответствии с пп.1-11) |
|
|
|
|
ПРЕПОДА- |
|
|
ВАТЕЛЬ |
Пестов Сергей Михайлович |
|
|
|
|
|
(фамилия, имя, отчество) |
|
СЕМЕСТР |
1, 2024/2025 учебный год |
|
|
|
|
|
(указать семестр обучения, учебный год) |
|

МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
Федеральное государственное бюджетное образовательное учреждение
высшего образования
«МИРЭА – Российский технологический университет» РТУ МИРЭА
Институт тонких химических технологий имени М.В. Ломоносова
Организация научно-исследовательской деятельности
Домашнее задание ИЗ–1
Вариант №35
Выполнил(а): студент(ка) группы Х_МО-00-24
Иванов И.И.
Проверил: проф., д.х.н.
Пестов С.М.
Москва 2024
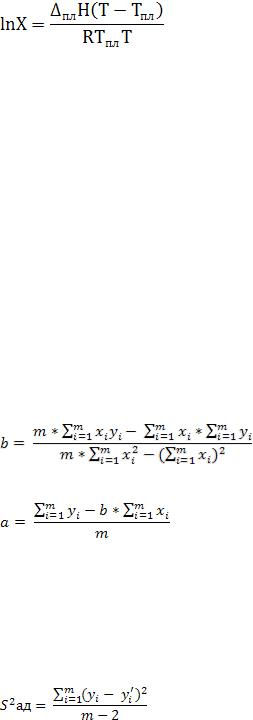
Задание 1. Рассчитайте энтальпию плавления (растворения) для
растворенного вещества и оцените погрешность ее определения
В рамках модели идеальных растворов для расчета растворимости используют уравнение Шредера:
или
ln x = Нопл./R * (1/Tопл. - 1/Т)
x – мольная доля растворенного вещества в насыщенном растворе при температуре Т; R = 8.314 Дж / (моль К) – универсальная газовая постоянная;
и Нопл. – температура и энтальпия плавления чистого вещества.
Это уравнение представляет собой линейную зависимость натурального логарифма мольной доли компонента (х) от обратной температуры (в К-1)
ln x = А – В / Т
Y = a + b X, a и b - константы
a = Нопл./(R Tопл.), b = - Нопл. / R
Значение коэффициента b позволяет рассчитать энтальпию плавления Нопл.
Формулы для расчета коэффициентов а и b:
m – количество экспериментальных точек.
Расчет удобно проводить с использованием программы Excel.
Оценить линейную зависимость Y (X) можно по коэффициенту корреляции rxy .
Перейдем к расчету погрешности определения энтальпии плавления.
Вычисление дисперсии адекватности модели:
yi и yi´ – экспериментальные и расчетные значения Вычисление дисперсий Sa2 и Sb2 для коэффициентов а и b:
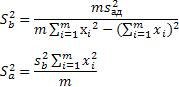
Расчет погрешности для коэффициентов a и b:
a= ±t(α=0,95; m-1) * Sa
b= ±t(α=0,95; m-1) * Sb
t ,f – критерий Стьюдента, f = m-1 - число степеней свободы
Расчет погрешности для энтальпии
H = |
b * R |
|
|
Ответ: |
H ± H |

ВАРИАНТ
Рассмотрим расчет энтальпии плавления салициловой кислоты по данным растворимости в гептане
Таблица 1. Исходные данные для расчета энтальпии плавления
T, K |
x1 |
|
|
365,4 |
0,0152 |
|
|
385,6 |
0,0395 |
|
|
397,9 |
0,0765 |
|
|
407,5 |
0,155 |
|
|
415,2 |
0,341 |
|
|
418,7 |
0,523 |
|
|
422,7 |
0,760 |
|
|
Вопрос: сколько значащих цифр в исходных данных?
В ответе никогда не будет больше значащих цифр!
Таблица 2. Исходные данные и массивы Y (X)
T, K |
x1 |
Х = 1/T, K-1 |
Y = lnx1 |
||
|
|
|
|
|
|
365,4 |
0,0152 |
0,002737 |
-4,18 |
646 |
|
|
|
|
|
|
|
385,6 |
0,0395 |
0,002593 |
-3,23 |
145 |
|
|
|
|
|
|
|
397,9 |
0,0765 |
0,002513 |
-2,57046 |
|
|
|
|
|
|
|
|
407,5 |
0,155 |
0,002454 |
-1,86433 |
|
|
|
|
|
|
|
|
415,2 |
0,341 |
0,002408 |
-1,07587 |
|
|
|
|
|
|
|
|
418,7 |
0,523 |
0,002388 |
-0,64817 |
|
|
|
|
|
|
|
|
422,7 |
0,760 |
0,002366 |
-0,27444 |
|
|
|
|
|
|
|
|
Получаем уравнение Y = -10528Х + 24,281 (коэффициент корреляции R2 = 0,952), по
которому найдем значение энтальпии:
Hпл. = 10528•8,314 = 87529 Дж моль-1 = 87,5 кДж моль-1

Рисунок 1. Зависимость растворимости салициловой кислоты в
гептане от температуры
 Должны быть обозначения осей, масштаб, размерность
Должны быть обозначения осей, масштаб, размерность
Таблица 3. Экспериментальные и рассчитанные значения lnx1
1/T, K-1 |
Y = lnx1 |
lnx1 (расч) |
|
|
|
0,002737 |
-4,186 |
-4,531 |
|
|
|
0,002593 |
-3,231 |
-3,022 |
|
|
|
0,002513 |
-2,570 |
-2,178 |
|
|
|
0,002454 |
-1,864 |
-1,555 |
|
|
|
0,002408 |
-1,076 |
-1,075 |
|
|
|
0,002388 |
-0,648 |
-0,863 |
|
|
|
0,002366 |
-0,274 |
-0,626 |
|
|
|
значащие цифры Вычислим дисперсию для проверки адекватности данных:
Sад2 = ? Sад = ?
 Вычисление дисперсий Sa2 и Sb2 для коэффициентов а и b:
Вычисление дисперсий Sa2 и Sb2 для коэффициентов а и b:

Sb = ? Sb2 = ?
Sa = ? Sa2 = ?
Вычислим дисперсии Sa2и Sb2: и рассчитаем |
a и b: |
Расчет погрешности для коэффициентов a и |
b: |
a = ±t(α=0,95; m-1) * Sa |
|
b = ±t(α=0,95; m-1) * Sb |
|
t ,f – критерий Стьюдента, f = m-1 - число степеней свободы
а = ?
b = ±t(α=0,95; m-1) * Sb
Расчет погрешности для энтальпии
H = |
b * R |
|||
H = 2586, |
|
= 2,6*103 |
||
084 |
||||
|
|
|||
Ответ: |
H ± H |
|
||
Выводы: сравнить с лит. данными
справочник, сайт NIST
//webbook.nist.gov
