
- •1. Мембранные технологии, их использование в биотехнологии.
- •1. Пластинчатый диализатор
- •2. Диализатор типа «фильтр-пресс»
- •2. Роль мембранных технологий в очистке генно-инженерных белков.
- •1. Ультрафильтрация
- •2. Диализ
- •3. Электродиализ
- •3. Предложить вариант мембранной технологии для концентрирования большого количества раствора генно-инженерного белка
- •1. Ультрафильтрация: Первичный этап концентрирования
- •2. Диализ: Удаление остаточных солей и буферных компонентов
- •3. Электродиализ: Регулировка ионного состава
- •4. Центрифугирование, основные методы.
- •1. Этапы применения центрифугирования
- •1.1. Удаление клеточного мусора (клеточный лизат)
- •1.2. Концентрация белка
- •Тип ротора:
- •Условия центрифугирования:
- •Особенности
- •Виды колориметрии
- •Пример работы фотоколориметра
- •Строение и принцип работы спектрофотометра на диодной матрице:
- •Преимущества и особенности:
- •1. Поглощение белков в уф-области
- •2. Поглощение нуклеиновых кислот (нк) в уф-области
- •3. Изобестическая точка
- •Применение в бт:
- •1. Ультрафиолетовая видимая спектроскопия (uv-Vis)
- •1. Источник инфракрасного излучения
- •2. Монохроматор
- •3. Оптическая система
- •4. Образец
- •5. Приемники излучения
- •Принцип работы
- •Особенности и преимущества Фурье-ик-спектрометра
- •1. Инфракрасная (ик) спектроскопия Описание метода:
- •Применяемые техники:
- •Применение:
- •2. Раман-спектроскопия (спектроскопия комбинационного рассеяния) Описание метода:
- •Применяемые техники:
- •3. Спектроскопия комбинационного рассеяния ближнего ик-диапазона (nir-спектроскопия)
- •Применение флуоресценции в биотехнологии
- •Тушение флуоресценции
- •Иммунофлуоресценция
- •Основные элементы устройства
- •Импульсные спектрометры с преобразованием Фурье (ft-nmr)
- •Основные этапы maldi масс-спектрометрии:
- •1. Время удерживания:
- •2. Время удерживания несорбируемого компонента или мертвое время:
- •3. Мертвый объём
- •4. Фактор удерживания к (коэффициент ёмкости)
- •5. Селективность (α):
- •6. Эффективность - число теоретических тарелок
- •7. Высота теоретической тарелки (h):
- •8. Пиковая емкость колонки
- •9. Разрешение Rs:
- •10. Фактор асимметрии для Асимметричные пики («с хвостом»)
- •1. Экстракция водорастворимых биологически активных соединений
- •2. Экстракция жирорастворимых биологически активных соединений
- •1. Лиофильные сушилки (фриз-драйеры)
- •Принцип действия:
- •2. Ротационные испарители
- •3. Сушильные шкафы
- •2. Спрей-сушилки (распылительные сушилки)
- •3. Вакуумные сушилки Принцип действия:
- •Применение:
- •1) Источники питания
- •38.Сравнительный анализ хроматографических и электрофоретических задач в биотехнологии.
- •2. Типы анализируемых веществ:
- •5. Оборудование и сложность:
- •40. Капиллярный электрофорез, особенности и достоинства метода в сравнении с планарным электрофорезом.
Импульсные спектрометры с преобразованием Фурье (ft-nmr)
Основной принцип: генерация коротких радиочастотных импульсов, которые возбуждают ядерные спины. Сигнал свободной индукции (FID) преобразуется в частотный спектр с использованием преобразования Фурье.
Преимущества:
Высокое разрешение.
Быстрая запись спектров.
Возможность анализа сложных образцов.
Используются современные высокопольные магниты (сверхпроводящие магниты).
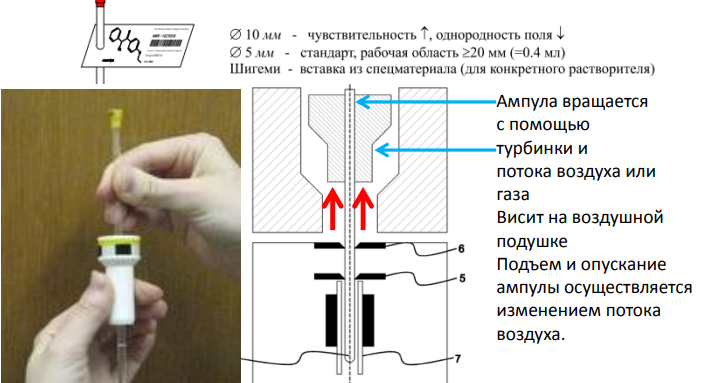
Основные параметры спектров ЯМР высокого разрешения.
Количество сигналов => количество неэквивалентных ядер данного типа.
Положение сигналов (химический сдвиг) => распределение электронной плотности по молекуле.
Форма сигналов (спиновое расщепление) = тип и количество соседних ядер, конформационные эффекты.
Площадь сигналов (интенсивность)-> количество магнитно эквивалентных ядер, давших сигнал
Химические сдвиги, δ м.д. |
Тип структурного фрагмента, относительная электронная плотность. |
Интенсивность сигнала, I |
Количество ядер данного типа в молекуле (концентрация) |
Константы косвенного спин- спинового взаимодействия, J, (Гц) |
Тип структурного фрагмента, стереохимия |
Константы прямого диполь-дипольного взаимодействия, D (Гц) |
Межатомные расстояния, валентные и двугранные углы |
Времена релаксации Т1 Т2 |
Динамические параметры , геометрические параметры |
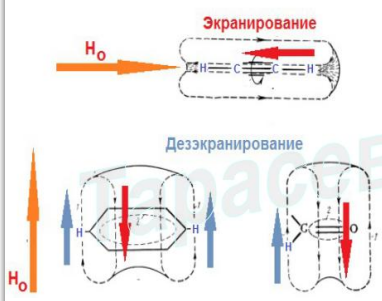
Экранирование и дезэкранирование магнитных ядер электронами в молекулах. Химический сдвиг.
Во внешнем магнитном поле движущиеся электроны порождают локальные магнитные поля (правило Ленца), которые могут экранировать или дезэкранировать ядра
σ- константа экранирования.
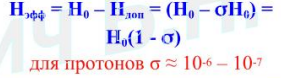
Величина определяется электронной плотностью около ядра и распределением электронной плотности в соседних структурных фрагментах. Поскольку значения электронной плотности в различных частях молекулы разные, ядра одного типа, находящиеся в химически неэквивалентных положениях в молекуле дают различные сигналы. Это явление называется химический сдвиг.
Измерение химического сдвига.
•Степень экранирования зависит от электронной плотности вокруг атома => значение резонансной частоты конкретного ядра зависит от молекулярной структуры.
•Химический сдвиг δ - основная характеристика атома (группы экв. атомов), входящих в состав молекулы, представляющая собой разность между резонансными частотами ядра и стандарта:

ТМС (тетраметилселан) ОБЫЧНО ДОБАВЛЯЮТ В КАЧЕСТВЕ ВНУТРЕННЕГО СТАНДАРТА К КАЖДОМУ ОБРАЗЦУ ПЕРЕД РЕГИСТРАЦИЕЙ СПЕКТРА ЕСЛИ ТМС ПРИМЕНИТЬ НЕЛЬЗЯ (НАПРИМЕР, ТМС НЕ РАСТВОРЯЕТСЯ В ВОДЕ), ДОБАВЛЯЮТ ДРУГОЕ ВЕЩЕСТВО СРАВНЕНИЯ И ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ ПРЕОБРАЗУЮТ К ШКАЛЕ ТМС.
Факторы, определяющие химические сдвиги сигналов в спектрах ЯМР.
1. Электронная плотность на измеряемом ядре.
2. Влияние магнитных полей, возникающих за счет соседних анизотропных групп. Наиболее ярко оно проявляется в спектроскопии ЯМР-1Н (эффекты «кольцевого тока» в ароматических соединениях).
3. Образование водородных связей и координационных связей, в том числе эффекты сольватации.
Магнитно эквивалентными мы называем такие ядра, которые имеют одну и ту же резонансную частоту и общее для всех характеристическое значение константы спин-спинового взаимодействия с ядрами любой соседней группы. Ядра с одинаковой резонансной частотой называют изохронными. Часто они и химически эквивалентны, т.е. имеют одинаковое химическое окружение. Однако химически эквивалентные ядра не обязательно являются магнитно эквивалентными.
Спин-спиновое взаимодействие возникает за счет магнитного взаимодействия между отдельными протонами, которое передается через спиновые состояния электронов химических связей, косвенно соединяющих эти протоны.
Величины J (констана спин-спинового взаимодействия) зависят от :
Природы взаимодействующих ядер
Числа и характера разделяющих эти ядра химических связей.
Стереохимии всей цепочки, по которой передается взаимодействие.
Электронных свойств заместителей в молекуле.
На них также оказывают заметное влияние сольватационные эффекты.
Константы J могут быть положительными и отрицательными. Константы через нечетное число связей, в своем большинстве, положительны.
Константы через четное число связей могут иметь любой знак.
Вид спектров первого порядка не зависит от знака J.
Правила мультиплетности
1. Мультиплетность рассчитывается по уравнению: М = n + 1 (I = 1/2) M = 2nI + 1 (I 1)
2. Интенсивности сигналов внутри мультиплетов можно рассчитать с помощью треугольника паскаля
3. Взаимодействия эквивалентных ядер в спектре наблюдать нельзя
4. Константы спин-спинового взаимодействия j не зависят от магнитной индукции Bo и выражаются в гц
5. В насыщенных соединениях взаимодействия между протонами, разделёнными более чем тремя связями, обычно очень незначительны и в спектре не проявляются
Правило (n+1) для протонов в спектрах первого порядка. Число компонент мультиплета:
2nI+1, n - число атомов, с которыми происходит взаимодействие, I - спиновое квантовое число.
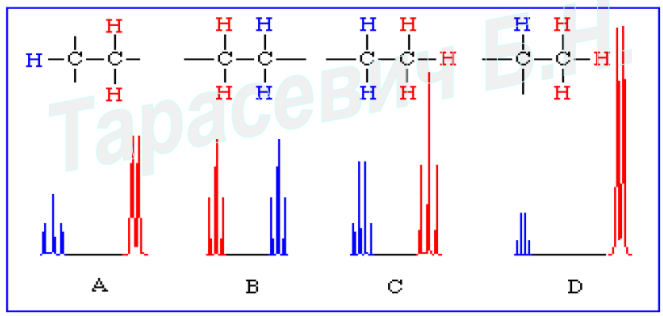
14. Методы расшифровки спектров первого и более высоких порядков. ( Не отредактировано, нет сил)
Основные параметры спектров ЯМР высокого разрешения.
Количество сигналов => количество неэквивалентных ядер данного типа.
Положение сигналов (химический сдвиг) => распределение электронной плотности по молекуле.
Форма сигналов (спиновое расщепление) = тип и количество соседних ядер, конформационные эффекты.
Площадь сигналов (интенсивность)-> количество магнитно эквивалентных ядер, давших сигнал
Химические сдвиги, δ м.д. |
Тип структурного фрагмента, относительная электронная плотность. |
Интенсивность сигнала, I |
Количество ядер данного типа в молекуле (концентрация) |
Константы косвенного спин- спинового взаимодействия, J, (Гц) |
Тип структурного фрагмента, стереохимия |
Константы прямого диполь-дипольного взаимодействия, D (Гц) |
Межатомные расстояния, валентные и двугранные углы |
Времена релаксации Т1 Т2 |
Динамические параметры , геометрические параметры |
Во внешнем магнитном поле движущиеся электроны порождают локальные магнитные поля (правило Ленца), которые могут экранировать или дезэкранировать ядра
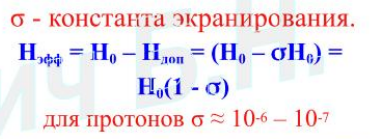
Величина о определяется электронной плотностью около ядра и распределением электронной плотности B соседних структурных фрагментах. Поскольку значения электронной плотности Б различных частях молекулы разные, ядра одного типа, находящиеся в химически неэквивалентных положениях в молекуле дают различные сигналы. Это явление называется химический сдвиг.
Измерение положения сигналов в спектрах ЯМР. Что такое миллионные доли?
С учетом экранирования Ѵο = Ηο(1 - σ), в спектрах одного и того же соединения, записанных на приборах с разными напряженностями полей магнитов Ho значения резонансных частот линий будут разными. Такие спектры трудно сравнивать. Преодолеть эту трудность можно, если разделить значения резонансных частот на рабочую частоту прибора. Для удобства перед измерением спектра в образец добавляют небольшое количество эталонного соединения. Для спектров ЯМР-Н И ЯМР-13С это тетраметилсилан (TMC, Si(CH3)4). Соединение устойчиво, инертно химически, дает сильный и узкий сигнал (12 эквивалентных протонов) на краю спектра, легко удаляется (т.кип. 27° С). (На рис. рабочая частота прибора 60 МГц)
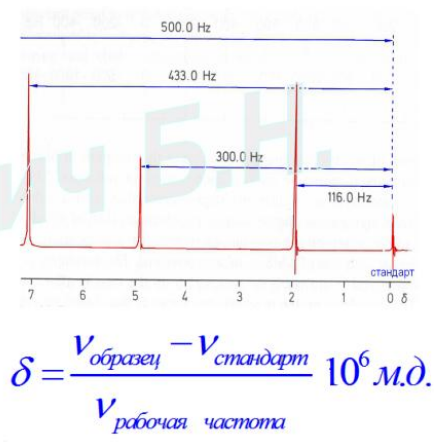
Измерение химического сдвига.
•Степень экранирования зависит от электронной плотности вокруг атома значение резонансной частоты конкретного ядра зависит от молекулярной структуры.
• Химический сдвиг б - основная характеристика атома (группы экв. атомов), входящих B состав молекулы, представляющая собой разность между резонансными частотами ядра и стандарта:

•Сигнал Н в СН3ОСН3 отстоит от сигнала ТМС на 228 Гц при Но = 1,41 Тс и = 60 МГц. Тогда:
![]()
ТМС ОБЫЧНО ДОБАВЛЯЮТ В КАЧЕСТВЕ ВНУТРЕННЕГО СТАНДАРТА К КАЖДОМУ ОБРАЗЦУ ПЕРЕД РЕГИСТРАЦИЕЙ СПЕКТРА ЕСЛИ ТМС ПРИМЕНИТЬ НЕЛЬЗЯ (НАПРИМЕР, ТМС НЕ РАСТВОРЯЕТСЯ В ВОДЕ), ДОБАВЛЯЮТ ДРУГОЕ ВЕЩЕСТВО СРАВНЕНИЯ И ПОЛУЧЕННЫЕ РЕЗУЛЬТАТЫ ПРЕОБРАЗУЮТ К ШКАЛЕ ТМС.
Влияние рабочей частоты прибора на разрешение сигналов в спектрах.
Спектры ЯМР 1Н ди(хлорэтилового) эфира в CDCI3, зарегистрированные на приборах с рабочими частотами 60 (a), 300 (6), 600 МГц (в).
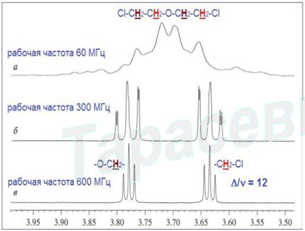
На частоте 600 МГц спектр состоит из двух простых триплетов первого порядка. На частоте 300 МГц происходит некоторое возмущение спектра, и в нем появляется несколько слабых дополнительных линий. На частоте 60 МГц сигналы с очевидностью перекрываются, и появляются дополнительные линии. (Совмещение растянутых мультиплетов возможно потому, что во всех спектрах использовалась 6-шкала.) Отношение Дѵ/J составляет 12 при 600 МГц (бесспорно, спектр первого порядка), 6 при 300 МГц (еще легко распознается спектр первого порядка, если пренебречь дополнительными расщеплениями). На частоте 60 МГц перекрывание мультиплетов и появление дополнительных линий описывается как возмущения «более высокого» (чем первый) порядка. Резюме: Таким образом, с ростом рабочей частоты увеличивается способность различать сигналы с близкими химическими сдвигами.
Магнитная эквивалентность ядер
Ядра химически эквивалентны, если они занимают в молекулах одинаковые структурные положения. Такие ядра имеют одинаковые химические сдвиги. Однако такие ядра магнитно неэквивалентны, если константы спин-спинового взаимодействия у них с любым третьим ядром в данной системе различны.
Влияние электроотрицательности заместителя на химический сдвиг сигналов протонов в CH3Hal. Индуктивный эффект галогенов. Смещение сигналов в слабые поля.
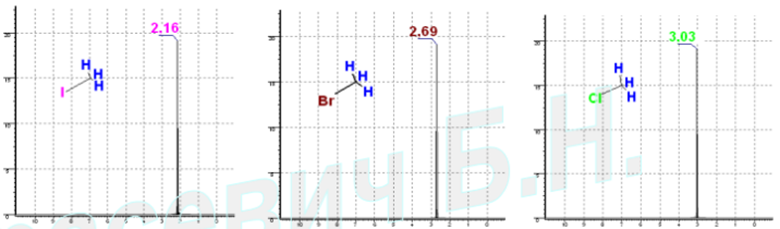
Факторы, определяющие химические сдвиги сигналов в спектрах ЯМР.
1. Электронная плотность на измеряемом ядре.
2. Влияние магнитных полей, возникающих за счет соседних анизотропных групп. Наиболее ярко оно проявляется в спектроскопии ЯМР-Н (эффекты «кольцевого ток тока» в ароматических соединениях).
3. Образование водородных связей И координационных связей, в том числе эффекты сольватации.
Магнитно эквивалентными мы называем такие ядра, которые имеют одну и ту же резонансную частоту и общее для всех характеристическое значение константы спин-спинового взаимодействия с ядрами любой соседней группы. Ядра C одинаковой резонансной частотой называют изохронными. Часто они и химически эквивалентны, т.е. имеют одинаковое химическое окружение. Однако химически эквивалентные ядра не обязательно являются магнитно эквивалентными.
Константа спин-спинового взаимодействия
Спин-спиновое взаимодействие возникает за счет магнитного взаимодействия между отдельными протонами, которое передается через спиновые состояния электронов химических связей, косвенно соединяющих эти протоны.
Константа спин-спинового взаимодействия
Величины Ј зависят от :
Природы взаимодействующих ядер
Числа и характера разделяющих эти ядра химических связей.
Стереохимии всей цепочки, по которой передается взаимодействие.
Электронных свойств заместителей в молекуле.
На них также оказывают заметное влияние сольватационные эффекты.

Типы констант спин-спинового взаимодействия (J)

Знаки констант спин-спинового взаимодействия • Константы спин-спинового взаимодействия могут быть как положительными, так и отрицательными
Константы J могут быть положительными и отрицательными.
Константы через нечетное число связей, в своем большинстве, положительны.
Константы через четное число связей могут иметь любой знак.
Вид спектров первого порядка не зависит от знака J.
Константа взаимодействия j, в отличие от химического сдвига, не зависит от магнитной индукции и всегда выражена в Гц. Химический сдвиг всегда соответствует середине сигнала.
Правила мультиплетности
1.Мультиплетность рассчитывается по уравнению: М = n + 1 (I = 1/2) M = 2nI + 1 (I=1)
2. Интенсивности сигналов внутри мультиплетов можно рассчитать с помощью треугольника паскаля
3. Взаимодействия эквивалентных ядер в спектре наблюдать нельзя
4. Константы спин-спинового взаимодействия j не зависят от магнитной индукции Bo и выражаются в гц
5. В насыщенных соединениях взаимодействия между протонами, разделёнными более чем тремя связями, обычно очень незначительны и в спектре не проявляются
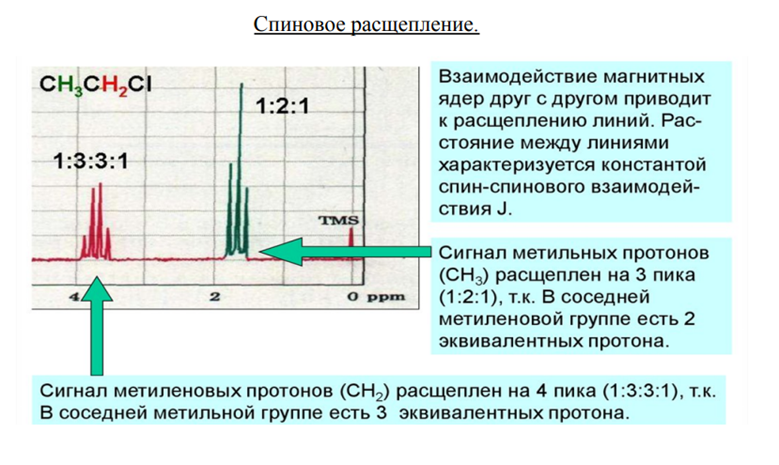
Правило (n+1) для протонов в спектрах первого порядка.
Число компонент мультиплета:
2n/+1, п – число атомов, с которыми происходит взаимодействие, - / - спиновое квантовое число.
Спектры первого порядка: Av/J ≥ 6
1. Расщепление сигнала данного протона происходит на соседних протонах, число компонент мультиплетов равно п+1, где n число соседних эквивалентно взаимодействующих протонов, на которых происходит расщепление.
2. Относительные интенсивности линий в мультиплете определяются из треугольника Паскаля.
Номенклатура Попла для спиновых систем.
Если отношение Дѵ/J достаточно велико, мультиплеты рассматриваются как хорошо разделенные (а взаимодействующие группы ядер как слабо связанные); тогда результирующая спиновая система обозначается буквами алфавита, далеко отстоящими друг от друга, например АХ. Если это отношение невелико, используют набор близких букв алфавита, например АВ. Если три ядра слабо взаимодействуют между собой, то они обозначаются буквами АМХ. Число ядер в группе обозначается нижним индексом.
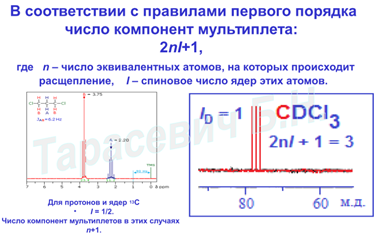
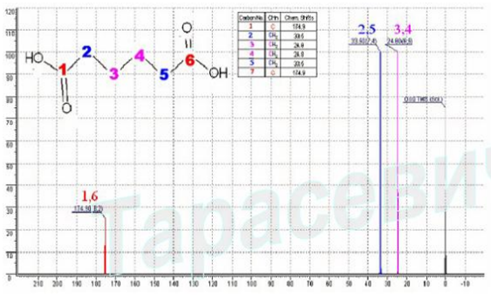
Подавление спин-спинового взаимодействия (развязка от протонов) в спектре ЯМР 13C гександиовой кислоты.
КОНСТАНТЫ СПИН-СПИНОВОГО ВЗАИМОДЕЙСТВИЯ ЗАПИСЫВАЮТ ПРИ ПОМОЩИ СТАНДАРТНОЙ СИСТЕМЫ ОБОЗНАЧЕНИЙ, КОТОРАЯ УКАЗЫВАЕТ ВЗАИМОДЕЙСТВУЮЩИЕ ЯДРА И КОЛИЧЕСТВО СВЯЗЕЙ МЕЖДУ НИМИ.
1J – ЯДРА ВЗАИМОДЕЙСТВУЮЩИХ АТОМОВ СВЯЗАНЫ ДРУГ С ДРУГОМ (Н2 )
2J – ОБОЗНАЧАЕТ ГЕМИНАЛЬНОЕ ВЗАИМОДЕЙСТВИЕ
3J – ВИЦИНАЛЬНОЕ ВЗАИМОДЕЙСТВИЕ
3+nJ – «ДАЛЬНЕЕ» ВЗАИМОДЕЙСТВИЕ
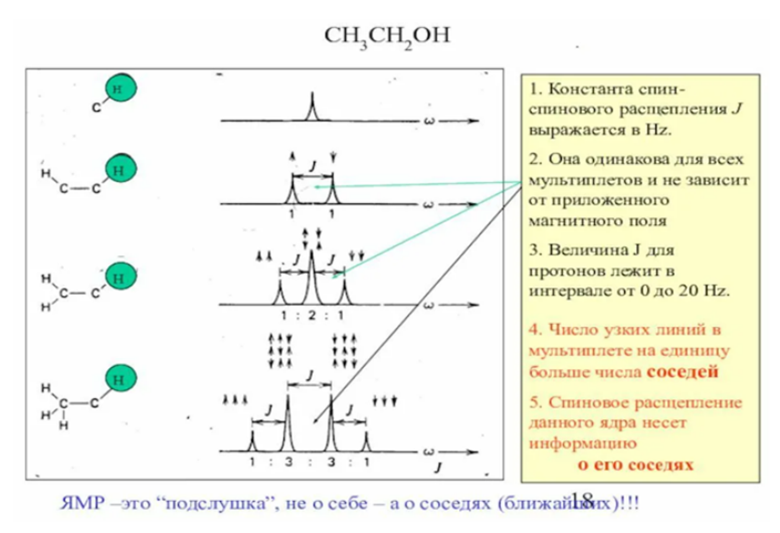
Эффект крыши. Эффект крыши - изменение относительной интенсивности линий в мультиплете из-за взаимного влияния энергетических состояний взаимодействующих ядер, это изменение может быть рассчитано квантово-химическими методами, а для простейшей AB-системы есть даже графический метод - при помощи циркуля и линейки. Эффект можно предвидеть, рассчитать, использовать для отнесения и описания спектров. Эффект сильнее для сильно-связанных систем с близкими хим.сдвигами магнитных ядер, с увеличением рабочей частоты он становится менее заметным.

15.Современные методы ЯМР. Двумерная спектроскопия ЯМР: корреляционная спектроскопия (COSY). (Еще потом добавлю и отредактирую)
1. Многомерная ЯМР-спектроскопия:
* Принцип работы: Основана на корреляции сигналов ядер в разных измерениях. Пульсовые последовательности создают когерентность между спинами, позволяя наблюдать взаимодействие через связи (J-coupling) или пространство (NOE).
* Особенности: Различные типы экспериментов (COSY, TOCSY, NOESY, HSQC, HMBC и др.) предоставляют специфическую информацию о структуре.
* Достоинства: Определение связности атомов, пространственной структуры, взаимодействий между молекулами.
* Недостатки: Сложная интерпретация, длительное время эксперимента, требует высокой концентрации образца.
* Область применения: Определение структуры органических молекул, биомолекул (белки, ДНК, РНК), изучение взаимодействий лиганд-рецептор.
COSY (COrrelation SpectroscopY) — это метод двумерной ЯМР-спектроскопии, используемый для изучения спин-спиновых взаимодействий между ядрами. Основное назначение COSY — выявление корреляций между протонами, которые находятся в ‘J‘−`J`-‘J‘−спиновом взаимодействии. Два измерения двухмерной ЯМР — две оси частот химических сдвигов. Каждая ось частот ассоциирована с одной или двумя временными переменными — длина эволюционного периода (эволюционное время) и время протекающее во время периода детекции (время детекции). Оба этих времени конвертируются из серии времени в серию частот посредством двухмерного преобразования Фурье.
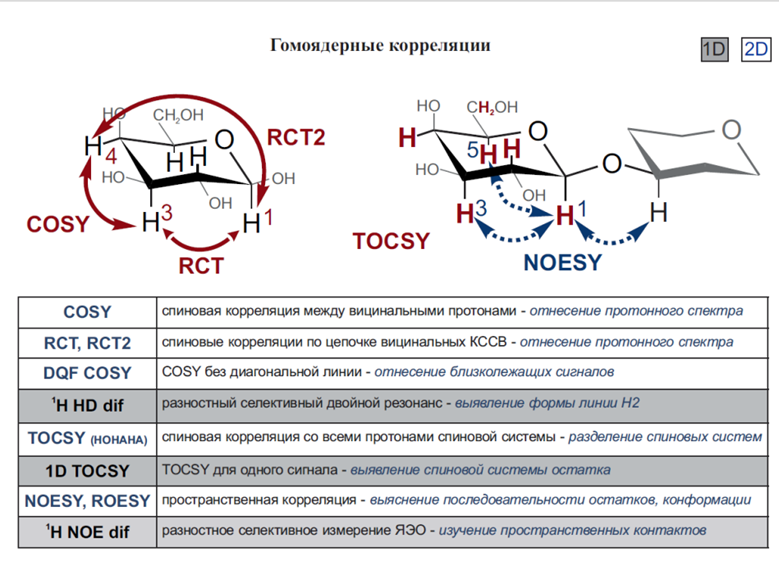
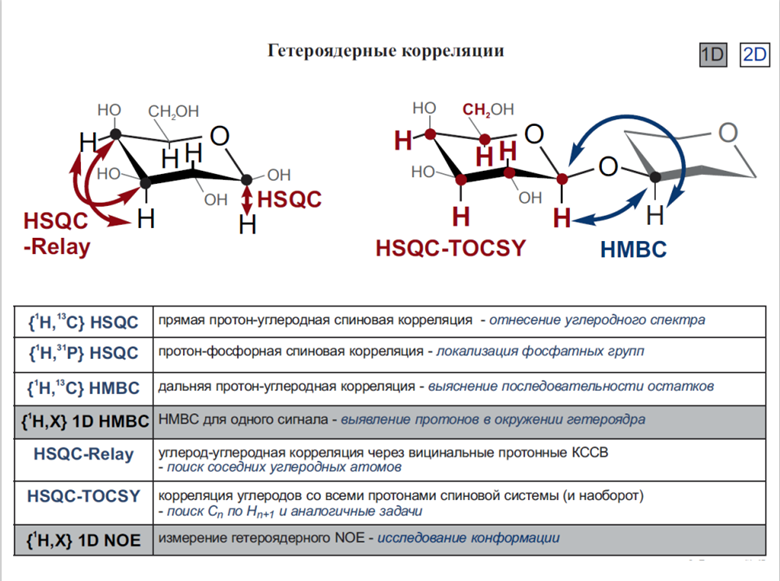
2. Гетероядерная ЯМР-спектроскопия:
* Принцип работы: Наблюдение ЯМР-сигналов ядер, отличных от 1H (например, 13C, 15N, 19F, 31P).
* Особенности: Часто используется в сочетании с многомерными экспериментами (HSQC, HMBC).
* Достоинства: Дополнительная структурная информация, изучение динамики молекул.
* Недостатки: Низкая чувствительность некоторых ядер (например, 13C, 15N), может требовать изотопного мечения.
* Область применения: Структурная биология, химия материалов, изучение метаболизма.
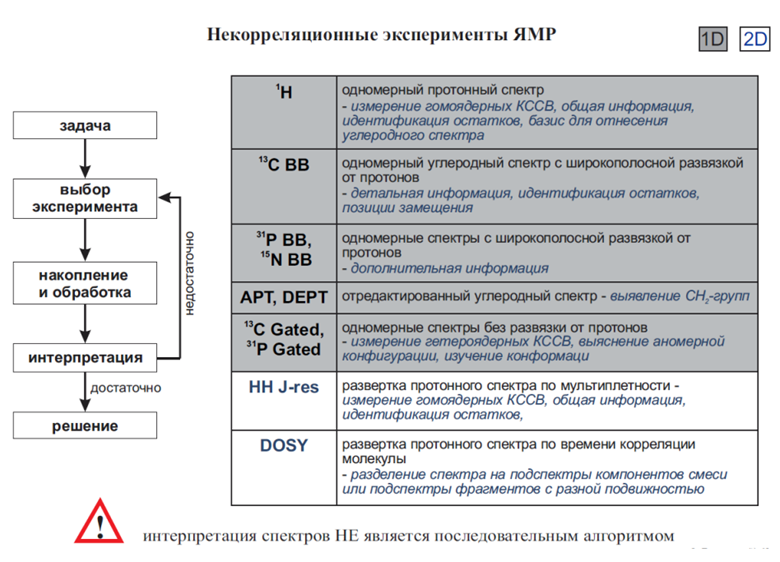
* 15N ЯМР:
* Особенности: 15N является спином 1/2, но имеет низкую природную распространенность (0.37%) и низкую чувствительность. Часто требуется изотопное мечение.
* Достоинства: Предоставляет важную информацию о структуре и динамике молекул, содержащих азот, таких как белки, пептиды и нуклеиновые кислоты.
* Недостатки: Низкая чувствительность, необходимость мечения.
* Примеры веществ: Белки, пептиды, нуклеиновые кислоты, амины, амиды.
* 31P ЯМР:
* Особенности: 31P является спином 1/2 и имеет 100% природную распространенность и относительно высокую чувствительность.
* Достоинства: Высокая чувствительность, нет необходимости в мечении.
* Недостатки: Ограниченная область применения.
* Примеры веществ: Фосфолипиды, нуклеотиды, фосфорилированные белки, фосфорорганические соединения.
3. ЯМР твердого тела:
* Принцип работы: Регистрация ЯМР-сигналов от образцов в твердом состоянии. Для преодоления анизотропных взаимодействий используются специальные техники, такие как вращение под магическим углом (MAS).
* Особенности: Позволяет изучать нерастворимые и аморфные материалы.
* Достоинства: Информация о структуре и динамике твердых тел.
* Недостатки: Более сложная аппаратура и интерпретация спектров.
* Область применения: Химия полимеров, материаловедение, фармацевтика.
4. ЯМР-микроскопия:
* Принцип работы: Получение пространственно-разрешенных ЯМР-спектров, позволяющих создавать изображения.
* Особенности: Разрешение зависит от напряженности магнитного поля и градиентных систем.
* Достоинства: Неразрушающий метод визуализации, информация о химическом составе и структуре.
* Недостатки: Ограниченное пространственное разрешение по сравнению с другими методами микроскопии.
* Область применения: Медицинская диагностика, изучение растений и животных, материаловедение.
5. Диффузионная ЯМР-спектроскопия (DOSY):
Диффузия молекул:
Молекулы в растворе движутся хаотично (диффундируют) из-за теплового движения. Скорость этого движения описывается коэффициентом диффузии (DDD), который зависит от размера молекулы, формы и взаимодействия с окружающей средой.
Импульсные градиенты магнитного поля:
В DOSY используются импульсные градиенты магнитного поля, которые создают локально изменяющееся магнитное поле.
Под действием градиента спины ядер в молекуле становятся зависимыми от их положения в пространстве.
Декогеренция сигналов:
Из-за диффузии молекулы перемещаются в пространстве, и их спиновые сигналы размываются. Чем быстрее движется молекула (более высокий DDD), тем сильнее ее сигнал ослабляется.
Двумерный спектр:
В результате DOSY формируется двумерный спектр:
Одна ось соответствует химическим сдвигам (δ\deltaδ) — как в обычном ЯМР.
Вторая ось соответствует коэффициентам диффузии (DDD)
* Достоинства: Информация о размерах и форме молекул, изучение взаимодействий.
* Недостатки: Требует специальных пульсовых последовательностей и обработки данных.
* Область применения: Химия полимеров, супрамолекулярная химия, биохимия.
6. ЯМР релаксация:
* Принцип работы: Измерение времени релаксации ядерных спинов (T1, T2).
* Особенности: Информация о динамике молекул и взаимодействиях.
* Достоинства: Чувствительность к молекулярным движениям.
* Недостатки: Интерпретация может быть сложной.
* Область применения: Изучение динамики белков, химия полимеров.
Двумерная спектроскопия ЯМР: корреляционная спектроскопия (COSY):
COSY (Correlation Spectroscopy) – это гомоядерный 2D эксперимент, который показывает корреляции между протонами, связанными через две или три связи (геминальные и вицинальные протоны).
* Достоинства: Позволяет определить, какие протоны в молекуле взаимодействуют друг с другом, что помогает установить связность атомов и фрагменты структуры.
* Недостатки: Может быть сложен для интерпретации в случае перекрывания сигналов или сложных молекул.
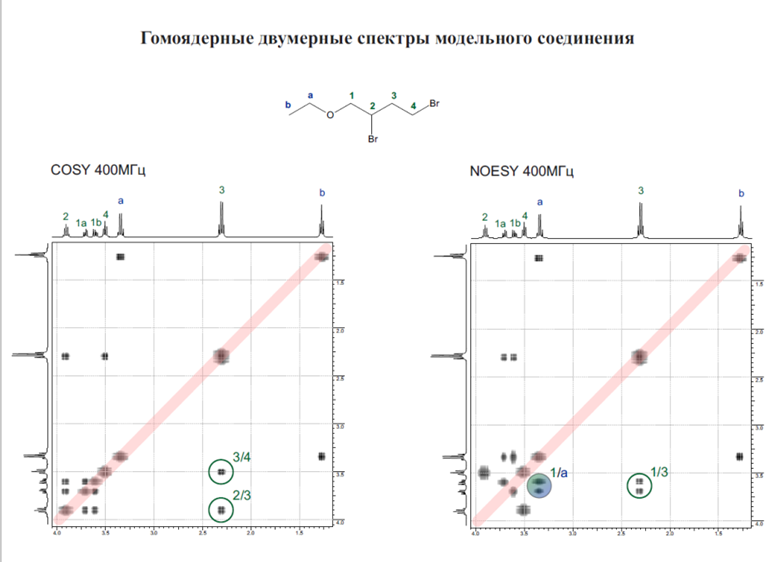
Вид двумерного спектра формируется из обычных одномерных спектров, расположенных вверху и слева. Шкалы хим. сдвигов (δ) приведены снизу и справа. Анализируются пики, находящиеся на диагонали (диагональные пики) и вне диагонали (поперечные пики) Семь диагональных пиков соответствуют семи мультиплетам в одномерном спектре. Поперечные пики позволяют определить корреляции между химическими сдвигами двух взаимодействующих протонов с различными хим. сдвигами.
COZY взамодействие вицинальное, через жесткую скалярную связь с углеродами (Корреляция протонов испытывающих спин-спиновое взаимодействие.) Спектр COSY позволяет обнаруживать слабые взаимодействия через 4-5 простых связей, которые на одномерных спектрах не обнаруживаются, поскольку J для них меньше естественной ширины сигнала и лежат в интервале от 0,1 до 0,5 Гц.
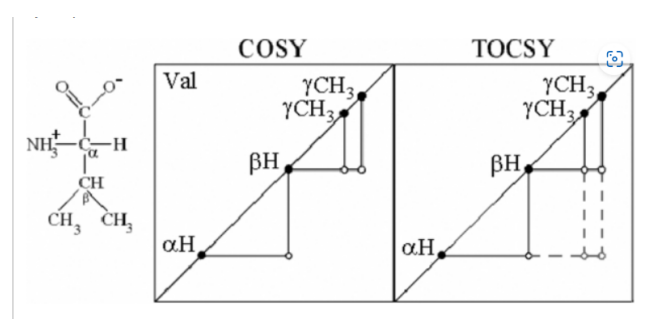
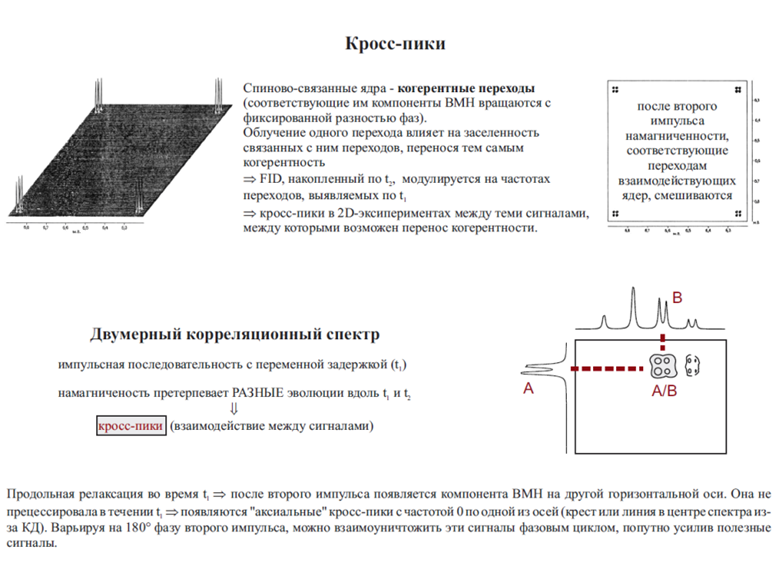
Рассмотренный 2D-COSY эксперимент позволяет наблюдать только корреляции между соседними протонами спиновой системы. Для установления взаимодействия через связи для цепи всех связанных протонов спиновой системы используется методика 2D-TOCSY. Различие между COSY и TOCSY(все протоны,а не вценальные и геминальные) заключается в другой последовательности импульсов и несколько иным воздействием на намагниченнсти ядер. Это отличие методик можно как пример продемонстрировать на спектрах валина (рис. 7.8). Как видно из рисунка, в COSY спектре присутствуют кросс-пики, свидетельствующие о взаимодействии только ближайших по химическим связям протонов, между которыми не более чем 3 химические связи. В TOCSY спектре видны более дальние взаимодействия, например, протонов аН и уСНз через 4 химические связи. Дополнительные взаимодействия через связи, выявляемые с помощью TOCSY, на рис. 7.8 выделены пунктиром.
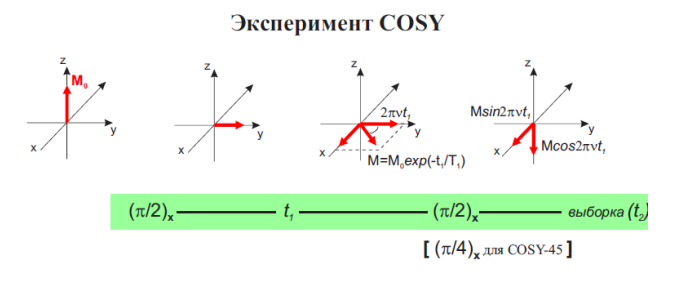
Эксперимент COSY включает в себя несколько ключевых этапов:
Возбуждение образца. Это происходит с помощью серии радиочастотных импульсов, которые переводят ядерные спины в состояние с более высокой энергией.
Свободное развитие системы. После первого радиочастотного импульса система свободно развивается в течение периода t1, в течение которого вращения прецессируют с частотами, соответствующими их химическим сдвигам.
Корреляция между ядрами. Она достигается путём постепенного изменения времени эволюции (t1) для улавливания косвенных взаимодействий. Эта серия экспериментов позволяет обнаруживать химические сдвиги в ядрах, которые могут не наблюдаться непосредственно в одномерном спектре. Нужна для определения связности, пространственной близости и динамических взаимодействий внутри молекулы.
Подача второго радиочастотного импульса. Он позволяет передавать намагниченность между связанными ядрами. С помощью второго импульса возникают кросс-пики, которые указывают на связывание между атомными ядрами и помогают определить наличие химической связи (общих электронов) между ними.
Регистрация сигнала. Результирующий сигнал регистрируется непрерывно в течение периода обнаружения (t2) после второго радиочастотного импульса.
Обработка данных. Данные обрабатываются с помощью преобразования Фурье по обеим осям t1 и t2, создавая 2D-спектр с пиками, нанесёнными по диагонали и вне диагонали.
16. Двумерная спектроскопия ЯМР: спектроскопия с эффектом Оверхаузера (NOESY). ( Я помолчу)
Спектроскопия ядерного эффекта Оверхаузера (NOESY) – это двумерный метод ЯМР, который предоставляет информацию о пространственной близости ядер в молекуле. Это особенно полезно для определения конформации и трехмерной структуры, особенно в крупных молекулах, таких как белки и нуклеиновые кислоты. Если один атом "возбудить" (например, с помощью радиоволны), его сосед начнёт вести себя по-другому. Этот эффект называется ядерным эффектом Оверхаузера.
Характеристика |
COSY |
NOESY |
Тип корреляций |
Спин-спиновые взаимодействия (JJJ-взаимодействия через связи). |
Пространственные взаимодействия (расстояние до 5 Å).(ван-дер-ваальсовы ) |
Информация |
Указывает на химические связи между атомами |
Показывает близость атомов в пространстве, даже без химической связи. |
Дальность действия |
Обычно взаимодействия через 2-3 связи (2J^2J2J, 3J^3J3J спин-спиновые) |
Диполь-дипольные взаимодействия до 5 Å. |
Принцип работы:
NOESY основан на ядерном эффекте Оверхаузера (NOE), который представляет собой изменение интенсивности сигнала одного ядра (A) при насыщении сигнала другого ядра (B). Этот эффект возникает из-за диполь-дипольного взаимодействия между ядрами и проявляется только тогда, когда ядра находятся пространственно близко друг к другу (обычно менее 5 Å).
В эксперименте NOESY используется последовательность импульсов, которая включает период смешивания, во время которого происходит кросс-релаксация между спинами через NOE. В результате, в 2D спектре NOESY появляются кросс-пики, которые соединяют сигналы ядер, находящихся близко в пространстве. Интенсивность кросс-пика пропорциональна расстоянию между ядрами в шестой степени.
Особенности:
* NOESY является гомоядерным экспериментом, то есть используется для изучения взаимодействий между ядрами одного типа (например, 1H-1H).
* Интенсивность NOE зависит от расстояния между ядрами и молекулярной динамики.
* Для больших молекул NOE может быть отрицательным, а для малых – положительным.
Достоинства:
* Предоставляет информацию о пространственной близости ядер, что позволяет определить трехмерную структуру молекул.
* Особенно полезен для изучения больших молекул, таких как белки и нуклеиновые кислоты.
* Может быть использован для изучения динамики молекул.
Недостатки:
* Интерпретация спектров может быть сложной, особенно для больших молекул.
* Сигналы от ядер, находящихся на расстоянии более 5 Å, обычно не наблюдаются.
* Эффект NOE может быть слабым, что требует высокой концентрации образца.
* Перекрывание сигналов может затруднить интерпретацию.
Примеры использования:
* Определение конформации малых молекул: NOESY может быть использован для определения конформации циклических молекул, например, для различения цис- и транс-изомеров.
* Определение структуры белков: NOESY является одним из основных методов, используемых для определения трехмерной структуры белков в растворе. Кросс-пики между аминокислотными остатками, находящимися близко в пространстве, позволяют определить фолдинг белка.
* Изучение взаимодействий лиганд-рецептор: NOESY может быть использован для определения сайтов связывания лигандов с рецепторами.
* Изучение динамики молекул: Изменение интенсивности NOE в зависимости от температуры или других параметров может дать информацию о динамике молекул.
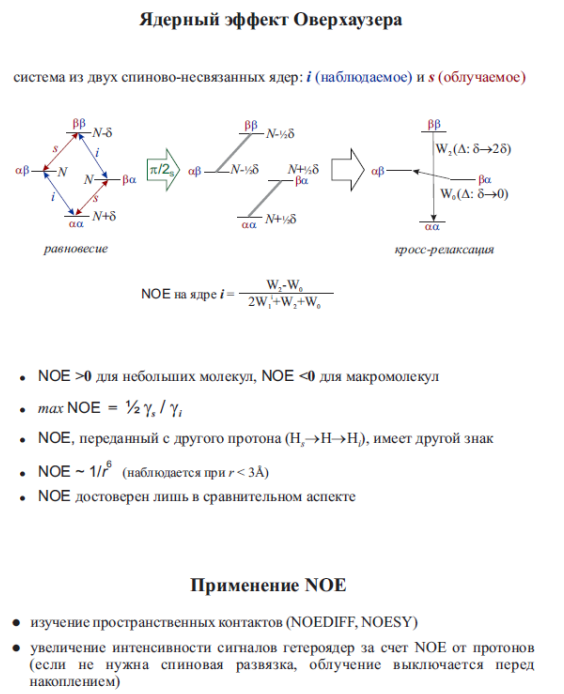
Ядерный эффект Оверхаузера.
Данный эффект связан с взаимодействием двух ядер непосредственно через пространство (а не по цепочке связей, как это было в случае спин-спинового взаимодействия). Слабое радиочастотное облучение одного из ядер на его резонансной частоте приводит к выравниванию заселенностей в двухуровневой системе. Этот процесс приводит к изменению заселенностей уровней ядер, располагающихся вблизи облучаемого ядра. Этот эффект зависит исключительно от расстояния между двумя ядрами (интенсивность взаимодействия обратно пропорциональна расстоянию между взаимодействующими ядрами в шестой степени). Как правило, ЯЭО можно обнаружить в случае протонов, находящихся на расстоянии до 5Å. Измерение расстояний таким образом часто применяют для определения точных структур белков и нуклеиновых кислот в растворе.
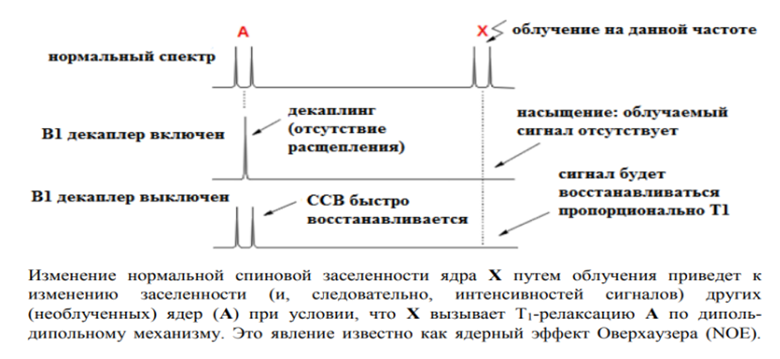
1. Развязка. Облучение сигнала на резонансной частоте устраняет любые спин-спиновые связи ядра с другими ядрами в молекуле. Эффект развязки практически мгновенен - после включения развязки связь исчезает за доли миллисекунды (при условии, что мощность развязки достаточно высока), когда развязка отключается, связь вновь появляется в аналогичном масштабе времени.
2. Когда протон облучается, индуцируются переходы между α- и β состояниями, и заселенности двух состояний будут стремиться к выравниванию. Скорость, с которой это происходит, зависит от напряженности поля развязки, но, как правило, будет быстрее, чем релаксация T1. Если поле достаточно мощное (то есть, если индуцированные переходы значительно превышают скорость нормальной релаксации T1), заселенности состояний α и β станут одинаковыми, а сигнал исчезнет (станет насыщенным).
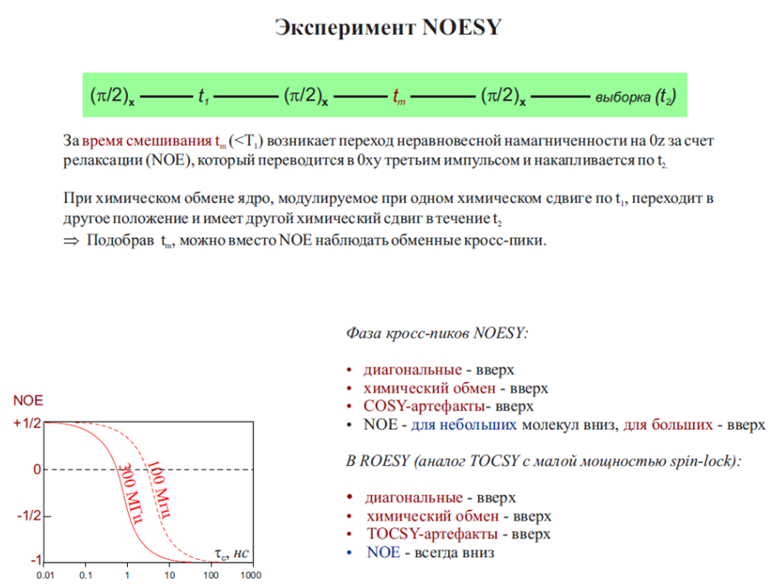
Возбуждение, намагничивание ядер H и их эволюция в течение времени t1. Импульс создаёт для протонов неравновесную заселённость, которая через диполь-дипольное взаимодействие переносится на ближайшие ядра. Таким образом происходит обмен намагниченностью между этими спинами. 1
Перенос продольной намагниченности в плоскость xy (за счёт ещё одного импульса) и смешивание в интервале времени τmix, при этом происходит кросс-релаксация. 1
Третий импульс возвращает продольную намагниченность в плоскость xy для регистрации сигнала в течение времени t2.
NOESY Корреляция протонов, близко расположенных в пространстве. В NOESY для установления корреляций используется перекрестная релаксация ядер Оверхаузера между ядерными спинами во время периода перемешивания. Полученный спектр похож на COSY, с диагональными пиками и кросс-пиками, однако кросс-пики соединяют резонансы от ядер, которые пространственно близки, а не те, которые связаны между собой сквозными связями. Спектры NOESY также содержат дополнительные осевые пики которые не предоставляют дополнительной информации и могут быть устранены с помощью другого эксперимента, изменив фазу первого импульса на обратную.
Одним из применений NOESY является изучение больших биомолекул, таких как белок ЯМР, в которых отношения часто можно назначить с помощью последовательная ходьба. COZY и NOEZY гомоядерная корреляция HMBC, HSQC- гетероядерная HSQC (Heteronuclear Single Quantum Coherence) — корреляция между химическими сдвигами протонов и химическими сдвигами ядер X (как правило, 13C или 15N) через прямое спин-спиновое взаимодействие (1J) между ядрами. Детектируемым ядром в данной методике являются протоны, что позволят существенно сократить время эксперимент Корреляция протонов напрямую связанных с ядром X (обычно X=13C). НMBC Корреляция протонов и ядер X через несколько связей (обычно X=13C). HMBC (Heteronuclear Multiple Bond Correlation) — корреляция между протонами и ядрами X (как правило, 13C или 15N), разделенными двумя или тремя связями (в редких случаях большим числом связей). В данной методике детектируемым ядром являются протоны, что позволяет значительно сократить время эксперимента.
17.Применение ЯМР для изучения АФС in vitro и in vivo. (Это пиздец)
Спектроскопия ядерного магнитного резонанса – вид спектроскопии, которая регистрирует переходы между магнитными энергетическими уровнями атомных ядер, вызванные радиочастотным излучением. Только ядра со спиновым квантовым числом I, отличным от «0», могут вызывать сигнал ЯМР, или быть активными в ЯМР.
Выбор растворителя определяется растворимостью анализируемого вещества и наиболее полным разделением сигналов резонанса вещества и растворителя, если последний содержит ядра, по которым проводится регистрация спектра ЯМР. Для проведения анализа удобно использовать дейтерированные растворители, поскольку дейтерий не дает сигнала в спектре.
Для неполярных соединений почти во всех случаях можно использовать тетрахлорид углерода, а для полярных соединений в большинстве случаев подходит хлороформ. Для того чтобы избежать наложения резонансного сигнала протона хлороформа, используется дейтерохлороформ (изотопическая чистота 99,8 %). Эти два растворителя используют в 90 % случаев, а для слаборастворимых образцов доступны другие дейтерированные растворители: диметилсульфоксид, ацетон-d6, ацетонитрил, бензол и D2O.
Применение ЯМР для изучения АФС обширно и охватывает как in vitro, так и in vivo исследования.
In vitro:
* Идентификация и подтверждение структуры АФС: ЯМР является золотым стандартом для определения структуры органических молекул, включая АФС. 1D и 2D эксперименты позволяют определить связность атомов и пространственное расположение атомов в молекуле.
* Контроль качества АФС: ЯМР используется для определения чистоты АФС, идентификации примесей и оценки стабильности.
* Изучение взаимодействия АФС с другими молекулами: ЯМР может быть использован для изучения взаимодействия АФС с белками, ДНК и другими биомолекулами.
* Изучение физико-химических свойств АФС: ЯМР позволяет определить растворимость, pKa, коэффициент распределения и другие важные свойства АФС.
In vivo:
* Фармакокинетика: ЯМР позволяет следить за распределением, метаболизмом и выведением АФС в живых организмах.
* Фармакодинамика: ЯМР может быть использован для изучения взаимодействия АФС с мишенями в организме.
* Метаболомика: ЯМР используется для идентификации и количественного определения метаболитов АФС в биологических жидкостях и тканях.
ЯМР (ядерный магнитный резонанс) предоставляет информацию о структуре, свойствах, метаболизме и взаимодействиях АФС следующим образом:
1. Структура:
* Химические сдвиги: Положение сигналов в спектре ЯМР (химический сдвиг) зависит от химического окружения ядер. Это позволяет определить типы функциональных групп и их расположение в молекуле.
* Константы спин-спинового взаимодействия: Расщепление сигналов в спектре ЯМР (мультиплетность) обусловлено взаимодействием ядер через химические связи. Анализ констант спин-спинового взаимодействия позволяет определить связность атомов в молекуле.
* Двумерные (2D) эксперименты ЯМР: COSY, HSQC, HMBC и NOESY предоставляют информацию о пространственной структуре молекулы и взаимодействии ядер через пространство.
2. Свойства:
* pKa: ЯМР титрование позволяет определить pKa АФС, что важно для понимания ее растворимости и распределения в организме.
* Растворимость: Изменение химических сдвигов в зависимости от растворителя может дать информацию о растворимости АФС.
* Динамика: ЯМР позволяет изучать динамические процессы в молекуле, такие как вращение вокруг связей и конформационные переходы.
3. Метаболизм:
* Идентификация метаболитов: Сравнивая спектры ЯМР образцов до и после метаболизма, можно идентифицировать метаболиты АФС.
* Количественный анализ метаболитов: ЯМР позволяет определить концентрацию метаболитов в образце.
* Метаболические пути: Использование меченых изотопами АФС позволяет изучать метаболические пути.
4. Взаимодействия:
* Связывание с белками: ЯМР может быть использован для изучения взаимодействия АФС с белками, определения констант связывания и идентификации сайтов связывания.
* Связывание с ДНК: ЯМР позволяет изучать взаимодействие АФС с ДНК.
* Образование комплексов: ЯМР может быть использован для изучения образования комплексов АФС с другими молекулами.
Исследование метаболитов методом ЯМР:
Пробоподготовка:
* Экстракция: Метаболиты обычно экстрагируются из биологических образцов (кровь, моча, ткани) с использованием органических растворителей или твердофазной экстракции. Биологические образцы (кровь, моча, ткани) обычно подвергаются экстракции для удаления белков и других макромолекул.
* Очистка: Экстракты могут быть дополнительно очищены с помощью хроматографии для удаления примесей, которые могут мешать ЯМР анализу.
* Растворение в дейтерированном растворителе: Для ЯМР анализа образцы растворяют в дейтерированном растворителе.
Ограничения:
* Чувствительность ЯМР ниже, чем у масс-спектрометрии.
* Сложность анализа сложных смесей метаболитов.
* Необходимость в больших количествах образца для некоторых экспериментов.
Примеры:
* Идентификация метаболитов лекарственных препаратов в моче.
* Изучение метаболических путей в клетках и тканях.
Пробоподготовка для анализа твердых, жидких и вязких АФС методом ЯМР:
* Твердые: Растворение в подходящем дейтерированном растворителе.
* Жидкие: Могут быть проанализированы напрямую или после разбавления дейтерированным растворителем.
* Вязкие: Могут быть растворены в подходящем растворителе или проанализированы с использованием твердофазного ЯМР.
Определение примесей в АФС методом ЯМР:
ЯМР позволяет детектировать и идентифицировать примеси в АФС даже в низких концентрациях. Высокое разрешение ЯМР позволяет различать сигналы от примесей и основного вещества.
* Выделение примесей: Если примеси присутствуют в значительных количествах, их можно выделить с помощью хроматографии или других методов разделения.
* Обогащение примесей: Если примеси присутствуют в низких концентрациях, их можно обогатить перед ЯМР анализом.
Возможности анализа близкородственных соединений методом ЯМР:
ЯМР может быть использован для различения близкородственных соединений, таких как изомеры и диастереомеры, благодаря высокой разрешающей способности и возможности получения информации о пространственной структуре молекул. 2D ЯМР эксперименты особенно полезны для анализа таких соединений.
*Чтобы приготовить образец, 20—30 мг или 50 мкл вещества помещают в ампулу внешним диаметром 5 мм и растворяют это вещество, добавляя около 0,5 мл растворителя. Раствор должен заполнять ампулу до уровня 3—4 см. Наконец добавляют стандарт (т. е. эталонное вещество), обычно тетраметилсилан. Тетраметилсилан (TMC) имеет низкую температуру кипения (26 0C) и высокое давление паров; с ним трудно работать в малых количествах. Поэтому нужно иметь под рукой 5 % (об.)-ные растворы TMC в наиболее часто используемых растворителях.
18.Масс-спектрометрия.
- Масс-спектрометрия (мс) основана на ионизации молекул изучаемого вещества (аналита) с последующим разделением ионов по величине отношения массы к заряду (m/z)
- Масс-спектр – это график зависимости (относительного) количества полученных ионов от отношения m/z (от интенсивности в %)
- Метод позволяет зарегистрировать молекулярную массу соединения, являющуюся его индивидуальной характеристикой. Масс-спектрометрия высокого разрешения дает информацию об элементном составе соединения.
- Современные масс-спектрометрические техники позволяют устанавливать молекулярные массы сверхсложных соединений. Зарегистрированный рекорд составляет 110,000,000 Дальтон.
- Структурная информация о веществах становится доступной благодаря набору фрагментных ионов, образующихся при распаде исходных молекул. Для получения структурной информации можно использовать как компьютерные библиотеки масс-спектров, так и проводить ручную расшифровку спектра с использованием известных закономерностей фрагментации.
Классификация масс- спектрометрических методов
По назначению:
•Элементная
•Изотопная
•Органическая
По технике ввода пробы:
•Масс-спектрометрия прямого ввода
•Хромато-масс-спектрометрия:
•Газовая
•Жидкостная
По разрешению:
•Низкого разрешения
•Высокого разрешения
По технике выполнения:
•Одномерная
•Тандемная
СУЩЕСТВУЮТ ТРИ ПОНЯТИЯ
МАССЫ СРЕДНЯЯ молекулярная масса вычисляется на основании элементного состава и средних атомных масс
НОМИНАЛЬНАЯ молекулярная масса Мт вычисляется с учетом элементного состава и номинальных атомных масс наиболее распространенных в природе изотопов
ТОЧНАЯ молекулярная масса вычисляется из значений точных масс наиболее распространенных изотопов ТОЧНЫЕ ЗНАЧЕНИЯ АТОМНЫХ МАСС ОПРЕДЕЛЕНЫ ПО ОТНОШЕНИЮ К МАССЕ ИЗОТОПА 12С, РАВНОЙ 12,0000
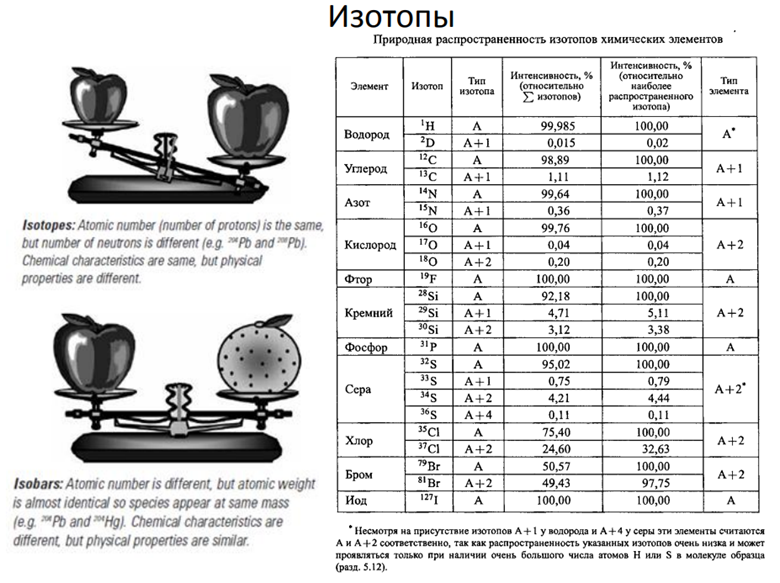
Для некоторых элементов за счет изотопного состава образуются характеристичные кластеры в масс-спектре фрагментов, содержащих эти элементы
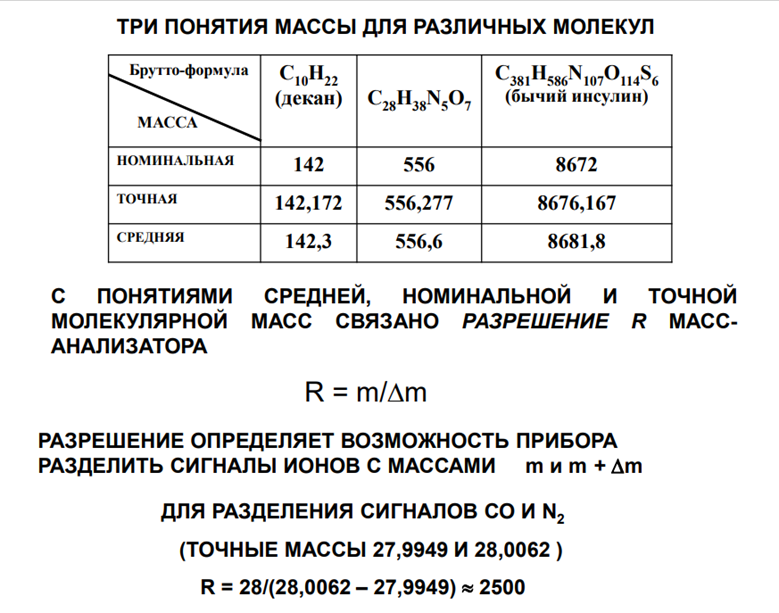
•Метод МС - метод исследования и анализа веществ •основан на ионизации атомов и молекул вещества и последующем разделении образующихся ионов в соответствии с их массовым числом m/z -отношением массы иона к его заряду - в электрическом или магнитном поле
Преимущество метода в том, что для анализа достаточно очень малое количество вещества, основной недостаток – метод является разрушающим, т. е. исследуется не само вещество, а продукты его превращения
Масс-спектрометрия – совокупность трех основных процессов:
1. ионизация молекул – превратить нейтральные частицы определяемого вещества – атомы или молекулы в частицы заряженные.
2. разделение ионов по массам – разделить образовавшиеся ионы в пространстве в соответствии с их массой посредством электрического или магнитного поля.
3. детектирование катион-радикалов и катионов и получение масс-спектра – измеряя электрический ток, образуемый движущимися ионами, можно судить об изотопном, атомарном и молекулярном составе анализируемого вещества, как на качественном, так и на количественном уровне.
Масс-спектральный анализ
1. Определение молярной массы
Источник информации положение молекулярного пика М+ или его производных (М+1)+ (M-1)+
2. Определение брутто-формулы - используют соотношение интенсивностей пиков изотопов элементов
3. Определение структуры органических соединений основано на изучении пиков «осколочных» ионов (образующихся с начальной кинетической энергией, но изменяющих величину эффективного угла собирания, что приводит к изменению формы пика)
• При столкновении электронов с органической молекулой вначале образуется катион-радикал
![]()
• С увеличением энергии электронов происходит его распад, фрагментация
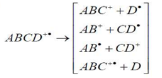
Одновременно происходит внутремолекулярные перегруппировки
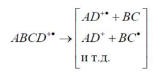
Качественный анализ
• Кроме того сравнивают масс-спектры изучаемого соединения с каталогом спектров (до 150 000 спектров различных соединений)
Количественный анализ
• Возможны вещественный и элементный анализ
Количественный анализ смесей органических соединений часто ограничен сложностью масс- спектра. Поэтому метод МС сочетают с различными видами хроматографии и капиллярного зонного электрофореза
1) Для вещественного анализа используют ГХ
• В ходе хроматографирования регистрируют во времени интенсивность какого-либо пика с определенным массовым числом
• В результате получается зависимость сигнала детектора от времени, как в хроматографии
2) Сочетание метода разделения и МС-определения возможно в виде тандемной МС
• Один масс-спектрометр служит для выделения молекулярных пиков отдельных веществ из масс- спектра их смеси
• Второй для фрагментации выделенных веществ и дальнейшей идентификации
3) непосредственный анализ по масс-спектру
Для этого измеряют интенсивность пика определяемого компонента и внутреннего стандарта - обычно это меченая изотопом разновидность определяемого вещества или его гомолог
• Для построения масс-хроматограммы берут интенсивности пиков нескольких ионов из каждого записанного масс-спектра и строят график зависимости этих интенсивностей от номера масс- спектра, соответствующего времени удерживания
Аналитические возможности метода
• Позволяет определять массы ядер и атомов и оценивать распространенность изотопов в природе
• По соотношению масс изотопов материнского и дочернего излучений определяют возраст горных пород, археологических и др. объектов
МС применяют:
• для элементного анализа твердых неорганических веществ и материалов
• для идентификации и установления структуры органических соединений, включая определение молярной массы
• для исследования состава и структуры поверхностей твердых тел (локальный, послойный и фазовый анализ)
19.Конструкции современных масс-спектрометров.
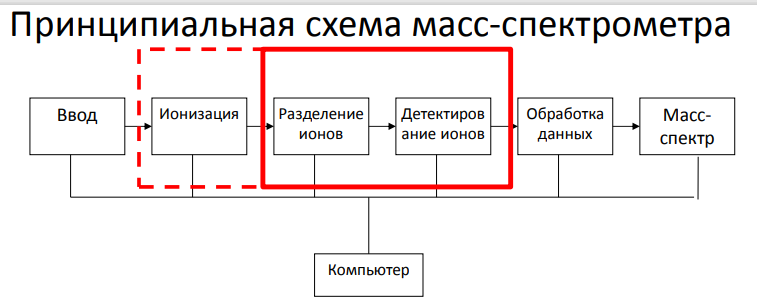
Источник ионизации Масс-спектрометрия оперирует заряженными частицами – ионами. Задача источника ионизации генерировать заряженные частицы из молекул исследуемого вещества. Задача интерфейса – сопрягать зону высокого (атмосферного) давления и зону глубокого вакуума Сегодня в большинстве приборов источник ионизации и интерфейс конструктивно объединены в один узел. Мы будем называть его «источник ионизации».
Вакуумная система масс-спектрометра:
•Источник ионизации/интерфейс –рабочее давление 10-6 – 1 атм.
•Зона фокусировки и подготовки ионов – рабочее давление 10-3 атм.
•Зона масс-анализатора и детектора ионов рабочее давление 10-8 - 10-6 атм.
Вакуумная система масс-спектрометра:
Двухступенчатая система:
•Форвакуумный масляный насос высокой производительности вакуум 10-3 атм.
•Один или два турбомолекулярных насоса высокой производительности вакуум 10-7атм.
Детектирование ионов в масс-спектрометрии
Задача детектора – считать ионы
Типы детекторов: •Фотопластинка (исторический) •Чашка Фарадея (в наст. время только в масс-спектрометрии изотопных отношений) – самый точный, но медленный детектор
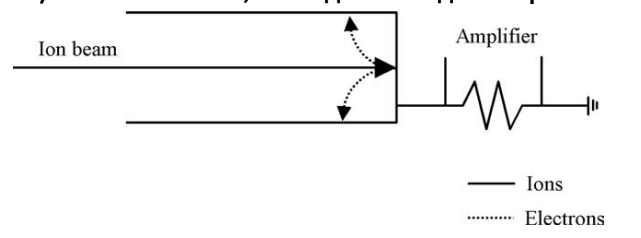
Электронные умножители
•Динодные •Канальные •Электрооптические детекторы
Поток электронов ускоряется электрическим полем и попадает на серию металлических пластин — динодов. Каждый динод покрыт материалом, который выбивает несколько вторичных электронов при попадании первичного электрона. Таким образом, ток усиливается каскадно.
Вторичный электронный умножитель
Коэффициент усиления 106 – 109 На диноды нанесены материалы с низкой работой выхода электрона Динодов 10 – 20 Разница напряжений между динодами около 100 В
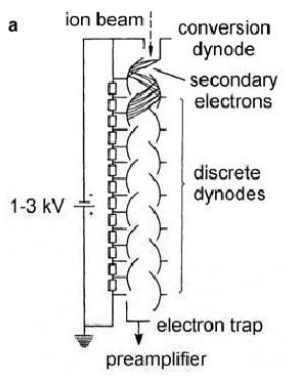
Канальные электронный умножитель
Коэффициент усиления зависит от отношения длины к диаметру Оптимальное значение 40 – 80 Коэффициент усиления 104 - 108 Материал – кремний, стекла допированные свинцом (полупроводники) Достоинство – доступность, минимальный эффект дискриминации масс
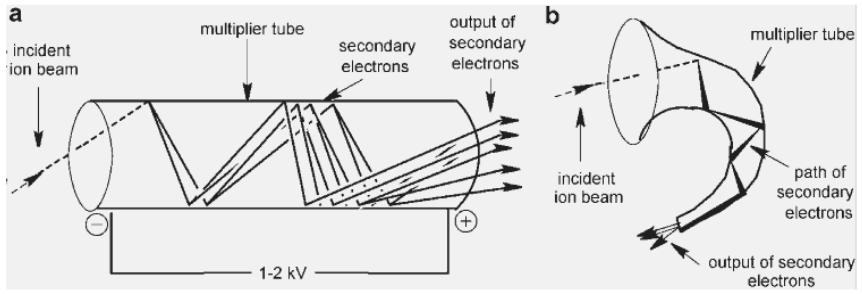
Микроканальный пластинчатый детектор (Microchannel plate) Достоинство – самый быстрый детектор Коэффициент усиления 10^5
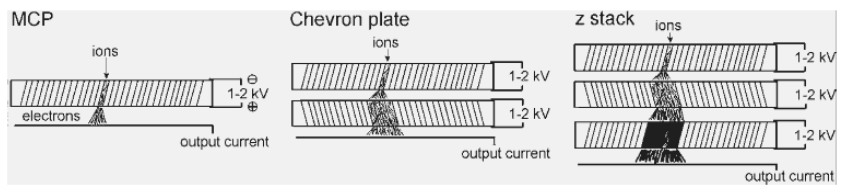
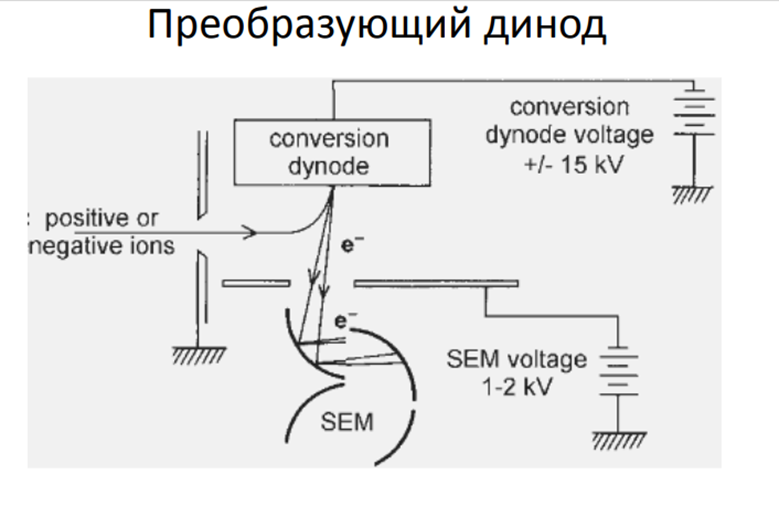
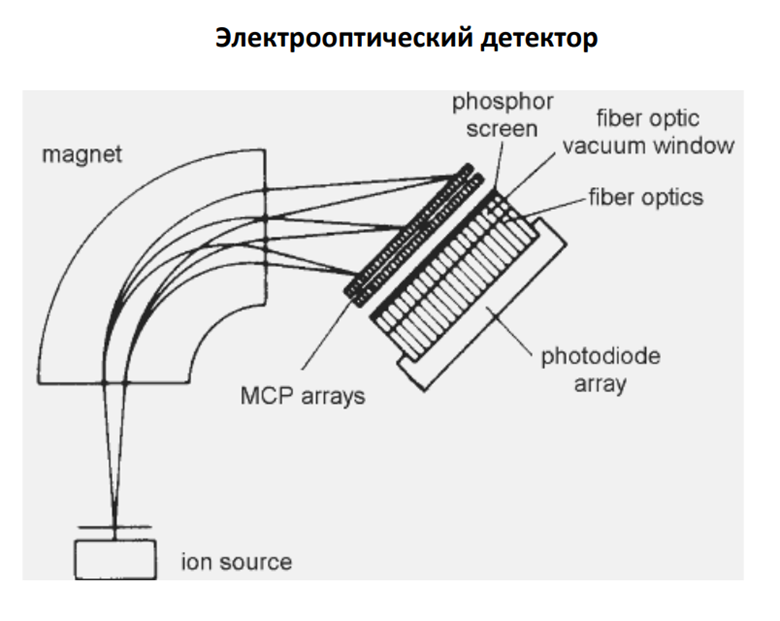
Источник ионизации /интерфейс
Электронный удар: метод широко применяется для ионизации органических соединений
• Пары образца бомбардируют ускоренными электронами
• При столкновении электронов с органической молекулой вначале образуется катион-радикал М + e → M+ + 2e
• затем происходит его распад (фрагментация), и образуются дочерние ионы с меньшими массами
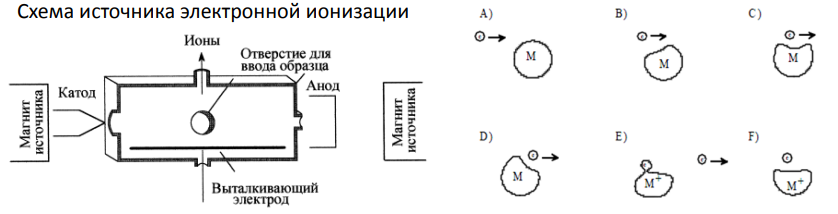
При уменьшении энергии ионизирующих электронов относительная интенсивность пиков М+ и перегруппировочных ионов увеличивается относительно пиков осколочных ионов. Абсолютная интенсивность всех без исключения пиков становится ниже. Если пик молекулярного иона отсутствует в спектре при энергии электронов 70 eV, он будет отсутствовать и при более низкой энергии электронов.
Фрагментация молекулярных ионов M + ē = M+ + 2 ē
10^-16 секунды – потеря электрона Согласно принципа Франка-Кондона геометрия молекулы во время этого процесса не изменяется 10-13 секунды – атомы начинают осциллировать
10^-8 секунды – электронно возбужденные ионы переходят в невозбужденное состояние или фрагментируют
10^-6 секунды – ионы покидают ионный источник
! Масс-спектрометр регистрирует лишь положительные ионы, отрицательные ионы, нейтральные радикалы и молекулы не регистрируются!
Достоинства метода:
• Метод ионизации электронным ударом дает богатые фрагментами масс-спектры, которые однозначно характеризуют структуру молекулы, что удобно для идентификации веществ
• Масс-спектрометрия электронного удара - высокочувствительный метод анализа, позволяет анализировать пикомольные количества вещества
• Существуют "библиотеки" масс-спектров, содержащие спектры более 70000 органических соединений, по которым можно проводить их идентификацию с применением ЭВМ
• Воспроизводимость; Чувствительность; Универсальность; Наличие библиотек спектров; Задействованы все пути; фрагментации
Недостатки метода:
• Молекулярные ионы образуются лишь у 20% органических соединений
• Метод применим только для определения легколетучих термически стабильных соединений;
• Ионы с большими значениями т/г, дающие информацию о молекулярной массе и наличии функциональных групп обеспечивают небольшой вклад в значения полного ионного тока
• Отрицательно заряженные ионы, имеющие большое значение в структурном анализе, образуются в очень небольшом количестве и ограниченным числом органических соединений
• Высокая избыточная энергия часто приводит к нестабильности молекулярного иона
• Необходимость испарения образца
Отсутствие монохроматичности
Химическая ионизация:более мягкий способ ионизации
Пары пробы смешивают с большим избытком газа-реагента (метан, изобутан, аммиак или NO), газ-реагент ионизируют действием электронного удара. Ионизация молекул газа происходит за счет электронной ионизации с дальнейшим химическим превращением газа- ионизатора. Сталкиваясь с молекулами образца, ионизированные молекулы газа передают свой заряд в виде протона исследуемой молекуле:
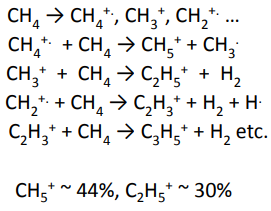
•Определяемые молекулы АВ ионизируются:
*Протонирование ( недостаток - депротонирование)

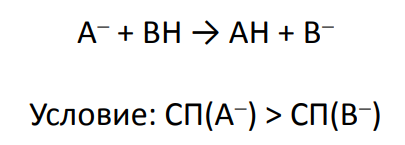
*Перезарядка
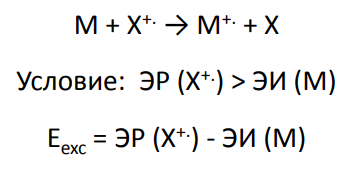
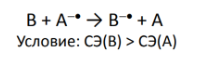
*Электрофильное присоединение ( недостаток - нуклеофильное присоединение)
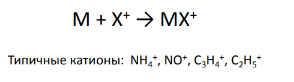
![]()
*Отрыв аниона (недостаток - нуклеофильное замещение)
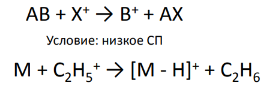
![]()
• Далее протонированная молекула образца выталкивается электрическим полем в сторону масс-анализатора
Достоинства:
1. Мягкий метод ионизации, молекуле образца передается около 5 эВ избыточной энергии, что препятствует процессам фрагментации и позволяет подвергать анализу нестойкие молекулы
2. Интенсивный пик молекулярного иона, что позволяет определить молекулярную массу
Недостатки:
1. Отсутствие фрагментации, очень простые масс-спектры, что не позволяет судить о структуре вещества и сравнить спектр с базами масс-спектральных данных
2. Возможно провести анализ только тех соединений, которые можно перенести в газовую фазу (испарить)
Фотоионизация
Фотоионизация монохроматичные пучки фотонов (разброс энергий 0.01-0.02 eV) Энергия 1 eV соответствует длине волны 12395Å Диапазон энергий фотонов, эмиттируемых инертными газами - 10-40 eV
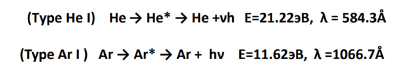
Преимущества: монохроматичность, полная передача энергии иону Очень полезен для измерения ЭИ и ЭП
Десорбция
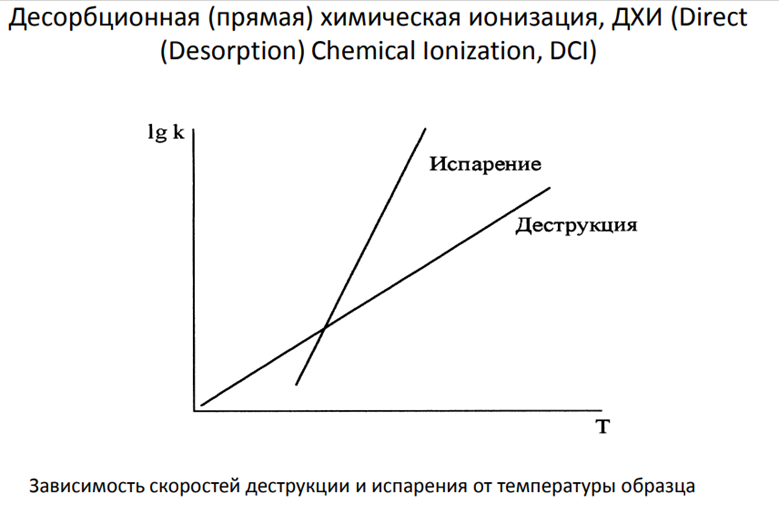
При использовании более высоких температур вместо деструкции и ионизации образца происходит его испрение - искать компромисс.
Полевая десорбция (Field Desorption, FD)
V = 8-10 кВ Высокая напряженность электрического поля (до 1В/Å). Механизм - туннелирование электрона Избыточная энергия <1 эВ М+ в основном (невозбужденном) электронном состоянии. Среднее время присутствия М+ в источнике - 1 0-12 секунды Нанесение раствора образца непосредственно на эмиттер. В основном четноэлектронные протонированные молекулярные ионы MH+ . Добавка к анализируемому образцу кислот или неорганических солей облегчает процесс ионизации с образованием ионов МН+ и [M + Катион]+ . В этом случае, поскольку ионы присутствуют уже в конденсированной фазе, для их извлечения требуется меньший потенциал (около 10-2В/Å). Проблемы – изготовление эмиттеров и малая интенсивность спектров.
Бомбардировка быстрыми атомами, ББА (Fast Аtom Вombardment, FAB);
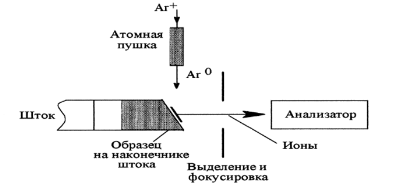
Интерфейсы ВЭЖХ-МС
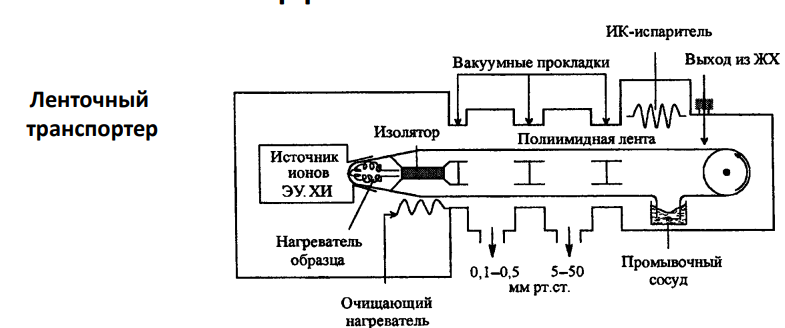
Образец наносится на полиамидную ленту, и при ее прокручивании происходит перенос образца внутри прибора, в которых происходит ионизация пробы с дальнейшем детектированием
Проблемы: дороговизна, быстрый износ возможно даже с однократным использованием, загрязнение ленты.
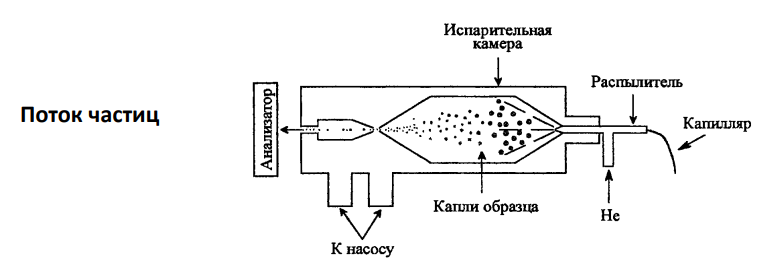
Образец впрыскивается в испарительную камеру, где помимо испарения происходит его ионизация
Проблемы: испарение образца, большое разнообразие ионов.
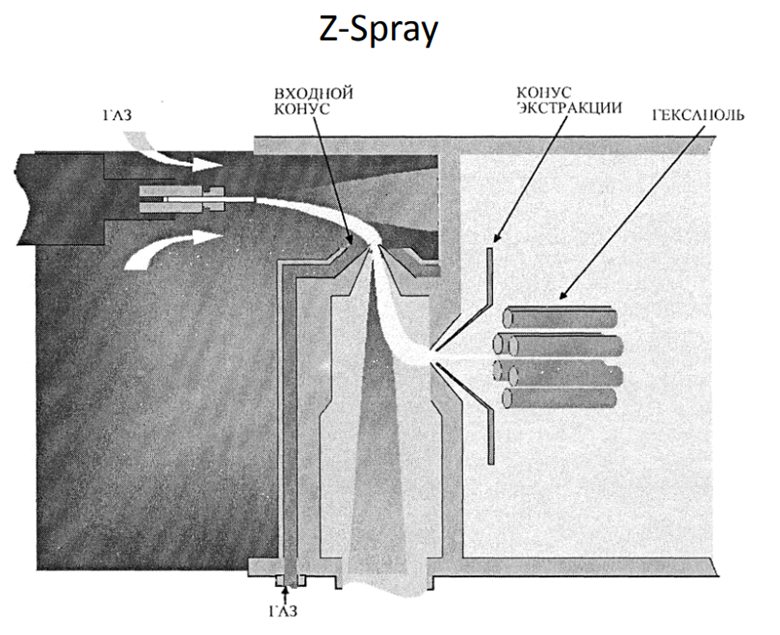
Исследуемый образец в виде раствора поступает в систему введения образца (генератор аэрозоля).
Распылитель генерирует аэрозоль, который проходит через распылительную камеру и транспортируется потоком аргона к плазменной горелке.
Транспортирующий поток аргона пробивает осевую часть плазмоида, создавая центральный канал плазменного факела.
В центральном канале плазменного факела происходит высушивание капель аэрозоля, испарение и распад частиц до молекул, диссоциация молекул до атомов и ионизация атомов.
Образующиеся ионы вакуумной экстракцией (засасываются внутрь прибора из плазмы) через специальный интерфейс — сборку двух металлических конусов (сэмплер и скиммер) с небольшими осевыми проходными отверстиями.
Движущей силой экстракции является огромная разница давлений между плазмой (атмосферное давление) и полостью спектрометра (высокий вакуум).
Пространство между конусами откачивается форвакуумным насосом для обеспечения необходимого переходного согласования разницы давлений.
После интерфейса экстрагированная плазменная струя попадает во входную ионно-оптическую систему масс-спектрометра, где происходит очистка ионов от ненужных частиц и электронов, коррекция кинетической энергии ионов и фокусирование их для введения в масс-анализатор.
Электроспрей (электрораспыление) ESI
• Вещество на ионизацию поступает в полярном растворителе (вода, метанол, ацетонитрил и др.), содержащем ионы водорода и катионы щелочных металлов (натрий, калий), через металлический капилляр (распылитель), к которому приложено высокое напряжение
• Продвигаясь в электрическом поле капля раствора испаряется под действием нагретого потока инертного газа (азот) и распадается на ряд мелких положительно заряженных капель, которые попадают в масс-анализатор
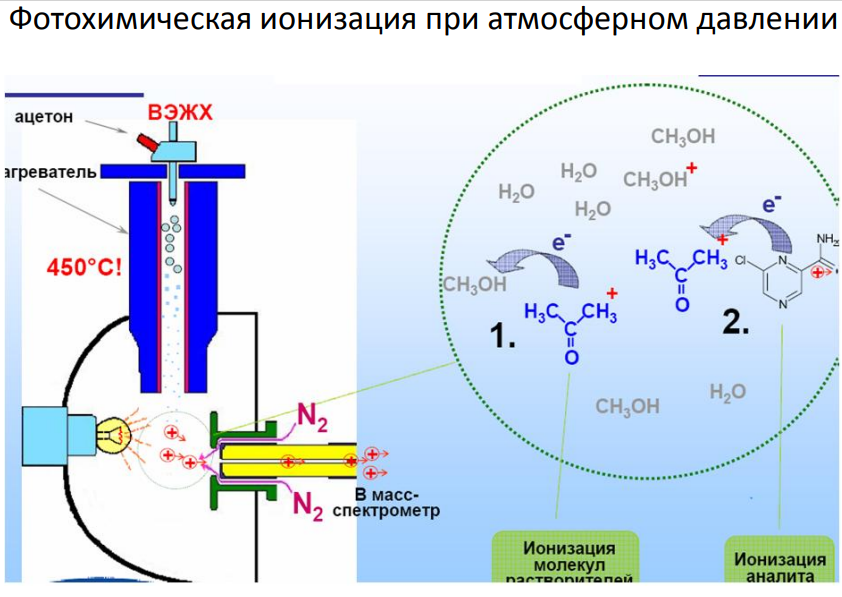
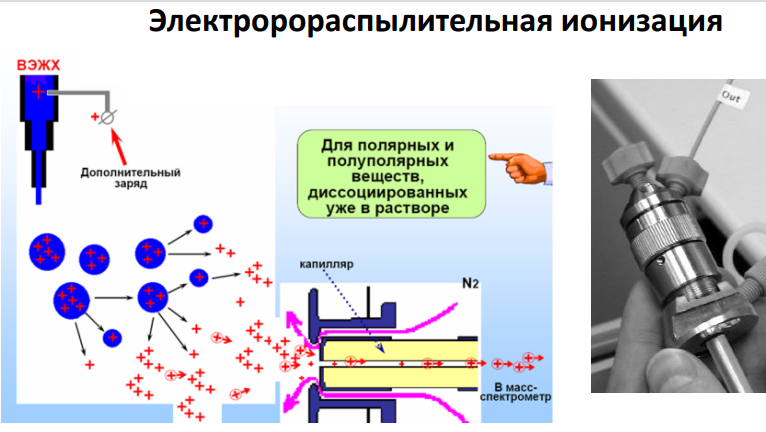
Особенности масс-спектров низкомолекулярных соединений
•Интенсивные сигналы молекулярных ионов (MH+ , M- )
•Фрагментных ионов нет вообще или присутствует их небольшое количество
•Фрагментация обычно происходит по связи углерод-гетероатом
•Характерно образование «аддуктных ионов»: [2M]H+ , M*Kt+ , M*Sol+ , MA+ Где Kt – катионы щелочных металлов и аммония, Sol – растворитель (чаще всего вода), A – добавки в подвижную фазу, например органические кислоты
Особенности ионизации
Хорошо ионизируются вещества с ярковыраженными кислотными или основными свойствами
Выход ионизации напрямую зависит от рН подвижной фазы
Соединения, не обладающие ионогенной природой не ионизируются
ФАКТОРЫ, ВЛИЯЮЩИЕ НА ЭФФЕКТИВНОСТЬ ЭЛЕКТРОРАСПЫЛЕНИЯ
Размеры капель
Поверхностный заряд капли
Поверхностное натяжение элюента
Летучесть элюента
Сила растворителя Большие капли с большим поверхностным натяжением, высоким поверхностным зарядом, низкой летучести и высокой проводимости мешают эффективному электрораспылению.
Достоинство:
Возможность ионизации нелетучих и термически нестабильных веществ
Мягкая ионизация – интенсивный сигнал молекулярного иона
Образование многозарядных ионов – расширение возможностей масс-спектрометрии в области больших молекул
Недостатки:
Низкие интенсивности фрагментных ионов
Сильная зависимость сигнала от рН
Не ионизируются малополярные веществ
Химическая ионизация при атмосферном давлении(APCI)
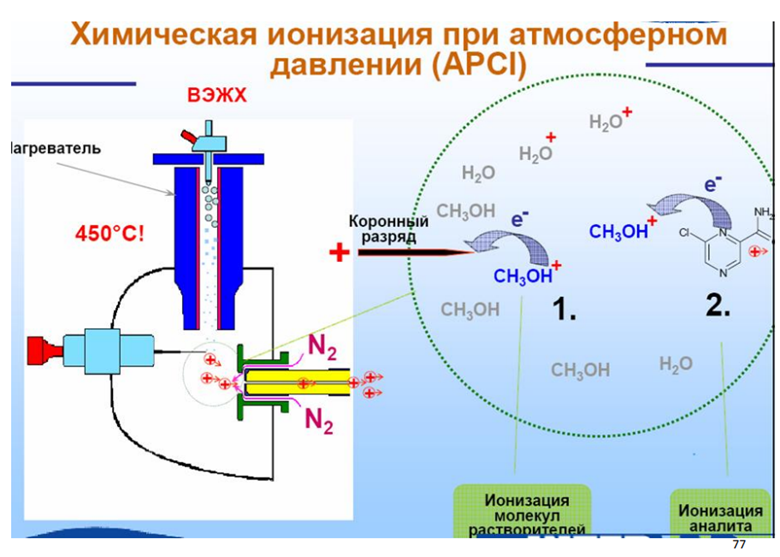
Особенности масс-спектров APCI
•Интенсивные сигналы молекулярных ионов (MH+ , M- )
•Фрагментных ионов нет вообще или присутствует их небольшое количество
•Фрагментация обычно происходит с отщеплением «хороших уходящих групп»
•Характерно образование «аддуктных ионов»: [2M]H+ , M*Kt+ , M*Sol+ , MA+ Где Kt – катионы щелочных металлов и аммония, Sol – растворитель (чаще всего вода), A – добавки в подвижную фазу, например органические кислоты
Особенности ионизации
Хорошо ионизируются вещества как с ярко выраженными кислотными или основными свойствами, так и вещества неионогенной природы
Выход ионизации напрямую зависит от содержания и природы органического растворителя в подвижной фазе
Возможность ионизации нелетучих веществ
Мягкая ионизация – интенсивный сигнал молекулярного иона
Низкие интенсивности фрагментных ионов
Хорошо ионизируются малополярные вещества
Не подходит для ионизации термически нестабильных веществ
Образуются преимущественно однозарядные ионы
Лазерная десорбция (MALDI)
