
Орг_Хим_Все лекции_презы
.pdf
Изомерия органических соединений
Изомерия – явление существования соединений, имеющих одинаковую молекулярную формулу, но отличающихся порядком связывания атомов в молекуле или расположением атомов в пространстве и вследствие этого отличающихся по свойствам.
Такие соединения называются изомерами.

Структурная изомерия
Структурные изомеры отличаются друг от друга последовательностью связывания атомов в молекуле, т. е. структурой.
1. Изомерия углеродной цепи
Изомерия углеродной цепи обусловлена различной последовательностью связывания атомов, образующих углеродный скелет молекулы.

Структурная изомерия
2. Изомерия положения
Изомерия положения обусловлена разным положением функциональных групп, заместителей или кратных связей при одном и том же углеродном скелете молекулы

Структурная изомерия
3. Изомерия функциональных групп
Изомерия функциональных групп обусловлена присутствием в изомерах одинакового состава функциональных групп различной природы
Изомерия углеродной цепи и изомерия положения проявляются, как правило, в пределах одного класса органических соединений, а в случае изомерии функциональных групп изомеры принадлежат к разным классам.
В некоторых случаях два структурных изомера могут находиться в состоянии динамического равновесия друг с другом. Такое явление называют таутомерией, а структурные изомеры –
таутомерами:

Пространственная изомерия
Пространственные изомеры, или стереоизомеры – вещества,
имеющие одинаковый состав и порядок связывания атомов в молекуле, но отличающиеся друг от друга их расположением в пространстве, называют.
Конфигурация – то или иное относительное расположение атомов молекулы в пространстве.
Конформация – различное пространственное расположение атомов или атомных групп в молекулах определенной конфигурации, обусловленное вращением вокруг σ-связей. Понятие «конформация» отражает более тонкие особенности пространственного строения молекул.
Конфигурационными изомерами – органические соединения, отличающиеся друг от друга только конфигурацией молекул (без учета возможных конформаций).
Различают оптические и геометрические конфигурационные изомеры.
Конформационными изомерами – стереоизомеры, имеющие различное пространственное расположение атомов или атомных групп, обусловленное вращением вокруг простой углерод-углеродной связи.

Молекулярные модели
Молекулярные модели – это наглядное изображение молекул органических и неорганических соединений, позволяющее судить о взаимном расположении атомов, входящих в состав молекулы.
1. Шаростержневые модели (модели Кекуле–Вант–Гоффа)
В шаростержневых моделях молекул атомы представлены разноцветными шарами, а химические связи – стержнями.
Шары связаны друг с другом стержнями с учетом взаимного расположения атомов в пространстве.
Шаростержневые модели удобны для рассмотрения валентных углов и вращения вокруг простых связей, однако они не отражают относительных размеров атомов и межатомных расстояний в молекуле.

Молекулярные модели
2. Скелетные модели (модели Драйдинга)
Скелетные модели, в отличие от шаростержневых, ограничиваются изображением лишь скелета молекулы, т. е. химических связей между атомами, причем межатомные расстояния в этих моделях пропорциональны истинным (в масштабе 0,1 нм = 2,5 см).

Молекулярные модели
3. Полусферические модели (модели Стюарта–Бриглеба)
Полусферические модели изображают реальные молекулы с учетом пространственного расположения атомов, межатомных расстояний и размеров атомов.
В таких моделях атомы представлены разноцветными, частично срезанными шарами, радиус которых пропорционален вандерваальсову радиусу, а расстояние от центра шарика до поверхности среза – ковалентному радиусу).
Атом углерода в sp3-гибридизации изображают в виде шара с четырьмя, в sр2 – с тремя, в sр – с двумя срезами, атом водорода представляют шаром с одним срезом и т. д.
Несмотря на то, что полусферические модели наиболее удачно отражают реальные молекулы, они не пригодны для рассмотрения валентных углов между атомами и вращения вокруг простых связей.
Стереоформулы
Для изображения пространственного строения молекулы на плоскости чаще всего используют
•стереохимические формулы
•перспективные формулы
•проекционные формулы Ньюмена
•проекционные формулы Фишера
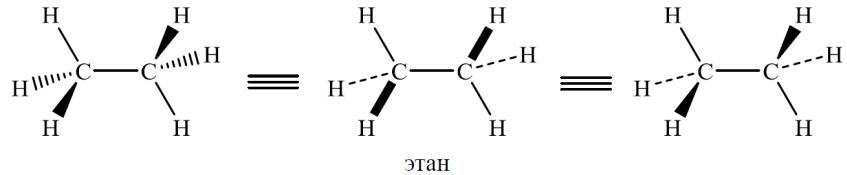
1. Стереохимические формулы
В стереохимических формулах химические связи, расположенные в плоскости чертежа, изображают обычной чертой; связи, находящиеся над плоскостью – жирным клином или жирной чертой, а связи, расположенные под плоскостью, – штриховым клином или пунктирной линией:

Стереоформулы
2. Перспективные формулы
Перспективные формулы описывают пространственное строение на плоскости при рассмотрении молекулы вдоль одной из углерод-углеродных связей.
По внешнему виду они напоминают лесопильные ко́злы
