
- •Ионная полимеризация
- •Катионная полимеризация
- •Анионная полимеризация.
- •Собственно анионная полимеризация
- •Анионно-координационная полимеризация.
- •Полимеризация с вероятным образованием карбенов
- •Миграционная полимеризация
- •Полициклоприсоединение
- •Стро.Ение мономеров и их способность к полимеризации
- •Практические способы проведения полимеризации
Полициклоприсоединение
В этом варианте используются хорошо известные в органической химии реакции циклоприсоединения. Мономеры для этих реакций содержат по два или более фрагмента, способных участвовать в циклоприсоединении.
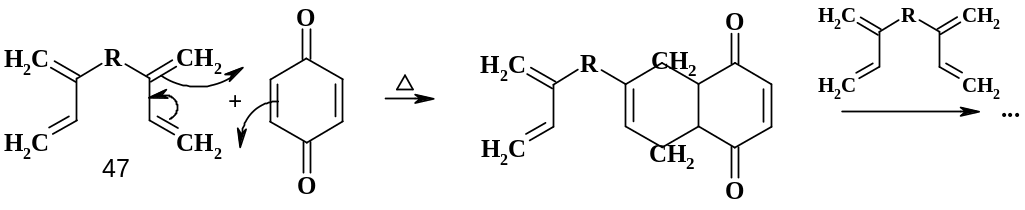 Наиболее характерный случай –
использование реакции диенового синтеза.
Полимер, в частности, может быть получен
при взаимодействии бис-1,3-диена (47) и
бис-диенофила (например, хинона):
Наиболее характерный случай –
использование реакции диенового синтеза.
Полимер, в частности, может быть получен
при взаимодействии бис-1,3-диена (47) и
бис-диенофила (например, хинона):
При использовании триена типа (48), возможно получение «лестничного» полимера, т.к. при каждом акте взаимодействия диен-диенофил генерируется новая диеновая структура:
Н етрудно
заметить, что в реакциях полициклоприсоединения
миграции фрагментов не происходит
(«мигрируют» только электроны). В то же
время эти реакции протекают по типичному
ступенчатому механизму, с образованием
устойчивых структур при каждом акте
циклоприсоединения.
етрудно
заметить, что в реакциях полициклоприсоединения
миграции фрагментов не происходит
(«мигрируют» только электроны). В то же
время эти реакции протекают по типичному
ступенчатому механизму, с образованием
устойчивых структур при каждом акте
циклоприсоединения.
Резюме
Рассмотренные в данном разделе процессы формально относятся к полимеризации, т.к. элементарное звено полимера идентично мономеру по составу. Однако механизмы формирования полимерных цепей не цепные, а ступенчатые: промежуточные продукты и формирования цепей – не эфемерные «живые» полимеры, а обычные молекулы, которые могут реагировать дальше, но в принципе могут и не реагировать.
Различают миграционную ступенчатую полимеризацию, в ходе которой между молекулами мономеров происходит миграция атомов или групп, и полициклоприсоединение, в ходе которой «мигрируют» только электроны.
Ступенчатая полимеризация протекает при действии активаторов (полимеризация гетероциклических мономеров), при нагревании (диеновый синтез) или при простом смешении мономеров (получение полиуретанов)
Процессы ступенчатой полимеризации используются реже, чем цепной, но приводят к ряду ценных и перспективных полимеров (поликапролактам, полиуретаны, продукты диенового синтеза)
Стро.Ение мономеров и их способность к полимеризации
Частично этот вопрос был затронут при рассмотрении радикальной сополимеризации (Q-e – схема). Здесь он будет рассмотрен в более общем виде.
Легкость протекания, да и сама возможность полимеризации, как и любой химической реакции, зависит от термодинамических и кинетических факторов.
Термодинамический фактор в самом общем виде выражен уравнением:
ΔG = ΔH - TΔS
Чем более отрицательно значение ΔG, тем более термодинамически выгодна полимеризация (тем более сдвинуто вправо равновесие мономер полимер); если ΔG > 0, полимеризация невозможна. Напомним, что термодинамическая характеристика реакции не зависит от ее механизма и учитывает только начальные и конечные состояния (левую и правую части суммарного уравнения реакции).
Кинетический фактор сводится к оценке энергии активации реакции, для чего необходимо оценить энергию начального и переходного состояний. Кинетический фактор накладывает дополнительные ограничения на способность к полимеризации; целый ряд соединений, термодинамически склонных к полимеризации, тем не менее, полимеризуется с трудом или вовсе не полимеризуется из-за кинетических затруднений (слишком высокой энергии активации). Как известно, структура и энергия переходного состояния определяется механизмом реакции; поэтому при смене механизма полимеризации может значительно измениться ее скорость. Поэтому большое значение имеет подбор «правильного» механизма полимеризации, при котором энергия активации наименьшая.
Целесообразно рассмотреть связь строения и способности к полимеризации отдельно для соединений со связью С=С и для циклических мономеров.
Соединения со связью С=С: n >C=С< [-CC-]n
Термодинамический фактор. При полимеризации мономеров cо связью С=С энтальпия уменьшается (H < 0), т.е. полимеризация экзотермична. Это связано с тем, что при полимеризации раскрывается относительно малоустойчивая -связь и образуются устойчивые -связи. Таким образом, энтальпийный фактор благоприятен для протекания полимеризации. Энтропия системы при полимеризации уменьшается (S < 0), т.к., соединяясь в полимерную цепь, молекулы мономера теряют поступательные степени свободы. Следовательно, энтропийный фактор неблагоприятен для протекания полимеризации. Поскольку полимеризация термодинамически разрешена только при G < 0, то условие протекания полимеризации: H > TS. Очевидно, с ростом температуры полимеризация все менее термодинамически выгодна, но ниже 100 оС в большинстве случаев это условие выполняется. Однако величина G, а значит и термодинамическая выгодность полимеризации в значительной степени зависит от строения мономеров. Изменение энтропии мало зависит от строения мономеров; зависимость касается, в основном, изменения энтальпии.
Величина Н, в зависимости от строения мономера, может меняться в интервале 30-100 кДж/моль (например, для -метилстирола Н = 34 кДж/моль, а для винилацетата Н = 88 кДж/моль). Особенности строения мономеров, влияющие на величину Н:
1. Сопряжение. Если в мономере двойная связь сопряжена с -электронной системой заместителя, то при полимеризации сопряжение теряется; это энергетически невыгодно и приводит к снижению величины Н (например, для стирола Н = 60 кДж/моль).
 2. Пространственные особенности.
Если мономер содержит при двойной
связи объёмные заместители, то при
полимеризации пространственное
напряжение возрастает, т.к. при sp3-
атоме углерода полимерного звена более
«тесно», чем при sp2-
атоме углерода мономера. Это также
снижает величину Н.
Пространственный фактор становится
заметным уже при полимеризации
1,1-дизамещенных производных этилена:
2. Пространственные особенности.
Если мономер содержит при двойной
связи объёмные заместители, то при
полимеризации пространственное
напряжение возрастает, т.к. при sp3-
атоме углерода полимерного звена более
«тесно», чем при sp2-
атоме углерода мономера. Это также
снижает величину Н.
Пространственный фактор становится
заметным уже при полимеризации
1,1-дизамещенных производных этилена:
Для примера можно сравнить приведенные выше величины Н для стирола и - метилстирола.
Кинетический фактор. На величину энергии активации влияют особенности как электронного, так и пространственного строения мономеров.
Особенности электронного строения – степень поляризации и поляризуемости связи С=С; чем больше поляризация и выше поляризуемость связи С=С, тем легче она раскрывается. При этом важен характер поляризации – он может определять наиболее подходящий механизм полимеризации (донорные заместители – катионный, акцепторные – анионный, см. выше).
Особенности пространственного строения: чем более объёмные заместители находятся при связи С=С, тем выше энергия активации и, следовательно, ниже скорость полимеризации (т.е. объёмные заместители уменьшают и термодинамическую выгодность и скорость полимеризации).
Резюмируя сказанное, можно сказать, что большинство монозамещенных производных этилена можно полимеризовать, даже если этот единственный заместитель имеет большой объём и (или) -электронную систему (исключение – аллильные мономеры, для которых полимеризации препятствует аутоингибирование (стр. 20). Для дизамещенных производных этилена уже наблюдаются ограничения; при этом 1,1-дизамещенные полимеризуются труднее, чем 1,1-дизамещенные. Три – и тетразамещенные производные этилена не полимеризуются, за исключением тетрафторэтилена и хлортрифторэтилена, т.е. мономеров, содержащих заместители малого объёма.
Ц
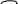 иклические
мономеры n
А─ В
[-A B-]n
иклические
мономеры n
А─ В
[-A B-]n
Термодинамический фактор. А. Изменения энтальпии. В отличие от полимеризации производных этилена, здесь при полимеризации обычно образуются такие же связи, что и разрываются. Поэтому изменения энтальпии (тепловой эффект реакции) связан не с разными типами связей, а в первую очередь с напряженностью циклов (их угловым и торсионным напряжением). Для 3- и 4-членных циклов характерно большое угловое и торсионное напряжение, поэтому полимеризация с их раскрытием ведет к значительному уменьшению энтальпии. Для 5-членных, а также 7-11-членных циклов характерно определенное торсионное напряжение при отсутствии углового; поэтому при их полимеризации энтальпия также уменьшается, но не столь значительно. Для 6-членных циклов, а также для макроциклов (с числом членов 12 и более) напряжение отсутствует, и их полимеризация не изменяет энтальпию системы.
Б. Изменения энтропии. Энтропия цикла определяется вероятностью образования цикла из ациклического предшественника: чем меньше вероятность такого замыкания, тем меньше энтропия цикла. Очевидно, чем больше размер цикла, тем меньше его энтропия, т.к. меньше вероятность встречи концов цепи, необходимой для его замыкания. Следовательно, по энтропийной составляющей увеличение размеров цикла увеличивает его термодинамическую склонность к полимеризации. [Сказанное относится к обычным процессам, при которых замыкание цикла происходит при случайном столкновении концов цепи; действительно, из органической химии хорошо известна трудность получения макроциклических соединений. Если же замыкание цикла идет «по программе» в ходе ферментативной реакции, то достаточно легко образуются циклические структуры, содержащие многие тысячи звеньев, в частности кольцевые ДНК].
Если теперь оценить термодинамическую склонность к полимеризации циклических мономеров, то можно сделать следующие обобщения:
1. Полимеризация 3- и 4-членных циклов термодинамически выгодна вследствие значительного увеличения энтальпии при раскрытии этих напряженных циклов. Энтропийный фактор здесь особой роли не играет; энтропия этих циклов достаточно велика.
2. Полимеризация средних циклов (7-11-членных) термодинамически достаточно выгодна т.к. при полимеризации исчезает некоторое торсионное напряжение (некоторое уменьшение энтальпии), а также несколько возрастает энтропия системы, т.к. энтропия средних циклов уже достаточно невелика.
3. Полимеризация макроциклов (с числом членов 12 и более) термодинамически выгодна благодаря увеличению энтропии при их раскрытии (как уже упоминалось, энтальпия при этом не изменяется).
4. Полимеризация 5- и 6-членных циклов термодинамически наименее выгодна, т.к. напряжение в этих циклах мало или вовсе отсутствует, а их энтропия еще достаточно велика.
Кинетический фактор. Здесь ситуация аналогична случаю мономеров со связью С=С: должны учитываться полярность связи и пространственные особенности строения мономера. Роль полярности отражена в том, что преимущественно полимеризуются гетероциклические соединения; при этом разрывается полярная связь углерод-гетероатом. Из карбоциклических мономеров полимеризуются циклопропаны (содержащие не «классические -связи, а связи «с частичным -характером»), а также циклоалкены по механизму метатезиса (стр. 49); это подчеркивает роль выбора подходящего механизма .
Роль пространственных особенностей отражена в том, что если у связи, которая разрывается при полимеризации, имеются объемные заместители, полимеризация затруднена.
