1. Регенерація: визначення, види і біологічне значення, зв'язок із запаленням. Морфогенез регенераторного процесу.
Регенерация -- восстановление элементов ткани взамен погибших в результате их гибели.
-
Виды регенерации
Клеточная регенерация — размножение клеток митотическим и амитотическим путями
Лабильные ткани (клетки): пограничные ткани, кожа, слизистые оболочки, а также кроветворной, лимфатической систем, костей, костного мозга
Клеточная и внутриклеточная регенерация
Стабильные ткани (клетки): печень, почки, вегетативная нервная система
Внутриклеточной регенерации – восстановление ультраструктур клетки (ядра, ядрышек, митохондрий, рибосом, пластинчатого комплекса) и их компонентов
Перманентные ткани (клетки): сердце и головной мозг
-
Лабильные ткани (клетки)
Стабильные ткани (клетки)
Перманентные ткани (клетки)
Примеры
эпителиальные клетки, ростковые гемопоэтические клетки
паренхиматозные клетки (гепатоциты, ациноциты поджелудочной железы и т.д.] и мезенхимальные клетки (фибробласты, эндотелиальные клетки
высокодифференцированные клетки (нейроны, кардиомиоциты и др
Регенерация
Физиологическая регенерация
Репаративная регенерация
субституция
Могут легко регенерировать после повреждения до тех пор, пока сохраняется пул стволовых кл
Способны пролиферировать в ответ на повреждение или в результате потери тканевой массы развиваясь из G0
Окончательно дифференцированные и непролиферирующие
Адаптационные механизмы
гиперплазия, метаплазия, атрофия
гипертрофия, гиперплазия, атрофия
гипертрофия, атрофия
Чем выше дифференцировка клеток, тем меньше вероятность кл.регенерации!
Различают три вида регенерации: физиологическую, репаративную и патологическую
Физиологическая регенерация -- восстановление всех элементов живой материи, гибнущих в процессе жизнедеятельности; самообновление. Стимулируется CFS (колониестимулирующий фактор)
Патологическая регенерация -- извращение регенераторного процесса (гипер- или гипорегенерации, метаплазии и дисплазии)
Репаративная регенерация -- восстановление утраченной части в результате патологических процессов. Стимулируется факторами роста
Полная регенерация, или реституция -- восстановление идентичной утраченной ткани за счет пролиферации и дифференциации (клеточная регенерация) при умеренном повреждении, без задевания экстрацеллюлярного матрикса (ЭЦМ)
Неполная регенерация, или субституции -- образование на месте повреждения соединительнотканного рубца при глубоком повреждении, с задеванием экстрацеллюлярного матрикса (ЭЦМ)

Инкапсуляция, переходящая в петрификацию -- омертвевшие массы, животные паразиты, инородные тела не рассасываются, а обрастают соединительной тканью, которая отграничивает их от остальной части органа
Организация -- замещение участка некроза или тромба соединительной тканью. Она происходит, если омертвевшие или тромботические массы рассасываются и одновременно в них врастает молодая соединительная ткань, превращающаяся затем в рубец

Контроль клеточной популяции |
|
Аутокринные сигналы |
|
Паракринные сигналы |
|
Эндокринные сигналы |
Спец.секр.кл выделяющие гормоны которые по крови распространяются по организму |
Юкстакринные сигналы |
Контакт кл. с межкл.матриксом |
Морфогенез полной регенерации:
Пролиферация: размножаются молодые, недифференцированные клетки — камбиальные (от лат. cambium — обмен, смена), стволовые, клетки-предшественники.
Стволовые клетки характеризуются тремя важными особенностями:
длительного самоподдержания в недифференцированном состоянии (самовосстановление симметричным разделением, при котором обе дочерние клетки остаются стволовыми);
дифференцировка одной из дочерних клеток после асимметричного деления материнской стволовой клетки (одна дочерняя клетка остается стволовой клеткой, а другая дочерняя клетка становится комитированной -- способной к дальнейшему развитию);
способностью к миграции полипотентных и комитированных стволовых клеток в органы, где они формируют ниши фиксированных стволовых клеток.
Клетки, обновляемые путем митотического деления, находятся в ткани либо в состоянии выполнения специфических функций (фазе G-0 или интерфазе), либо в состоянии деления (в одной из фаз митоза).


Факторы роста |
полипептиды синтезируемые и выделяющиеся в межклеточный матрикс, которые через специфические трансмембранные клеточные рецепторы влияют на клетки ближайшего микроокружения |
эпидермальные, инсулиноподобные, тромбоцитные, трансформирующие, эндотелиальные, ангиогенные, факторы роста нервных клеток, фибробластов, плацентарный и печеночный факторы роста, мозговой нейротрофный фактор, цилиарный нейротрофный фактор, эритропоэтин |
Цитокины |
подтип ФР -- короткоживущие гликопротеины, синтезируемые и секретируемые в межклеточное пространство неспециализированными клетками, которые через специфические рецепторы оказывают локальное влияние на соседние клетки и межклеточный матрикс. |
интерлейкины-1, 4, 6, фактор некроза опухолей, гемопоэтические колониестимулирующие цитокины, интерфероны фиброгенные цитокины.
|
Дифференцировка: молодые клетки созревают, происходит их структурно-функциональная специализация.
Дифференцировку новообразованных клеток обеспечивают гены-регуляторы дифференцировки этих клеток (синтез ранних и поздних специфических рецепторов к молекулам регулирования роста + синтез цитоплазматических сигналопреобразовательных протеинов.), а также факторы роста, цитокины и гормоны внеклеточной среды. В кл формируются новые рецепторы, чувствительных к определенным молекулам регулирования роста, благодаря чему клетка приобретает целенаправленно изменяющуюся избирательную чувствительность (компетентность) к факторам роста = фенотипная направленность клеточного дифференцирования и формирование из вновь незрелых клеток необходимых популяций специализированных клеток.
Морфогенез неполной регенерации (фиброплазия)
Основные стадии фиброплазии:
неоангиогенез (постройка новых сосудов)
миграция и пролиферация фибробласты (→миофибробласты)
синтез БСТ (коллаген – синий при трихромная окраска по Массону)
ремоделирование (сжатие и уплотнение) соединительной ткани
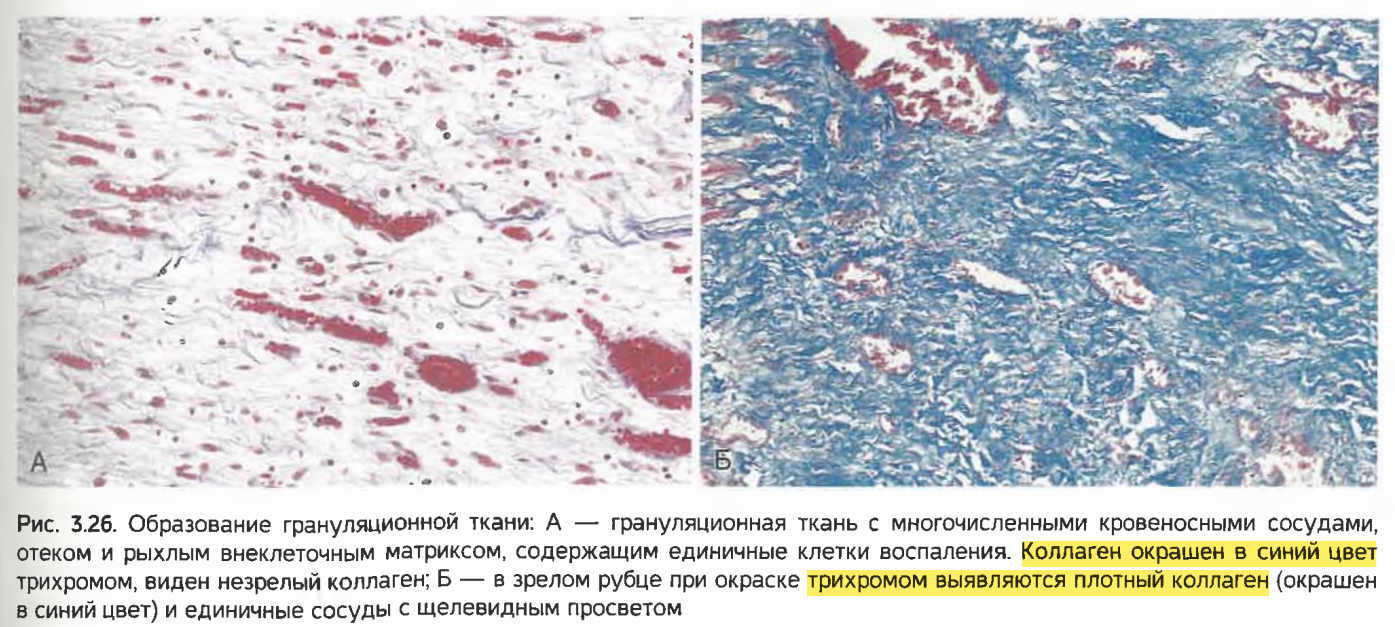
*На 2 рисунке изображен плотный коллаген с некоторыми расширенными кровеносными сосудами, характерный для завершающей фазы заживления ран, развивающейся к концу первого месяца после повреждения. В первый день рана заполняется только фибрином и воспалительными клетками. Макрофаги и грануляционная ткань наблюдаются через 2–3 дня после операции. Неоваскуляризация наиболее заметна к 4 и 5 дням. К 2 неделе коллаген заметен, и наблюдается меньше сосудов и воспалительных клеток.
2. Регенерація окремих видів тканин та органів. Регенерація сполучної тканини. Грануляційна тканина: морфологічна характеристика ії стадій. Види загоювання ран.
Реституция (эпителий)
Роговица глаза и слизистых органов
Кожа
Любой орган
Субституция:
Постинфарктный кардиосклероз
Причины: коронарный атеросклероз (атеросклеротический кардиосклероз), ведущий к развитию инфаркта миокарда (крупноочаговый кардиосклероз), а за ним рубец; хроническая аневризма сердца с гипертрофией
Исход: СН, аритмии, развития хронической аневризмы сердца.
Микро: Менее окрашенные участки – разрастание соединительной ткани, кардиомиоцитов немного, они поярче, гипертрофированы


Макро: размеры и масса увеличены вследствие разрастания соединительной ткани, в мышце сердца образуются различной величины белесоватые тяжистые участки (рубцы). Они пронизывают толщу мышцы сердца и представляют обширные поля + гипертрофия

Репарация в ЦНС: микроинфаркт замещается фибриллами, которые синтезируют фибрилообразующие астроциты


Макро: киста на месте инфаркта

Репаративная регенерация крови.
Замещение ЖКК на ККМ. Жировые клетки вытесняются растущими островками кроветворной ткани, которая заполняет костно-мозговой канал и выглядит сочной, темно-красной. Кроме того, кроветворение начинает происходить вне костного мозга — внекостномозговое, экстрамедуллярное кроветворение (селезенке, печени, лимфатических узлах, слизистых оболочках, жировой клетчатке).
Репаративные возможности органов кроветворной и иммунокомпетентной систем.
Костный мозг может восстанавливаться даже при значительных повреждениях.
Лимфатические узлы хорошо регенерируют, если сохранены связи приносящих и выносящих лимфатических сосудов с окружающей их соединительной тканью.
Селезенка рубцуется.
Регенерация кровеносных и лимфатических сосудов.
Микрососуды: в стенке появляются боковые выпячивания усиленно делящихся эндотелиальных клеток (ангиобластов). Образуются тяжи из эндотелия с просветом, в них поступает кровь или лимфа из материнского сосуда. В сосудистую стенку врастают нервные волокна из предсуществующих нервов.
Крупные сосуды: при повреждении восстанавливаются лишь структуры внутренней оболочки, ее эндотелиальная выстилка; элементы средней и наружной оболочек обычно замещаются соединительной тканью, что нередко ведет к сужению или облитерации просвета сосуда
Регенерація сполучної тканини. Грануляційна тканина: морфологічна характеристика ії стадій
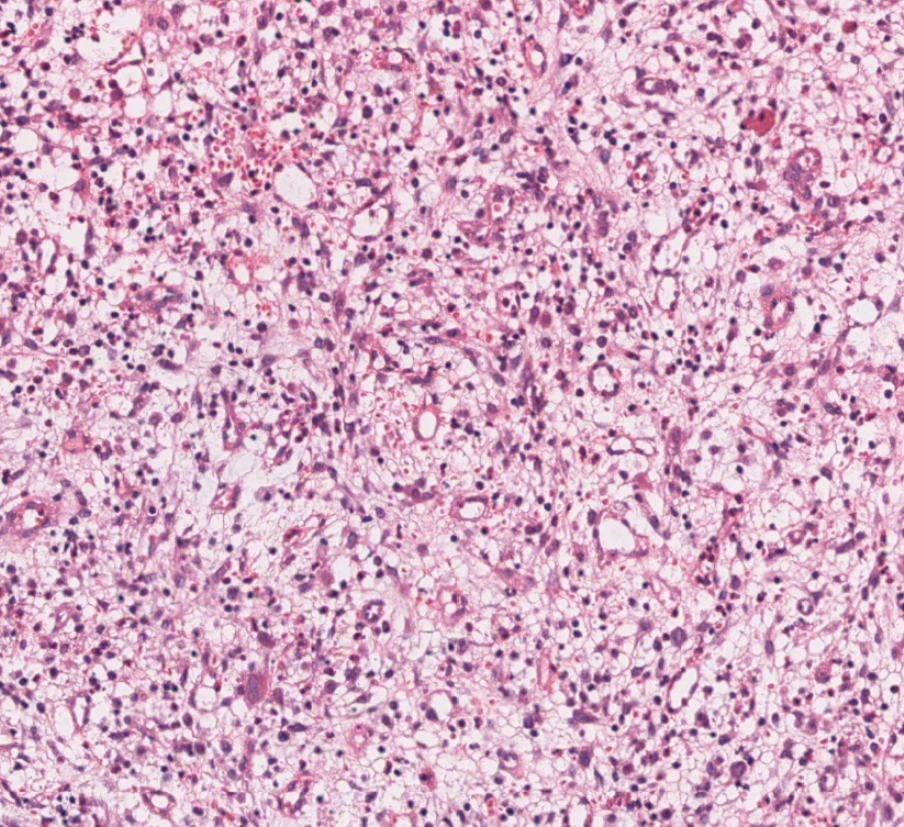
Новообразования микрососудов + пролиферации молодых мезенхимальных элементов. Образуется молодая, богатая клетками и тонкостенными сосудами соединительная ткань — сочная, темно-красная ткань с зернистой, усыпанной крупными гранулами поверхностью, — грануляционная ткань. Между сосудами расположены недифференцированные лимфоцитоподобные клетки соединительной ткани, лейкоциты, плазматические клетки и лаброциты. Количество гематогенных элементов уменьшается, а фибробластов — увеличивается. В связи с синтезом фибробластами коллагена в межклеточном пространстве образуются аргирофильные, а затем и коллагеновые волокна. Синтез фибробластами гликозаминогликанов способствует образованию основного вещества соединительной ткани. По мере созревания фибробластов количество коллагеновых волокон увеличивается, они группируются в пучки; одновременно уменьшается количество сосудов, они дифференцируются в артерии и вены. Созревание грануляционной ткани завершается образованием грубоволокнистой рубцовой ткани.
|
|
|
|
||
Регенерация жировой ткани происходит за счет новообразования соединительнотканных клеток, которые превращаются в жировые клетки (адипозоциты) путем накопления в цитоплазме липидов.
Регенерация костей.
Первичное сращение (при неподвижных отломках):