
- •Общая химическая технология
- •Лабораторная работа №1 Синтез гидрокарбоната и карбоната натрия
- •Ход работы
- •Анализ полученных гидрокарбоната и карбоната натрия
- •Ход определения
- •Лабораторная работа №2 Определение содержания карбонатов в пробе потенциометрическим методом Теоретические основы метода
- •Выполнение определения
- •Расчет результатов определений
- •Условие не выполняется
Министерство науки и высшего образования Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
высшего образования
«Уфимский государственный нефтяной технический университет»
Институт химических технологий и инжиниринга ФГБОУ ВО УГНТУ
в г. Стерлитамаке
Кафедра «Общая химическая технология»
Общая химическая технология
Лабораторные работы
Выполнил: студент группы БТСз-20-31 |
|
|
Проверил: |
|
|
Стерлитамак 2024
Лабораторная работа №1 Синтез гидрокарбоната и карбоната натрия
Целью работы является определение времени необходимого для полной карбонизации аммиачно-солевого раствора.
Карбонизация служит примером сложного гетерогенного некаталитического процесса, происходящего при невысоких температурах в системе Г-Ж, а затем Г- Ж-Т.
В основе применяемого в промышленности аммиачного способа получения соды лежат химические реакции:
NH3 + H2O + CO2 → NH4HCO3
NH4HCO3+ NaCl → NaHCO3+ NH4Cl
NaHCO3 → Na2CO3 + CO2 + H2O
Практическая необратимость второй реакции обусловлена очень малой растворимостью гидрокарбоната натрия в холодной воде, содержащей диоксид углерода.
В настоящей работе изучаются основные стадии производства соды - карбонизация аммиачно-солевого раствора. Карбонизация в производстве кальцинированной соды является основной решающей операцией, от которой зависит выход и качество продукта.
Приборы и реактивы
- Аппарат Киппа или Кирюшкина для получения СО2
- Цилиндр вместимостью 100-150 см с пробкой, через которую проходит трубка-барботер
- Установка вакуумного фильтрования.
- Фарфоровая чашка, фарфоровые тигли
- Бюретки, вместимостью 25, 50 мл
- Пипетки вместимостью 10 мл
- Колбы конические вместимостью 100-200 мл
- Колбы мерные вместимостью 100 мл
- Хлорид натрия (мелкокристаллический), ч.д.а. - Раствор аммиака 10 %
- Хлороводородная кислота, 1 н. раствор
- Гидроксид натрия, 0,1 н. раствор - Фенолфталеин
- Метиловый оранжевый
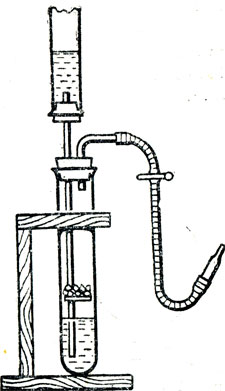
Прибор Кирюшкина состоит из пробирки с трубкой для выхода газа и вставленной в неё пробки с длинной воронкой, на нижней части которой укреплена прокладка. Газоотводная трубка снабжена краном, регулирующим ток выделяющегося газа. Выньте пробку с воронкой из пробирки, но не полностью, а на 2-3 см и в образовавшийся зазор опустите несколько кусочков мрамора так, чтобы они оказались на прокладке. После этого плотно закройте пробирку пробкой. Налейте в воронку разбавленный раствор соляной кислоты 1:4, в таком количестве, чтобы кислота полностью покрыла мрамор. Закрываем кран на газоотводной трубке. Если кислота поднимается вверх по воронке, значит, прибор герметичен и готов K использованию.
Ход работы
Приготовить 25 мл 10 %-ного раствора аммиака, насыщенного хлоридом натрия при комнатной температуре. Для этого по плотности аммиачного раствора (по справочнику) вычислить массу воды, содержащейся в 50 мл аммиачного раствора, и, зная растворимость NaCl (по справочнику), рассчитать количество хлорид натрия, способное раствориться и вычисленном количестве воды. Отвесить соль на технических весах на 2-3 г больше рассчитанного количества и растворить се в стакане (или в колбе) в 50 мл 10 %-ного раствора аммиака.
m (NaCl) = 5,385+3 г при растворимости 35,9/100 г воды; m (NH4OH) = 9,1 г; m (H2O)=15 г.
Полученный насыщенный раствор профильтровать в цилиндр вместимостью 100-150 мл. Воронку с не растворившимся хлоридом натрия поместить сушильный шкаф, высохшую соль собрать и взвесить для учета при вычислении выхода. Цилиндр закрыть пробкой с газоотводной трубкой, доходящей почти до дна склянки, и пропускать через раствор диоксид углерода из аппарата Киппа или прибора Кирюшкина 50-55 мин.
Карбонизацию проводить в вытяжном шкафу (или в боксе). Ток газа регулировать таким образом, чтобы он создавал в цилиндре некоторое давление, но не вышибал пробку, Температуру раствора поддерживать 25-26 "С. В случае повышения температуры выше 30 "С поместить цилиндр с реакционной смесью в сосуд с холодной водой.
Полученный осадок NaHCO3 отфильтровать на воронке Бюхнера, промыть небольшим количеством ледяной воды и тщательно высушить между листами фильтровальной бумаги. Полученный гидрокарбонат натрия взвесить, c точностью до 0,0002 г. перенести в фарфоровую чашку и осторожно, во избежание разбрызгивания, прокалить до прекращения выделения водяных паров, периодически помешивая стеклянной палочкой в сушильном шкафу при температуре 270-300°С, до постоянной массы.
Охладить чашку с Na2CO3 и взвесить полученный карбонат. Вычислить выход кальцинированной соды по хлориду натрия.
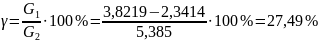
где: G1 - масса сухого остатка, полученного в ходе работы, г
G2 - количество NaCl в исходном растворе, г.
