
Микра (экз)
.pdf
Ответы на экзаменационные вопросы по Микробиологии
Препараты коррекции дисбактериоза
1)Пробиотики – живые микроорганизмы, обитатели нормальной микрофлоры кишечника (бифидосодержащие препараты, лакто содержащие препараты, коли содержащие препараты).
2)Симбиотики – это пробиотики, включающие в себя два или более штамма живых пробиотических микроорганизмов, оказывающих стимулирующие друг друга эффекты.
3)Пребиотики – препараты немикробного происхождения, способны стимулировать рост и процессы метаболизма представителей нормальной микрофлоры – это олигосахариды.
4)Синбиотики – это пробиотические комплексные продукты, в состав которых введены живые пробиотические микроорганизмы и пребиотические субстанции, стимулирующие их рост.
5)Комбиотики – варианты синбиотических средств, в состав которых помимо пробиотических микроорганизмов и пребиотиков, добавлены другие функциональные пищевые ингредиенты (вита- минно-минеральные премиксы, фенолсодержащие растительные соединения).
6)Аутобиотики – это пробиотики и продукты функционального питания на основе аутоштаммов
иаутоассоциаций симбиотических микроорганизмов.
17. Генетический аппарат бактерий и его особенности. Плазмиды бактерий.
Основное генетический материал представлен 2-нитевой суперспирализованной молекулой ДНК, замкнутой в кольцо и прикрепленной к ЦПМ – нуклеоид (хромосома)
Внехромосомный набор генов:
•Плазмиды – несет доп. Информацию, молекулярная масса меньше нуклеоида
•Подвижные элементы: IS-последовательности, транспозоны и интегроны
ОСОБЕННОСТИ ГЕНЕТИЧЕСКОГО АППАРАТА БАКТЕРИАЛЬНОЙ КЛЕТКИ:
а) цитологические:
•основной генетический материал представлен нуклеоидом;
•у прокариотов структурно-неоформленное ядро, т.е. без мембраны и ядрышек;
•в нуклеоиде одна хромосома, поэтому нуклеоид=хромосома
•в бактериальной клетке может быть дополнительное наследственное вещество – плазмида;
•молекула ДНК нуклеоида и плазмиды прикрепляются одной нитью к ЦПМ
•ДНК находится в цитоплазме
б) молекулярные:
•хромосома бактерий имеет кольцевую структуру, суперспирализована
•хромосома бактерий – чистая двунитчатая ДНК, не содержит гистонов (их роль выполняют полиамины)
•в ДНК бактерий повышенное содержание метиллированных (минорных) азотистых оснований, они выполняют защитную функцию гистонов;
•ДНК бактерий содержит IS-последовательности, строение которых аналогично таким же участкам ДНК у высших организмов;
•отмечается выраженная изменчивость нуклеотидного состава: соотношение гуанина и цитозина (Г/Ц – индекс) у бактерий имеет видовые отличия
Плазмиды – дополнительные, внехромосомные элементы наследственности
•плазмида, как и хромосома, представлена кольцевой молекулой двунитчатой ДНК, но ее размеры значительно меньше хромосомы
•плазмида содержит структурные гены, кодирующие тот или иной признак, гены автономной репликации, IS-последовательности
•у некоторых плазмид есть гены, ответственные за ее трансмиссивность (перенос, передачу). Такие плазмиды называют трансмиссивными (конъюгативными).
•гены плазмид не несут обязательную информацию клетки, сообщают селективные преимущества
•молекулярная масса значительно меньше, чем у хромосомы
21

Ответы на экзаменационные вопросы по Микробиологии
•плазмиды способны к автономной репликации ИЛИ их репликация находится под ослабленным контролем хромосомы
•для плазмид с низкой молекулярной массой характерно явление амплификации (многокопийности);
•молекула ДНК плазмид более подвержена воздействию физических и химических агентов, чем хромосомы; частота плазмидных мутаций выше, чем хромосомных
•некоторые физические (УФ, СВЧ и др.) и химические агенты вызывают элиминацию (удаление, потеря) плазмид
•плазмиды могут содержать tra-гены и самостоятельно передаваться в процессе конъюгации, это конъюгативные плазмиды
•в клетке могут находиться несколько разных плазмид, но некоторые плазмиды несовместимы между собой; по этому признаку различают группы несовместимости плазмид
Вклетке могут находится в одном из двух альтернативных состояний:
1.Либо они лежат свободно в цитоплазме и тогда их репликация идет автономно, то есть независимо от репликации хромосом. А так как они значительно меньших размеров, то реплицируются быстрее и в короткое время накапливается большое количество копий плазмид.
2.Если они находятся в интегрированом состоянии, то репликация их синхронна с репликацией хромосомы.
Функции плазмид:
1)регуляторная – в случае повреждения хромосомы, могут взять на себя ее функции
2)кодирующая – помогает выжить в определенных условиях; содержит структурные гены, отвечающие за устойчивость к АБ; отвечают за синтез экзотоксинов (энтеротоксинов в толстой кишке)
Плазмиды могут детерминировать разные свойства бактерий:
1.R-плазмиды – кодируют лекарственную устойчивость (АБ-устойчивость);
2.F-плазмида – определяет пол бактерий (передача генетической информации);
3.Col-плазмиды – синтез колицинов;
4.Hly-плазмиды – кодируют синтез гемолизинов;
5.Ent-плазмида – синтез энтеротоксинов;
6.Плазмиды биодеградации – расщепление органических и неорганических соединений Наличие F-плазмиды (фактор фертильности, половой фактор) придает бактериям функции до-
нора, и такие клетки способны передавать свою генетическую информацию другим, F – клеткам. Таким образом, наличие F-плазмиды является генетическим выражением пола у бактерий.
С F-плазмидой связана не только донорская функция, но и некоторые другие фенотипические признаки. Это, в первую очередь, наличие F-пилей (половых ресничек), с помощью которых и устанавливается контакт между донорскими и реципиентными клетками. Через их канал и передается донорская ДНК при рекомбинации. На половых ресничках расположены рецепторы для мужских fiфагов. F – клетки не имеют таких рецепторов и не чувствительны к таким фагам.
Особое значение в медицинской микробиологии занимают R-плазмиды, которые содержат набор генов, определяющих синтез ферментов, разрушающих антибиотики.
Такая плазмида делает бактериальную клетку невосприимчивой (резистентной) к определённому набору антибиотиков.
Многие R-плазмиды являются трансмиссивными, и они передаются между бактериальными клетками. Часто это приводит к появлению популяций, очень устойчивых к различным препаратам, что лежит в основе развития внутрибольничных инфекций.
18. Мобильные генетические элементы бактерий. CRISPR-CAS бактерий.
К мобильным генетическим элементам относят:
IS-последовательности – нуклеотидные последовательности, не кодирующие вырезку белка, а ответственные за выделение транспозонов в молекулу ДНК.
IS-последовательности - короткие фрагменты ДНК
22
Ответы на экзаменационные вопросы по Микробиологии
Они не несут структурных (кодирующих тот или иной белок) генов, а содержат только гены, ответственные за транспозицию (способность IS-последовательностей перемещаться по хромосоме и встраиваться в различные ее участки)
* IS-последовательности одинаковы у разных бактерий
Отличительной особенностью IS элементов является наличие на концах вставочной последовательности инвертированных повторов. Эти инвертированные повторы узнает фермент транспозаза.
Транспозоны – участки ДНК, способные к перемещению внутри молекул и от одной к другой, могут быть переданы из клетки в клетку.
Функционируют подобно IS-элементам, однако содержат не только гены перемещения, но и некоторое количество структурных генов (в среднем транспозон содержит от 1500 до 3000 п.н.). Это могут быть, например, гены устойчивости к антибиотикам; гены, определяющие продукцию факторов вирулентности и т.д.
Интегроны — генетические элементы, которые содержат в себе ген интегразы, специфический сайт и рядом с ним промотор, что придает им способность интегрировать в себя мобильные генные кассеты и экспрессировать присутствующие в них беспромоторные гены.
Помимо плазмид и подвижных генетических элементов у бактерий существует еще одна система, способствующая распространению генов - система ИНТЕГРОНОВ. Интегроны являются системой захвата малых элементов ДНК, называемых генными кассетами.
Важное свойство мобильных генетических элементов: они не являются самостоятельными генетическими структурами. То есть они не способны к автономной репликации, а реплицируются только в составе ре-пликона.
Роль мобильных генетических элементов:
1.Могут «выключать» ген при перемещении в новый участок;
2.Нередко приводят к мутациям: делеции или вставки новых последовательностей;
3.Определяют эволюцию микробных клеток.
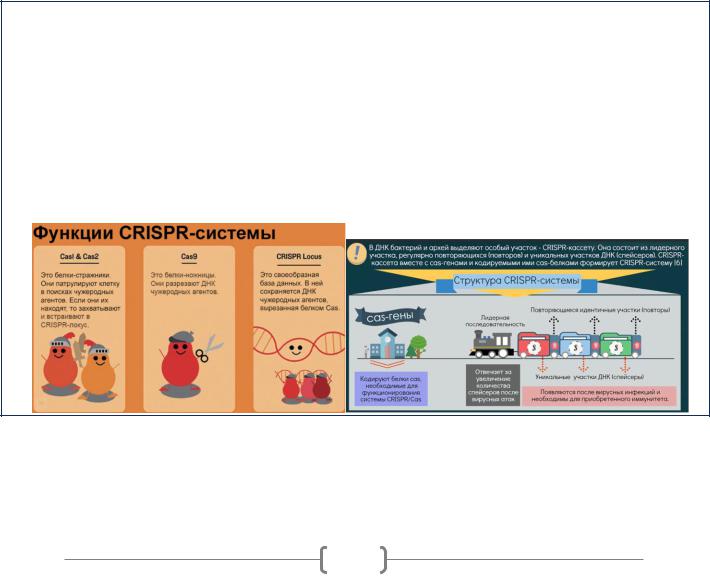
CRISPR/Cas — это короткие палиндромные повторы, регулярно расположенные группами (равноудаленно расположенные в геноме)
ЗДЕСЬ, ПО СУТИ, ВСЯ ИНФОРМАЦИЯ ПО ЭТОЙ СИСТЕМЕ (ВЕСЬ МЕХАНИЗМ)
Эти равноудаленно расположенные повторы различают отличающиеся участки – фрагменты встроившихся генов бактериофагов, которые в норме должны убить бактерию, но бактерия какимто образом выжила (оставлю ссылку на видео, откуда взяла информацию). Однако оказалось, что у бактерий вырабатывается так ИС (белок Cas1/2, после внедрения бактериофагом фрагмента своего ДНК в клетку, опережает его и отрезает кусочек ДНК вируса (это обезвреживает вирусную ДНК) и сам вставляет в геном бактерии, и т.к. это неполная вирусная ДНК, она не нанесет вред бактерии.
Формирование бактериологической «иммунологической памяти»: клетка транскрибирует в РНК тот участок внедренного вирусного ДНК и второй белок Cas9 с помощью этой РНК обнаруживает идентичный фрагмент вирусной ДНК и срезает ее (она больше не несет опасности после этого).
ИММУНИТЕТ: Cas1/2 – отражает первую атаку и собирает данные. Cas9 – поднимает данные и отражает повторную атаку. (похож на адаптивный иммунитет человека)
– это система адаптивного приобретенного иммунитета бактерий и архей, направленная на уничтожение проникшей в клетку чужеродной ДНК, например, фагов или плазмид
— это метод редактирования генома организма
С помощью систем CRISPR-Cas бактерии способны «записывать» в собственный геном и передавать потомству информацию о фагах, с которыми они сталкивались в течение жизни. Наличие
23

Ответы на экзаменационные вопросы по Микробиологии
таких «воспоминаний» позволяет распознавать ДНК фага и эффективней противостоять ему при повторных инфекциях.
CRISPR-системы состоят из геномных кассет, в которые записывается информация о вирусных или плазмидных инвазиях, и Cas-белков, обеспечивающих молекулярный механизм иммунитета. В ответ на инфекцию клетка с CRISPR вырезает из чужеродного генома небольшой фрагмент и встраивает его в кассету.
*используется бактериями для защиты от очередной НК (прежде всего вирусов-фагов) Палиндром – это нуклеотидная последовательность, которая одинаково читается справа налево
и наоборот.
Кроме палиндромных повторов есть лидерные и спейсеры.
Спейсеры – это копии чужой, ранее проникшей в клетку НК. Бактериальная клетка оставляет в своем геноме копию, чтобы защитить от повторного попадания
Лидерные последовательности – к ним присоединяются спейсеры, отделяемые друг от друга палиндромными повторами.
Механизм действия: вирус второй раз попадает в клетку, впрыскивает НК (протоспейсер). В ККС есть гены, отвечающие за образование белков:
•Интерфирирующие РНК – связываются с протоспейсером
•Другие белки эндонуклеазы – разрушают образовавшийся комплекс
Практическое использование криспр кас системы в медицине (для общего развития лучше знать)
Белок Cas9 можно снабдить любой соответствующей РНК, чтобы с ее помощью он мог найти участок уже в геноме и порезать его. При этом не только в вирусах и бактериях, а вообще практически в любом организме (т.е. при помощи Cas9 вырезать ген, отвечающий за то или иное заболевание и заменить его здоровым).
***белки, которые режут ДНК – нуклеазы, но в отличие от Cas9 остальные делают это строго в определенных местах. Cas9 – единственная нуклеаза, которая может резать белок в любом месте, в котором ему «укажут».
19. Механизмы изменчивости бактерий. Рекомбинации у бактерий, их особенности.
Механизма изменчивости бактерий:
1)Фенотипическая изменчивость – модификации (изменяются внешние признаки) − не затрагивает генотип.
Модификации затрагивают большинство особей популяции. Они не передаются по наследству и
стечением времени затухают, т.е. возвращаются к исходному фенотипу через большее (длительные модификации) или меньшее (кратковременные модификации) число поколений.
2)Генотипическая изменчивость затрагивает генотип. Связана с изменением генетического аппарата. В ее основе лежат мутации и рекомбинации.
Мутации бактерий – это спонтанные изменения в последовательности отдельных нуклеотидов ДНК.
По протяженности изменений повреждения ДНК - различают мутации точечные, когда повреждения ограничиваются одной парой нуклеотидов и протяженные или аберрации.
* Мутации могут быть спонтанными, то есть возникающими самопроизвольно и индуцированные.
По локализации различают:
a)гниение – затрагивают один ген;
b)хромосомные – затрагивают группу генов;
c)плазмидные – затрагивают гены плазмид.
Механизмы мутаций:
•выпадения нескольких пар нуклеотидов – делеции;
•удвоение генетического фрагмента – дупликации;
•перемещение фрагментов хромосомы – транслокации;
24

Ответы на экзаменационные вопросы по Микробиологии
•переворот участка ДНК на 180о – инверсии.
•вставка нового гена
Рекомбинации у бактерий, их особенности
Рекомбинация – перераспределение генетического материала родителей в потомстве (обмен генетического материала, приводящий к появлению новых сочетаний генов)
В процессе рекомбинации условно выделяют клетку-донор, которая отдаёт часть своего генетического материала, и клетку-реципиент, которая этот материал воспринимает. В клетку-реципиент попадает часть генетического материала, поэтому говорят о формировании так называемой мерозиготы. В мерозиготе образуется один рекомбинант, большая часть генов которого представлена ДНК клетки-реципиента, а меньшая – гены клетки-донора.
Особенности рекомбинаций у бактерий:
1.У них отсутствует мейоз и образуется не зигота, а мерозигота.
2.Однонаправленность переноса генетической информации (от донора к реципиенту)
3.Рекомбинанты содержат всю генетическую информацию реципиента и плюс часть генетической информации донора.
4.наличие нескольких механизмов рекомбинаций: конъюгация, трансформация, трансдукция, слияние протопластов.
Механизмы рекомбинаций:
I. Трансформация – обмен генетической информацией путем введения в бактериальную клетку готового препарата ДНК
*При этом клетки реципиента должны быть компетентными, то есть готовыми воспринимать генетическую информацию. Компетентность реципиента обусловлена наличием особого белка компетентности, который - повышает проницаемость клеточной стенки и ЦПМ для ДНК, -ингибирует ДНК-азы и активирует синтез рестриктаз.
Это состояние наблюдается в процессе деления клетки. Таким образом, деление является оптимальным условием для трансформации.
*происходит при культивировании реципиента на питательной среде, содержащей ДНК до-
нора (передаются единичные признаки)
II. Трансдукция – обмен генетической информации путем передачи ее от донора к реципиенту с помощью умеренных (ТРАНСДУЦИРУЮЩИХ) фагов.
*способны переносить 1 и более генов (признаков)
*Трансдуцирующий фаг – это умеренный фаг, который в процессе лизогении захватывает соседние бактериальные гены и при инфицировании новых клеток встраивает эти гены в новый геном. При строгой специфичности фага захватываются и переносятся строго определенные гены.
Трансдукция бывает:
1)Специфическая – всегда переносит один и тот же ген; располагается в одном месте хромосомы
2)Неспецифическая – передаются разные гены; их локализация постоянна
III. Конъюгация – обмен генетической информации путем передачи ее от донора к реципиенту при их прямом контакте (конъюгировании)
1)Передача ДНК осуществляется с помощью половых пилей
2)Необходима F-плазмида – определяют и контролируют процесс конъюгации
3)F-плазмиды кодируют образование половых пилей, по которой плазмидная ДНК передается в новую клетку
IV. Трансфекция – процесс введения нуклеиновой кислоты в клетки эукариот невирусным методом. Трансфецирование клеток — один из ведущих методов генной инженерии, заключающийся в изменения фенотипа путем введения в клетку чужеродной нуклеиновой кислоты.
25

Ответы на экзаменационные вопросы по Микробиологии
20. Молекулярно-генетические методы диагностики инфекционных заболеваний. Метагеномный анализ.
Генетические методы применяются для обнаружения микроба в исследуемом материале без выделения чистой культуры и определения таксономического положения микроба и внутривидовой идентификации.
Методы, используемые для внутривидовой идентификации бактерий
1.Рестрикционный анализ – метод анализа двух-
цепочечных молекул ДНК, образованных после обработки ферментами – рестриктазами. Метод проходит
в3 этапа: выделение ДНК, рестрикция ДНК, электрофорез. Бактериальную хромосому нарезают рестриктазами на множество фрагментов. Затем проводят электрофорез в пульсирующем электрическом поле, в результате которого фрагменты ДНК выстраиваются
взависимости от размера в шеренгу, образуя уникальный видоспецифический профиль. По сходству рестрикционных профилей изучаемого и известных видов микроорганизмов можно идентифицировать и типировать микроорганизмы
2.Определение плазмидного профиля – из бактериальной клетки выделяют плазмидную ДНК, которую выделяют электрофорезом в агарозном геле для определения количества и размеров плазмид.
3.Риботипирование – позволяет с помощью гибридизации обнаружить количественные различия по рибосомным оперонам и нуклеотидным последовательностям. Проводят гидролиз ДНК, которую разделяют в агарозном геле и затем гибридизируют с ДНК-зондами на 1 или более генов, кодирую-
щих 16S-, 23S-, 5S-рРНК.
Методы, используемые для обнаружения микроба без выделения его в чистую культуру
1. Метод молекулярной гибридизации – позволяет выявить степень сходства различных ДНК (при идентификации МО – сравнение ДНК выделенного штамма с ДНК эталонного штамма). Принцип метода:
2.Метод ДНК-чипов – ДНК-микрочипы используют для анализа изменения экспрессии генов, выявления однонуклеотидных полиформизмов, генотипирования или повторного секвенирования мутантных геномов. Микрочипы отличаются по конструкции, особенностям работы, точности, эффективности и стоимости
3.ПЦР являющаяся одним из методов ДНК-диагностики, позволяет увеличить число копий детектируемого участка генома (ДНК) бактерий или вирусов в миллионы раз с использованием фермента ДНК-полимеразы.
Тестируемый специфический для данного генома отрезок нуклеиновой кислоты многократно умножается (амплифицируется), что позволяет его идентифицировать. Сначала молекула ДНК бактерий или вирусов нагреванием разделяется на 2 цепи, затем в присутствии синтезированных ДНК-праймеров (последовательность нуклеотидов специфична для
26

Ответы на экзаменационные вопросы по Микробиологии
определяемого генома) происходит связывание их с комплементарными участками ДНК, синтезируется вторая цепь нуклеиновой кислоты вслед за каждым праймером в присутствии термостабильной ДНК-полимеразы. Получается две молекулы ДНК. Процесс многократно повторяется.
Для диагностики достаточно одной молекулы ДНК, то есть одной бактерии или вирусной частицы. Введение в реакцию дополнительного этапа - синтеза ДНК на молекуле РНК при помощи фермента обратной транскриптазы - позволило тестировать РНКвирусы, например, вирус гепатита С. ПЦР - это трехступенчатый процесс, повторяющийся циклично: денатурация, отжиг праймеров, синтез ДНК (полимеризация). Синтезированное количество ДНК идентифицируют методом иммуноферментного анализа или электрофореза.
В ПЦР может быть использован различный биологический материал - сыворотка или плазма крови, соскоб из уретры, биоптат, плевральная или спинномозговая жидкость и т.д. В первую очередь ЦПР применяют для диагностики инфекционных болезней, таких как вирусные гепатиты В, С, D, цитомегаловирусная инфекция, инфекционные заболевания, передающиеся половым путем (гонорея, хламидийная, микоплазменная, уреаплазменная инфекции), туберкулез, ВИЧ-инфекция и т.д.
Преимущество ПЦР в диагностике инфекционных заболеваний перед другими методами исследований заключается в следующем:
 возбудитель инфекции может быть обнаружен в любой биологической среде организма, в т.ч. и материале, получаемом при биопсии;
возбудитель инфекции может быть обнаружен в любой биологической среде организма, в т.ч. и материале, получаемом при биопсии;
 возможна диагностика инфекционных болезней на самых ранних стадиях заболевания;
возможна диагностика инфекционных болезней на самых ранних стадиях заболевания;
 возможность количественной оценки результатов исследований (сколько вирусов или бактерий содержится в исследуемом материале);
возможность количественной оценки результатов исследований (сколько вирусов или бактерий содержится в исследуемом материале);
 высокая чувствительность метода; например, чувствительность ПЦР для выявления ДНК вируса гепатита В в крови составляет 0,001 пг/мл (приблизительно 4,0.102 копий/мл), в то время как метода гибридизации ДНК с использованием разветвленных зондов - 2,1 пг/мл (приблизительно 7,0.105 копий/мл).
высокая чувствительность метода; например, чувствительность ПЦР для выявления ДНК вируса гепатита В в крови составляет 0,001 пг/мл (приблизительно 4,0.102 копий/мл), в то время как метода гибридизации ДНК с использованием разветвленных зондов - 2,1 пг/мл (приблизительно 7,0.105 копий/мл).
4. Опосредованная транскрипцией амплификация рРНК –
Метод ДНК-чипов
Одним из основных методов лабораторной диагностики инфекционных заболеваний является серологическое обследование пациентов с целью выявления антител к отдельным возбудителям.
При смешанных инфекциях, когда организм поражается сразу несколькими возбудителями, а также при дифференциации заболеваний, имеющих сходную клиническую картину, часто бывает необходимо выполнение иммунологических тест-систем - иммуночипов.
Иммуночипы для многопрофильного анализа антител представляет собой плотную подложку, на поверхности которой дискретно нанесены в определенном порядке антигены различных возбудителей инфекционных заболеваний. Результаты после выполнения анализа на иммуночипах расшифровываются по наличию сигнала в определенных зонах нанесения антигенов.
ПЦР
Суть ПЦР заключается в избирательном копировании in vitro небольшого фрагмента гена в котором предположительно может быть локализована мутация с использованием в качестве матрицы геномной ДНК обследуемого Небольшие размеры копируемого или амплифицируемого фрагмента гена в сочетании с их огромным числом позволяют в дальнейшем использовать очень простые методы для анализа этого участка ДНК выявления его особенностей у обследуемого пациента
Цель: обнаружение в исследуемом материале (или в чистой культуре бактерий) нуклеотидных последовательностей, отвечающих либо за видовую принадлежность возбудителя, либо за продукцию основного фактора вирулентности.
Принцип метода основан на естественной репликации ДНК которая включает:
-денатурацию спирали ДНК,
-расхождение нитей
-комплементарный синтез новых нитей ДНК.
27

Ответы на экзаменационные вопросы по Микробиологии
ПЦР обеспечивает амплификацию фрагментов генома и быстрое накопление определенной последовательности ДНК. В результате получают большое количество ДНК, которое достаточно для проведения анализа различными методами детекции.
Для реализации реакции используют набор праймеров-фрагментов ДНК, которые являются маркерами данного возбудителя при добавлении такого праймера к пробе исследуемого материала содержащую денатурированную одноцепочечную ДНК возбудителя происходит их соединение с комплементарным участком ДНК Образовавшиеся двунитевые фрагменты ДНК служат матрицей для синтеза новых нитей в следующем цикле амплификации и так повторяется много раз поэтому реакция носит цепной характер За 2-3- часа происходит 30-40 циклов амплификации что приводит к образованию большого количества соответствующих копий нуклеотидных последовательностей которое можно зарегистрировать
Компоненты реакции:
1.Праймеры-олигонуклеотиды которые состоят из 15-30 нуклеотидов комплементарных участкам на идентифицируемой матричной ДНК
2.Смесь дезоксинуклеотидтрифосфатов которые являются строительным материалом, используемым Tag -полимеразой для синтеза второй цепи ДНК
3.Tag -полимераза обладает ДНКполимеразной термостабильной активностью Оптимум ее действия при 720 С Она способна удлинять праймеры присоединяя их к 3’ концу
4.Буферный раствор катализатор фермента Tag -ДНК- полимеразы
5 Исследуемый образец - препарат, который служит мишенью для последующей амплификации Главными из этих методов являются электрофорез амплифицированной ДНК ее окрашивание разрезание специфическими ферментами – рестриктазами и определение нуклеотидной последовательности этого фрагмента - секвенирование ПЦР лежит в основе ДНК-диагностики любых наслед-
ственных заболеваний Данный подход широко используется и для анализа генетических факторов риска, предраспола-
гающих к развитию широко распространенных мультифакториальных заболеваний. В случае молекулярной диагностики инфекций амплифицируется фрагмент ДНК специфичный для определенного возбудителя, а затем с помощью электрофореза и окрашивания на ДНК тестируется наличие этого фрагмента, а значит и самого возбудителя в том биологическом образце, который был взят для анализа Использование ПЦР в судебной медицине основано на амплификации высоко изменчивых областей генома, позволяющих проводить идентификацию личности – метод геномной дактилоскопии.
Молекулярно-генетическое секвенирование
Эти методы позволяют анализировать только небольшую часть хромосомы микроорганизма, которая может варьировать у разных штаммов бактерий. Такая часть анализируемой ДНК должна быть информационно значимой для типирования различных штаммов определенного вида. Нуклеотидных последовательностей, удовлетворяющих всем требованиям, немного. В связи с этим широкое использование методов секвенирования для типирования патогенных бактерий будет возможно только после того, как для каждого вида возбудителей будут идентифицированы видоспецифические генетические локусы, на основании которых можно дифференцировать штаммы.
21. Понятие о химиотерапии, основные классы химиотерапевтических веществ. Антибиотики, их классификация.
Понятие о химиотерапии
Химиотерапия – это специфическое лечение, инфекционных и опухолевых заболеваний, химическими препаратами, которые избирательно действуют на болезнетворные МО.
Требования к химиотерапевтическим препаратам:
1)Химиотерапевтический препарат (ХП) должен обладать этиотропностью (подавлять жизнедеятельность и развитие возбудителя болезни или опухолевых клеток, или уничтожать его в тканях и средах организма)
2)ХП должны достаточно хорошо растворяться в воде, т.к. только в таком виде они могут быть доставлены во внутреннюю среду организма.
28

Ответы на экзаменационные вопросы по Микробиологии
3)ХП, должны быть достаточно стабильны во внутренней среде организма, но, с другой стороны, они не должны иметь кумулятивного эффекта (способности накапливаться в макроорганизме).
4)ХП должны быть безвредны. Тератогенный (способность вызывать образование отклонений в развитии) и мутагенный (способность вызывать мутации) эффекты по возможности
отсутствовать. *Безвредность оценивается химиотерапевтическим индексом – отношение минимальной терапевтической дозы препарата к максимально переносимой. Очевидно, что, чем меньше химиотерапевтический индекс, тем лучше препарат; если же этот индекс близок или равен 1, то такое вещество не может быть использовано как средство химиотерапии.
Более короткий вариант требований:
1.Хорошая терапевтическая эффективность и минимальная токсичность для человека;
2.Отсутствие побочных эффектов;
3.Достаточный спектр антимикробной активности;
4.Высокая устойчивость к колебаниям pH, что позволяет принимать их перорально;
5.Высокий процент биодоступности;
6.Не должны вызывать у микроорганизмов лекарственную устойчивость
Нередко в клинической практике понятия “химиотерапия” и “антибиотикотерапия” используются как синонимы.
Однако это неверно, т.к. Антибиотики − только один из классов химиотерапевтических препаратов, и, следовательно, антибиотикотерапия − только один из видов химиотерапии
Основные классы химиотерапевтических веществ
По направленности действия все химиопрепараты делятся на:
1)противопротозойные − метронидазол, пентамидин.
2)противовирусные − азидотимидин, ацикловир.
3)противогрибковые – полиены, нистатин
4)антибактериальные – противотуберкулезные (антимикобактериальные) и противосифили-
тические средства
По способности накапливаться в тех или иных тканях, т.е. по фармакокинетике
1)цитостатики – накапливаются в опухолевых клетках и подавляют их рост
2)уросептики – накапливаются в моче и подавляют развитие возбудителей инфекций почек и мочевыводящих путей, и др.
По химическому строению:
1)Производные мышьяка, сурьмы и висмута – производные соответствующих соединений. Применение: для лечения паразитарных инфекций и сифилиса.
2)Сульфаниламиды – производные сульфаниловой кислоты
Примеры: сульфаметоксазол, сульфаметизол, сульфацетамид, сульфадиметоксин Механизм действия: нарушение синтеза фолиевой кислоты. Через него происходит синтез
ДНК (т.е. они являются микробными антиметаболитами)
3)Диаминопиримидины – так же являются антиметаболитами (но спектр действия шире, чем у сульфаниламидов); производные пиримидиновых оснований
Примеры: тетроксоприм, триметаприм, пириметамин Механизм действия: триметоприм ингибирует образование фолиевой кислоты, но на более
поздних этапах ее синтеза усиливает действие сульфаниламида
4)Нитрофураны – производные фурана
Примеры: фурацилин, нитрофуразон, фурагин Механизм действия – одновременная блокада нескольких ферментных систем микробной
клетки.
5)Хинолоны – на основе следующих веществ
•собственно, хинолоны (налидиксовая кислота, циноксацин)
•производные хинолонов (4-аминохинолоны, 8-аминохинолоны)
6)Фторхинолоны: офлоксацин, норфлоксацин, ципрофлоксацин
Механизм действия: нарушение различных этапов синтеза ДНК (репликация, дупликация, транскрипция, репарация) микробной клетки
29

Ответы на экзаменационные вопросы по Микробиологии
Недостатки: фторхинолоны – не оказывают действие на аэробные бактерии; налидиксовая кислота – активна только в отношении Грамбактерий.
7)Азолы – являются противогрибковыми. Примеры:
•производные имидазола – миконазол, эконазол, клотримазол
•другие азолы – бифоназол, флуконазол Механизм действия:
1)ингибирование биосинтеза стероидов, что приводит к повреждению наружной КМ грибов и повышению ее проницаемости.
2)ингибирование синтеза ТАК, ФЛ; уменьшение активности ферментов окисления и фер-
ментов, тормозящих образование свободных радикалов.
Азолы для местного (поверхностные микозы, кандидозы) и системного (пневмонии, менингиты, перитониты) применения.
По способу получения
1)Природные
2)Синтетические
3)Полусинтетические (на начальном этапе препарат получают естественным путем, но
дальше синтез ведут искусственно).
Продуцентами большинства антибиотиков являются актиномицеты, плесневые грибы, но их можно получить и из бактерий (полимиксины), высших растений (фитонциды) и даже тканей животных и рыб (эритрин, эктерицид).
По направленности действия:
1)антибактериальные
2)противогрибковые
3)противоопухолевые.
По спектру действия (числу видов микроорганизмов, на которые действуют антибиотики):
1)широкоспекторные (цефалоспорины 3-го поколения, макролиды)
2)препараты узкого спектра действия (циклосерин, линкомицин, бензилпенициллин, клиндамицин).
Заметим, что препараты узкого спектра в некоторых случаях могут быть предпочтительнее, т.к. не подавляют нормальную микрофлору.
Антибиотики. Определение. Классификация АБ
Антибиотики – химиотерапевтические вещества природного происхождения или их полусинтетические и синтетические аналоги, обладающие антимикробным или противоопухолевым действием
Классификация антибиотиков:
По происхождению:
а) природные б) полусинтетические
в) синтетические
По продуцентам (в основе получения АБ лежит принцип антагонизма)
а) грибы б) актиномицеты
в) ткани животных и растений
По химической структуре:
1. β-лактамы. К ним относятся: пенициллины, цефалоспорины, монобактамы, карбапенемы, цефамицины.
1)Пенициллины:
•природные – бензилпенициллин, феноксиметил-пенициллин
•резистентные к пенициллиназе – оксациллин, клоксациллин
•аминопенициллины – амоксициллин, ампициллин
•карбоксипенициллины – карбенициллин, тикарциллин
•уреидопенициллин – азлоциллин, пиперациллин
2)Цефалоспорины:
•1-го поколения − цефазолин, цефалексин, цефаклор
30
