
5 курс / Факультетская педиатрия / Осенний семестр 5к / Занятие 3 / Надпочечники + НСД
.pdf
29. Болезнь и синдром Иценко-Кушинга. Определение. Этиология. Клиническая картина. Осложнения. Диагностика. Дифференциальный диагноз. Лечение.
Болезнь Иценко-Кушинга (БИК) – это тяжелое нейроэндокринное заболевание, обусловленное хронической гиперпродукцией АКТГ опухолью гипофиза. Увеличение секреции АКТГ приводит, в свою очередь, к хронической повышенной выработке кортизола корой надпочечников и развитию симптомокомплекса эндогенного гиперкортицизма.
Синдром Иценко-Кушинга – в русскоязычной литературе термин используется для обозначения опухоли надпочечника, секретирующей кортизол; в англоязычной литературе объединяет весь симптомокомплекс гиперкортицизма.
Этиология и патогенез:
Болезнь Иценко-Кушинга является наиболее частой причиной (80-85%) органической гиперпродукции кортизола – эндогенного гиперкортицизма (ЭГ). В 10-20% случаев ЭГ развивается из-за первичной патологии надпочечников, а в 5-10% случаев – АКТГ продуцирует карциноидная опухоль любой внегипофизарной локализации.
Причиной БИК является АКТГ-секретирующая аденома гипофиза (кортикотропинома), почти всегда доброкачественного характера. Соотношение микро- и макроаденом составляет 4:1.
Патогенез развития БИК до конца не изучен. Имеется две теории развития болезни Иценко-Кушинга:
●«Гипофизарная» теория: мутация кортикотрофов, приводящая к образованию АКТГсекретирующей аденомы гипофиза, что подтверждается моноклональным строением опухоли;
●«Гипоталамическая» теория: гиперсекреция КРГ (кортикотропин-рилизинггормона, кортиколиберина) с формированием вторичной опухоли или развитием гиперплазии гипофиза.
Вобоих случаях происходит нарушение циркадного ритма секреции АКТГ, которое выражается в повышении амплитуды и длительности пиков секреции гормона. Гиперпродукция АКТГ не подавляется высокими значениями глюкокортикоидов в периферической крови, что в результате усиленной стимуляции надпочечников вызывает диффузную гиперплазию их коры и повышение содержания кортизола в крови и других биологических жидкостях. Именно гиперкортизолемия и определяет клиническую картину заболевания.
При естественном течении БИК (без лечения) 5-летняя выживаемость составляет 50%, но значительно улучшается даже при паллиативном лечении – двухсторонней адреналэктомии – до 86%. При своевременной диагностике и лечении в высокоспециализированном центре ремиссии удаётся добиться в 80% случаев, и смертность у пациентов в ремиссии не отличается от популяционной.
Клиническая картина:
Клиническая картина болезни Иценко-Кушинга определяется проявлениями гиперкортицизма, поэтому на первом этапе дифференцировать этиологию эндогенного гиперкортицизма затруднительно.
Клинические симптомы эндогенного гиперкортицизма достаточно разнообразны и неспецифичны.
Из наиболее типичных для болезни Иценко-Кушинга симптомов, которые могут позволить заподозрить наличие гиперкортицизма при первичном посещении эндокринолога, можно выделить центральное ожирение (с отложением жировой клетчатки на туловище – животе, груди, спине с формированием т.н. «надключичных подушечек» и «климактерического горбика» в проекции VII шейного позвонка, часто на лице – «лунообразное» лицо) с одновременным уменьшением верхних и нижних конечностей в обхвате из-за атрофии мышечной и жировой ткани, «матронизм» (яркий румянец цианотического оттенка в совокупности с округлившимися чертами лица), скошенные ягодицы (вследствие атрофии мышц), широкие (часто более 1 см) багровофиолетовые стрии на животе, внутренней поверхности бедер и плеч, у женщин – на молочных железах, множественные подкожные кровоизлияния, возникающие даже при незначительных травмах.
Осложнения и их коррекция:
►Нарушение липидного обмена (гиперхолестеринемия, гипертриглицеридемия) – статины, фибраты;
►Артериальная гипертензия – комбинированная гипотензивная терапия, возможно, применение α1-адреноблокаторов при резистентной гипертензии;
►Нарушение углеводного обмена – гипогликемические препараты, в том числе инсулинотерапия, согласно рекомендациям по лечению сахарного диабета;
►Гипокалиемия – коррекция проводится спиронолактоном, препаратами калия внутрь и внутривенно капельно;
►Низкотравматические переломы на фоне стероидного остеопороза – витамин Д.
Диагностика:
Жалобы и анамнез:
-Прибавка массы тела (важно не само значение массы тела, а динамика набора массы тела, отсутствие снижения массы тела на фоне соблюдения диеты, физических нагрузок, отложения жира в области лица, шеи, спины, живота);
-Мышечная слабость (рано устает, плохо поднимается со стула, садится, играет);
-Легкое возникновение кровоподтеков (даже от трения полотенцем после душа);
-Отечность, появление стрий (распад белка в ПЖК и её расхождение, багровый цвет обусловлен просвечиванием сосудов);
-Хронические воспалительные заболевания мягких тканей / органов (долго и часто болеющие дети: пиелонефриты, циститы, синуситы);
-Оволосенение (раннее, на нехарактерных местах для ребенка и в большом количестве);
-Эмоциональная лабильность (плаксивость, раздражительность и т.п.).
! Обязательно уточнение получаемой лекарственной терапии, наличие в перечне
принимаемых препаратов глюкокортикоидов (для исключения возможности развития экзогенного гиперкортицизма).
Физикальное обследование:Выявление клинической картины – см.выше.
Лабораторная диагностика:
! Перед проведением любых лабораторных исследований необходимо исключить введение экзогенных глюкокортикоидов. В некоторых случаях пациенты не связывают изменение внешности с приемом ГК, и факт применения препаратов выявляется только при активном расспросе. Просим принести все ЛС, крема, мази, всё-всё чем пользуется ребенок, родители (ребенок может втихую что-то использовать родительское).
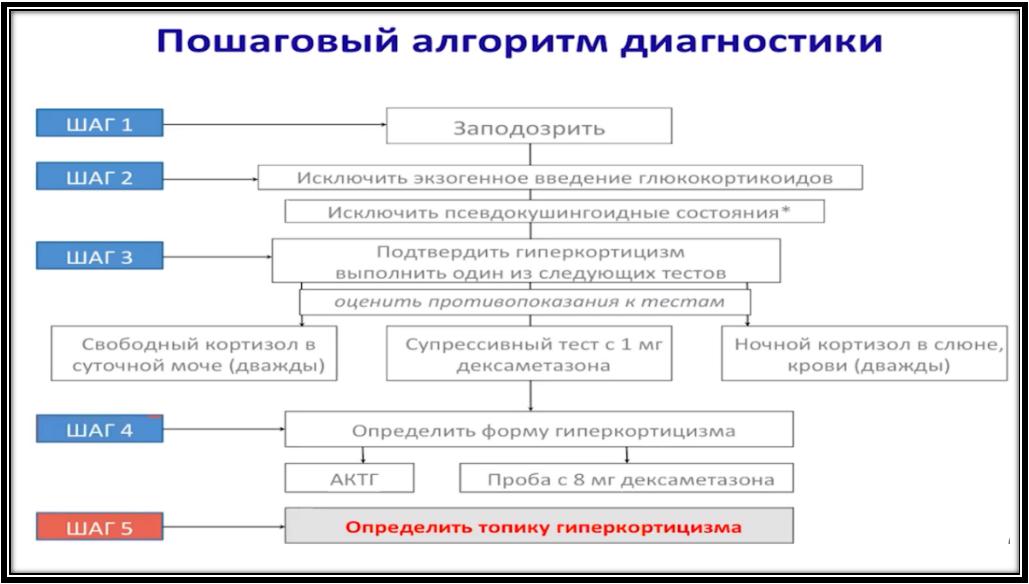
Основные методы визуализации надпочечников – КТ, МРТ и УЗИ. В первую очередь КТ или МРТ надпочечников показаны при лабораторно подтвержденной гиперпродукции кортикостероидов кортикостероидов или катехоламинов. Преимущество КТ – возможность определения злокачественного потенциала выявленного объемного образования при оценке нативной КТ-плотности. Если последняя превышает 20 ед. Хаунсфилда, вероятность злокачественного характера объемного образования высока. Значительную ценность в топической диагностике феохромоцитомы представляет сцинтиграфия.

Дифференциальный диагноз:
- Дифференциальная диагностика болезни Иценко-Кушинга и АКТГ-эктопированного
синдрома (эндогенный гиперкортицизм при АКТГ-эктопированном синдроме может быть при медуллярном рак щитовидной железы, раке клеток островков Лангерганса, хромаффиноме, раке яичников, яичек, предстательной железы; карциноиде легких, бронхов, тимуса, аппендикса, опухоли желудочнокишечного тракта, мочевого пузыря, околоушных и слюнных желез и т.д);
-Болезнь Иценко-Кушинга (опухоль гипофиза) необходимо дифференцировать с синдромом Иценко-Кушинга (опухоль надпочечников).
-Эндогенный гиперкортицизм следует отличать от экзогенного, который обусловлен приемом глюкокортикоидов в супрафизиологических дозах (уже упоминалось выше).
Лечение:
Цели лечения:
1)Контроль гиперсекреции глюкокортикоидов;
2)Удаление / разрушение опухолевой ткани с сохранением функций гипофиза (как осложнение может быть ожирение по гипоталамическому типу (читай выше));
3)Восстановление нормальной функции гипоталамус-гипофиз-надпочечниковой оси;
4) Исчезновение клинических проявлений хронического избытка глюкокортикоидов.
Виды лечечния:
Болезни Иценко-Кушинга:
1) Хирургический способ (транссфеноидальный доступ);
2)Радиотерапия (стереотаксическая радиохирургия);
3)Медикаментозная терапия (каберголин, пасиреотид).
Синдрома Иценко-Кушинга:
1)Хирургический способ (двусторонняя адреналэктомия);
2)Медикаментозная терапия – ингибиторы стероидогенеза (метирапон, кетоконазол), адренолитики (лизодрен), антагонисты рецепторов глюкокортикоидов (мифепристон).
30. Врождённая дисфункция коры надпочечников (адреногенитальный синдром). Классификация. Клиника вирильной и сольтеряющей форм. Дифференциальный диагноз. Неонатальный скрининг. Лечение и профилактика.
Врожденная дисфункция коры надпочечников (ВДКН) (адреногенитальный синдром, врожденная надпочечниковая гиперплазия) — группа заболеваний с аутосомнорецессивным типом наследования, в основе которых лежит дефект одного из ферментов или транспортных белков, принимающих участие в биосинтезе кортизола в коре надпочечников. На сегодняшний день известно 7 форм врожденной дисфункции коры надпочечников (ВДКН): 7 форм по названию дефекта конкретного фермента.
Самой частой формой ВДКН, на которую приходится более 90% больных, является дефицит 21-гидроксилазы. Распространенность дефицита 21-гидроксилазы в мире, рассчитанная по данным неонатального скрининга, составляет 1 случай на 14 000 живых новорожденных. В России, по данным скрининга, распространенность составляет 1:9500. Поскольку заболевание наследуется по аутосомно-рецессивному типу, существуют популяции, где оно встречается чаще, например некоторые этнические группы на Северном Кавказе, где распространены близкородственные браки.
Классификация (НПС):
► Неклассическая форма.
- Классические формы:
►Простая вирильная форма (Вирильный синдром – появление мужских вторичных половых признаков у женщин);
►Сольтеряющая форма.
Патогенез:
При всех формах ВДКН отмечается дефицит кортизола, что по механизму отрицательной обратной связи приводит к повышению уровня АКТГ и гиперплазии надпочечников. В результате стимуляции надпочечников происходит избыточное накопление стероидов, предшествующих ферментативному блоку. Клиническая картина каждой формы ВДКН обусловлена дефицитом гормонов, синтез которых невозможен при данном ферментативном блоке, и избытком предшественников.
Характерный для всех форм ВДКН дефицит кортизола проявляется склонностью к гипогликемическому синдрому, особенно в стрессовых ситуациях и у грудных детей. Специфическим симптомом дефицита кортизола является гиперпигментация кожи вследствие высокого уровня проопиомеланокортина и его производных. В крови определяется повышенный уровень АКТГ.
Клиника вирильной и сольтеряющей форм:
При сольтеряющей форме ВДКН отмечается дефицит минералокортикоидов. Недостаток альдостерона вызывает снижение реабсорбции натрия в почках, вследствие чего снижаются ОЦК и АД. У детей отмечаются неукротимая рвота, жидкий стул, боли в животе, резкое падение АД. Наблюдаются гиперкалиемия, гипонатриемия и повышение активности ренина плазмы.
При вирильной форме ВДКН отмечается только дефицит кортизола, что при отсутствии лечения проявляется мышечной слабостью, утомляемостью, потемнением кожных покровов на фоне симптомов гиперандрогении (гирсутизм — усиленный рост волос по мужскому типу, сбои менструального цикла, проявляющиеся в виде олигоменории либо аменореи, маскулинизация (сужение бедер, снижение тембра голоса), угревая сыпь, себорея, очень жирная кожа, увеличение клитора, уменьшение молочных желез, черный акантоз, появление мягких фибром).
Дифференциальный диагноз:

Диагностика неклассической формы ВДКН является более частой задачей и рутинно встречается в практике эндокринологов и акушеров-гинекологов, так как по клиническим проявлениям это заболевание схоже с синдромом поликистозных яичников. Именно с этим заболеванием и проводится чаще всего дифференциальная диагностика нВДКН.
Неонатальный скрининг:
В России неонатальный скрининг существует с середины 2006 г., в результате чего частота встречаемости данного заболевания выросла более чем в 2 раза. Кроме того, сократились срок постановки диагноза и степень гипонатриемии, что, по данным литературы, улучшает в дальнейшем способности детей к обучению. Процедура скрининга включает в себя забор крови у доношенных новорожденных на 4-е сутки жизни, у недоношенных на 7—10-е сутки с дальнейшим определением 17-ОН-прогестерона (17ОНР)
– это стероид, продуцируемый в надпочечниках, половых железах и плаценте. При положительном результате скрининга сведения передаются в поликлинику по месту жительства ребенка, после чего проводится повторный забор крови для ретестирования.
! При существующем в России порядке скрининга его положительная предсказательная ценность составляет от 1 до 5%, т. е. среди всех положительных результатов только от 1 до 5 детей из 100 положительных образцов действительно имеют ВДКН, в остальных случаях это ложноположительные результаты.
Лечение:
Препаратом выбора для лечения детей с ВДКН является таблетированный гидрокортизон.
Применение сиропа гидрокортизона и пролонгированных форм глюкокортикоидов у детей в период активного роста не показано.
Всем детям с сольтеряющей формой ВДКН показано назначение флудрокортизона, детям грудного возраста показано дополнительное введение в пищевой рацион поваренной соли.
Основой терапии при всех формах ВДКН является назначение глюкокортикоидов, которые позволяют заместить дефицит кортизола и тем самым подавить избыточную секрецию АКТГ.
Профилактика:
Пренатальная диагностика не является обязательной, проводится только по желанию родителей в семьях, имеющих больного ребенка, и только при условии, что родители будут прерывать беременность больным плодом. Диагностика проводится на 9—10-й неделях гестации путем получения ДНК из ворсин хориона и определения наличия мутаций гена, ответственного за развитие данной формы ВДКН.
Возможно проведение пренатальной терапии – экспериментальная разработка.
31. Хроническая недостаточность коры надпочечников. Этиология. Патогенез, клиническая картина, дифференциальный диагноз. Неотложная помощь. Лечение. Прогноз.
Хроническая надпочечниковая недостаточность (ХНН) — синдром,
обусловленный хроническим дефицитом синтеза и секреции кортизола в коре надпочечников.
Взависимости от уровня поражения в системе гипоталамус-гипофиз-надпочечники,
ННбывает первичной, которая обусловлена патологией самих надпочечников, и центральной — вторичной (связанной со сниженной секрецией адренокортикотропного гомона гипофиза — АКТГ) или третичной (связанной с нарушением секреции кортикотропин-рилизинг-гормона в гипоталамусе (КРГ).
Будем говорить дальше о первичной (ПХНН) – патологии в самих надпочечниках.
Этиология и патогенез:
В большинстве случаев (но не во всех) дефицит глюкокортикоидов (кортизола) сочетается с дефицитом минералокортикоидов (альдостерона). При отсутствии заместительной терапии надпочечниковая недостаточность является смертельно опасным заболеванием. Пациент, страдающий хронической первичной надпочечниковой недостаточностью (ПНН), нуждается в постоянной заместительной терапии глюкокортикоидами (и, в большинстве случаев, минералокорикоидами).
ПХНН — этиологически гетерогенное заболевание. Поражение надпочечников может развиваться в результате воздействия внешних факторов — кровоизлияние (чаще у детей до 1 года), инфекционное (туберкулез), опухолевое (лимфома, метастазы), адреналэктомия (при опухолях надпочечников, болезни Кушинга).
У детей чаще причиной ПХНН является одно из наследственных заболеваний, сопровождающихся нарушением эмбриогенеза, деструкцией надпочечников или дефектами стероидогенеза.
Клиническая картина:
Недостаточность глюкокортикоидов (кортизола) проявляется слабостью, быстрой утомляемостью, снижением аппетита и потерей веса, обмороками, судорогами с потерей сознания. Судорожный синдром обусловлен низким уровнем глюкозы в крови (гипогликекмией), чаще развивается после длительного ночного перерыва в приемах пищи.
Недостаточность минералокортикоидов (альдостерона) проявляется тошнотой, повышенной потребности в соли, рвотой, повторной и не приносящей облегчения, приводящей к обезвоживанию, что принято называть «сольтеряющими кризами». Симптомы обычно резко усиливаются на фоне других заболеваний, высокой температуры, стрессовых ситуаций.
Почти все симптомы дефицита кортизола и альдостерона являются неспецифичными, то есть могут быть признаком заболеваний других органов и систем (желудочно-кишечного тракта, центральной нервной системы и д.р.).
Наиболее специфическими проявлениями первичной надпочечниковой недостаточности являются гиперпигментации кожи и /или слизистых и повышенная потребность в соли. Часто окружающие впервые замечают гиперпигментацию на открытых участках тела (лицо, кисти рук). Максимальные проявления гиперпигментации отмечаются
на коже наружных половых органов, подмышечных областей, коленей, локтей, а также пигментируются соски, пупок, перианальная область и рубцы на месте повреждения кожи. Участки гиперпигментации могут быть на слизистых оболочках полости рта.
Дифференциальная диагностика:
Для того, что определить нозологическую форму ХНН, необходимо оценить:
1.Возраст манифестации надпочечниковой недостаточности;
2.Наличие глюкокортикоидного и минералокортикоидного компонентов;
3.Семейный анамнез;
4.Наличие других клинических компонентов.
При отсутствии дополнительных клинических компонентов, которые позволяют предположить этиологию ХНН, необходимо:
1.Всем мальчикам с дебютом ХНН в возрасте после трех лет провести исследование ОДЦЖК (очень длинноцепочечных жирных кислот) для исключения Х-сцепленной адренолейкодистрофии;
2.Пациентам обоего пола с дебютом заболевания в возрасте после трех лет провести исследование антител к 21-гидроксилазе;
3.Провести генетические исследования для выявления мутаций в известных генах, ответственных за развитие надпочечниковой недостаточности.
Неотложная помощь:
—увеличивать дозу кортефа (ГКС для перорального применения) в 2—3 раза в стрессовой ситуации, при инфекционных заболеваниях с температурой выше 38 °С;
—иметь в домашней и походной аптечке набор экстреной помощи гидрокортизон для внутримышечно (или внутривенно) введения. Уметь пациенту или сопровождающему лицу в случае необходимости (резкое ухудшение состояния, рвота, потеря сознания, судороги) самостоятельно сделать внутримышечноинъекцию до приезда медицинской помощи.
Всем пациентам с НН рекомендуется ношение браслета с указанием имени, необходимости постоянной терапии глюко- и минералокортикоидов и рекомендаций по оказанию экстренной медицинской помощи, телефона доверенного лица.
Лечение:
Цели лечения:
1.Подобрать режим и дозы препаратов глюкокортикоидов так, чтобы они максимально соответствовали физиологическому и циркадному ритму кортизола;
2.Избежать развития адреналового криза;
3.Избежать хронической передозировки и ее отдаленных нежелательных эффектов (остеопороз, повышение кардиоваскулярных рисков, метаболический синдром);

4. Улучшить качество жизни пациента, обеспечив его психосоциальную адаптацию.
Прогноз:
При своевременной диагностике и достижении целей лечения – благоприятный.
43. Феохромоцитома. Этиология, патогенез, клинические синдромы, диагностика. Дифференциальная диагностика гипертензионного синдрома в подростковом возрасте, лечение.
Феохромоцитома (ФХЦ) – это опухоль мозгового слоя надпочечника, состоящая из хромаффинных клеток, продуцирующая катехоламины (адреналин, норадреналин и дофамин).
!Что должен знать каждый врач:
-Если вовремя НЕ выставлен диагноз и НЕ назначено адекватное лечение – это фатальное заболевание;
-Распространены бессимптомные формы;
-Диагностика: определение норметанефрина, метанефрина в плазме, суточной моче;
-Если диагностирована феохромоцитома, то назначение бета-блокаторов возможно только после достижение альфа-блокирующего эффекта;
-Необходима предоперационная подготовка минимум за 2 недели до операции (профилактика возникновения симпато-адреналового криза на операционном столе).
Этиология:
Большинство ФХЦ являются результатом спорадической мутации, однако в более, чем в 30% случаев опухоль возникает в результате герминальной мутации. По меньшей мере, у 40% детей с ФХЦ выявляется генетическая причина болезни.
Патогенез:
В клетках феохромоцитомы происходит синтез и накопление катехоламинов, как и в нормальных клетках мозгового вещества надпочечников. Выброс катехоламинов может провоцироваться изменениями кровотока, некрозом в ткани опухоли и другими причинами.
Разнообразие адренергического рецепторного аппарата, большое количество органов, в которых он представлен, возможность смешанной опухолевой секреции — это факторы, объясняющие, почему клинические проявления феохромоцитомы, в основе которых лежат столь различные патофизиологические механизмы, чрезвычайно разнообразны.
Изменение чувствительности адренорецепторов, нарушение механизмов инактивации катехоламинов и энергетическое истощение сосудистых миоцитов на фоне повышенного содержания катехоламинов в сосудистом русле может приводить к развитию катехоламинового шока, для которого характерно резко повышенное АД в центральных сосудах (вазоконстрикторный статус) и значительное снижение АД на периферии.
Клинические синдромы:
