
Водка3
.docxСАНКТ-ПЕТЕРБУРГСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
ПЕТРА ВЕЛИКОГО
Институт Энергетики
Высшая школа атомной и тепловой энергетики
Лабораторная работа №3
«Определение окисляемости воды»
Студент гр. 3231401/20101 А. С. Школьников
Студент гр. 3231401/20101 Д.М. Ферима
Студент гр. 3231401/20101 К.Э. Закиров
Преподаватель В.В. Сероштанов
СодержаниеY
Введение 3
Обработка результатов 4
Вывод 5
Введение 3
Обработка результатов 4
Вывод 5
Введение
Окисляемость воды характеризует наличие в ней органических веществ и легко окисляющихся неорганических соединений (Fe2+, сульфитов, нитритов, H2S и др.). Окисляемость – один из показателей степени загрязнения воды органическими примесями. Окисляемость органических веществ, растворенных в воде, характеризуется количеством кислорода, расходуемого на их окисление в определенных условиях. Окисляемость воды выражают массой кислорода, израсходованного на окисление органических веществ, содержащихся в 1 л. воды.
В качестве окислителя в лабораторной работе применяется перманганат калия (перманганатная окисляемость). Если концентрация хлоридов в исследуемой воде не превышает 100 мг/л, то органические вещества окисляют перманганатом калия в кислой среде. При более высоком содержании хлоридов используется реакция окисления перманганатом калия в щелочной среде. Органические вещества, содержащиеся в исследуемой воле, при кипячении в присутствии серной кислоты окисляются перманганатом калия. К пробе воды добавляют заведомо избыточное количество раствора KMnO4 определенной концентрации (нормальность раствора 0,01 н.). В этих условиях окисляются не все органические вещества, поэтому окисляемость характеризует содержание только легкоокисляющихся примесей. Для получения более точных результатов используют обратное титрование: к прокипяченной пробе прибавляют избыток щавелевой кислоты; часть ее окисляется оставшимся перманганатом калия, а остальное количество H2C2O4 оттитровывают перманганатом калия.
Обработка результатов
Перманганатная окисляемость рассчитывается как:

где
 – объем раствора KMnO4,
прилитого к пробе воды до кипячения, мл;
– объем раствора KMnO4,
прилитого к пробе воды до кипячения, мл;
 – объем раствора KMnO4,
необходимого для титрирования избытка
щавелевой кислоты, мл;
– объем раствора KMnO4,
необходимого для титрирования избытка
щавелевой кислоты, мл;
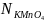 – нормальность раствора KMnO4,
мг-экв/л;
– нормальность раствора KMnO4,
мг-экв/л;
 – объем 0,01 н. раствора щавелевой кислоты,
необходимой для связывания избытка
KMnO4, мл;
– объем 0,01 н. раствора щавелевой кислоты,
необходимой для связывания избытка
KMnO4, мл;
 – нормальность раствора щавелевой
кислоты, мг-экв/л;
– нормальность раствора щавелевой
кислоты, мг-экв/л;
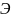 – эквивалент кислорода;
– эквивалент кислорода;
 – объем пробы исследуемой воды, мл.
– объем пробы исследуемой воды, мл.

Вывод
В
данной лабораторной работе мы сначала
подготовили колбу, чтобы избавиться от
примесей, которые могли повлиять на
результаты лабораторной. Далее мы
добавляли перманганат калия, до тех
пор, пока жидкость в колбе не поменяла
цвет. По полученным данным рассчитали
значение перманганатной окисляемости,
которое получилось равным 2,16
 .
По данным СанПин 1.2.3685.3-21 перманганатная
окисляемость питьевой воды должна быть
менее 5
.
По данным ГОСТ 26841-86 для водного
теплоносителя реактора РБМК-1000
окисляемость должна быть не больше
0,05÷0,1
для воды контура многократной
принудительной циркуляции и не больше
0,015÷0,02
для питательной воды. Для ВВЭР нормы
качества воды устанавливаются РД ЭО
1.1.2.11.0805-2010. Для охлаждения обмоток
статора турбогенератора перманганатная
окисляемость воды при бескислородном
водно химическом режиме должна быть
меньше 0,05
.
По этим нормам можно сделать вывод, что
воду с данной окисляемостью, которую
мы получили в лаборатории можно
использовать в качестве питьевой, но
ее нельзя использовать в качестве
теплоносителя на АЭС с реактором РБМК
и охлаждающей воды на реакторе ВВЭР.
.
По данным СанПин 1.2.3685.3-21 перманганатная
окисляемость питьевой воды должна быть
менее 5
.
По данным ГОСТ 26841-86 для водного
теплоносителя реактора РБМК-1000
окисляемость должна быть не больше
0,05÷0,1
для воды контура многократной
принудительной циркуляции и не больше
0,015÷0,02
для питательной воды. Для ВВЭР нормы
качества воды устанавливаются РД ЭО
1.1.2.11.0805-2010. Для охлаждения обмоток
статора турбогенератора перманганатная
окисляемость воды при бескислородном
водно химическом режиме должна быть
меньше 0,05
.
По этим нормам можно сделать вывод, что
воду с данной окисляемостью, которую
мы получили в лаборатории можно
использовать в качестве питьевой, но
ее нельзя использовать в качестве
теплоносителя на АЭС с реактором РБМК
и охлаждающей воды на реакторе ВВЭР.
Санкт-Петербург
2024
