
- •Ответы к экзамену структурная бх
- •1)Основные разделы и направления в биохимии.
- •2. Теоретическая и практическая значимость биохимии, связь с другими естественными науками. Краткая история развития биохимии.
- •3. Аминокислоты. Классификация аминокислот. Химическая структура и физико-химические свойства аминокислот.
- •4. Белки, виды их классификации и биологическая роль.
- •5. Первичная структура белка. Характеристика пептидной связи. Принципы организации и биологическая роль пептидов.
- •6. Вторичная структура белка. Альфа-спираль и бета складчатый слой.
- •7. Третичная структура белка и силы ее стабилизирующие. Денатурация белков.
- •8. Четвертичная структура белка на примере молекулы гемоглобина. Кооперативный эффект связывания кислорода гемоглобином.
- •9. Методы изучения структуры белков.
- •10. Методы очистки и идентификации белков.
- •11. Понятие о ферментах. Принципы структурной и функциональной организации энзимов.
- •12. Классификация и номенклатура ферментов.
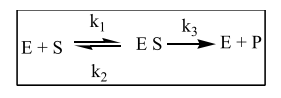
- •13. Механизм действия ферментов. Взаимодействие субстрата с ферментом.
- •14. Кинетика ферментативных реакций.
- •15. Применение ферментов. Использование ферментов в медицине, промышленности и сельском хозяйстве.
- •17. Строение и упаковка днк.
- •18. Компактизация днк. Уровни укладки (компактизации) днк.
- •19. Особенности строения рнк. Виды рнк и их характеристика.
- •20. Методы исследования нуклеиновых кислот.
- •21. Классификация и номенклатура углеводов. Биологическая роль и распространение в природе.
- •22. Особенности строения, изомерии, конформации и биохимических свойств моносахаридов.
- •23. Дисахариды, строение, восстановительные свойства, гидролиз дисахаридов
- •24. Полисахариды. Гомополисахариды: крахмал, гликоген, декстраны, целлюлоза
- •25. Строение, физико-химические свойства и функциональная роль липидов.
- •26. Характеристика жирных кислот.
- •27. Принципы химического строения и функции эйкозаноидов.
- •28. Ацилглицерины. Воски. Биологическая роль и практическое использование липидов.
- •29. Фосфолипиды: глицерофосфолипиды и сфингомиелины. Гликолипиды: цереброзиды и ганглиозиды.
- •30. Стероиды: структура, свойства важнейших представителей (холестерол желчные кислоты, стероидные гормоны, витамины группы д).
- •31. Классификация и номенклатура витаминов.
- •32. Структура, свойства, роль в обмене веществ и использование отдельных представителей водорастворимых витаминов.
- •34. Гормоны. Классификация, распространение и биологическая роль.
13. Механизм действия ферментов. Взаимодействие субстрата с ферментом.


14. Кинетика ферментативных реакций.
Ферментативная
кинетика изучает влияние различных
факторов (концентрация S и E, рН,
температура, давление, ингибиторы и
активаторы) на скорость ферментативных
реакций. Главной целью изучения кинетики
ферментативных реакций является
получение информации, позволяющей
глубже понять механизм действия
ферментов.
Скорость
ферментативных реакций зависит от 6
факторов: концентрации фермента,
субстрата, температуры, рН, наличия
активаторов и ингибиторов.
Зависимость
скорости реакции от концентрации
фермента.
В условиях избытка субстрата скорость
реакции прямо пропорциональна
концентрации фермента.
!Увеличение Км означает уменьшение сродства Е и S.
|
S=Km V=1/2Vmax S>Km Vp=max S<Km V прямопропорциональна S |
График Линевайвера-Берка — это линейная форма модели Михаэлиса-Ментен, которая используется для определения константы Михаэлиса (Km) и максимальной скорости (Vmax). График строят в координатах 1/скорость vs 1/концентрация субстрата. Пересечение с осью ординат дает 1/Vmax, а пересечение с осью абсцисс дает -1/Km.
Зависимость скорости реакции от рН среды. Графическое изображение за имеет колоколообразную форму. Значение рН, при котором фермент проявляет максимальную активность, называется оптимумом рН. Для большинства ферментов оптимум рН равен 6-8. Исключение составляет пепсин, оптимум которого равен 1,5-2,0. При изменении рН в ту или другую сторону от оптимума скорость реакции уменьшается, вследствие ионизации функциональных групп фермента и субстрата, что нарушает образование фермент-субстратного комплекса.
Зависимость скорости реакции от температуры. Скорость химической реакции повышается в 2 раза при повышении температуры на 10С. Однако вследствие белковой природы фермента при дальнейшем повышении температуры наступает денатурация фермента. Температура, при которой скорость реакции максимальна, называется температурным оптимумом. Для большинства ферментов оптимум температуры составляет 37-40С.
15. Применение ферментов. Использование ферментов в медицине, промышленности и сельском хозяйстве.
Их промышленное применение затруднено из-за неустойчивости при хранении и температурных воздействиях.
Изоферменты – группа или семейство ферментов с четвертичной структурой, которые катализируют одну и ту же реакцию, но отличаются по строению (т.е. первичной структуре) субъединиц и физико-химическим свойствам. Исследование множественных молекулярных форм ферментов и изоферментов используется в медицине и ветеринарии для поиска поврежденных тканей.
Секреторные ферменты (псевдохолинэстераза) поступают из клеток гемолимфу или в плазму крови и выполняют в этих биологических жидкостях специфические функции.
Эктоферменты выделяются клетками в окружающую среду и выполняют в ней специфические функции (внеклеточное переваривание продуктов питания или гидролиз компонентов межклеточного вещества для активного перемещения клетки)
Экскреторные ферменты образуются органами пищеварительной системы (поджелудочной железой, слизистой оболочкой кишечника, печенью, эндотелием желчных путей) для функционирования вне органа. К ним относится α-амилаза, щелочная фосфатаза и др.
Для выявления нарушений структурно-функционального состояния клеток и тканей используют оценку эндогенных ингибиторов ферментов. В тканях и крови млекопитающих имеются ингибиторы протеолитических ферментов пептидной природы
Применение ферментов в медицине:
Медицина: Диагностика, Лечение, Генная терапия, Антибактериальные и противовирусные препараты.
Промышленности: Пищевая промышленность, Текстильная промышленность, Химическая промышленность, Производство стиральных порошков
В сельском хозяйстве: Производство кормов, Защита растений, Улучшение урожайности
16. Понятие о нуклеиновых кислотах.
Нуклеиновые кислоты — это сложные органические макромолекулы, которые играют ключевую роль в хранении и передаче генетической информации во всех живых организмах. Они являются основой жизни и определяют все наши свойства и характеристики.
Нуклеиновые кислоты состоят из мономерных единиц, называемых нуклеотидами. Каждый нуклеотид состоит из трех компонентов: азотистое основание, петозный сахар, фосфатная группа.
Существует два основных типа нуклеиновых кислот: днк, рнк,
Функции нуклеиновых кислот: Хранение генетической информации, Передача генетической информации, Синтез белка.

