
- •Органическая химия
- •Состав органических веществ, их многообразие. Место органической химии в системе естественных наук. Источники органических соединений.
- •Формирование и основные положения теории строения органических соединений (а.М. Бутлеров, а. Кекуле, а. Купер).
- •Основные признаки классификации органических веществ. Основные классы органических веществ.
- •Номенклатура органических соединений. Основные принципы построения названий органических соединений.
- •Типы связей в молекулах органических соединений. Σ- и π-связи. Гибридизация, понятие о молекулярных орбиталях.
- •Представление о механизмах реакций. Представление о промежуточных частицах: радикалы, карбокатионы, карбанионы. Классификация реагентов: радикалы, нуклеофилы, электрофилы.
- •Энергетический профиль реакции; энергетический барьер реакции, энергия активации, энергия переходного состояния, тепловой эффект реакции. Кинетический и термодинамический контроль.
- •Кислоты и основания (Бренстед, Льюис). Сопряженные кислоты и основания. Кислотно-основые равновесия. Константа кислотной ионизации и ее показатель (рКа).
- •Взаимное влияние атомов в молекулах, ионах, радикалах. Электронные и пространственные эффекты в органических реакциях (индуктивный эффект, эффект поля, мезомерный эффект, гиперконьюгация).
- •Гомологический ряд, номенклатура, электронное строение, sp3-гибридизация и физические свойства алканов.
- •Химические свойства алканов. Общие представления о механизме цепных радикальных реакций замещения в алканах (на примере реакции галогенирования).
- •Номенклатура, структурная и пространственная изомерия, электронное строение, sp2-гибридизация и физические свойства алкенов.
- •Химические свойства алкенов: каталитическое гидрирование, реакции электрофильного присоединения к двойной связи алкенов, их механизмы.
- •Химические свойства алкенов: реакции присоединения галогенов, галогеноводородов, воды. Правило Марковникова и его объяснение.
- •Представление о стереохимии присоединения галогенов у алкенов. Перегруппировки карбокатионов. Реакции радикального присоединения (по Харашу).
- •Окислительное расщепление алкенов (восстановительный и окислительный озонолиз). Гидроборирование алкенов и использование в синтезе спиртов.
- •Полимеризация алкенов как важнейший метод получения высокомолекулярных соединений. Полиэтилен, полипропилен. Понятие о стереорегулярных полимерах.
- •Аллильное хлорирование алкенов, механизм. Аллильный радикал. Окисление алкенов кислородом воздуха (пероксидное окисление).
- •Номенклатура, классификация, изомерия диеновых углеводородов.
- •Классификация диенов:
- •Изопреновое звено в природных соединениях. Понятие об изопреноидах. Каучук. Синтетические каучуки.
- •Номенклатура, электронное строение, sp-гибридизация и физические свойства алкинов.
- •Химические свойства алкинов: каталитическое гидрирование и восстановление натрием в жидком аммиаке, использование в синтезе (z)- и (e)-алкенов.
- •Химические свойства алкинов: реакции электрофильного присоединения к тройной связи – галогенирование, гидрогалогенирование, гидратация (реакция Кучерова).
- •Кислотность ацетилена и терминальных алкинов. Димеризация, тримеризация ацетилена. Полиацетилен.
- •Классификация, номенклатура, структурная изомерия и пространственное строение циклоалканов.
- •Классификация и номенклатура аренов. Природа связей в молекуле бензола. Конденсированные ароматические углеводороды: нафталин, антрацен, фенантрен, бензпирен.
- •Ароматичность, критерии ароматичности. Правило Хюккеля.
- •Влияние заместителей в бензольном кольце на изомерный состав продуктов и скорость реакции. Активирующие и дезактивирующие заместители. Орто-, пара- и мета-ориентанты.
- •Классификация, номенклатура, изомерия галогенуглеводородов.
- •Литий- и магнийорганические соединения и их использование в органическом синтезе.
- •Биологическое действие галогенпроизводных, их применение в народном хозяйстве. Хлороформ, иодоформ, перфторуглеводороды, перфторполиэтилен (тефлон). Инсектициды.
- •Одноатомные спирты. Номенклатура, изомерия. Электронное строение. Физические свойства спиртов, роль водородной связи.
- •Химические свойства спиртов: кислотно-основные свойства. Алкоголяты металлов, их основные и нуклеофильные свойства.
- •Реакции нуклеофильного замещения с участием спиртов. Биологически важные реакции нуклеофильного замещения с участием эфиров фосфорных кислот.
- •Внутри- и межмолекулярная дегидратация спиртов (образование алкенов и простых эфиров). Окисление первичных и вторичных спиртов.
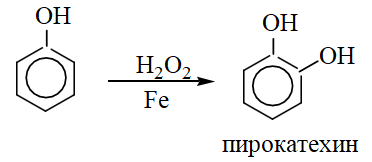
- •Фенолы. Номенклатура и изомерия. Простейшие представители: фенол, крезолы, пирокатехин, резорцин, гидрохинон, флороглюцин, пирогаллол. Электронное строение фенола. Кислотность фенолов.
- •Образование простых и сложных эфиров фенолов. Реакции электрофильного замещения в ряду фенолов (галогенирование, сульфирование, нитрование, алкилирование).
- •Карбоксилирование фенолятов щелочных металлов (реакция Кольбе). Окисление фенолов.
- •Хиноны и их биологическая роль. Фенольные соединения в природе. Витамин е. Флавоноиды.
- •Простые эфиры. Номенклатура, классификация. Расщепление кислотами. Образование гидропероксидов, их обнаружение и разложение. Циклические простые эфиры. Тетрагидрофуран. 1,4-Диоксан.
Карбоксилирование фенолятов щелочных металлов (реакция Кольбе). Окисление фенолов.
Карбоксилирование (синтез фенолокарбоновых кислот). При нагревании натрия фенолята в токе углерода (IV) оксида образуется натрия салицилат, который под действием минеральных кислот превращается в салициловую кислоту:
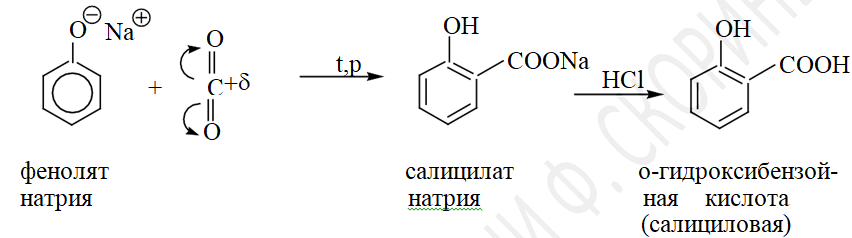
Окисление. Фенол и многие замещенные фенолы при хранении постепенно окисляются кислородом воздуха, образуя сложную смесь соединений. Если пара-положения бензольного кольца фенолов свободны, то одним из основных превращений феноксильных радикалов является димеризация по пара-положению с образованием 4,4'- дигидроксидифенила.
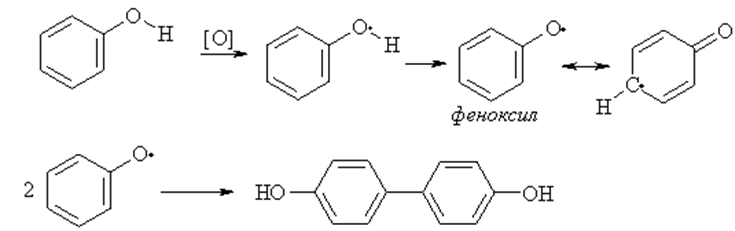
Феноксильные радикалы, имеющие в орто- и пара-положениях объемные заместители, настолько стабильны, что могут существовать в растворе длительное время и даже быть выделенными в кристаллическом виде.
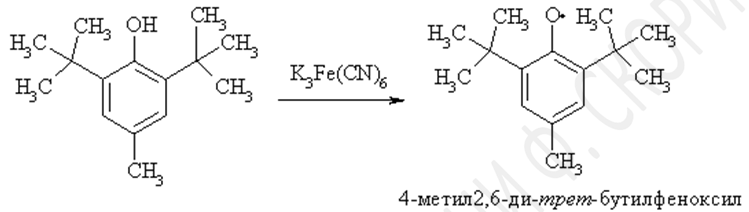
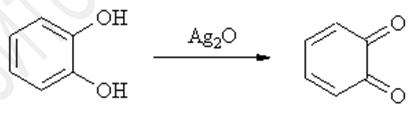
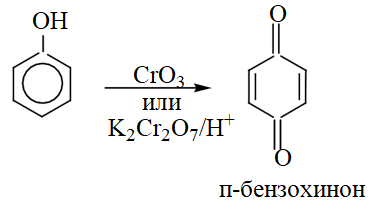
Фенол окисляется бихроматом калия или солью Фреми (нитрозодисульфонатом калия) до пара-бензохинона. При окислении двухатомных фенолов пирокатехина и гидрохинона, образуются орто- и пара-бензохиноны, соответственно.
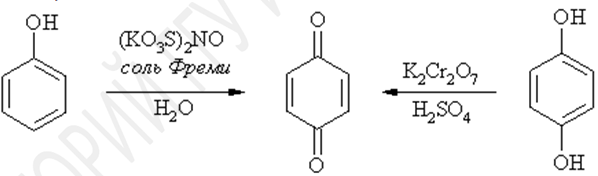
Хиноны и их биологическая роль. Фенольные соединения в природе. Витамин е. Флавоноиды.
Хиноны. Представляют собой циклические α,β-ненасыщенные дикетоны. Простейшими представителями этого класса соединений являются о-хинон и п-хинон:

Хиноны представляют собой окрашенные кристаллические вещества: о-хинон — ярко-красный, п-хинон — желтый.
Хиноны широко распространены в природе в качестве пигментов и биологически активных веществ, играющих важную роль в окислительно-восстановительных процессах, протекающих в живых организмах. Так, хиноидная структура входит в состав витаминов группы К, отвечающих за свертываемость крови, и убихинонов (коферментов Q), основная функция которых заключается в переносе электронов и протонов от различных субстратов к цитохромам при дыхании и окислительном фосфорилировании.
Фенольные соединения — вещества ароматической природы, содержащие одну или несколько гидроксильных групп. Фенольные соединения находятся в растениях, плодах и овощах преимущественно в виде гликозидов и реже в свободном виде Фенольные соединения являются основными антиоксидантами растительного происхождения, а их биологическая активность зависит от строения, количества, местонахождения гидроксильных групп в бензольном ядре и от степени полимеризации. Флавоноиды — основная группа природных полифенолов. Флавоноиды играют важную роль в растительном метаболизме и очень широко распространены в высших растениях. Многие флавоноиды — пигменты, придающие разнообразную окраску растительным тканям. Так, антоцианы определяют красную, синюю, фиолетовую окраску цветов, а флавоны, флавонолы, ауроны, халконы — жёлтую и оранжевую. Они принимают участие в фотосинтезе, образовании лигнина и суберина, в качестве защитных агентов в патогенезе растений, вовлечены в регуляцию процессов прорастания семян, а также пролиферации и отмирания (путём апоптоза) клеток удлиняющихся растущих частей растений.
Витами́н E — группа природных соединений производных токола. Важнейшими соединениями являются токоферолы и токотриенолы. Жирорастворим. Витамин Е является универсальным протектором клеточных мембран от окислительного повреждения. Он занимает такое положение в мембране, которое препятствует контакту кислорода с ненасыщенными липидами мембран. Токоферол является не только антиоксидантом, но и антигипоксантом (группа лекарственных средств, улучшающих утилизацию циркулирующего в организме кислорода и повышающих устойчивость к гипоксии (кислородной недостаточности), что объясняется его способностью стабилизировать митохондриальную мембрану и экономить потребление кислорода клетками. Витамин контролирует биосинтез убихинона — компонента дыхательной цепи и главного антиоксиданта митохондрий
