- •111Equation Chapter 1 Section 1
- •Рецензент
- •Теоретическая часть
- •1.1. Квантовая теория атома.
- •1.2. Структура атома и спектральные линии.
- •1.3. Дублеты щелочных металлов и спин электрона
- •1.4.Эффект Зеемана
- •4212Equation Chapter (Next) Section 1ii. Практическая часть4312Equation Chapter 2 Section 1
- •2.1. Описание экспериментальной установки
- •2.2. Порядок выполнения измерений
- •2.3. Определение величины расщепления 3p терма желтого дублета резонансной линии натрия
- •2.4. Определение постоянной Планка спектроскопическим методом
- •Контрольные вопросы
- •Список литературы
- •Оглавление
- •I.Теоретическая часть 3
- •4212Equation Chapter (Next) Section 1ii. Практическая часть4312Equation Chapter 2 Section 1 43
1.3. Дублеты щелочных металлов и спин электрона
Линии
главных серий щелочных металлов являются
дублетными. Хорошо известен пример
D-линии
натрия, дублетную природу которой
обнаруживают даже простейшие
спектроскопические приборы. Расщепление
линии довольно значительно - оно
составляет 6Å; две компоненты ее
обозначаются как D1
и
D2,
и
длины волн их равны
 и
и соответственно.Анализ
термов в спектрах щелочных металлов,
к которым принадлежит
и спектр натрия, совершенно определенно
показывает, что в этих спектрах
соответственно.Анализ
термов в спектрах щелочных металлов,
к которым принадлежит
и спектр натрия, совершенно определенно
показывает, что в этих спектрах
 термы
термы
 синглетны,
синглетны,
 термы
термы
 дублетны.
дублетны.
Этот
экспериментальный факт невозможно
объяснить ни с точки зрения теории
Бора, ни с точки зрения изложенной до
сих пор волновой механики. Рассмотрение
движениея электрона в атоме, исходя из
его трех степеней свободы приводит к
заключению, что движение полностью
определяется и описывается тремя
квантовыми числами
 .
Любое
дальнейшее расщепление термов, помимо
обусловленного этими квантовыми
числами, необъяснимо до тех пор, пока
мы придерживаемся
представления,
что движение электрона не более чем
троекратно периодично.
.
Любое
дальнейшее расщепление термов, помимо
обусловленного этими квантовыми
числами, необъяснимо до тех пор, пока
мы придерживаемся
представления,
что движение электрона не более чем
троекратно периодично.
Учитывая
полученные к 1925 г. экспериментальные
данные, Уленбек и Гаудсмит выдвинули
гипотезу о том, что если бы можно было
рассматривать электрон как тело конечной
протяженности, то, подобно всякому
протяженному телу, он обладал бы, помимо
трех поступательных, тремя вращательными
степенями свободы. Соответственно он
имел бы механический момент и, кроме
того, как всякое вращающееся заряженное
тело, магнитный момент. Авторы гипотезы
предположили, что экспериментальные
факты можно понять, приписав электрону
механический момент и магнитный момент
столь же формальным образом, как
приписываются ему масса
 и заряд
и заряд .
Что
же касается величин магнитного и
механического моментов, то в первую
очередь необходимо измерить их в
экспериментах, а впоследствии попытаться
вывести эти значения теоретически.
.
Что
же касается величин магнитного и
механического моментов, то в первую
очередь необходимо измерить их в
экспериментах, а впоследствии попытаться
вывести эти значения теоретически.
Свойство электрона, вследствие которого он обладает механическим и магнитным моментами, называется его спином. Величина механического момента следует непосредственно из фактов, известных о спектрах щелочных металлов.
Подобно
всякому моменту, момент электрона
должен, конечно, быть квантованным,
причем то же самое справедливо для его
компоненты
в выделенном направлении (внешнее
магнитное поле). Поэтому,
если величина механического спинового
момента равна
 (в единицах
(в единицах ),
то
по правилам пространственного квантования
для него должны быть возможны
),
то
по правилам пространственного квантования
для него должны быть возможны
 ориентации (или наклонов) относительно
выделенного направления, в которых
значения выбранной компоненты,
обозначаемые через
ориентации (или наклонов) относительно
выделенного направления, в которых
значения выбранной компоненты,
обозначаемые через ,
отличаются друг от друга на единицу.
,
отличаются друг от друга на единицу.
Аналогичные
соотношения имеют место в атоме Бора,
где плоскость орбиты, отвечающей моменту
 ,
имеет в точности
,
имеет в точности возможных ориентации относительно
выделенного направления. Эти ориентации
характеризуются компонентами
возможных ориентации относительно
выделенного направления. Эти ориентации
характеризуются компонентами момента в выбранном направлении. Такая
экстраполяция представлений об
орбитальном моменте на спиновый момент
не только оправдывается тем, что
выведенные из нее следствия полностью
согласуются с опытом, но и может быть
обоснована теоретически.
момента в выбранном направлении. Такая
экстраполяция представлений об
орбитальном моменте на спиновый момент
не только оправдывается тем, что
выведенные из нее следствия полностью
согласуются с опытом, но и может быть
обоснована теоретически.
|
|
|
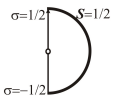
Рис.6. Ориентация спина по отношению к выделенному направлению |
Таким
образом, спин
 электрона должен иметь
электрона должен иметь возможных ориентации относительно
выбранного направления. Но опыт
показывает, что, за исключением
возможных ориентации относительно
выбранного направления. Но опыт
показывает, что, за исключением термов,
все термы натрия дублетны. Этот факт
позволяет сделать вывод о том, что спин
имеет только две возможные ориентации
(Рис.6). Но это только в том случае если
верно предположение, что спин определяет
расщепление термов. Следовательно,
должно быть
термов,
все термы натрия дублетны. Этот факт
позволяет сделать вывод о том, что спин
имеет только две возможные ориентации
(Рис.6). Но это только в том случае если
верно предположение, что спин определяет
расщепление термов. Следовательно,
должно быть ,
или
,
или (в
единицах
(в
единицах
 ).
Две возможные ориентации характеризуются
компонентами
).
Две возможные ориентации характеризуются
компонентами

На первый взгляд, появление полуцелых «квантовых чисел» противоречит представлениям о квантовании момента. Однако необходимо отметить, что представление о вращающемся протяженном электроне имеет лишь эвристическое значение, и строго говоряневерна. Если например рассмотреть точку на поверхности электрона, то она должна двигаться со сверхсветовой скоростью, чтобы вычисленные по классической теории значения механического и магнитного момента согласовались с экспериментально найденными значениями. Использование полуцелых компонент для спина приводит к результатам, находящимся в полном согласии с экспериментальными данными. С другой стороны, волновая механика обладающего спином электрона в форме, которую ей придал Дирак, приводит к полуцелым значениям спина автоматически вследствие только условий линейности и релятивистской инвариантности без каких-либо дополнительных предположений.
Вращающийся
вокруг ядра электрон обладает орбитальным
моментом
 и спиновым моментом
и спиновым моментом .
Возникает вопрос о правиле сложения
этих двух моментов. Теория Бора ответила
бы, что это должно происходить по
правилам сложения векторов. То же самое
правило сложения дает волновая механика,
хотя доказательство этого (Вигнер,Нейман,
1927 г.) требует современных математических
методов (теории
групп). Таким образом,
.
Возникает вопрос о правиле сложения
этих двух моментов. Теория Бора ответила
бы, что это должно происходить по
правилам сложения векторов. То же самое
правило сложения дает волновая механика,
хотя доказательство этого (Вигнер,Нейман,
1927 г.) требует современных математических
методов (теории
групп). Таким образом,
 и
и складываются векторно, образуя
результирующий (или полный) момент
складываются векторно, образуя
результирующий (или полный) момент (в единицах
(в единицах ),
так что
),
так что .
Следуя
Зоммерфельду,
.
Следуя
Зоммерфельду,
 иногда называют«внутренним
квантовым
числом» которое
представляет полный механический
момент атома.
Допустимые значения
иногда называют«внутренним
квантовым
числом» которое
представляет полный механический
момент атома.
Допустимые значения
 должны отличаться на целые числа. Так
как
должны отличаться на целые числа. Так
как ,
то
единственными возможностями будут
,
то
единственными возможностями будут
 следовательно, в этом случае значение
следовательно, в этом случае значение полуцелое.
Каждомузначению
полуцелое.
Каждомузначению
 соответствуют два возможных значения
полного механического
момента, так что соответствующие термы
оказываются дублетами. Одни лишь
соответствуют два возможных значения
полного механического
момента, так что соответствующие термы
оказываются дублетами. Одни лишь
 термы
термы составляют исключение. Они всегда
синглетны, поскольку в этом случае
допустимо
только значение
составляют исключение. Они всегда
синглетны, поскольку в этом случае
допустимо
только значение
 ,
ибо полный момент
,
ибо полный момент всегдадолжен
быть положительным. Двойная возможность
ориентации спина электрона относительно
его орбиты эквивалентна расщеплению
уровней энергии вследствие магнитного
взаимодействия спина и орбиты. Величина
расщепления прямо равна энергии,
необходимой для разворота спина в
магнитном поле орбиты из одной орентации
относительно
всегдадолжен
быть положительным. Двойная возможность
ориентации спина электрона относительно
его орбиты эквивалентна расщеплению
уровней энергии вследствие магнитного
взаимодействия спина и орбиты. Величина
расщепления прямо равна энергии,
необходимой для разворота спина в
магнитном поле орбиты из одной орентации
относительно
 в другую.
в другую.
Рассмотрим
в качестве примера
 линию
натрия. Анализ термов показывает, что
верхнее состояние представляет собой
линию
натрия. Анализ термов показывает, что
верхнее состояние представляет собой терм,
а нижнее
терм,
а нижнее терм.
Первый из них - дублет, соответственно
двум возможным значениям полного
момента:
терм.
Первый из них - дублет, соответственно
двум возможным значениям полного
момента:
 и
и

 нижний,
как и полагаетсяs-терму,
является синглетом
нижний,
как и полагаетсяs-терму,
является синглетом
 .
Линия
.
Линия
 соответствуетпереходу
с
соответствуетпереходу
с
 терма
(внутреннее квантовое число
терма
(внутреннее квантовое число ,
линия
,
линия -
переходу с
-
переходу с
 терма
для которого с
терма
для которого с .
.
Правило
векторного сложения можно применять
и к случаю нескольких электронов; в
этом случае орбитальные моменты
 отдельных электронов и их спины
отдельных электронов и их спины складываются, образуя полный момент
складываются, образуя полный момент .
Здесь
.
Здесь будет целым илиполуцелым,
в зависимости от того четно или нечетно
число электронов. Аналогично и проекция
полного момента в выбранном направлении
может быть целой или полуцелой.
будет целым илиполуцелым,
в зависимости от того четно или нечетно
число электронов. Аналогично и проекция
полного момента в выбранном направлении
может быть целой или полуцелой.
В
заключение упомянем еще тот факт, что
по самому смыслу
 как полного момента система как целое
вращается с постоянной угловой скоростью
вокруг направления
как полного момента система как целое
вращается с постоянной угловой скоростью
вокруг направления .
Это приводит к правилам отбора
.
Это приводит к правилам отбора для испускаемого излучения. Однако
теория указывает в полном согласии с
опытом, что имеются еще и переходы с
для испускаемого излучения. Однако
теория указывает в полном согласии с
опытом, что имеются еще и переходы с .
Они соответствуют такому изменению
состояния, при котором полный момент
не меняется. Что такие переходы разрешены,
тогда как переходы с
.
Они соответствуют такому изменению
состояния, при котором полный момент
не меняется. Что такие переходы разрешены,
тогда как переходы с запрещены, можно объяснить, опираясь
на принцип соответствия.
запрещены, можно объяснить, опираясь
на принцип соответствия.