
5 курс / Госпитальная терапия / Осенний семестр / Дифференциальная диагностика гипергликемии (часть 1) / Сахарный диабет. Этиология, патогенез, клиника, диагностика
.pdf1. Физиология углеводного обмена: основная информация
Краткая информация
Углеводы являются одним из трех макроэлементов в рационе человека, наряду с белками и жирами. Эти молекулы содержат атомы углерода, водорода и кислорода. Углеводы играют важную роль в организме человека. Они действуют как источник энергии, помогают контролировать метаболизм глюкозы и инсулина в крови, участвуют в метаболизме холестерина и триглицеридов и помогают ферментации. Пищеварительный участвует в расщеплении сложных углеводов до глюкозы, которая используется для получения энергии. У человека обмен углеводов подвержен сложным механизмам регуляции, в которых участвуют гормоны, метаболиты и коферменты. К гормонам, которые влияют на углеводный обмен, принадлежат инсулин и глюкагон, глюкокортикоиды, адреналин, тироксин и соматотропный гормон.
Классификация
По структуре
· Моносахарид: самая основная, фундаментальная единица углевода. Это простые сахара с общей химической структурой C6H12O6.
Примеры: глюкоза, галактоза, фруктоза.
· Дисахарид: соединение сахаров, содержащих два моносахарида с элиминацией молекулы воды с общей химической структурой C12H22O11
Примеры: сахароза, лактоза.
·Олигосахарид: Полимер содержит от трех до десяти моносахаридов Примеры: мальтодекстрины, рафиноза.
·Полисахариды: полимеры, содержащие длинные цепи моносахаридов, соединенные через гликозидные связи
Примеры: амилоза, целлюлоза.
По типу
· Простые углеводы: один или два сахара (моносахариды или дисахариды), объединенные в простую химическую структуру. Они легко используются для получения энергии, вызывая быстрое повышение уровня сахара в крови и секреции инсулина из поджелудочной железы.
Примеры: фруктоза, лактоза, мальтоза, сахароза, глюкоза, галактоза, рибоза.
Продукты питания: конфеты, газированные напитки, кукурузный сироп, фруктовый сок, мед, столовый сахар.
· Сложные углеводы: три или более сахара (олигосахариды или полисахариды), связанные вместе в более сложную химическую структуру. Они дольше перевариваются и поэтому оказывают более постепенное влияние на повышение уровня сахара в крови.
Примеры: целлобиоза, рутинулоза, амилоза, целлюлоза, декстрин.
Продукты питания: яблоки, брокколи, чечевица, шпинат, нерафинированные цельные зерна, коричневый рис.
· Крахмалы: сложные углеводы содержат большое количество молекул глюкозы. Растения производят эти полисахариды.
Примеры включают картофель, нут, макароны и пшеницу.
· Клетчатка: неперевариваемые сложные углеводы, которые стимулируют здоровый бактериальный рост в толстой кишке и действуют как наполнитель, облегчая дефекацию. Основные компоненты включают целлюлозу, гемицеллюлозу и пектин.
1)Нерастворимая: поглощает воду в кишечнике, тем самым размягчая и наполняя стул. Преимущества включают регулярность дефекации и снижение риска дивертикулеза.
Примеры: отруби, семена, овощи, коричневый рис, картофельная шелуха.
2)Растворимая: помогает снизить уровень холестерина и ЛПНП в крови, уменьшает напряжение при дефекации и притупляет уровень глюкозы в крови после приема пищи.
Примерами могут служить мясистые фрукты, овес, брокколи и сушеные бобы.
2. Физиология углеводного обмена: метаболизм углеводов
Гликолиз
Гликолиз — это катаболический путь обмена веществ в цитоплазме; он, по-видимому, протекает почти во всех организмах и клетках независимо от того, живут они в аэробных или анаэробных условиях.
Сахара подвергаются метаболическим превращениям преимущественно в виде сложных эфиров фосфорной кислоты. Глюкоза, которую ткани получают из крови, в клетке также предварительно активируется путем
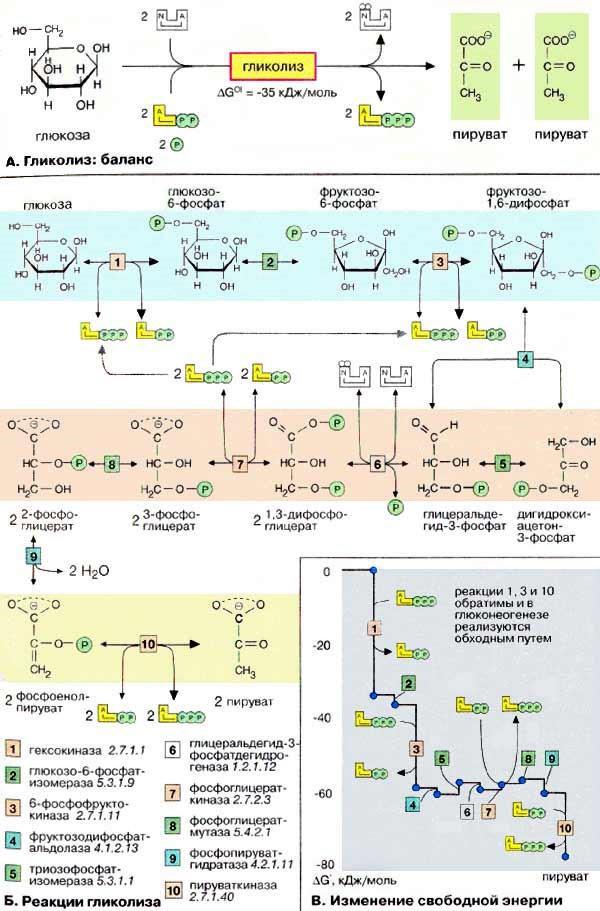
фосфорилирования. Фосфофруктокиназа [3], катализирующая эту стадию, является важным ключевым ферментом гликолиза.
Гексозомонофосфатный путь
Гексозомонофосфатный путь [ГМП (HMW), часто называемый также пентозофосфатным путем] является окислительным обменом веществ в цитоплазме, в котором, как и в гликолизе, исходным субстратом служит глюкозо-6-фосфат. ГМП поставляет два важных исходных соединения для анаболических процессов: НАДФН + Н+ (NADPH + Н+), необходимый для биосинтеза жирных кислот и изопреноидов, и рибозо-5-фосфат, предшественник в биосинтезе нуклеотидов.
Глюконеогенез
Некоторые ткани, такие, как мозг и эритроциты, зависят от постоянного снабжения глюкозой. Если получаемое с пищей количество углеводов недостаточно, необходимая концентрация глюкозы в крови может поддерживаться некоторое время за счет расщепления гликогена печенью. Если истощены также и эти запасы, в печени запускается синтез глюкозы de novo, глюконеогенез. Наряду с печенью высокой глюконеогенезной активностью обладают также клетки почечных канальцев. Исходными соединениями в глюконеогенезе являются аминокислоты мышечной ткани. При длительном голодании это приводит к массивному распаду мышечного белка. Другими важными исходными веществами для синтеза глюкозы служат лактат, образующийся в эритроцитах и мышечной ткани при недостатке О2 , а также глицерин, образующийся при расщеплении жиров. Напротив, жирные кислоты не могут трансформироваться в глюкозу в организме животных, так как в данном случае деградация жирных кислот не является анаплеротическим процессом. В организме человека за счет глюконеогенеза образуется несколько сотен граммов глюкозы в сутки.
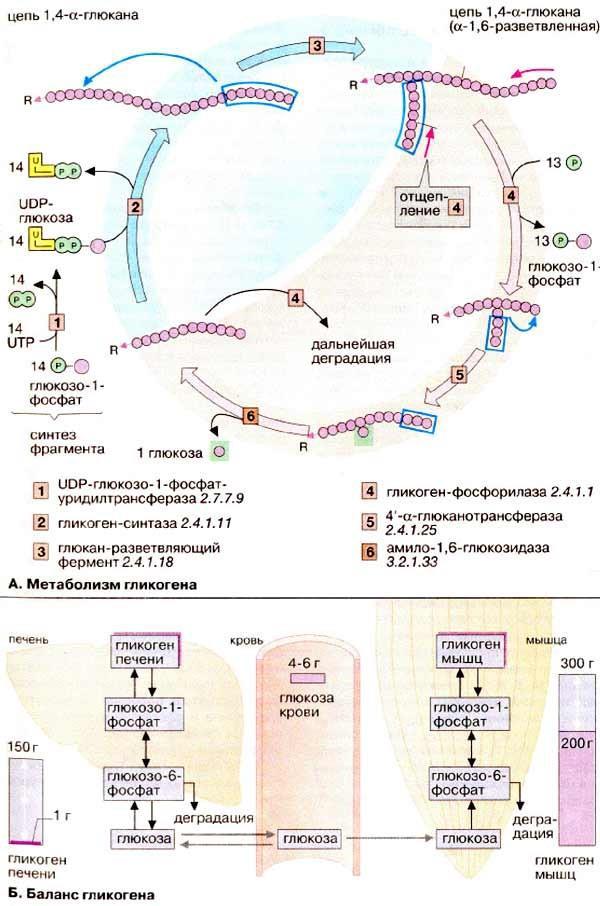
Метаболизм гликогена
Гликоген служит в животном организме резервом углеводов, из которого по мере метаболической потребности могут высвобождаться глюкозофосфат или глюкоза. Хранение в организме собственно глюкозы неприемлемо из-за ее высокой растворимости: высокие концентрации глюкозы создают в клетке высоко гипертоническую среду, что приводит к притоку воды. Напротив, нерастворимый гликоген осмотически почти неактивен.
Баланс гликогена
В организме человека может содержаться до 450 г гликогена, треть из которого накапливается в печени, а остальное — главным образом в мышцах. Содержание гликогена в других органах незначительно. Гликоген печени служит прежде всего для поддержания уровня глюкозы в крови в фазе пострезорбции. Поэтому содержание гликогена в печени варьирует в
широких пределах. При длительном голодании оно падает почти до нуля, после чего начинается снабжение организма глюкозой с помощью глюконеогенеза. Гликоген мышц служит резервом энергии и не участвует в регуляции уровня глюкозы в крови. В мышцах отсутствует глюкозо-6- фосфатаза, поэтому гликоген мышц не может быть источником глюкозы в крови. По этой причине колебания содержания гликогена в мышцах меньше, чем в печени.
3. Физиология углеводного обмена: регуляция углеводного обмена
Регуляция углеводного обмена
А. Регуляция углеводного обмена
У высших организмов обмен углеводов подвержен сложным механизмам регуляции, в которых участвуют гормоны, метаболиты и коферменты. Представленная здесь схема относится к печени, которая занимает в углеводном метаболизме центральное место. Некоторые из представленных механизмов не действуют в других тканях.
Одной из важнейших функций клеток печени является накопление избыточной глюкозы в виде гликогена и ее быстрое высвобождение по мере метаболической необходимости (буферная функция). После полной мобилизации запасов гликогена печень может поставлять глюкозу за счет синтеза de novo (глюконеогенез). Кроме того, как и все ткани, она потребляет глюкозу путем гликолиза. Функции накопления (синтеза) глюкозы в виде гликогена и его распада должны быть взаимосогласованы. Таким образом, совершенно невозможно одновременное протекание гликолиза и глюконеогенеза, как и синтеза и деградации гликогена. Согласование процессов обеспечивается тем, что синтез (анаболизм) и распад (катаболизм) катализируются двумя различными ферментами и контролируются независимо. На схеме показаны только эти ключевые ферменты.
Гормоны. К гормонам, которые влияют на углеводный обмен, принадлежат пептиды инсулин и глюкагон, глюкокортикоид кортизол и катехоламин адреналин. Инсулин индуцирует синтез de novo гликоген-синтазы [1], а также некоторых ферментов гликолиза [3, 5, 7]. Одновременно инсулин подавляет синтез ключевых ферментов глюконеогенеза (репрессия, [4, 6, 8, 9]). Глюкагон как антагонист инсулина действует в противоположном направлении: индуцирует ферменты глюконеогенеза [4, 6, 8, 9] и репрессирует пируваткиназу [7], ключевой фермент гликолиза. Другие аффекты глюкагона основаны на взаимопревращении ферментов и опосредованы вторичным мессенджером цАМФ (сАМР, см. с. 114). По этому механизму тормозится синтез гликогена [1] и активируется расщепление гликогена [2]. Подобным образом действует и адреналин. Торможение пируваткиназы [7] глюкагоном также обусловлено взаимопревращением ферментов.
Глюкокортикоиды, прежде всего кортизол, индуцируют все ключевые ферменты глюконеогенеза [4, 6, 8, 9]. Одновременно они индуцируют ферменты деградации аминокислот и обеспечивают тем самым глюконеогенез исходными соединениями.
Метаболиты. Высокие концентрации АТФ (АТР) и цитрата тормозят гликолиз путем аллостерической регуляции фосфофруктокиназы. Кроме
того, АТФ тормозит пируваткиназу. Ингибитором пируваткиназы является ацетил-КоА. Все эти метаболиты образуются при распаде глюкозы (торможение конечным продуктом). АМФ (AMP), сигнал дефицита АТФ, активирует расщепление гликогена и тормозит глюконеогенез.
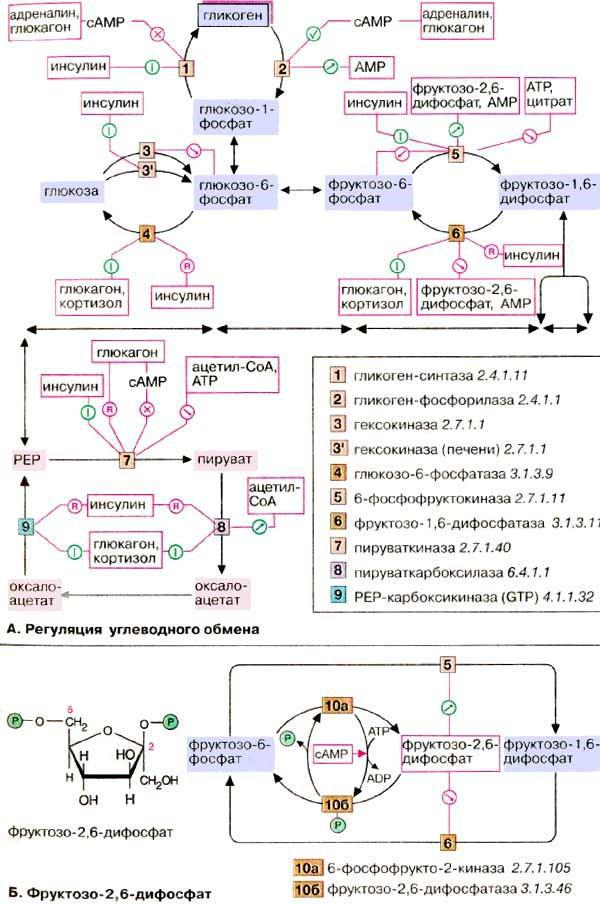
Б. Фруктозо-2,6-дифосфат
Важную роль в обмене веществ в печени играет фруктозо-2,6-дифосфат. Это сигнальное вещество образуется в незначительных количествах из фруктозо- 6-фосфата и выполняет чисто регуляторную функцию: стимулирует гликолиз путем активации фосфофруктокиназы и подавляет глюконеогенез с помощью торможения фруктозо-1,5-дифосфатазы.
Образование и распад фруктозо-2,6-дифосфата катализируются одним и тем же белком [10а и б]. В нефосфорилированной форме этот белок вызывает образование фруктозо-2,6-дифосфата [10а]. После фосфорилирования цАМФ-зависимой киназой он действует как фосфатаза [10б] и катализирует превращение фруктозо-2,6-дифосфата в фруктозо-6-фосфат. В присутствии адреналина и глюкагона в клетках печени повышается уровень цАМФ, т.е. оба гормона воздействуют как на гликолиз, так и на глюконеогенез. Суммарным результатом является быстрое повышение уровня глюкозы в крови.
4. Краткая информация
Сахарный диабет (СД) – характеризуется нарушением секреции инсулина и той или иной степенью инсулинорезистентности, обусловливающими гипергликемию. Ранние симптомы связаны с гипергликемией и включают полидипсию, полифагию, полиурию и сужение полей зрения. К поздним осложнениям относятся ангиопатии, периферическая нейропатия, нефропатия и предрасположенность к инфекционным заболеваниям. Диагноз устанавливают на основании результатов измерения уровня глюкозы в плазме. Лечение включает диету, физические нагрузки и применение средств, снижающих уровень глюкозы (инсулин и пероральные сахароснижающие препараты). Осложнения можно отсрочить или предотвратить надлежащим контролем гликемии; основной причиной смертности при СД остается поражение сердца.
Определение
Сахарный диабет (СД) – это группа метаболических (обменных) заболеваний, характеризующихся хронической гипергликемией, которая является результатом нарушения секреции инсулина, действия инсулина или обоих этих факторов. Хроническая гипергликемия при СД сопровождается повреждением, дисфункцией и недостаточностью различных органов, особенно глаз, почек, нервов, сердца и кровеносных сосудов.
5. Этиология и патогенез
Сахарный диабет 1 типа
