
- •Классификация.
- •Клиника.
- •Экссудативный перикардит
- •Диагностика.
- •Лечение.
- •Этиология
- •Клинические проявления
- •Диагностика
- •Лечение
- •3. Патогенез отёчного синдрома
- •Показатели контроля углеводного обмена (индивидуальные цели лечения)
- •Данным целевым уровням HbA1c будут соответствовать следующие целевые значения пре- и постпрандиального уровня глюкозы плазмы
- •Соответствие HbA1c среднесуточному уровню глюкозы плазмы (ссгп) за последние 3 мес.
- •Этиология. Гипогликемические состояния могут возникать при сахарном диабете вследствие:
- •Профилактика.
- •Клиническая картина
- •Лечение
- •28. Остеопороз этиология патогенез клиника диагностика лечение
мл/мин и менее. Гипокальциемия стимулирует секрецию паратгормона. Почечная осте одистрофия представляет собойкомбинацию остеомаляции, развивающеися̆ при дефиците 1,25-(ОН)2-Оз, и повышенной костной резорб ции в результате гиперпродукции паратгормона (рис. 8.7). В основе патогенеза интестинальной формы ВГП лежит мальабсорбция кальция и витамина D, которая приводит к гиперстимуляции П Щ Ж . При заболеваниях печени развитие ВГП связано с нарушением превращения холекальциферола в 25-OH-D3. Наиболее часто это про исходит при первичном билиарном циррозе. Патогенез третичного гиперпаратиреоза связан с постепенным формированием автономии гиперфункционирующих Г1ЩЖ.
Диагностика
1. Нормокальциемия в сочетании с повышенным уровнем ПТГ. Кроме того, характерна гиперфосфатемия, высокийуровень щелочнойфосфатазы,
низкийуровень l,25-(OH)2-D3. Определение уровня П Т Г рекомендуется |
|
|
|||||||
при нефропатии любого |
генеза |
со снижением |
|
скорости |
|||||
клубочковойфильтрации менее 60 %. |
|
|
|
|
|
|
|
||
2. Костные изменения |
сходны с |
таковыми |
при |
П |
Г |
П |
|||
(остеопороз, субпериостальная и субхондральная резорбция костей |
|||||||||
кисти и пр.). |
|
|
|
|
|
|
|
|
|
3. Диагностика основного заболевания (ХПН, мальабсорбция). |
|
|
|
|
|||||
Клиническая картина |
|
|
|
|
|
|
|
|
|
Доминируют симптомы |
основного |
заболевания, |
чаще |
всего Х П Н |
|||||
. Специфическимисимптомами |
являютсяболи |
в костях, |
слабость |
в |
|||||
проксимальных отделах мышц, артралгии. Могут возникать спон танные переломы и деформацияскелета. Образование внекостных
кальцинатов имеет различные клинические проявления. При кальцификации артерий могут развиваться ишемические изменения (кальцифилаксия). На руках и ногах могут быть выявлены периартикулярные кальцинаты. Кальцификация конъюнктивы и роговицы в сочетании с рецидивирующим конъюнктивитом обозначается как синдром «красного глаза».
Зачастую гиперпаратиреоз длительно протекает без выраженной клинической симптоматики. Существует пять основных признаков первичного гиперпаратиреоза, разные сочетания которых формируют его многоликую клиническую картину.
Остеопатия (остеопороз).
Нефропатия (нефрокальциноз и нефрокалькулёз).
|
Висцеропатия |
(желчекаменная |
болезнь, калькулёзный |
|
панкреатит, язвенная болезнь желудка). |
|
|
|
Психопатия. |
|
|
Миопатия.
Поскольку специфических признаков заболевания не существует, диагностический поиск базируется на комплексной оценке жалоб, анамнеза и данных объективного обследования.
Общие симптомы Слабость Апатия Обезвоживание
Признаки поражения почек
1.Полиурия
2.Нефролитиаз и/или нефрокальциноз
3.Снижение выделительной функции почек
признаки поражения ЖКТ
1.Потеря аппетита
2.Тошнота
3.Запор
4.Боль в животе
признаки поражения ЦНС
1.Депрессия
2.Снижение когнитивных функций
3.Изменения психоэмоционального статуса
4.Психоз
Признаки поражения сердечно-сосудистой системы
1.Артериальная гипертензия
2.Укорочение интервала QT
3.Повышенная чувствительность к препаратам наперстянки
Лабораторная диагностика:
o Рутинные методы:
1.Повышение сывороточной концентрации кальция и его ионизированной формы.
2.Гиперкальциемия в сочетании со снижением уровня неорганических фосфатов.
3.Резко положительная проба Сулковича (экскреция кальция с мочой превышает 200 мг/сут), однако при нарушении функции почек этого может не наблюдаться[4].
Инструментальная диагностика:
1.Ультразвуковое исследование — начальный метод лучевой диагностики образований паращитовидных желез — УЗИ может применяться интраоперационно для поиска желёз. Обладает высокой чувствительностью, но, к сожалению, не высокой специфичностью.

Поэтому выявленные на УЗИ образования требуют дальнейшей верификации другими методами диагностики.
2.Компьютерная томография с внутривенным контрастированием — очень чувствительный метод исследования, его примущество заключается в том, что можно выявлять загрудинные паращитовидные железы.
3.Радионуклидная диагностика — оценка функциональной активности образований паращитовидных желёз.
Лечение
На |
сегодняшний |
день |
консервативные |
методы |
лечения |
|
(форсированный диурез, инфузия |
растворов хлорида или сульфата натрия, |
|||||
введение бифосфонатов и глюкокортикостероидов) |
не |
показали |
||||
эффективности |
в |
качестве |
самостоятельного |
метода |
лечения |
|
гиперпаратиреоза. |
|
|
|
|
|
|
«Золотым стандартом» в лечении гиперпаратиреоза является хирургический метод. В руках опытных хирургов его эффективность достигает 95—98%.
Оперативное вмешательство осуществляется под наркозом (общей анестезией). Для осуществления доступа к паращитовидным железам выполняется разрез передней поверхности шеи длиной 5—7 см. Поиск паращитовидных желез чаще всего затруднён, в связи с чем для топической диагностики паращитовидных желез и контроля эффективности проведенного оперативного вмешательства интраоперационно выполняют:
исследование |
уровня кальция |
и паратгормона в крови, УЗИ и |
гамма- |
||
детекцию |
паращитовидных |
желез. |
Серьёзным |
и |
редким |
осложнением паратиреодэктомии является — |
повреждение возвратного |
||||
гортанного нерва (одноили двустороннее). Клиническими проявлениями
повреждения |
возвратного |
гортанного нерва |
являются: осиплость |
|
или отсутствие |
голоса, стридорозное дыхание. |
Немаловажно, |
чтобы |
|
оперативное вмешательство |
|
|
|
|
осуществлялось |
в |
специализированной |
клинике |
опытным |
эндокринным хирургом. |
|
|
|
|
28. Остеопороз этиология патогенез клиника диагностика лечение
Остеопороз – системное заболевание скелета, характеризующееся уменьшением массы кости в единице объема и расстройством микроархитектоники костной ткани, приводящим к повышению хрупкости костей и высокому риску их переломов, остеопороз в большинстве случаев вторичен по отношению к тому или иному заболеванию и, строго говоря, является синдромом.
Согласно данным ВОЗ остеопороз как причина инвалидизации и смертности больных от переломов костей занимает 4-е место среди неинфекционных заболеваний, уступая лишь болезням сердечно-сосудистой системы, онкологической патологии и сахарному диабету. Это обусловлено широкой распространенностью остеопороза, его многофакторной природой, поздней диагностикой и несвоевременным началом лечения.
Остеопороз – одно из наиболее известных метаболических заболеваний скелета, плотность которого повышается с возрастом. Каждая третья женщина после наступления менопаузы и более половины всех лиц в возрасте 75–80 лет имеют остеопороз, последствия которого заключается в переломах тел позвонков и трубчатых костей, что определяет существенное увлечение заболеваемости, инвалидности и летальности среди лиц пожилого возраста. Около 20 % больных с переломами шейки бедра умирают в течение 6 месяцев после перелома, а из оставшихся 50 % становятся инвалидами. Частота переломов бедра является одним из показателей распространенности остеопороза.
Этиология и патогенез
Большинство форм остеопороза должны рассматриваться как симптоматические при целом ряде заболеваний. Так, в МКБ-10 различаются остеопороз с аномальными переломами костей и без аномальных переломов.
По морфологическим признакам выделяют трабекулярный,
кортикальный и смешанный остеопороз, по метаболической активности
– остеопороз с повышенным костным обменом, с низкой степенью метаболизма костной ткани и с нормальными показателями костного метаболизма. Скорость потери костного вещества может зависеть от многих факторов. При любом патофизиологическом механизме масса костной ткани будет сбавляться, достигая некоторого порогового значения, после которого наступает стадия переломов.
При остеопорозе с высоким костным обменом высокая резорбция кости не компенсируется нормальным или повышенным костеобразованием, а при остеопорозе с низким костным обменом скорость резорбции кости нормальная или снижена, а темп костеобразования замедлен. И та, и иная формы могут обнаруживаться как разные этапы остеопоротического процесса у одного больного.
В патогенезе постменопаузального остеопороза пусковым фактором является эстрогенная недостаточность, резко ускоряющая потерю костной массы. Доказано наличие эстрогенных рецепторов на остеобластах, а дефицит эстрогенов способствует продукции остеобластами фактора, стимулирующего и дифференцировку, и активность остеокластов, что
обусловливает повышенную резорбцию кости. Недостаток эстрогенов способствует снижению выделения кальцитонина и увеличенной ощутимости кости к резорбтивному влиянию паратиреоидного гормона, а также вторично обусловленному дефициту витамина D и снижению абсорбции кальция в кишечнике.
В патогенезе сенильного остеопороза наряду с дефицитом половых стероидов и кальцитонина большое значение придают негативному кальциевому балансу, обусловленному дефицитом витамина D, и сниженной абсорбции кальция в кишечнике, что в результате приводит к формированию повторного гиперпаратиреоза и повышенной резорбции костной ткани. Нарушение обмена витамина D объясняют как уменьшением инсоляции вследствие снижения пребывания на улице, так и нарушением образования активных форм из-за дефицита половых гормонов. Избыточная или недостаточная секреция большего количества гормонов в любом возрасте ведет к остеопорозу. Примерами резкого преобладания резорбции костной ткани могут служить костная форма первичного гиперпаратиреоза и патология метаболизма костной ткани при тяжелом рецидивирующем течении тиреотоксикоза.
Избыток глюкокортикоидов при синдроме Кушинга подавляет
костеобразование, при этом снижается всасывание кальция в кишечнике и повышается экскреция его почками, что создает отрицательный кальциевый баланс, приводит к вторичному гиперпаратиреозу и повышенной костной резорбции.
Механизм развития остеопороза при гипогонадизме у женщин в
репродуктивном периоде сходен с таковым при постменопаузе. Снижение андрогенной функции у мужчин ведет к уменьшенному костеобразованию и формированию остеопороза с низким костным обменом.
Характерными переломами для остеопороза могут быть переломы проксимальных отделов бедра, тел позвонков и дистальных отделов костей предплечья, хотя могут наблюдаться переломы любой локализации. Переломы тел позвонков являются одним из классических признаков остеопороза, а их последствия в виде болей в спине, расстройства функции и деформаций позвоночника обусловливают уровень нетрудоспособности и значимость этого вопроса для здравоохранения.
Распространенность данных переломов в России составила 11,8 %. Почти в 50 % случаев остеопороз протекает бессимптомно или малосимптомно и выявляется лишь при наличии переломов костей. Для постменопаузального, стероидного и гипогонадального остеопороза характерны преимущественные потери трабекулярной костной ткани и в соответствии с этим переломы тел
позвонков, ребер и переломы лучевой кости в типичном месте (остеопороз I типа).
Преимущественное поражение кортикальной костной ткани присуще сенильному остеопорозу, гиперпаратиреозу и тиреотоксикозу (остеопороз II типа), при этом чаще встречаются переломы трубчатых костей и шейки бедра; но часты (особенно в старших возрастных группах) и переломы тел позвонков. Типичны жалобы на боли в спине, обостряющиеся после физической нагрузки, при длительном пребывании в одном положении. Эти боли пропадают после отдыха лежа. Выраженность болевого синдрома может быть различной не только у разных больных, но и у одного и того же пациента в разные этапы болезни.
При обследовании нужно обращать внимание на трансформацию осанки пациента, деформацию грудной клетки, уменьшение роста, формирование кожных складок на боковой поверхности грудной клетки, нарушения походки.
Диагностика остеопороза предполагает решение следующих задач:
1)выявление остеопении и переломов костей;
2)оценку уровня метаболизма в костной ткани (исследование биохимических или морфологических маркеров костной резорбции и костеобразования, а также показателей кальциевого обмена);
3)выяснение причин остеопении и дифференциальная диагностика с другими формами метаболических остеопатии. Первичный остеопороз прежде всего дифференцируют с остеомаляцией, костной формой первичного гиперпаратиреоза, остеопоротической формой болезни Педжета, миеломной болезниью и костными метастазами. Диагноз первичного остеопороза ставится после исключения перечисленных заболеваний.
Основные задачи лечения остеопороза:
1)замедление или прекращение потери массы кости (в идеале ее прирост);
2)предотвращение новых переломов костей;
3)нормализация костного ремоделирования;
4)уменьшение болевого синдрома, расширение двигательной активности;
5)улучшение качества жизни пациента.
Нормализация костного ремоделирования (подавление повышенной костной резорбции или стимуляция костеобразования) является основой лечения. Лечение основного заболевания при вторичном остеопорозе или отмена препаратов, отрицательно влияющих на метаболизм костной ткани, зачастую трудны в практической деятельности. Симптоматическая терапия является обязательной составной частью лечения.
Препараты для лечения остеопороза условно делятся на 3 группы:
1)преимущественно снижающие резорбцию костной ткани (эстрогены, кальцитонины, бисфосфонаты);
2)преимущественно усиливающие костеобразование (фториды, анаболические стероиды, андрогены, фрагменты синтетического паратгормона, гормон роста);
3)влияющие на оба процесса костного ремоделирования (активные метаболиты витамина D, оссеингидроксиапатитный комплекс, иприфлавон (остеохин)).
Выбор конкретного препарата определяется как формой остеопороза, так и преобладающей клинической симптоматикой. Кроме того, учитываются показания и противопоказания к тому или иному виду терапии.
При постменопаузальном остеопорозе, а также при остеопорозе другого генеза женщинам в постменопаузе при отсутствии противопоказаний назначается заместительная терапия эстрогенами (прогинова, циклопрогинова, климен, климонорм, ливиал, клиогест и пр.).
Лечение кальцитонином (миакальциком) показано при постменопаузальном, стероидном, сенильном и идиопатическом остеопорозе, особенно при выраженном болевом синдроме. Продолжительность курса лечения кальцитонином в прерывистом режиме может составлять 2–5 лет. Лечение желательно сочетать с препаратами кальция, а также витамином D.
Бисфосфонаты (ксидифон, алендронат) показаны при лечении постменопаузального и сенильного остеопороза у лиц без выраженных нарушений функций желудочно-кишечного тракта.
Показанием к применению фторидов (фторида натрия, оссина, кореберона) служит остеопороз с низким уровнем костного обмена. Для предупреждения развития остеомаляции (деминерализации) при лечении фторидами добавляют препараты кальция и витамина D. При применении фторидов относительно высока частота побочных эффектов (20–30 %) в виде диспепсических явлений, глосситов и гингивитов, артралгий. Медленное
развитие лечебного действия фторидов требует терпения от больного и врача.
Анаболические стероиды не имеют самостоятельного значения при лечении остеопороза, хотя часто включаются в схемы комплексного лечения.
Активные метаболиты витамина D применяются в дозе 0,5–1,0 мкг в день в течение нескольких лет. В качестве монотерапии они показаны при сенильном, стероидном и постменопаузальном остеопорозе; являются препаратами выбора при остеомаляции (1–3 мкг/сут), почечной остеодистрофии, реабилитации после удаления паратиром. Активные метаболиты используются и в комбинированной терапии совместно с эстрогенами, кальцитонином, бисфосфонатами, иприфлавоном, фторидами.
Побочные эффекты встречаются в 2–3 % случаев и проявляются в виде диспепсических расстройств, слабости, сонливости, сухости во рту. Для предотвращения гиперкальциемии лечение желательно проводить в индивидуально подобранных дозах с контролем уровня кальция и креатинина в крови 1 раз в 2 месяца.
Иприфлавон (остеохин) – производное флавоноидов, синтезирующихся в папоротниках и цветущих растениях, усиливает костеобразование, снижает частоту новых переломов костей и оказывает умеренный анальгетический эффект в течение 12 месяцев применения.
Соли кальция самостоятельного значения в лечении остеопороза не имеют, но обязательно должны применяться в комплексе с другими средствами как основа патогенетической терапии, а также для первичной профилактики остеопороза.
Симптоматическая терапия подразумевает аналгезию, назначение корсетов, лечебную физкультуру. Боль в спине снижает двигательную активность пациента и качество его жизни.
Для уменьшения болей наряду с патогенетическими средствами используются анальгетики, нестероидные противовоспалительные средства, а также миорелаксанты.
Корсеты абсолютно показаны при наличии компрессионных переломов тел позвонков и при тяжелом остеопорозе. Наиболее часто рекомендуют полужесткие корсеты и полукорсеты. Возможность атрофии мышц при ношении корсетов невелика и не подтверждается в работах последних лет. При выраженном болевом синдроме рекомендуется только дыхательная гимнастика, при уменьшении боли – изометрические упражнения.
В дальнейшем назначаются упражнения для мышц живота, спины, нижних и верхних конечностей. Затем присоединяют упражнения, проводимые в положении стоя, дозированную ходьбу, плавание. Массаж назначают не ранее 4–6 месяцев после начала медикаментозной терапии.
Первичная профилактика остеопороза подразумевает контроль за достаточным потреблением кальция в детском возрасте, в периоды беременности и лактации, достаточное пребывание на солнце пожилых людей, активный образ жизни и занятия физкультурой с умеренной физической нагрузкой, отказ от злоупотребления алкоголем и курением, от увлечения различными несбалансированными диетами и голоданием.
29. Синдром гиперкортицизма/ синдром Кушинга
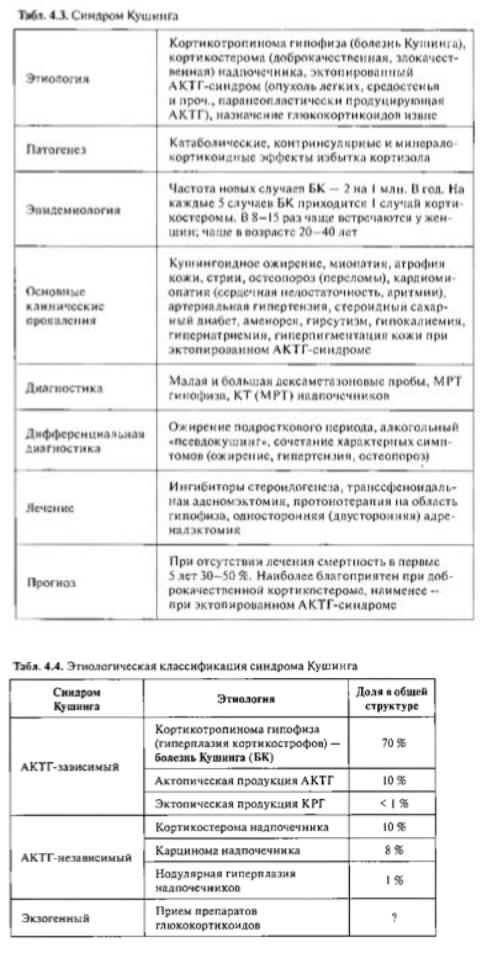
Синдром Кушинга (гиперкортицизм, СК) — клинический синдром, обусловленныйэндогеннойгиперпродукциейили длительным экзогенным приемом кортикостероидов (табл. 4.3). Впервые клиническая картина эндогенного гиперкортицизма была описана в 1912 г. Гарвеем Кушингом
(1864—1939).
Этиология В соответствии с этиологией С К подразделяется на АКТГ-зависимый и
АКТГ-независимый: в первом случае гиперпродукция кортикостероидов связана с избытком А К Т Г (крайне редко КРГ), во втором — нет. Гипофизарный АКТГ-зависимый синдром Кушинга традиционно обозначается термином болезнь Кушинга (БК). Последняя представляет собой нейроэндокринное заболевание, патогенетической основой которого является формирование кортикотропиномы или гиперплазии кортикотрофов гипофиза, сочетающееся с повышением порога чувствительности гипоталамо-гипофизарнойсистемы к ингибирующему влиянию кортизола, что приводит к нарушению суточнойдинамики секреции А К Т Г с развитием двустороннейгиперплазии коры надпочечников. Таким образом, несмотря на порой значительную гиперпродукцию кортизола, последний не подавляет продукцию АКТГ, как это происходит внорме.
Таким образом, имеется нарушение механизма отрицательнойобратной связи секреции кортизола. Морфологическим субстратом БК является аденома гипофиза (в 90 % случаев микроаденома), которая представляет собой моноклональную опухоль. При БК, вотличие от эктопированного АКТГ-синдрома, продукция АКТГ аденомой гипофиза не полностью автономна.
Этиология С К , обусловленного кортизолпродуцирукнцей опухолью надпочечника (кортикостерома, злокачественная кортикостерома), неизвестна. Вданном случае речь идет гиперпродукции кортизола, которая не зависит от А К Т Г и абсолютно автономна. Эктопированныи АКТГсиндром, или синдром эктопической(внегипофизарной) продукции АКТГ
(значительно реже КРГ) обусловлен гиперпродукцией АКТГ некоторыми опухолями (мелкоклеточный рак легких, тимома, опухоль поджелудочной железы). Причины, по которым эти опухоли приобретают способность к паранеопластическойпродукции АТКГ, неизвестны.
Патогенез В основе патогенеза патологических изменении,̆ которые при С К развиваются со стороны большинства органов и систем, лежит в первую очередь гиперпродукция кортизола. Последнийв нефизиологических концентрациях оказывает катаболическое деиствиӗ на белковые структуры и матрицы большинства тканейи структур (кости, мышцы, в том числе гладкие и миокард, кожа, внутренние органы и т.п.), в ко торых постепенно развиваются выраженные дистрофические и атро фические изменения. Нарушения углеводного обмена заключаются в стоикой ̆ стимуляции глюконеогенеза и гликолиза в мышцах и печени, что приводит
кгипергликемии (стероидный диабет). На жировой обмен избыток кортизола оказывает комплексное деиствиӗ : на одних участках тела происходит избыточное отложение, а на других — атрофия жировой клетчатки, что объясняется разнойчувствительностью отдельных жировых компартментов к ГК. Важным компонентом патогенеза С К являются электролитные расстроиствӑ (гипокалиемия, гипернатриемия), которые обусловлены влиянием избытка кортизола на почки. Прямым следствием этих электролитных сдвигов является артериальная гипертензия и усугубление миопатии, в первую очередь кардиомиопатии, которая приводит
кразвитию сердечнойнедостаточности и аритмиям. Иммуносупрессивное деиствиӗ ГК обуславливает склонность к инфекциям.
Диагностика 1. Определение базального уровня кортизола иАКТГ имеет низкое
диагностическое значение в диагностике С К . В качестве скринингового теста более информативно определение суточной
экскреции свободного кортизола с мочой, но это исследование уступает по чувствительности и специфичности малойдексаметазоновойпробе.
2.При наличии у пациента симптомов или проявлений С К в первую очередь необходимо доказать или отвергнуть эндогенную гипер продукцию кортизола при помощи малойдексаметазоновойпробы. В соответствии с наиболее распространенным протоколом в 1-й день в 8—9 часов утра у пациента определяется уровень кортизола в сы воротке крови. В 24 часа этого же дня (ночью) пациент принимает внутрь 1 мг дексаметазона. В 8-9 часов утра следующего дня у паци ента опять определяется уровень кортизола сыворотки. В норме и при состояниях, не сопровождающихся эндогенным гиперкортицизмом, после назначения дексаметазона уровень кортизола снижается более чем в 2 раза. При любом варианте С К продукция кортизола адекватно не подавляется.
3.В том случае, если в малой дексаметазоновой пробе не произошло должного подавления уровня кортизола, необходимо прове-дение дифференциальнойдиагностики между патогенетическими вариантами С К , как правило, между БК и кортикостеромойнадпочечника. С этойцелью проводят большую дексаметазоновую пробу. Ее протокол отличается от такового при малой дексаметазоновой пробе только дозой препарата: пациенту назначается 8 мг дексаметазона. При БК после приема дексаметазона происходит снижение уровня кортизола более чем на 50 % от исходного; при кортикостероме и эктопированном АКТГ-синдроме указанного снижения уровня кортизола не происходит.
4. Топическая диагностика при Б К подразумевает проведение МРТ с целью выявления аденомы гипофиза. Кроме того, проводит ся КТ или МРТ надпочечников, при которых в случае БК выявля ется двусторонняя гиперплазия. Эти же методы используются для визуализации кортикостеромы (рис. 4.11). Визуализация опухоли, обусловливающей эктопированный АКТГ-синдром, в ряде случаев затруднена. Как правило, она локализуется влегких или средос тении (значительно реже вЖ КТ) и на момент диагностики имеет обширные метастазы.
5. Диагностика осложнений СК подразумевает проведение рентгенографии позвоночника для выявления компрессионных перело
Лечение
1.Ингибиторы стероидогенеза (хлодитан, аминоглютетимид) после постановки диагноза назначают большинству пациентов с эндоген ным гиперкортицизмом. Пациенты, которым назначается протонотерапия на область гипофиза, вынуждены получать препараты длитель но, до года и более в ожидании развития эффекта протонотерапии.
2.Тренссфеноидалыюе удаление кортитропиномы гипофиза является
методом выбора при БК вситуации, когда при МРТ удается визуализировать аденому. Ремиссия развивается у 90 % проопериро ванных
пациентов. Прогностически благоприятным после аденомэктомии является развитие транзиторного гипокортицизма, который может сохраняться от нескольких месяцев до года.
3.Протонотерапия на область гипофиза показана пациентам с БК, у которых не визуализируется аденома гипофиза. Развития стоикой ̆ремиссии БК можно ожидать примерно через год после проведения протонотерапии.
4.Адреналэктомия является основным методом лечения кортикостеромы надпочечника. В ряде случаев при тяжелом течении БК, когда пациенту показано проведение протонотерапии, производится односторонняя адреналэктомия, которая позволяет несколько уменьшить выраженность гиперкортицизма. Двусторонняя адреналэктомия для лечения БК последние несколько десятилетий практически не используется. Тем не менее вряде случаев при краинӗ тяжелом течении заболевания к ней приходится прибегать. После двустороннейадреналэктомии при БК может происходить значительныйрост аденомы гипофиза (синдром Нельсона).
5.При эктопированном АКТГ-синдроме лечение будет зави сеть от локализации и распространенности опухолевого процесса. В большинстве
случаев радикальное лечение |
из-за |
распространен- |
ного |
метастазирования невозможно. |
В отдельных случаях |
показано |
|
симптоматическое проведение двустороннейадреналэктомии.
6. Симптоматическая терапия при гиперкортицизме включает назна чение гипотензивных препаратов, калия, сахароснижающих препаратов, а также препаратов лечения остеопороза.
30. Острая надпочечниковая недостаточность |
|
|
||
Надпочечниковая |
недостаточность |
(НН, |
недостаточность |
коры |
надпочечников, гипокортицизм,болезнь Аддисона, «аддисонский криз») - клинический синдром, обусловленный недостаточной секрецией гормонов коры надпочечника в результате нарушения функционирования одного или нескольких звеньев гипоталамо-гипофизарно-надпочечниковой системы. НН
подразделяется на первичную, являющуюся результатом деструкции самой коры надпочечников, и вторичную (гипоталамо-гипофизарную), возникающую вследствие недостаточности секреции АКТГ аденогипофизом. В клинической практике наиболее часто встречается первичная хроническая надпочечниковая недостаточность (95 % случаев) (1-ХНН)(т.е. Острая недостаточность коры надпочечников чаще всего возникает у больных с хронической надпочечниковой недостаточностью. )
Этиология. Острая надпочечниковая недостаточность (аддисонический
криз), в подавляющем большинстве случаев, имеет те же причины, что и хроническая и представляет собой ее декомпенсацию.
1.Аутоиммунная деструкция коры надпочечников (аутоиммунный адреналит) (98 % случаев). В крови большинства пациентов обнаруживаются антитела к ферменту 21-гидроксилазе (P450c21)
2.Туберкулез надпочечников (1-2 %) развивается вследствие гематогенного распространения микобактерий. Большинство пациентов страдает туберкулезным поражением легких.
3.Адренолейкодистрофия (АЛД) (1-2 %) - Х-сцепленное рецессивное заболевание, при котором наследуется дефект ферментных систем, осуществляющих обмен длинноцепочечных жирных кислот, в результате происходит их аккумуляция в белом веществе ЦНС и коре надпочечников, приводящая к дистрофическим изменениям.
4.Редкие причины (коагулопатии, дусторонний геморрагический инфаркт надпочечников (синдром Уотерхауса-Фридериксена) метастазы опухолей, двусторонняя адреналэктомия, ВИЧ-ассоциированный комплекс. Основными причинами вторичного гипокортицизма являются различные опухолевые и деструктивные процессы в гипоталамо-гипофизарной области Патогенез. При первичном гипокортицизме в результате разрушения более
90% коры обоих надпочечников формируется дефицит альдостерона и кортизола. Дефицит альдостерона приводит к потере натрия, задержке калия (гиперкалиемия) и прогрессирующему обезвоживанию. Следствием водных и электролитных расстройств являются изменения со стороны сердечнососудистой и пищеварительной систем. Дефицит кортизола приводит к снижению адаптивных возможностей организма, снижению процессов глюконеогенеза и синтеза гликогена. В связи с этим 1-ХНН манифестирует на фоне различных физиологических стрессов (инфекции, травмы, декомпенсация сопутствующей патологии).
Дефицит кортизола по механизму отрицательной обратной связи приводит к повышению продукции АКТГ и его предшественника проопиомеланокортина (ПОМК). В результате протеолиза последнего помимо АКТГ образуется еще и меланоцитстимулирующий гормон (МСГ),который обуславливает наиболее яркий симптом 1-ХНН - гиперпигментацию кожи и слизистых.
В связи с тем, что продукция альдостерона корой надпочечников происходит практически независимо от эффектов АКТГ, при вторичном гипокортицизме вследствие недостатка АКТГ развивается дефицит одного только кортизола, а продукция альдостерона сохраняется.()поэтому вторичный протекает легче,чем первичный)
Клиника.
Клиническая картина острой надпочечниковой недостаточности (аддисонического криза) представлена комплексом симптомов, по преобладанию которых можно выделить три клинические формы:
• Сердечно-сосудистая форма. При этом варианте доминируют явления острой недостаточности кровообращения: бледность лица с акроцианозом,
похолодание конечностей, выраженная артериальная гипотония, тахикардия, нитевидный пульс, анурия, коллапс.
•Желудочно-кишечная форма. По симптоматике может напоминать пищевую токсико-инфекцию или даже состояние острого живота. Преобладают боли в животе спастического характера, тошнота, неукротимая рвота, жидкий стул, метеоризм.
•Нервно-психическая форма. Преобладают головная боль, менингеальные симптомы, судороги, очаговая симптоматика, бред, заторможенность, ступор.
Диагностика.
1.Лабораторное подтверждение гипокортицизма. Для 1-ХНН характерна гиперкалиемия, гипонатриемия, лейкопения, лимфоцитоз, сниженный уровень кортизола и альдостерона, высокий уровень АКТГ и ренина. Информативность определения базального уровня кортизола ограничена. В основе лабораторной диагностики 1-ХНН лежит тест с 1-24АКТГ (синактеном). 1-24АКТГ вводится внутривенно в дозе 250 мкг, либо внутримышечно в дозе 500-1000 мкг (синактен-депо). В первом случае уровень кортизола оценивается через 60 минут, во втором - через 8-12 часов. Если уровень кортизола на фоне стимуляции превышает 500 ммоль/л, диагноз 1-ХНН может быть исключен.
2.Этиологическая диагностика. Маркером 1-ХНН аутоиммунного генеза являются антитела к P450c21. Для адренолейкодистрофии характерно повышение в крови уровня длинноцепочечных жирных кислот (С24:0 - С26:0), а также достаточно специфичные изменения, выявляемые при МРТ головного и спинного мозга (симметричная демиелинизация, вовлекающая мозолистое тело и перивентрикулярное периокципитальное белое вещество). При 1-ХНН туберкулезного генеза практически всегда выявляются изменения со стороны легких.
Лечение.
Лечение острой надпочечниковой недостаточности базируется на следующих основных принципах:
•Регидратационная терапия: изотонический раствор в объеме 2-3 литра в первые сутки в сочетании с 10-20 % раствором глюкозы.
•Массированная заместительная терапия гидрокортизоном: 100 мг в/в, затем каждые 3-4 часа по 50-100 мг в/в или в/м. По мере стабилизации состояния пациента доза снижается до поддерживающей. При отсутствии гидрокортизона, например на время доставки пациента в клинику возможно назначение эквивалентных доз преднизолона.
• Симптоматическая терапия сопутствующих заболеваний, вызвавших декомпенсацию ХНН (чаще всего - антибактериальная терапия инфекционных заболеваний).
