
- •Классификация.
- •Клиника.
- •Экссудативный перикардит
- •Диагностика.
- •Лечение.
- •Этиология
- •Клинические проявления
- •Диагностика
- •Лечение
- •3. Патогенез отёчного синдрома
- •Показатели контроля углеводного обмена (индивидуальные цели лечения)
- •Данным целевым уровням HbA1c будут соответствовать следующие целевые значения пре- и постпрандиального уровня глюкозы плазмы
- •Соответствие HbA1c среднесуточному уровню глюкозы плазмы (ссгп) за последние 3 мес.
- •Этиология. Гипогликемические состояния могут возникать при сахарном диабете вследствие:
- •Профилактика.
- •Клиническая картина
- •Лечение
- •28. Остеопороз этиология патогенез клиника диагностика лечение

Для профилактики отека головного мозга назначают в/в 5 мл 25 % р-ра сернокислой магнезии (вводить медленно) или капельное в/в введение маннитола по 0,5–1 г/к в виде 15 % или 20 % р-ра (200–250 мг). Больным необходима оксигенотерапия.
После выведения из гипогликемической комы рекомендуется применение средств, улучшающих микроциркуляцию и стимулирующих метаболизм углеводов и белков в клетках.
При развитии гипогликемических реакций в результате лечения сахароснижающими таблетированными препаратами или пролонгированными инсулинами следует помнить о возможности рецидивирования гликемии в течение суток, пока продолжается действие соответствующего препарата.
Профилактика.
Профилактика гликемических состояний у больных сахарным диабетом складывается из двух компонентов. Первый из них заключается в назначении адекватной сахароснижающей терапии инсулином (избегая синдрома передозировки) или таблетированными препаратами с учетом функционального состояния печени и почек.
Второй компонент профилактики в значительной степени обусловлен распределением углеводов в пищевом рационе в соответствии с эффектом развертывания сахароснижающих препаратов, а также правильной регламентации физических нагрузок в течение дня.
16. Гестационный сахарный диабет: определение, патогенез, клиника, диагностика, лечение.
Гестационный сахарный диабет (ГСД) (ВОЗ, 1999) – гипергликемия, относящаяся к категориям сахарный диабет (СД) или нарушенная толерантность к глюкозе, возникшая или впервые выявленная во время беременности, причем не исключается возможность того, что нарушение углеводного обмена могло предшествовать беременности, но оно не было установлено.
Патогенез ГСД. Во время беременности, по мере созревания плаценты, постепенно нарастает инсулинорезистентность. Основную роль в этом процессе играют фетоплацентарные гормоны (плацентарный лактоген и прогестерон) и гормоны матери (кортизол, эстрогены, пролактин), концентрация которых в крови также возрастает с увеличением сроков
беременности. |
Этот процесс компенсируется |
повышением продукции |
|||
и снижением |
клиренса |
эндогенного |
инсулина |
матери. |
|
Инсулинорезистентность |
усугубляется |
увеличением |
калорийности |
||
принимаемой |
матерью пищи, снижением |
физической |
активности |
||
и прибавкой веса. |
|
|
|
|
|
При наличии эндогенных факторов, таких как наследственная предрасположенность к СД типа 2, ожирение и т.д., секреция инсулина становится недостаточной для преодоления инсулинорезистентности, что и приводит к появлению гипергликемии.
Патогенез СД типа 1, других типов СД, которые могут впервые дебютировать во время беременности и также относятся к категории ГСД, ничем не отличается от такового у небеременных женщин.
Клинические проявления и симптомы
ГСД чаще не имеет клинических проявлений, связанных с гипергликемией, таких как полиурия, полидипсия, снижение веса, зуд, поэтому необходимо проводить активный скрининг этого заболевания.
Диагностика ГСД (рекомендации ВОЗ, 1999)
У женщин с высоким |
риском развития ГСД |
(СД |
у ближайших |
||||||
родственников, |
ожирение, |
нарушение |
углеводного |
обмена |
|||||
в анамнезе, глюкозурия) |
при |
первом |
обращении |
проводится |
ОГТТ |
||||
с 75 г глюкозы. Если ГСД не выявляется, |
тест повторяется между 24 |
и 28 |
|||||||
неделями беременности. |
|
|
|
|
|
|
|
|
|
Всем женщинам |
со средним |
риском |
развития |
ГСД |
оральный |
тест |
|||
с 75 г глюкозы проводится между 24 и 28 неделями беременности.
Женщинам с низким риском развития ГСД оральный тест с 75 г глюкозы не проводится.
Методика проведения ОГТТ с 75 г глюкозы
До проведения теста пациентка в течение 3 дней должна находиться на обычной диете, богатой углеводами (более 150 г углеводов в день) и придерживаться обычной для себя физической активности. Вечером перед проведением теста следует принять пищу, содержащую 30–50 г углеводов. ОГТТ необходимо проводить утром после ночного голодания в течение 8–14 часов, во время которого можно пить только воду. Во время проведения теста не разрешается курить, ходить. Необходимо учитывать все факторы, которые могут повлиять на результаты теста. Так, например, некоторые лекарственные препараты (глюкокортикоиды и токолитики), а также
интеркурентные инфекции могут снижать толерантность к углеводам. После забора первой пробы плазмы венозной крови натощак уровень гликемии измеряется немедленно, так как при получении результатов, характерных для диагноза ГСД, тест прекращается. При выявлении нормогликемии или нарушенной гликемии натощак пациентка в течение 5 минут должна выпить раствор, приготовленный из 75 г глюкозы в виде сухого вещества и 250–300 мл воды. Начало приема раствора глюкозы считается началом теста. Через 2 часа проводится повторный забор проб плазмы венозной крови.
При исследовании уровня гликемии в венозной плазме пробы крови берутся в пробирку с фторидом натрия (6 мг на 1 мл цельной крови) и EDTA. Затем немедленно (в течение ближайших 30 минут) центрифугируются для предотвращения спонтанного гликолиза. Известно, что даже при наличии консервантов уровень гликемии в цельной крови при комнатной температуре
может снизиться |
на 10% и более. Если |
сразу после центрифугирования |
не проводится |
определения гликемии, |
плазму следует заморозить. |
У пациентов с нормальным гематокритом концентрация глюкозы в цельной крови ~ на 15% ниже, чем в плазме, а в артериальной крови ~ на 7% выше, чем в плазме.
Беременным женщинам, у которых показатели гликемии по рекомендациям ВОЗ соответствуют критериям диагностики СД или нарушенной толерантности к глюкозе, ставится диагноз ГСД. Значение нарушенной гликемии натощак во время беременности еще не установлено (ВОЗ, 1999). Всем беременным с НГН рекомендуется проведение ОГТТ с 75 г глюкозы. Если результаты исследования соответствуют норме, повторно тест обязательно проводится на 24–28 неделях беременности. На более ранних сроках ГСД часто не выявляется, а установление диагноза после 28 недель не всегда предотвращает развитие диабетической фетопатии. Всем женщинам, имеющим факторы риска развития ГСД, даже при нормогликемии, проводится ОГТТ с 75 г глюкозы.
Случайное определение уровня гликемии лабораторным методом (ВОЗ, 1999) ³11,1 ммоль/л (³ 200 мг/дл) в цельной капиллярной крови или в плазме венозной крови в течение дня или гликемия натощак ³ 7,0 ммоль/л (³ 126 мг/ дл) в плазме венозной крови и ³ 6,0 ммоль/л в цельной капиллярной крови достаточно для диагностики ГСД и не требует дальнейшего подтверждения.
Измерение |
уровня гликемии проводится в лаборатории |
с помощью |
ферментных |
методов (глюкозо-оксидазного, гексо-киназного |
или глюкозо- |
дегидрогеназного).Средства самоконтроля не используются для скрининга и диагностики ГСД. Анализ уровня HbA1c также не зарекомендовал себя как чувствительный диагностический тест для выявления ГСД. Гликирование белков является неферментным процессом, который зависит
от длительности гипергликемии. В связи |
с этим существует несколько |
проблем в использовании определения |
уровня гликированных белков |
вкачестве диагностических тестов:
у беременных женщин уровень гликемии натощак ниже, чем
у небеременных;
во время беременности постпрандиальный уровень глюкозы выше;
в связи с ускорением эритропоэза во время беременности уровень HbA1c ниже нормативных показателей на 20%;
во время проведения скрининга ГСД продолжительность любого потенциального нарушения толерантности к глюкозе может быть слишком коротким.
Глюкозурия не является диагностическим критерием ГСД, так как у многих беременных женщин несколько раз в течение дня может появляться глюкозурия. Это связано с повышением скорости клубочковой фильтрации, снижением почечного порога для глюкозы и канальцевой реабсорбции глюкозы во время беременности. Однако наличие глюкозурии требует измерения уровня гликемии и при наличии факторов риска проведения ОГТТ с 75 г глюкозы.
Лечение. Клинические рекомендации и оценка эффективности леченияПротокол ведения женщин с ГСД
Начиная с первого обращения и далее в течение всей беременности, пациентки, входящие в группу риска по ГСД, и женщины с выявленным ГСД наблюдаются амбулаторно в специализированном центре «Беременность
исахарный диабет». Наблюдение предполагает:
обучение в школе «Гестационный сахарный диабет»;
до 29 недели беременности визиты в центр осуществляются пациентками каждые 2 недели, а с 29 недели – 1 раз в неделю;
прием ведется одновременно эндокринологом и акушером-
гинекологом;при необходимости пациентки активно вызываются
на дополнительные визиты по телефону медицинской сестрой;
пациентки ведут дневник самоконтроля, где ежедневно фиксируют показатели самоконтроля (табл. 5). Записи в дневнике обсуждаются во время каждого запланированного и дополнительного визита в центр или консультации по телефону;
для экстренных консультаций обеспечивается доступ к врачуэндокринологу по мобильной телефонной связи;
после выявления ГСД всем пациенткам подбирается соответствующее лечение, даются рекомендации по диете, физическим нагрузкам, при необходимости подбирается режим инсулинотерапии.
Рекомендации |
по диетотерапии должны |
быть нацелены на ограничение |
||
употребления |
с пищей легко |
усвояемых углеводов для |
достижения |
|
и стабильного |
поддержания |
целевых |
уровней гликемии. |
Женщинам |
с нормальным весом тела рекомендуется суточная калорийность пищи 30 ккал/кг, а при избыточной массе тела – 25 ккал/ кг при весе 120–150% от идеальной массы тела, 12–15 ккал/ кг при весе > 150% от идеальной массы
тела. |
Исключается |
|
употребление |
в пищу |
углеводов |
|||
с высоким гликемическим |
индексом. Углеводы |
с высоким |
содержанием |
|||||
пищевых |
волокон |
должны |
составлять |
не более |
38–45% |
от суточной |
||
калорийности пищи, белки – 20–25% (1,3 |
г/ кг), жиры – до 30%. Продукты, |
|||||||
содержащие углеводы, равномерно распределяются |
в течение дня на 3 |
|||||||
основных |
приема |
пищи |
и 2–3 |
перекуса |
с минимальным их |
содержанием |
||
в рационе завтрака.
Женщины проводят самоконтроль гликемии не менее 4 раз в день – натощак и через 1–2 часа после основных приемов пищи. Пациентки, находящиеся на инсулинотерапии, помимо постпрандиальной гликемии, контролируют гликемию перед едой, на ночь и в 3 часа ночи.
Беременным, находящимся на гипокалорийной диете, ежедневно натощак в утренней порции мочи или цельной капиллярной крови необходимо контролировать кетоновые тела для выявления недостаточного употребления углеводов или калорий с пищей.
Если на фоне диетотерапии в течение 1 недели не удается достичь целевых показателей гликемии, назначается инсулинотерапия. Во время беременности назначаются только генно-инженерные инсулины человека или аналоги инсулина ультракороткого действия (аспарт, лизпро). Использование пероральных сахароснижающих препаратов во время беременности не разрешено. Применяется режим многоразовых инъекций инсулина: комбинация инсулинов короткого или ультракороткого действия перед каждым приемом пищи, содержащей углеводы, в зависимости от углеводного коэффициента и с целью коррекции гипергликемии с учетом коэффициента чувствительности и инсулина изофанового человеческого в 2- х или 3-х инъекциях. Возможно использование фиксированных смесей инсулинов человека или вышеуказанных аналогов. Инсулин вводится подкожно при помощи инсулиновых шприцев или инсулиновых дозаторов (ручек). При суточной дозе инсулина > 100 Ед возможен перевод беременной на постоянную подкожную инфузию инсулина с помощью инсулиновой помпы. Схемы и дозы инсулинотерапии пересматриваются во время каждого визита в зависимости от данных самоконтроля, динамики роста плода, уровня HbA1c.
Появление ультразвуковых признаков диабетической фетопатии или повышение уровня инсулина в амниотической жидкости при установленном
диагнозе ГСД у женщин, находящихся на диетотерапии, также являются
показаниями к назначению инсулинотерапии, даже если поддерживаются целевые уровни гликемии.
Для каждой женщины индивидуально подбирается программа физических упражнений, в соответствии с ее возможностями.
Необходимые динамические обследования пациентки проходят либо в центре «Беременность и сахарный диабет», либо в женской консультации по месту жительства.
при СД рекомендуется родоразрешение на 38 неделе беременности. Сахароснижающая терапия во время родов зависит от особенностей лечения во время беременности, способа и экстренности родоразрешения. Целевой уровень гликемии в цельной капиллярной крови во время родов не превышает 4–6 ммоль/л.
Во время самостоятельных родов контроль гликемии в цельной капиллярной крови проводится каждые 2 часа при достижении целевых
уровней и ежечасно при тенденциях |
развития гипоили гипергликемии. |
Пациенткам, находившимся ранее |
на инсулинотерапии, во время |
самостоятельных родов инсулин короткого действия вводится внутривенно с помощью инфузомата. Внутривенная инфузия глюкозо-калиевой смеси начинается только при сохраняющейся тенденции к гипогликемии на фоне уже сниженной скорости инфузии инсулина или ее остановки.
При ГСД после отделения последа отменяется инсулинотерапия, при
тенденции |
к развитию гипогликемии |
возможна |
внутривенная |
||
инфузия глюкозо-калиевой |
смеси. Целевые |
уровни гликемии |
в цельной |
||
капиллярной крови после родоразрешения: натощак, перед едой, |
перед сном |
||||
4,0–6,0 ммоль/л, через 2 |
часа после еды 6,0–7,8 ммоль/л, |
ночью (в 3:00 |
|||
часа) – не менее 5,5 ммоль/л. |
|
|
|
||
Во время операции кесарева сечения контроль гликемии проводится до операции, перед извлечением плода, после отделения последа, далее каждые 2 часа при достижении целевых уровней и ежечасно при тенденции к развитию гипоили гипергликемии до возобновления самостоятельного энтерального питания.
Женщинам, находящимся до родов на диетотерапии, в периоперационном периоде инсулин не вводится. Следует избегать в/в инфузии растворов, содержащих глюкозу и лактат.
Женщинам на инсулинотерапии в периоперационном периоде инсулин короткого действия вводится внутривенно с помощью инфузомата. Внутривенная инфузия глюкозо-калиевой смеси начинается только при
сохраняющейся тенденции к развитию гипогликемии на фоне уже сниженной скорости инфузии инсулина или ее остановки. После отделения последа инфузия инсулина прекращается. При необходимости начинается внутривенная инфузия глюкозо-калиевой смеси. Целевые уровни гликемии
вцельной капиллярной крови в интраоперационном периоде 4,0–6,0 ммоль/л,
впостоперационном периоде: натощак, перед едой, перед сном 4,0–6,0 ммоль/л, через 2 часа после еды 6,0–7,8 ммоль/л, ночью (в 3:00 часа) не менее
5,5 ммоль/л. Женщинам, находящимся на постоянной подкожной инфузии инсулина с помощью инсулиновой помпы, во время родов продолжается введение инсулина со стандартной базальной скоростью. После отделения последа скорость инфузии снижается в 2 раза, начинается внутривенная инфузия глюкозо-калиевой смеси, возможна полная отмена инсулина.
17. Лабораторные исследования функции щитовидной железы. Инструментальные методы исследования щитовидной железы. Дифференциальная диагностика узловых образований щитовидной железы.
Лабораторные исследования функции щитовидной железы
Анализы крови включают определение тиреотропного гормона гипофиза, тироксина, трийодтиронина, антител к тиреоидной пероксидазе и тиреоглобулину.
ОПРЕДЕЛЕНИЕ УРОВНЯ ТТГ И ТИРОИДНЫХ ГОРМОНОВ
Исследование уровня ТТГ и тироидных гормонов (свободный тироксин и трийодтиронин) показано всем больным узловым зобом, а особенно пациентам, у которых имеются клинические симптомы пониженной или повышенной функции ЩЖ, а также при проведении консервативного лечения узлового зоба препаратами тироидных гормонов в целях контроля адекватности терапии.
Нормальная концентрация тиреоидных гормонов и ТТГ ТЗ = 1,2-2,8 нмоль/л
св.ТЗ = 2,5-5,8 пг/мл Т4 = 64-146 нмоль/л св.Т4 = 11-25 пг/мл, ТТГ = 0,3-4,0 мЕд/мл.
Тиреотропный гормон повышен при: гипотиреозе при хроническом аутоиммунном тиреоидите Хашимото; дефиците йода при эндемическом зобе; наследственном снижении образования тиреоидных гормонов;
врожденных аномалиях развития железы; удалении органа; новообразованиях гипофиза; опухолях легких, молочной железы; недостаточности надпочечников; длительных, изнуряющих заболевания внутренних органов; устойчивости к гормонам щитовидной железы; позднем токсикозе; психических расстройствах; отравлении свинцом; продолжительном применении определенных препаратов, йода в больших дозах.
Низкий уровень тиреотропного гормона в основном бывает при тиреотоксикозе. Его провоцируют: Базедова (Грейвса) болезнь (диффузный токсический зоб); узловой токсический зоб или токсическая аденома; тиреоидная автономия; гипертиреоз беременных; лекарственная терапия левотироксином; травма гипофиза; недостаточность гипоталамуса при инфекционных болезнях, врожденных аномалиях развития; применение препаратов.
Уровень свободного тироксина (Т4) при заболеваниях с низким ТТГ повышен (гипертиреоз, тиреотоксикоз), а при высоком ТТГ – снижен (гипотиреоз). При субклинических (скрытых) вариантах течения меняется только ТТГ, а тироксин остается в пределах нормы.
Инструментальные методы исследования щитовидной железы
УЛЬТРАЗВУКОВОЕ ИССЛЕДОВАНИЕ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
УЗИ позволяет верифицировать достаточно субъективные данные пальпации, подтвердить или опровергнуть наличие у пациента узлового и\или диффузного зоба. Протокол УЗИ должен дать ответы на следующие вопросы:
ТОНКОИГОЛЬНАЯ ПУНКЦИОННАЯ БИОПСИЯ ЩЖ
Тонкоигольная пункционная биопсия ЩЖ является единственным дооперационным методом прямой оценки структурных изменений и установления цитологических параметров образований в щитовидной железе
Задачи метода:
•подтверждение или опровержение диагноза опухоли ШЖ, в том числе и злокачественной;
•выявление морфологических изменений в ткани узла.
РАДИОИЗОТОПНОЕ ИССЛЕДОВАНИЕ (сцинтиграфия)
Сканирование щитовидной железы не является скрининг-тестом при узловых образованиях щитовидной железы и выполняется по определенным показаниям:
1.состояние после операции на ЩЖ по поводу рака для суждения о радикальности операции (выявление количества и функции оставшейся после операции тиреоидной ткани);
2.функционирующие метастазы дифференцированного рака ЩЖ (визуализация метастазов с помощью 131-йода возможна при отсутствии нормально функционирующей ШЖ, при наличии ее применяют 99тТс);
3."кольцевидный зоб", охватывающий трахею, загрудинный зоб;
4.эктопическое расположение щитовидной железы.
5.иногда, перед операцией по поводу рецидива узлового зоба (для выяснения топики тиреоидной ткани)
Сканирование позволяет судить о расположении ЩЖ, форме, размерах, контурах: распределение и интенсивность накопления радионуклида указывают на диффузное или очаговое поражение, функциональную активность узловых образований.
РЕНТГЕНОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ ГРУДНОЙ КЛЕТКИ С КОНТРАСТИРОВАНИЕМ ПИЩЕВОДА БАРИЕМ
Данное исследование позволяет выявить наличие сужения или смещения трахеи и пищевода у больного узловым зобом, а также диагностировать загрудинный зоб.
КОМПЬЮТЕРНАЯ И МАГНИТНО-РЕЗОНАНСНАЯ ТОМОГРАФИЯ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
КТ и МРТ являются высокоинформативными неинвазивными методами, при помощи которых визуализируется щитовидная железа. Наряду с оценкой локализации ЩЖ, ее контуров, формы, размеров, структуры, соотношения с прилежащими тканями, размеров и структуры регионарных лимфоузлов, КТ позволяет определить денситометрическую плотность образований в щитовидной железе.
Дифференциальная диагностика узловых образований щитовидной железы

18. Синдром гипотиреоза. Этиология. Патогенез. Клиника. Диагностика. Принципы терапии.
Синдром гипотиреоза - симптомокомплекс, обусловленный недостаточной секрецией щитовидной железой тиреоидных гормонов, что приводит к угнетению всех видов обмена, утилизации кислорода тканями, снижению активности различных ферментных систем, газообмена и основного обмена.
Этиология
Первичный гипотиреоз вызван действием следующих факторов
—Гипоили аплазией щитовидной железы;
—Врожденное нарушение синтеза тиреоидных гормонов;
—Тиреоидиты;
—Особенности питания (дефицит йода, избыток тиоционатов, присутствующих в капусте, брюкве, репе, турнепсе, маниоке, избыток ионов кальция и лития, блокирующих захват йода);
—Врачебные действия (удаления железы, лучевая терапия, приём лекарственных препаратов).
Вторичный гипотиреоз (гипофизарный и гипоталамический)
—Связан с гипопитуитаризмом;
—Дефектом синтеза и транспорта тиролиберина из гипоталамуса в гипофиз.
Третичный (постжелезистый)
—Связан с инактивацией циркулирующих в крови Т3 и Т4, ТТГ аутоантителами, протеазами при сепсисе, панкреатите, шоке;
—Связан с низкой чувствительностью рецепторов клеток-мишеней к гормонам;
—Возможной причиной является дейодирование гормонов в периферической крови.
Патогенез
Определяется снижением уровня тиреоидных гормонов, имеющих спектр влияния на физиологические функции и метаболические процессы в организме. В результате угнетаются все виды обменов, утилизация кислорода тканями, тормозятся окислительные реакции и снижается активность различных ферментных систем, газообмен и основной обмен. Замедление синтеза и катаболизма белка и белковых фракций, а также процесса их выведения из организма ведет к значительному увеличению продуктов белкового распада во внесосудистых пространствах органов и тканей, в коже, в скелетной и гладкой мускулатуре. В частности, в миокарде и в других мышечных группах накапливается креатинфосфат. В сердце, легких, почках, серозных полостях и прежде всего во всех слоях кожи избыточно депонируются кислые гликозоаминогликаны (ГАГ), преимущественно глюкуроновая кислота и в меньшей степени — хондроитинсерная. Избыток ГАГ меняет коллоидную структуру соединительной ткани, усиливает ее гидрофильность и связывает натрий, что в условиях затрудненного лимфооттока формирует микседему. Замедляются утилизация и выведение продуктов липолиза, повышается уровень холестерина, триглицеридов, в-липопротеидов. Дефицит тиреоидных гормонов тормозит развитие ткани мозга и угнетает высшую нервную деятельность, что особенно ощутимо в детском возрасте. Ограничивается физиологическая активность других эндокринных желез и в первую очередь коры надпочечников, быстро снижающих свою функцию в условиях гипотермии. Нарушается также периферический метаболизм кортикостероидов и половых гормонов (последнее ведет к ановуляции).
Клиника
Обменно-гипотермический синдром: ожирение, понижение температуры, зябкость, непереносимость холода, гиперкаротинемия, вызывающая желтушность кожных покровов.
Микседематозный отёк: периорбитальный отёк, одутловатое лицо, большие губы и язык с отпечатками зубов по латеральным краям, отёчные конечности, затруднение носового дыхания (связано с набуханием слизистой оболочки носа), нарушение слуха (отёк слуховой трубы и органов среднего уха), охрипший голос (отёк и утолщение голосовых связок), полисерозит.
Синдром поражения нервной системы: сонливость, заторможенность, снижение памяти, внимания, интеллекта, брадифрения, боли в мышцах, парестезии, снижение сухожильных рефлексов, полинейропатия, депрессия, мозжечковая атаксия. Нелеченный гипотиреоз у новорожденных приводит к умственной и физической отсталости (редко обратимо), кретинизму.
Синдром поражения сердечно-сосудистой системы: микседематозное сердце (брадикардия, низкий вольтаж, отрицательный зубец Т при ЭКГ, недостаточность кровообращения), гипотония, полисерозит, возможны нетипичные варианты (с гипертонией, без брадикардии, с постоянной тахикардией при недостаточности кровообращения и с пароксизмальной тахикардией по типу симпатико-адреналовых кризов в дебюте гипотиреоза).
Синдром поражения выделительной системы: снижении фильтрации и абсорбции.
Синдром поражения опорно-двигательной системы: отёчность суставов, боли при движении, генерализованная гипертрофия скелетной мускулатуры, умеренная мышечная слабость, синдром Хоффмана.
Синдром поражения пищеварительной системы: гепатомегалия, дискинезия желчевыводящих протоков, дискинезия толстой кишки, склонность к запорам, снижение аппетита, атрофия слизистой оболочки желудка, тошнота, иногда рвота.
Анемический синдром: анемия — нормохромная нормоцитарная, гипохромная железодефицитная, макроцитарная, В12-дефицитная.
Синдром гиперпролактинемического гипогонадизма: дисфункция яичников (меноррагия, олигоменорея или аменорея, бесплодие), галакторея — у женщин, у мужчин — снижение либидо, эректильная дисфункция.
Синдром эктодермальных нарушений: изменения со стороны волос, ногтей, кожи. Волосы тусклые, ломкие, выпадают на голове, бровях, конечностях, медленно растут. Сухость кожи. Ногти тонкие, с продольной или поперечной исчерченностью, расслаиваются.
Диагностика
Для постановки диагноза гипотиреоза врачом-эндокринологом устанавливается факт снижения функции щитовидной железы на основании осмотра пациента, его жалоб, и результатов лабораторных исследований:
определения уровня тироксина - Т4 и трийодтиронина – Т3 (тиреоидных гормонов) и уровень тиреотропного гормона - ТТГ (гормона гипофиза) в крови. При гипотиреозе отмечается пониженное содержание тиреоидных гормонов в крови, содержание ТТГ может быть как повышено, так и понижено;
определения уровня аутоантител к щитовидной железе (АТ-ТГ, АТТПО).
биохимического анализа крови (при гипотиреозе повышается уровень холестерина и других липидов);
УЗИ щитовидной железы (для определения ее размеров и структуры);
сцинтиграфии щитовидной железы или тонкоигольной биопсии.
Принципы терапии
Благодаря достижениям фармацевтической промышленности, позволяющим искусственно синтезировать тиреоидный гормон, современная эндокринология имеет эффективный способ лечения гипотиреоза. Терапия проводится путем замены недостающих в организме тиреоидных гормонов их синтетическим аналогом - левотироксином (L-тироксином).
Манифестный (клинический) гипотиреоз требует назначения заместительной терапии независимо от возраста пациента и сопутствующей патологии. Индивидуально назначается вариант начала лечения, исходная доза препарата и скорость ее возрастания. При латентном (субклиническом) гипотиреозе абсолютным показанием для проведения заместительной терапии является его диагностирование у беременной женщины или планирование беременности в ближайшее время.
Вбольшинстве случаев нормализация общего состояния больного гипотиреозом начинается в первую неделю начала приема лекарственного препарата. Полное исчезновение клинических симптомов происходит обычно в течение нескольких месяцев. У пожилых людей и ослабленных больных реакция на препарат развивается медленнее. Пациентам с сердечнососудистыми заболеваниями, требуется особо тщательно подбирать дозу препарата (избыточный прием L-тироксина повышает риск стенокардии, мерцательной аритмии).
Вслучае гипотиреоза, возникшего в результате удаления щитовидной железы или лучевой терапии, показан прием синтетических гормонов в течение всей жизни. Пожизненное лечение гипотиреоза также необходимо на
фоне аутоиммунного тиреоидита (болезни Хашимото). В процессе лечения пациенту необходимо регулярно посещать врача для коррекции дозы препарата, контролировать уровень ТТГ в крови.
Если гипотиреоз возникает на фоне других заболеваний, нормализация функции щитовидной железы чаще всего происходит в процессе излечения основной патологии. Симптомы гипотиреоза, вызванного приемом некоторых лекарств, устраняются после отмены данных препаратов. Если причина гипотиреоза – недостаток употребления йода с пищей, больному назначают йодсодержащие препараты, употребление в пищу йодированной соли, морепродуктов. Лечение гипотиреоидной комы проводят в отделениях интенсивной терапии и реанимации с назначением внутривенных введений больших доз тиреоидных гормонов и глюкокортикостероидов, коррекцией состояния гипогликемии, гемодинамических и электролитных нарушений.
19. Аутоиммунный тиреоидит. Определение. Клиника. Диагностика. Лечение
Определение.
Аутоиммунный тиреоидит (АИТ) - хроническое воспаление ткани щитовидной железы, имеющее аутоиммунный генез и связанное с повреждением и разрушением фолликулов и фолликулярных клеток железы.
Клиника
Большинство случаев хронического аутоиммунного тиреоидита (в эутиреоидной фазе и фазе субклинического гипотиреоза) длительное время протекает бессимптомно. Щитовидная железа не увеличена в размере, при пальпации безболезненна, функция железы в норме. Очень редко может определяться увеличение размера щитовидной железы (зоб), больной жалуется на неприятные ощущения в области щитовидной железы (чувство давления, кома в горле), легкую утомляемость, слабость, боли в суставах. Клиническая картина тиреотоксикоза при аутоиммунном тиреоидите обычно наблюдается в первые годы развития заболевания, имеет преходящий характер и по мере атрофии функционирующей ткани щитовидной железы переходит на некоторое время в эутиреоидную фазу, а затем в гипотиреоз. Послеродовый тиреоидит, обычно проявляется легким тиреотоксикозом на 14 неделе после родов. В большинстве случаев наблюдается утомляемость, общей слабость, снижение веса. Иногда тиреотоксикоз значительно выражен (тахикардия, чувство жара, избыточная потливость, тремор конечностей, эмоциональная лабильность, инсомния). Гипотиреоидная фаза аутоиммунного тиреоидита проявляется на 19-той неделе после родов. В некоторых случаях она сочетается с послеродовой депрессией. Безболевой (молчащий) тиреоидит выражается легким, часто субклиническим тиреотоксикозом. Цитокин-индуцированный тиреоидит также обычно не сопровождается тяжелым тиреотоксикозом или гипотиреозом.
Диагностика
До проявления гипотиреоза диагностировать АИТ достаточно сложно. Диагноз аутоиммунного тиреоидита эндокринологи устанавливают по клинической картине, данных лабораторных исследований. Наличие у других членов семьи аутоиммунных нарушений подтверждает вероятность аутоиммунного тиреоидита.
Лабораторные исследования при аутоиммунном тиреоидите включают в себя:
общий анализ крови - определяется увеличение количества лимфоцитов
иммунограмму – характерно наличие антител к тиреоглобулину, тиреопероксидазе, второму коллоидному антигену, антитела к тиреоидным гормонам щитовидной железы
определение Т3 и Т4 (общих и свободных), уровня ТТГ в сыворотке крови. Повышение уровня ТТГ при содержании Т4 в норме свидетельствует о субклиническом гипотиреозе, повышенный уровень ТТГ при сниженной концентрации Т4 – о клиническом гипотиреозе
УЗИ щитовидной железы - показывает увеличение или уменьшение размеров железы, изменение структуры. Результаты этого исследования служат дополнением к клинической картине и другим результатам лабораторных исследований
тонкоигольная биопсия щитовидной железы - позволяет выявить большое количество лимфоцитов и другие клетки, характерные для аутоиммунного тиреоидита. Применяется при наличии данных о возможном злокачественном перерождении узлового образования щитовидной железы.
Критериями диагностики аутоиммунного тиреоидита служат:
повышение уровня циркулирующих антител к щитовидной железе (АТ-ТПО);
обнаружение при УЗИ гипоэхогенности щитовидной железы;
признаки первичного гипотиреоза.
При отсутствии хотя бы одного из данных критериев диагноз аутоиммунного тиреоидита носит лишь вероятностный характер. Так как повышение уровня АТ-ТПО, или гипоэхогенность щитовидной железы сами по себе еще не доказывают аутоиммунный тиреоидит, это не позволяет установить точный диагноз. Лечение показано пациенту только в гипотиреоидную фазу, поэтому острой необходимости в постановке диагноза в эутиреоидной фазе, как правило, нет.
Лечение
Специфическая терапия аутоиммунного тиреоидита не разработана. Не смотря на современные достижения медицины, эндокринология пока не имеет эффективных и безопасных методов коррекции аутоиммунной
патологии щитовидной железы, при которых процесс не прогрессировал бы до гипотиреоза.
В случае тиреотоксической фазы аутоиммунного тиреоидита назначение препаратов, подавляющих функцию щитовидной железы - тиростатиков (тиамазол, карбимазол, пропилтиоурацил) не рекомендовано, так как при данном процессе отсутствует гиперфункция щитовидной железы. При выраженных симптомах сердечно-сосудистых нарушений применяют бетаадреноблокаторы.
При проявлениях гипотиреоза индивидуально назначают заместительную терапию тироидными препаратами гормонов щитовидной железы - левотироксином (L-тироксином). Она проводится под контролем клинической картины и содержания ТТГ в сыворотке крови.
Глюкокортикоиды (преднизолон) показаны только при одновременном течении аутоиммунного тиреоидита с подострым тиреоидитом, что нередко наблюдается в осенне-зимний период. Для снижения титра аутоантител применяются нестероидные противовоспалительные средства: индометацин, диклофенак. Используют также препараты для коррекции иммунитета, витамины, адаптогены. При гипертрофии щитовидной железы и выраженном сдавливании ею органов средостения проводят оперативное лечение.
20. Синдром тиреотоксикоза. Этиология. Патогенез. Клиника. Диагностика. Принципы терапии.
Гипертиреоз (тиреотоксикоз) – клинический синдром, вызванный повышением гормональной активности щитовидной железы и характеризующийся избыточной продукцией тиреоидных гормонов - Т3 (трийодтиронина) и Т4 (тироксина). Перенасыщение крови гормонами щитовидной железы вызывает ускорение в организме всех обменных процессов.
Этиология
Различают первичный и вторичный тиреотоксикоз.
Основной причиной развития первичного тиреотоксикоза (болезнь Грейвса, болезнь Базедова) является психический (острый или длительный, рецидивирующий) стресс. Как правило, при этом имеется умеренное увеличение ЩЖ диффузного характера, у ряда больных ЩЖ бывает практически не увеличена. Таким образом, тяжесть первичного тиреотоксикоза не зависит от величины ЩЖ.
Предрасполагающие факторы:
тип высшей нервной деятельности;
тяжелые травмы;
продолжительные острые инфекции;
нарушение функции эндокринной системы и в частности половых гормонов.
Вторичный тиреотоксикоз возникает вследствие тех же причин, но на фоне длительно существующего узлового или смешанного зоба – вторичная «базедовификация». Тиреотоксикоз при одиночном узле в ЩЖ именуют тиреотоксической аденомой.
Патогенез
тиреоидные гормоны увеличивают потребление кислорода тканями, повышая образование тепла и энергетический обмен
повышается чувствительность тканей к катехоламинам и симпатической стимуляции
увеличивается превращение андрогенов в эстрогены в тканях и возрастает содержание циркулирующего глобулина, связывающего половые гормоны, что повышает соотношение эстрогенов к андрогенам. Эти гормональные изменения могут вызвать гинекомастию у мужчин
быстрое разрушение кортизола под влиянием тиреоидных гормонов обусловливает клиническую картину гипокортицизма (обратимая надпочечниковая недостаточность).
Клиника
1. Легкая форма Раздражительность, плаксивость, плохой сон, быстрая утомляемость,
снижение трудоспособности, внимания, лабильный пульс от 90 до 100 ударов в мин, хорошего наполнения, тремор пальцев рук (симптом Мари), потеря веса около 10% должной массы тела, основной обмен повышен до
+30…+40%.
2. Тиреотоксикоз средней тяжести.
Легкая возбудимость, настороженность, раздражительность, плаксивость, повышенная обидчивость, резкое снижение трудоспособности, плохой сон. Пульс частый 100...120 ударов в мин, приступы параксизмальной тахикардии, экстрасистолия. Одышка, к вечеру появляются отеки нижних конечностей. Потеря веса более 20% должной массы тела. Отчетливый тремор рук, умеренный экзофтальм. Основной обмен +40…+50%.
3. Тяжелая форма.
Состояние тяжелое, психическое возбуждение, бессонница, моторная возбудимость (тиреотоксическая гиперкинезия), нарастающая мышечная слабость, тремор всего тела, дистрофические нарушения паренхиматозных
органов, отеки ног, иногда асцит. Тахикардия (> 120 ударов в мин), нередко - мерцательная аритмия. Прогрессирующая потеря веса при сохранившемся аппетите, дефицит массы тела достигает 40-50%. Нередко выраженный экзофтальм. Основной обмен +60% и более. Трудоспособность полностью утрачена.
Диагностика
Гипертиреоз диагностируется по характерным клиническим проявлениям (внешнему виду больного и жалобам), а также результатам исследований. При гипертиреозе информативно определение содержания в крови гормонов ТТГ (содержание снижено), Т 3 и Т 4 (содержание повышено).
При УЗИ щитовидной железы определяют ее размеры и наличие в ней узловых образований, при помощи компьютерной томографии уточняется место образования узлов. Проведение ЭКГ фиксирует наличие отклонений в работе сердечно-сосудистой системы. Радиоизотопная сцинтиграфия щитовидной железы проводится для оценки функциональной активности железы, определения узловых образований. При необходимости проводят биопсию узла щитовидной железы.
Лечение
Современная эндокринология располагает несколькими методами лечения гипертиреоза, которые могут применяться изолированно или в комбинации друг с другом. К такими методам относятся:
Консервативная (медикаментозная) терапия.
Хирургическое удаление части или всей щитовидной железы.
Радиойодная терапия.
Однозначно невозможно определить самый лучший метод, который подходил бы абсолютно для всех пациентов с гипертиреозом. Выбор метода лечения, оптимально подходящего для конкретного больного гипертиреозом, осуществляется эндокринологом с учетом многих факторов: возраст больного, заболевание, вызвавшее гипертиреоз и его тяжесть, аллергия на лекарства, наличие сопутствующих заболеваний, индивидуальные характеристики организма.
Консервативное лечение гипертиреоза
Медикаментозное лечение гипертиреоза направлено на подавление секреторной активности щитовидной железы и снижение выработки
избыточной |
продукции |
тиреоидных |
гормонов. |
Применяются |
|||
тиреостатические |
(антитиреоидные) |
препараты: |
метимазол |
или |
|||
пропилтиоурацил, которые затрудняют накопление йода, необходимого для секреции гормонов в щитовидной железе.
Важную роль в терапии и восстановлении пациентов с гипертиреозом играют немедикаментозные методы: диетотерапия, водолечение. Пациентам с гипертиреозом рекомендовано санаторное лечение с акцентом на сердечнососудистые заболевания (1 раз в полгода).
В питании должно быть включено достаточное содержание белков, жиров и углеводов, витаминов и минеральных солей, ограничению подлежат продукты, возбуждающие ЦНС (кофе, крепкий чай, шоколад, пряности).
Хирургическое лечение гипертиреоза
Прежде чем принять ответственное решение о хирургической операции, с пациентом обсуждаются все альтернативные методы лечения, а также вид и объем возможного хирургического вмешательства. Операция показана для некоторых пациентов с гипертиреозом и заключается в удалении части щитовидной железы. Показаниями к операции является одиночный узел или разрастание отдельного участка (бугра) щитовидной железы с повышенной секрецией. Оставшаяся после операции часть щитовидной железы выполняет нормальную функцию. При удалении большей части органа (субтотальная резекция), возможно развитие гипотиреоза, и пациенту необходимо получать заместительную терапию в течение всей жизни. После удаления значительной доли щитовидной железы значительно уменьшается риск рецидива тиреотоксикоза.
Лечение гипертиреоза радиоактивным йодом
Радиойодотерапия (лечение радиоактивным йодом) заключается в принятии пациентом капсулы или водного раствора радиоактивного йода. Препарат принимается один раз, не имеет вкуса и запаха. Попадая в кровь, радиойод проникает в клетки щитовидной железы с гиперфункцией, накапливается в них и разрушает их в течение нескольких недель. В результате этого размеры щитовидной железы уменьшаются, секреция тиреоидных гормонов и их уровень в крови снижаются. Лечение радиоактивным йодом назначается одновременно с медикаментозным. Полное выздоровление при данном методе лечения не наступает, и у пациентов иногда остается гипертиреоз, но уже менее выраженный: в этом случае может возникнуть необходимость проведения повторного курса.
Чаще, после лечения радиоактивным йодом наблюдается состояние гипотиреоза (через несколько месяцев или лет), которое компенсируется проведением заместительной терапии (пожизненным приемом тиреоидных гормонов).
Другие методы лечения гипотиреоза
При лечении гипертиреоза могут применяться ß-адреноблокаторы, блокирующие действие тиреоидных гормонов на организм. Пациент может почувствовать себя лучше в течение нескольких часов, несмотря на избыточный уровень тиреоидных гормонов в крови. К ß – адреноблокаторам относятся препараты: атенолол, метопролол, надолол, пропранолол, имеющие длительное действие. За исключением гипертиреоза, вызванного тиреоидитом, эти лекарственные препараты не могут использоваться как исключительный метод лечения. ß - адреноблокаторы могут применяться в сочетании с другими методами лечения заболеваний щитовидной железы.
21. Диффузный токсический зоб. Эт. Патоген.Клин.Диагн.Леч
Болезнь Грейвса (БГ, болезнь Базедова, диффузный токсический зоб) — системное аутоиммунное заболевание, развивающееся вследствие выработки антител к рецептору тиреоторопного гормона (ТТГ), кли нически проявляющееся поражением ЩЖ с развитием синдрома тиреотоксикоза в сочетании с экстратиреоиднойпатологией: эндокриннойофтальмопатией, претибиальноймикседемой, акропатией
Этиология Неизвестна; ассоциация с гаплотипами HLA-DR3, HLADQAH050I; протективный гаплотип: HLA-DQAl*070lмультифакторным заболевание, при котором генетические особенности иммунного реагирования реализуются на фоне деиствия̆ факторов окружающейсреды.
Патогенез. Выработка стимулирующих антител к рецептору ТТГ с развитием синдрома тиреотоксикоза и воспалительными изменениями в ретробульбарной клетчатке. Значительно повышается уровень основного обмена, что со временем приводит к дистрофическим изменениям. Особенно
ССС (особенно миокард предсердии)̆ и НС.
Клиника. ССС: Тахикардия, суправентрикулярные аритмии (фибриляция предсердий), сердечная недостаточность, Катаболический синдром: похудение на фоне повышенного аппе тита, горячая кожа, гипергидроз,чувство жара, не мерзнут. МИОПАТИИ: мышечная слабость, тяж осложнение БГтиреотоксический гипокалиемический периодический паралич. . НС: психич лабильность, раздражиельность, плаксивость, стойкие изменения психики и личности, тремор. Глазные симптомы: эндокринная офтальмопатия. ЖКТ: редко, диарея, мб дистрофические изенения в печени (тиреотоксический гепатоз). Синдром остеопении: ломкость волос/ногтей. Половая: у муж часто эректильная дисфункция. + Надпочечниковая нед-ть. увеличение ЩЖ (зоб), претибиальная микседема.
Диагностика. 1. Лабораторно подтвержденный тиреотоксикоз ТТГ снижен, Т4 и/или ТЗ повышен, 2. эндокринная офтальмопатия, 3. диффузное увеличение объема ЩЖ, 4. диффузное усиление захвата технеция по данным сцинтиграфии ЩЖ , 5. повышенный уровень антител к рецептору ТТГ.
Лечение. 1. Консервативная Тиреостатическая терапия препаратами
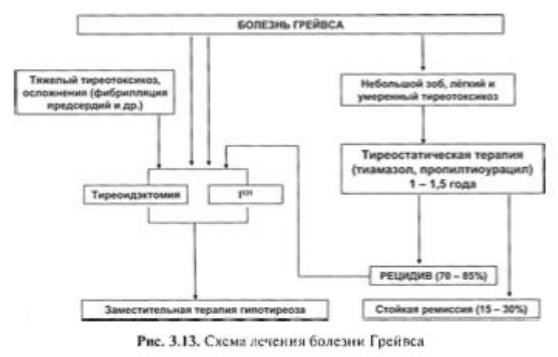
тиомочевины (тиамазол, пропилтиоурацил), которые активно блокируют синтез тиреоидных гормонов; Длительную (12—18месяцев) консервативную терапию имеет смысл планировать далеко не у всех пациентов. В первую очередь, речь идет о пациентах с умеренным увеличением объема ЩЖ (до 35—40 мл); при зобе больших размеров после отмены гиреостатиков неминуемо разовьется тиреотоксикоз. Кроме того, консервативную терапию не следует планировать у пациентов с тяжелыми осложнениями тиреотоксикоза (мерцательная аритмия, выраженный остеопороз идр.). Практически бесперспективно и небезопасно для пациента назначение повторных курсов лечения при развитии рецидива тиреотоксикоза спустя 12—18 месяцев тиреостатическойтерапии. Не эффективно, 70% рецидивов.
2. Радикальные методы: тиреоидэктомия (предельно субтотальная резекция ЩЖ). 3. Радиойодтерапия - эффективно, малоинвазивно, но нельзя беремен и на ГВ, нет рецидивов Т.о. в настоящее время целесообразно назначать радикальные методы
лечения, особенно женщинам в молодом возрасте. Схема "блокируй и замещай" по последним данным не используется!!!
Лечение тиреотоксического криза подразумевает интенсивные мероприятия с назначение больших доз тиреостатиков. Предпочтение отдается ПТУ вдозе 200—300 мг каждые 6 часов, при невозможности само стоятельного приема пациентом — через назогастральныйзонд. Кроме того, назначаются p-адреноблокаторы (пропранолол: 160—480 мг вдень p e r o s или в в/в из расчета 2—5 мг/час), глюкокортикоиды (гидрокорти зон: 50— 100 мг каждые 4 часа или преднизолон (60 мг/сут), дезинтоксикационную терапию (физиологическийраствор, 10 % раствор глюкозы) под контролем гемодинамики. Эффективным методом лечения тирео токсического криза является плазмаферез.
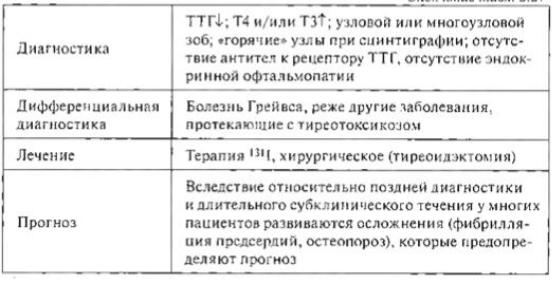
22.Функциональная автономия ЩЖ. Этиол. Патог. Клин. Диагнос. Леч
Функциональная автономия (ФА) ЩЖ —это независимое от регулирующих влиянийгипофиза продукция тиреоидных гормонов при отсутствии внешних стимуляторов.
Этиология
Хроническая гиперстимуляция Щ Ж , происходящая в условиях иодного̆ дефицита легкой и умеренной тяжести. Основной этиологической
подоплекойразвития ФА является микрогетерогенность тироцитов, у которых существенно отличается пролиферативныйпотенциал
Патогенез
Вусловиях легкого и умеренного йодного дефицита, ЩЖ находится в хроническойгиперстимуляции. На 1-м этапе, преимущественно вследствие гипертрофии тироцитов происходит диффузное увеличение ЩЖ (диффузный эутириоидный зоб). В силу того, что тироциты обладают разным пролиферативным потенциалом, в дальнеишем̆ часть из них делится более активно, в результате чего формируются узловые образования (многоузловой эутиреоидныйзоб).
На следующем этапе часть клеток ЩЖ приобретает свойства автономного функционирования, то есть начинает производить тире-оидные гормоны независимо от каких-либо регуляторных влияний. Считается, что причиной этого является развитие активирующих соматических мутаций делящихся клеток, в генетическом аппарате которых запаздывают репаративные процессы. Среди активирующих мутаций к настоящему времени описана мутация гена рецептора ТТГ.
Врезультате этих процессов в ЩЖ сначала формируются «горячие узлы», а когда количество автономных клеток превысит некийпороговыйуровень, развивается субклинический, а затем манифестныйтиреотоксикоз со всейего симптоматикой.
Весь процесс формирования ФА занимает многие годы, ачаще десятилетия, в связи с чем она манифестирует улиц пожилого возраста, чаще старше 60 лет. Патогенетическойособенностью тиреотоксикоза при функциональной автономии в отличие от БГ является длительное субклиническое течение,
предшествующее постепеннои,̆ олигосимптомной |
манифестации явного |
|
тиреотоксикоза. |
|
|
Клиника. Определяется синдромом тиреотоксикоза |
и его осложнениями. |
|
Симптоматика |
сходна с таковой при болезни |
Греивсӑ . Основными |
отличиями является отсутствие эндокриннойофтальмопатии, а также олигоили даже моносимптомное течение заболевания и развитие в пожилом возрасте. Многие пациенты указывают, что в прошлом у них выявлялись узловые образования ЩЖ без нарушения ее функции. На первый план могут выступать такие симптомы, как снижение аппетита,
похудение, мышечная слабость, субфебрилитет. Нередко ФА манифестирует нарушениями ритма сердца (фибрилляция предсердии),̆
которые патогенетически |
связаны |
с длительно, порой на |
|
протяжении десяти |
лет и |
более, |
существующим субклиническим |
тиреотоксикозом. |
|
|
|
Диагностика. субклинический или манифестный тиреотоксикоз, при УЗИ ЩЖ — чаще многоузловои,̆ реже узловойзоб. По результатам сцинтиграфии ЩЖ выделяют три варианта функциональной автономии: унифокальную,
мультифокальную и диссеминированную.
Первый и второй варианты отличаются числом «горячих» узловых образований. В последнем случае, которыйвстречается относительно редко, клинически значимые узлы ЩЖ отсутствуют, Этот вариант ФА бывает трудно дифференцировать с болезнью Греивсӑ .
Лечение. При компенсированной функциональной автономии («горячие» узлы при нормальном уровне ТТГ) у пожилых пациентов наиболее оправдана тактика активного наблюдения. При манифестировавшем тиреотоксикозе тиреостатическая терапия может использоваться только для временной блокады ЩЖ и достижения эутиреоза, поскольку отмена тиреостатиков, вне зависимости от того, как долго они использовались, приведет к возврату тиреотоксикоза. Методом выбора лечения ФА является терапия йодом. В качестве альтернативы может рассматриваться тиреоидэктомия после достижения эутиреоза на фоне приема тиреостатиков (тиамазол, пропилтиоурацил).
23. Йододефицитные заболевания. Нарушения псих и физ развития, связанные с дефицитом йода.
К иододефицитным̆ заболеваниям (ЙДЗ) относятся все патологические состояния, развивающиеся в популяции вследствие иодного̆ дефицита, которые могут быть предотвращены при нормализации потребления иодӑ .
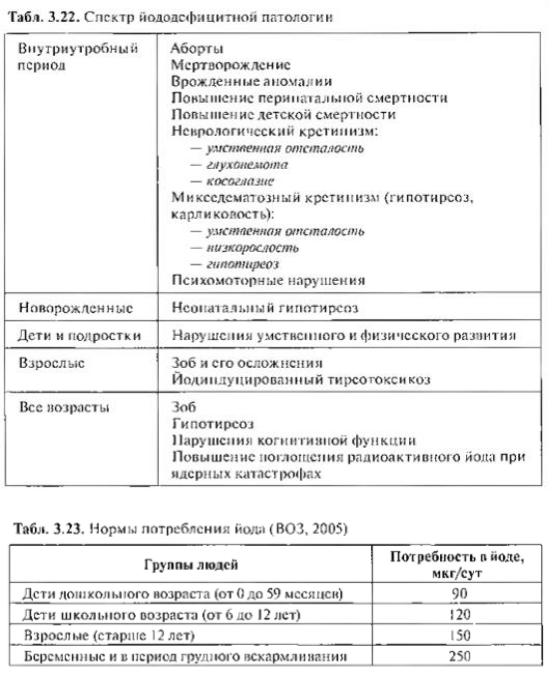
Кйододефицитным̆ заболеваниям ЩЖ относятся:
-Диффузныйэутиреоидныйзоб
-Функциональная автономия ЩЖ
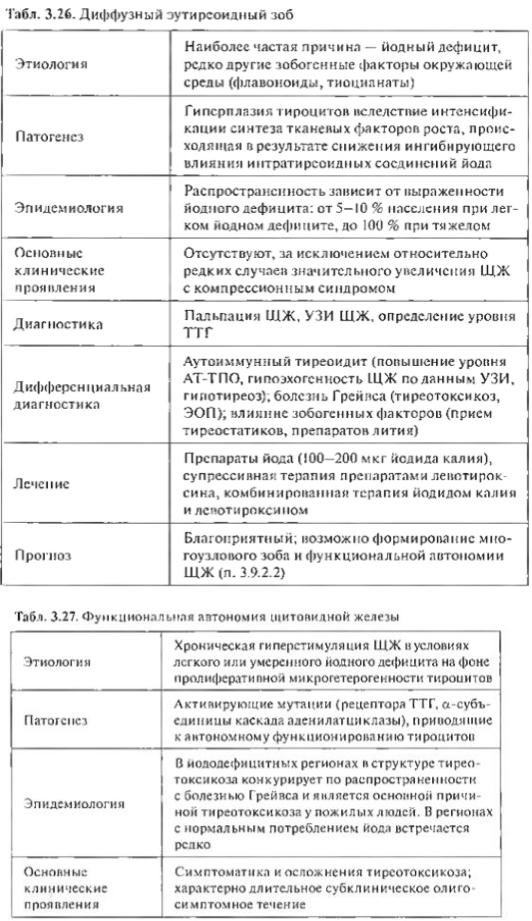
Нарушения психического и физического развития, связанные с дефицитом йода Этиология
Тиреоидные гормоны необходимы для адекватного развития большинства структур центральнойнервнойсистемы, а их дефицит на начальных этапах ее формирования в зависимости от выраженности может приводить к тяжелойпсихическойретардации (неврологическийкретинизм), а также к менее грубым нарушениям (пограничное снижение интеллекта).
Патогенез
ЩЖ у плода начинает производить Т4 только на 15—18 неделе внутриутробного развития, следовательно, развитие нервнойи других систем плода как минимум до этого строка обеспечивается за счет тиреоидных гормонов матери (рис. 3.31). В связи с этим продукция Т4 у женщины буквально с первых недель беременности возрастает примерно на
40 %.
При тяжелом иодном̆ дефиците уровень Т4 у женщины может быть снижен еще до наступления беременности, в случае наступления которойдефицит Т4 окажется столь выражен, что приведет к тяжелейшим нарушениям развития, которое обозначается терми ном неврологический кретинизм. Нарушение психического развития при этом связано не с недостаточностью продукции
собственного Т4 у плода, а с его тяжелым дефицитом в |
первой |
половине бере менности. |
|
В связи с этим в отличие микседематозного кретинизма, которыйсвязан с нарушением развития у плода собственнойЩЖ и развивается постнатально, при неврологическом кретинизме у новорожденных отсутствует
нарушение функции Щ Ж .
Кроме того, при неврологическом кретинизме, в отличие от врож денного гипотиреоза, терапия препаратами тиреоидных гормонов неэффективна, поскольку развивающиеся на начальных этапах эмб риогенеза неврологические нарушения необратимы.
При легком иодном̆ дефиците уровень тиреоидных гормонов у женщины вне беременностиостается в норме, поскольку Щ Ж в обычном состоянии довольно легко его компенсирует. Но во время беременности потребность в тиреоидных гормонах значительно возрастает, вследствие чего продукция Т4 может не достигать необходимого уровня, хотя и не выходит за рамки референсных значенийдля этого гормона. Этот феномен обозначается термином относительная гестационная гипотироксинемия. Ее результатом могут стать пограничные нарушения интеллектуального
развития, не достигающие уровня тяжелойолигофрении.
24. Гипотиреоидная кома, определение...
или микседематозная кома - это наиболее тяжелое осложнение гипотиреоза, но редко встречающееся.
-Развивается у пожилых с длительным гипотиреозом, тяж сопутствующими заб-ми при низком соц статусе или плохом уходе.
-Может быть спровоцирован интеркуррентными заб-ми, инфекциями, переохлаждениями, травмами, препаратами, угнеающими ЦНС
-Летальность 80%, лечение в отделении ОРИТ
Клиника: Явление комы возникает медленно, нарастает, прогрессирует постепенно. Вначале появляется усталость, апатия, заторможенность, после этого наблюдается похолодание конечностей, сухость, отечность стоп, бледность кожных покровов — этими признаками характеризуется гипотиреоидная кома. Статус локалис указывает на замедленное дыхание, проблемы с мочеиспусканием, проявления сердечной недостаточности. Понижается артериальное давление, констатируется отсутствие сухожильных рефлексов. При осмотре больного доктор наблюдает следующие симптомы гипотиреоидной комы: Ухудшается обмен веществ, масса тела увеличивается, кровообращение замедляется, температурные показатели снижаются до 35 градусов. Происходят нарушения в сердечнососудистой системе. Частота сердечных сокращений замедляется, наблюдается нитевидный пульс, снижение АД, водянка сердца. Нарушения функций органов дыхания. Сокращается число вдохов-выдохов, падает уровень кислорода в крови, во время сна возможны остановки дыхания. Нарушения функций нервной системы. Угнетение сухожильных рефлексов, прогрессирующий ступор. Кожные симптомы. Бледность, сухость, восковидные оттенки кожи, суставные гиперкератозы. Ломкость ногтей. Выпадение волос. Падает уровень натрия в крови. Выраженная отечность лица и конечностей. Анемия и все присущие ей симптомы. Гипогликемия. Расстройства пищеварения. Непроходимость кишечника. Увеличение печени гипотермия, гиповентиляция, гипонатриемия, гиперкапния, гиперволемия, брадикардия, АГ, острая задержка мочи, острая кишечн непроход-ть, гипогликемия, сердечная нед-ть, прогрессирующее торможение ЦНС.
Лечение. Алгоритм оказания неотложной помощи Если у человека гипотиреоидная кома, неотложная помощь алгоритм имеет следующий: 1.
Догоспитальный этап: Вызвать врача. Оказать первую врачебную помощь. Укутать тело одеялами для уменьшения теплоотдачи. Для ликвидации гипоксии через носовые катетеры дать увлажненный кислород. Обеспечить доступ к венам, установить катетер на вену. Если установлена гипотиреоидная кома, тактика медицинской сестры должна быть четкой, совместная работа с доктором - быстрой, слаженной: Для диагностики осложнений взять кровь на содержание тироксина, тиреотропина, трийодтиронина, глюкозы, кортизола, хлоридов, натрия, КЩР, газового состава. Для контроля диуреза проводится катетеризация мочевого пузыря. Для профилактики аспирации рвоты вводится в желудок зонд. Для диагностики осложнений — ЭКГ, контроль ЧДД, температуры, гемодинамики. "Реополиглюкин" внутривенно-капельно 500 мл. Дезинтоксикация — глюкоза 40 % в/в струйно — 20-30 мл; затем в/в капельно вводится глюкоза 5 % (500 мл). - 2. В стационаре: Для замещения недостатков гормонов в/в струйно каждые 6
часов вводят 250-500 мкг "Тироксина" (либо через желудочный зонд 100 мкг "Трийодтиронина"), затем через 12 часов дозу снижают до 25-100 мкг. Для купирования недостаточности надпочечников в/в струйно вводят гидрокортизона гемисукцинат (50-100 мг).
Для профилактики энцефалопатии 1 мл витамина В1. Для купирования брадикардии вводят подкожно "Атропин" 0,1 % (0,5-1 мл). Стимулирование дыхательного центра — "Кордиамин" (2-4 мл). Для купирования гипоксии мозга — "Милдронат" (250 мг). Для профилактики инфекций — антибиотики. Для ликвидации гипоксии — искусственная вентиляция легких.
25. Гипопаратиреоз
Гипопаратиреоз — заболевание, связанное с дефицитом паратгормона в результате недостаточности ПЩЖ, проявляющееся синдромом гипокальциемии.
Этиология |
|
|
|
|
|
Послеоперационный |
гипопаратиреоз. Идиопатический |
(аутоиммунный) |
|||
гипопаратиреоз: |
— |
изолированныи;̆ |
— |
при |
аутоиммунном |
полигландулярном синдроме 1-го типа (см. гл. 10). Облучение, инфильтративные заболевания. Аплазия П Щ Ж и тимуса (синдром Di George).
Наиболее частойформойявляется послеоперационныйгипопаратиреоз.
При этомон развивается не столько в результатеудаления желез, сколько за счет нарушения их кровоснабжения связи с воз никновением фиброза клетчатки в зоне оперативного вмешательства. Идиопатический гипопаратиреоз является очень редким заболеванием. Им обычно манифестирует аутоиммунныйполигландулярныйсиндром 1-го типа (см. гл. 10). Краинӗ редким заболеванием, при котором встречается гипопаратиреоз,
является синдром Ди Джорджи (Di George): сочетание агенезии ПЩЖ с аплазией тимуса и врожденными пороками сердца. Другой редкой причиной гипопаратиреоза является разрушение П Щ Ж опухолевой инфильтрациейв области шеи, а также при гемохроматозе и амилоидозе.
Клинические проявления
1. Тетания (тетанический приступ) проявляется парестезиями и фибриллярными подергиваниями, переходящими в болезненные тонические судороги, протекающие при сохраненном сознании, симметрично вовлекающие сгибатели конечностей («рука акушера», «конская стопа»), лицевые мышцы («рыбий рот»), реже разгибатели спины (опистотонус). Характерны, но неспецифичны для гипопаратиреоза симптомы Хвостека (сокращение мимической мускулатуры при постукивании в месте выхода лицевого нерва), Труссо (появление «руки акушера» через 2—3 мин после сдавления плеча манжеткой тонометра) и Вейса (поколачивание у наружного края глазницы вызывает сокращение круговой мышцы глаза). Спазмы гладкой мускулатуры проявляются ларинго- и бронхоспазмом, дисфагией, рвотой, поносом, запором. Из вегетативных проявлений для гипопаратиреоза характерны жар, озноб, сердцебиения, боли в области сердца. Эквивалентами тетанических судорог могут быть эпилептические припадки.2. Трофические нарушения и внекостная кальцификация: нарушение роста волос и ногтей, дефекты зубной эмали, сухость кожи, катаракта, кальцификация базальных ганглиев, которая клинически может проявиться экстрапирамидной симптоматикой с хореоатетозом или паркинсонизмом.
Патогенез |
|
|
|
Дефицит паратгормона |
приводит |
к повышению |
уровня |
фосфора в крови, |
а также к |
гипокальциемии, |
обусловленной |
снижением всасывания кальция вкишечнике, уменьшением его мобилизации из костей и недостаточной реабсорбцией в почечных канальцах, что отчасти связано с уменьшением синтеза в почках 1,25(ОН)2Оз, про дукция которого контролируется паратгормоном. Гипокальциемия и гиперфосфатемия приводят к универсальному нарушениюпроницаемости клеточных мембран и к повышению нервно-мышечнойвозбудимости и судорожнойготовности, вегетативной лабильности, а также к отложению солей кальция во внутренних органах и стенках крупных сосудов.
Диагностика
Гипокальциемия, гиперфосфатемия, сниженный уровень ПТГ в крови (для пациентов после оперативных вмешательств на щитовидной железе в анамнезе — необязательное исследование).
Лечение

1.Гипокальциемический криз. 20 мл 10 % раствора глюконата кальция, разведенного в 100—200 мл физиологического раствора или 5% раствора глюкозы внутривенно, в течение 10 минут. При повторении (сохранении) симптоматики введение глюконата кальция повторяется.
2.Поддерживающая терапия включает назначение 1,0-1,5 г элементарного кальция вдень (в виде кальция карбоната). У большинства пациентов монотерапия препаратами кальция не позволяет компенсировать ГПТ (поддерживать нормальный уровень кальция в крови). В связи с этим назначаются препараты витамина D: дигидротахистерол (0,5-2 мг вдень; 12-40 капель), холекальциферол
(25000-75000 ME); la-OH-D3 ( 2 - 4 мкг в день), l,25(OH)2D3 (1-3 мкг в день)
26. Первичный Гиперпаратиреоз (аденома паращитовидной железы) клиника Диагностика Лечение
Первичныйгиперпаратиреоз (ПГП)— заболевание ПЩЖ, проявляющееся избыточной продукцией паратгормона с развитием синдрома гиперкальциемии (табл. 8.2).
ЭТИОЛОГИЯ
В 85 % случаев причиной ПГП является солитарная аденома ПЩЖ (паратирома), значительно реже — аденомы множественные (5 %), еще реже (< 5%)— рак ПЩЖ. Гиперплазия всех ПЩЖ встречается примерно у 15 % больных. ПГП встречается при обоих вариантах синдрома множественных эндокринных неоплазий(см. гл. 10).
Патогенез
Гиперпродукция паратгормона приводит к избыточному выведению через почки фосфата. Снижение плазменного уровня последнего стимулирует
синтез |
1,25-(ОН)2- О з, который способствует |
всасыванию |
||
избытка С а 2+ |
в кишечнике. |
В далеко зашедших |
стадиях |
|
процесса гиперкальциемия усиливается за счет активации избытком паратгормона остеокластов. Избыток паратгормона приводит к ускорению обмена в костной ткани, ускорению костной резорбции и костеобразования, но образование новойкости отстает от ее рассасывания,
что приводит |
к генерализованному остеопорозу |
и остеодистрофии, |
||
вымыванию |
кальция |
из |
костных депо и гиперкальциемии, а |
|
также гиперкальциурии, способствующейповреждению эпителия почечных канальцев и образованию камней в почках. Нефрокальциноз,
в свою очередь, ведет к снижению функции почек. В возникновении язвенного поражения желудка и двенадцатиперстной кишки важную роль играют гиперкальциемия с артериолосклерозом и кальцификациейсосудов. Гиперкальциемия наряду с повышением артериально го давления создает предпосылки для формирования гипертрофии левого желудочка, функцию которого также ухудшают типичные для гиперпаратиреоза клапанные, коронарные и миокардиальные кальцинаты.
Клиниеские проявления У большинства пациентов ПГП протекает бессимптомно идиагноз устанавливается при обследовании по поводу гиперкальциемии.
1.Почечные симптомы включают полиурию, полидипсию, нефролитиаз (25 %), часто осложняющиися̆ пиелонефритом; редко — нефрокальциноз с развитием почечнойнедостаточности.
2.Желудочно-кишечная симптоматика: анорексия, тошнота, обстипация,
метеоризм, похудение. В 10 % случаев развиваются язвы желудка и/или двенадцатиперстнойкишки, в 10 % — панкреатит, реже пан-креакалькулез. В
2раза чаще, чем в популяции, встречается желчнокаменная болезнь.
3.Сердечно-сосудистая симптоматика: артери альная гипертензия и ее осложнения.
4.Костные изменения: остеопороз, хондрокальциноз; при тяжелом ПГП: субпериостальная резорбция, акроостеолиз концевых фаланг кистейи стоп (рис. 8.4), деформация скелета, пато логические переломы костей(рис. 8.5), кисты, гигантоклеточные опухоли и эпулиды (кистозные образования).
5.Центральная нервная система: депрессия, сонливость, спутанность сознания, возбуждение, кожныйзуд.
6. Гиперкальциемическийкриз — весьма редкое тяжелое |
осложнение |
||
П Г П . |
Характерны |
сонливость, ступор, кома, психоз, вслед |
|
за нарастающейанорексиеи,̆ рвотои,̆ болью вэпигастрии; быстро развивается резкая слабость, обезвоживание, ану
рия, коматозное состояние; тяже лое осложнение —миопатия с вов лечением проксимальных отделов туловища, межреберных мышц идиафрагмы; типична лихорадка до 38—39 °С. Криз развивается при уровне кальция в плазме более 4 ммоль/л и провоцируется дли тельным постельным режимом, тиазидными диуретиками, препа ратами кальция и
витамина D.
Диагностика
♦Гиперкальциемия, как правило,
выявляется улиц без какой- либо симптоматики при рутинном биохимическом анализе крови. Кроме того, характерны гипофосфатемия,
гиперкальциурия и гиперфосфатурия, повышение уровня щелочной фосфатазы в плазме и экскреции с мочойгидроксипролина и цАМФ.
♦Повышенный уровень паратгормона. Исследование показано при двукратно зарегистрированнойгиперкальциемии.
♦Топическая диагностика паратиром: УЗИ, сцинтиграфия стехнетрилом, КТ, МРТ (область шеи и средостения).
♦Диагностика осложненийПГП: остеопороз, нефрокальциноз идр.
Лечение
Подходы к лечению определяютсявыраженностью П Г П , возрастом и физическим состоянием пациента, поскольку единственным ради кальным вариантом лечения является хирургическое вмешательство.
1. Хирургическое лечение: при солитарнойпаратироме — ее удаление, при гиперплазии нескольких П Ж Щ проводится парциальная, либо
тотальная паратиреоидэктомия с последующейтерапиейгипопаратиреоза.
2.Динамическое наблюдение проводится при выявлении легкой
выраженности |
П Г П |
у л и ц |
пожилого |
возраста, |
т.е. |
В той |
возрастной группе, где ПГП |
чаще всего встречается. Оно допустимо |
|||||
вситуациях отсутствия |
абсолютных показаний к оперативному |
лечению |
||||
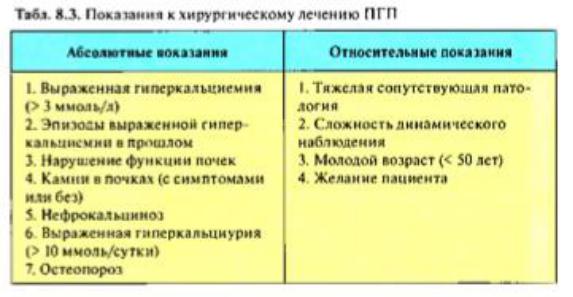
(табл. 8.3). Динамическое наблюдение подразумевает определение уровня
кальция, |
функции почек, артериального |
давления |
каждые |
6 |
|
—1 2 |
месяцев, проведение костнойденситометрии и УЗИ почек каждые |
||||
2—3 года.3. Медикаментозное лечение не разработано. Препаратами выбора для лечения остеопороза являются бисфосфонаты, которые оказывают транзиторное гипокальциемическое деиствиӗ . Их же в сочетании с регидратационной терапией используют при лечении гиперкальци емического криза.
Прогноз
После хирургического лечения того или иного объема нормокальцп емия
сохраняется менее чем у 10 % пациентов, половине из которых в дальнеишем̆ требуется повторная операция. Рецидивы ПГП разви ваются у V20 пациентов, прооперированных по поводу солитарнойпаратиромы иу */б—по поводу гиперплазии ПЩЖ.
Наиболее ярким примером клинической картины первичного гиперпаратиреоза служит гиперкальциемический криз, при котором вышеперечисленные признаки гиперкальциемии принимают жизнеугрожающий характер. Это осложнение обычно развивается при подъёме сывороточной концентрации кальция выше 14 мг/дл.
Проявляется тошнотой, неукротимой рвотой, паралитической кишечной непроходимостью, болями в животе, анурией, обезвоживанием организма. Кожа становится сухой, её тургор снижается, отмечается резкая мышечная слабость, пациенты не в состоянии обслуживать себя. Постоянная боль в
костях |
становится |
изнуряющей, |
в |
первые |
часы |
криза |
|
появляется артериальная |
гипертензия. Сухожильные рефлексы снижаются. |
||||||
Иногда |
возникают |
внутрисосудистые тромбозы, синдром |
|||||
диссеминированного внутрисосудистого свёртывания. |
|
|
|||||
Нейропсихические расстройства при гиперкальциемическом кризе
проявляются |
спутанностью |
сознания, депрессией, психозами или |
||||||
психомоторным |
возбуждением. |
При |
достижении |
сывороточной |
||||
концентрации |
кальция |
15—18 |
мг/дл |
возможно |
угнетение |
|||
деятельности ЦНС с |
торможением |
|
функции |
дыхательного |
и |
|||
сосудодвигательного центров и развитием необратимого шока. Больные в состоянии гиперкальциемического криза нуждаются в экстренной госпитализации и интенсивной терапии.
Диагностика гиперпаратиреоза (аденомы паращитовидной железы) Диагноз ставится на основании данных лабораторных исследований крови, где
обнаруживают повышение уровня кальция, снижение фосфатов и повышение активности щелочной фосфатазы. В моче повышается содержание кальция и фосфора. При исследовании уровня паратгормона в крови определяется его повышение. Проводится ультразвуковое исследование паращитовидных желез, термография и сцинтиграфия желёз, а также артериография, КТ и МРТ. Для точного подтверждения диагноза проводят тонкоигольную биопсию с цитологическим исследованием. Для оценки степени разрушения костной ткани проводят рентгенологическое исследованиекостей и денситометрию (оценка плотности) костей голени, стоп, тел позвонков. Лечение гиперпаратиреоза (аденомы паращитовидной железы)
Лечение при аденоме паращитовидных желез только хирургическое. На дооперационном этапе консервативное лечение направлено на снижение уровня кальция в крови. При поражении более, чем одной из четырёх желёз, показано их полное удаление с последующим мониторингом уровня кальция крови
27. Вторичный и третичный гиперпаратиреоз
.Вторичныйгиперпарат иреоз (ВГП) представляет собойкомпенсаторную гиперфункцию и гиперплазию П Щ Ж , развивающуюся при длительной
гипокальциемии и гиперфосфатемии различного генеза (табл. 8.4). При третичном гиперпаратиреозе происходит развитие автономной гиперпродукции паратгормона гиперплазированными ПЩЖ или формирование аденомы П Щ Ж при длительно существующем вторич ном гиперпаратиреозе.
Этиология
Почечная патология: хроническая почечная недостаточность, тубулопатии, почечный рахит. Кишечная патология: синдром мальабсорбции. Костная патология: остеомаляция (сенильная, пуэрперальная, идиопатическая), болезнь Педжета.
Недостаточность витамина D: заболевания почек, заболевания печени, наследственные ферментопатии. Злокачественные заболевания: миеломная болезнь.
Основными причинами ВГП являются почечная недостаточность и болезни системы пищеварения. В соответствии с этим выделяют почечный и
интестинальныйВГП. В связи с широким использованием |
гемодиализа |
||||||
и увеличением |
продолжительности |
жизни |
больных с |
Х П Н |
|||
ВГПстал встречаться |
значительно чаще. |
|
|
|
|||
Патогенез |
|
|
|
|
|
|
|
Развитие ВГП при |
Х П Н |
связано |
с |
нарушением |
|
||
образования |
в |
почках |
активного |
витамина D3 |
[l,25-(OH)2-D3]. |
||
Прогрессирующее увеличение плазменного уровня неорганического фосфора начинается уже при снижении скорости клубочковой фильтрации до 60
