
Fizikaliq ham kolloidliq ximiya paninen esaplar shigariw
.pdf
|
|
= |
4 |
|
= |
|
|
|
4 |
|
|
= 113,04 ∙ 10−24 3 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||
. á |
|
|
3 3 |
|
|
3 ∙ [3,14 ∙ (3 ∙ 10−8)3] |
|
||||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
= 3 = (10−6)3 = 10−18 3 |
|||||||
|
|
|
|
á |
|
|
|
|
|
|
|||||||
Bóleksheler sanın tabamız: |
|
|
|
|
|
|
|
|
|
||||||||
|
= |
|
. |
= |
|
|
0,5 |
|
= 4,4 ∙ 1021 (sfera tárizli) |
||||||||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
−24 |
||||||||||
|
|
|
|
|
|
|
|
113,04∙10 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
0,5 |
|
|
|
|
|
|
|
= |
. |
|
= |
= 0,5 ∙ 1018 |
(kub tárizli) |
||||||||||
|
|
|
−18 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Sfera tárizli bóleksheler tutqan sistemanıń salıstırma júzesin tómendegi
formula járdeminde esaplaymız: |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
= |
3 |
= |
|
3 |
|
|
|
|
= 108 −1 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
3 ∙ 10−8 |
|
|
|||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
= |
6 |
= |
|
|
6 |
= 6 ∙ 106 −1 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
( ) |
|
|
|
10−6 |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
Dispers |
fazanıń |
nıń |
hám |
bóleksheniń |
|
|
kólemininiń mánisin bile otırıp, |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
bóleksheniń ulıwma maydanın tabamız: |
|
|
|
|
|
|
|
||||||||
|
= |
|
|
= 108 ∙ 0,5 = 5 ∙ 107 |
2 (sfera tárizli); |
||||||||||
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
|
|
= 6 ∙ 106 ∙ 0,5 = 3 ∙ 106 2 |
(kub tárizli) |
||||||||||
|
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
Basqasha jol menen de tabıw múmkin:
Ssumm= nSból = n4 r2 = 4,4 1021 4 3,14 (6 10 8)2 = 4,97 107 5 107sm2.
Mısal 5. 50 mg/l pelargon kislotı 8 17 tutqan 100C temperaturaǵa iye suwlı eritpeniń suyıqlıqtıń sırt kerimligin (kmol/m2) anıqlań. Eritpeniń hám suwdıń sırt kerimligi sáykes túrde 57 ∙ 10−3 / hám 74,22 ∙ 10−3 / ge teń.
Sheshimi: Gibbs teńlemesinen paydalanamız:
∆= − ∆ ∙
Eritpeniń koncentraciyasın kmol/m3 de ańlatamız:
= 0,05/158 = 3,164 ∙ 10−4 / = 3,164 ∙ 10−4 / 3, (158 – pelargon kislotnıń molyar massası). Bunnan:
= − 57∙10−3 ∙ 3,164∙10−4 = 7,32 ∙ 10−9 / 3.
3,164∙10−4 8,314∙103∙283
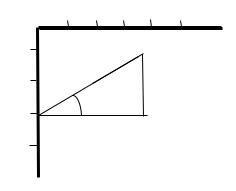
Mısal 6. Eger bir molekulanıń júze qabatdaǵı iyeleytuǵın maydanı 30 ∙ 10−20 2 ǵa teń bolsa, «eritpe - hawa» júzesindegi may kislotanıń molekulasınıń uzınlıǵın anıqlań. May kislotasınıń tıǵızlıǵı = 978 / 3.
Sheshimi: Molekulanıń uzınlıǵı l tómendegi formula járdeminde esaplanadı:
22
|
|
|
|
|
|
= |
∞ ∙ |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
∙ |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
∞ |
|
|
|
|
|
|
|
|
|
||
|
( – Avagadro |
sanı, 6,02 ∙ 1026 |
molekul/kmol) |
ekenligin |
esapqa alıp, |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
suyıqlıqtıń sırt kerimligin tabamız: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
= |
1 |
= |
|
1 |
|
|
|
|
|
|
= 0,055 ∙ 10−7 |
|
. |
|
|||||
∙ |
30 ∙ 10−20 ∙ 6,02 ∙ 1026 |
|
|
|||||||||||||||||
|
∞ |
|
|
|
2 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Onda, may kislotası molekulasınıń uzınlıǵı (M=88): |
|
|
|
|
|
|
|||||||||||||
|
= |
|
0,055 ∙ 10−7 ∙ 88 |
= 4,95 ∙ 10−10 ≈ 5 ∙ 10−10 = 5 Å |
|
|
|
|||||||||||||
|
|
|
978 |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Mısal 7. Aktivlengen |
kómirdegi etanoldıń |
|
puwınıń adsorbciyasın |
úyrengende |
||||||||||||||||
tómendegi maǵlıwmatlar alındı: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
∙ 10−2, Pa |
|
5,33 |
|
9,87 |
|
17,33 |
23,06 |
|
|
45,53 |
|
||||||||
|
∙ 103, m3/kg |
|
14,9 |
|
19,1 |
|
24,2 |
27,3 |
|
|
36,8 |
|
||||||||
(r puw basımınıń teppe - teńligi, A adsorbciyanıń muǵdarı). Freyndlix hám Lengmyur teńlemesindegi konstantanıń grafikalıq kórinisin anıqlań. = 3000 daǵı adsorbciyanıń muǵdarın anıqlań. Eki teńlemeni paydalanıp, 5 kg kómirge qansha etanol adsorbciyalanatuǵının esaplań.
Sheshimi: Freyndlix teńlemesiniń konstantasın tabıw ushın lg = (lg ) baylanıs grafigin dúzemiz. Bunıń ushın dáslepki berilgen maǵlıwmatlardı logarifmleymiz:
|
|
lg A |
|
–1,83 |
–1,72 |
|
–1,62 |
–1,56 |
–1,43 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
lg r |
|
2,72 |
2,99 |
|
3,24 |
3,36 |
3,66 |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
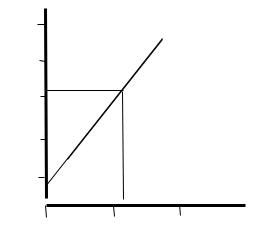
hám bul mánisler boyınsha grafik dúzemiz: |
||||||
0 |
1 2 |
3 4 5 lg p |
Ol |
ordinata |
kósherin |
lg − −3,02 |
|||||
|
|
|
|
|
tochkasında kesedi, bunnan = 9,55 ∙ 10−4 |
||||||
1 |
|
|
b |
boladı. Grafiktegi múyeshlik koefficientinen |
|||||||
|
|
|
|
||||||||
2 |
|
|
|
ekinshi koefficien-tin tabamız: |
1/ = |
||||||
3 |
|
|
c |
= / = 0,4/0,94 = 0,43. |
= ∙ |
||||||
|
d |
|
|
1⁄ |
|
|
|
|
|
||
|
|
|
|
kórinisindegi Freyndlix teńlemesinen |
|||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
adsorbciyanıń muǵdarın esaplaymız: |
|
|
||||
lg A |
|
|
|
|
|
= / = 9,55 ∙ 10−4 ∙ 30000,43 |
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
= 2,99 ∙ 10−2 3/ . |
|||
23
Bunda 5 kg kómirge:
= ∙ = 5 ∙ 2,99 ∙ 10−2 = 0,149 3 etanol adsorbciyalanadı.
Lengmyur |
teńlemesiniń |
konstantasın |
tabıw |
ushın |
1/ = |
(1/ )baylanısındaǵı grafik dúzemiz. Bunıń ushın dáslepki maǵlıwmatlardıń keri mánislerin tabıwımız kerek:
|
1/r |
|
|
0,00188 |
|
|
|
0,00101 |
0,00058 |
|
0,00043 |
|
|
0,00022 |
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
1/A |
|
|
|
|
67,11 |
|
|
|
52,36 |
|
41,32 |
|
|
36,63 |
|
|
27,17 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Bul maǵlıwmatlardan paydalanıp grafik dúzemiz hám ordinataǵa kesilisken |
||||||||||||||||||||||||||||
tochkasın anıqlaymız. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Grafik |
|
boyınsha |
|
|
|
|
tómendegi |
1/А |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
70 |
|
|
|
|
|
|
|
|
|||||||||||||||
kesindilerdiń mánisin anıqlaymız: |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
= |
1 |
= 26; |
|
= |
2 |
|
|
|
|
|
60 |
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
В |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
∞ |
|
|
|
|
|
|
|
|
|
∞ |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
50 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= 52 |
; = |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
3 |
|
|
40 |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
= 0,0011 −1. |
|
|
|
30 |
|
|
|
|
|
|
|
|
||||||||||
Bunnan |
A |
|
hám |
b |
konstantaların |
|
|
|
|
|
|
|
|
|||||||||||||||
|
D |
|
К |
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
1 |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
tabamız: = |
|
|
= 0,0385 |
|
; |
|
|
|
0 |
|
1 |
2 1/р 10 |
3 |
|
||||||||||||||
26 |
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
∞ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
= |
|
1 |
= 909 . |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
0,0011 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Konstantalardıń mánislerin bile otırıp, Lengmyur teńlemesi boyınsha |
||||||||||||||||||||||||||||
adsorbciyanıń muǵdarının esaplaymız: |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
= |
|
|
|
= 0,0385 |
|
3000 |
|
= 29,5 ∙ 10−3 |
3 |
. |
|
|
|||||||||||||
|
|
|
|
|
|
909 + 3000 |
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
∞ + |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Onda, 5 kg kómirge 5 ∙ 29,5 ∙ 10−3 = 0,148 3 etanol adsorbciyalanadı.
Mısal 8.
BaCl2 hám Na2SO4 lardıń suwlı eritpeleriniń óz – ara tásirlesiwi nátiyjesinde payda bolǵan bariy sulfatınıń kolloid eritpesiniń micellasınıń formulasın jazıń.
Sheshimi:
Zol alıw tiykarında tómendegi reakciya teńlemesi jatadı:
2 + 2 4 = 2 + 4 ↓
Zol alıwdıń shárti retinde, zoldiń stabilizatorı wazıypasın atqarıwshı dáslepki zatlardıń, 2 yamasa 2 4 artıqsha muǵdarı xızmet etedi. Eger stabilizator retinde 2 xızmet etse, onda micellanıń formulası:
24

{[ 4] ∙ 2+ ∙ 2( − ) −}2+ ∙ 2 ∙ − boladı.
1 |
2 |
3 |
4 |
Micellanıń quram bólegi: 1 - agregat
2- potencial anıqlawshı ion
3- adsorbcion qabatdaǵı qarama-qarsı ionlar
4– diffuziya qabatındaǵı qarama – qarsı ionlar
(1,2) - yadro; (1,2,3,) - granula, zaryadlanǵan bólekshe;
(1,2,3,4,) - elektroneytral micella
Mısal 9. Natriy sulfat eritpesiniń gúmis iodidiniń gidrozolina salıstırǵandaǵı koagulyaciyalawshı qásiyetin hám koagulyaciya bosaǵasın (porog) esaplań. 250 ml zol ushın 50 ml kólemdegi natriy sulfatı (koncentraciyası 0,15 mol/l) sarplanadı.
Sheshimi: Koagulyaciyanıń bosaǵası (porog) retinde liozoldı koagulyaciyalawshı koagulyator elektrolittiń koncentraciyası xızmet etedi.
Zoldiń koagulyaciyası – bul dispers faza bóleksheleriniń agregatlanıp shókpe (koagel) payda etiw processi bolıp esaplanadı. Koagulyaciya bosaǵasın (porog) γ menen belgileydi, ólshemin mmol/l ili mol/l de ólsheydi.
= . . ∙ . .+ . .
Bul jerde: |
|
|
|
|
|
|
|
|
|
|||
|
|
– koagulyator elektrolittiń koncentraciyası |
|
|
||||||||
. . |
|
|
|
|
|
|
|
|
|
|
|
|
|
. |
– koagulyator elektrolittiń kólemi |
|
|
|
|
||||||
.. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- zoldiń kólemi |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Elektrolittiń koagulyaciyalawshı qásiyeti: |
|
|
|
|
||||||||
|
|
|
|
|
= |
1 |
/ |
|
|
|||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
0,15 ∙ 0,05 |
|
||||||||
|
|
= |
|
|
= 0,025 |
|
. |
|||||
|
|
0,25 + 0,05 |
|
|||||||||
|
|
= |
|
1 |
|
|
= 40 / |
|||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
0,025 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
||||
Mısal 10. Ortalıqtıń jabısqaqlıǵı 10−3 Pa s, temperatura 293 K, bóleksheniń radiusı 50 nm bolsa, 10 sekund waqıtda bóleksheniń jılısıw birliginiń kvadratın X hám diffuziya koefficientin D esaplań.
Sheshimi: Eynshteyn–Smoluxovskiy nızamı boyınsha
∆ 2 = 2 ,
25

bul jerde – diffuziya koefficienti, bunı Eynshteyn teńlemesi boyınsha esaplaw múmkin:
|
|
|
|
|
|
|
|
||
|
|
|
= |
|
= |
|
|
|
|
|
|
|
6 r |
6 r |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
– universal gaz konstantası, -absolyut temperatura, –Bolcman turaqlısı, = |
||||||||
|
= 1,38 ∙ 10−23 / , |
-Avagadro sanı, |
η - dispersion ortalıqtıń jabısqaqlıq |
||||||
|
|||||||||
|
|
|
|
|
|
|
|
|
|
koeffcienti, r -bólekshe radiusı, |
|
|
|
|
|||||
Mánislerin qoyamız: |
|
|
|
|
|
|
|
|
|
|
= |
|
1,38 ∙ 10−23 ∙ 293 |
= 4,29 ∙ 10−12 |
2 |
. |
|||
|
6 ∙ 3,14 ∙ 10−3 ∙ 50 ∙ 10−9 |
|
|||||||
|
|
|
|
|
|||||
Bunnan:
∆ = √2 = √2 ∙ 4,29 ∙ 10−12 ∙ 10 = 9,26 ∙ 10−6 .
Mısal 11. Kolloid eritpe 0,08% kolloid gúmis tutadı. 370C temperaturada bul kolloid eritpeniń osmoslıq basımı 0,08 Pa ǵa teń. Zoldiń sfera túrindegi kolloid bóleksheleriniń ortasha diametrin esaplań. Gúmistiń tıǵızlıǵı 10,5 ∙ 103 / 3..
Sheshimi: Zoldiń osmoslıq basımı tómendegi teńleme tiykarında esaplanadı:
|
= |
ʋ ∙ ∙ |
= ʋ ∙ ∙ |
|
|||
|
|
|
|
|
|
|
|
bul jerde ʋ – kólem birligindegi bóleksheler sanı;
– Bolcman konstantası, 1,38 ∙ 10−23 / .
ʋ- dispers faza massasınıń bir bóleksheniń massasına qatnasına teń bolǵanlıǵı sebepli: ʋ = . / ó boladı, al bóleksheniń massası onıń
radiusı hám tıǵızlıǵı |
arqalı |
tabıladı: ó = 4 3/3 . |
Osmoslıq basımnıń |
|||||
mánisin bile otırıp, bóleksheniń radiusınıń ortasha mánisin esaplaw múmkin: |
||||||||
|
|
|
|
|
|
|
|
|
|
3 ∙ |
|
∙ ∙ |
|
3 ∙ 0,8 ∙ 1,38 ∙ 10−23 ∙ 310 |
|
||
= √ |
. ó |
|
|
= √ |
|
|
= 0,99 ∙ 10−8 |
|
4 ∙ |
∙ ∙ |
4 ∙ 0,08 ∙ 10,5 ∙ 103 ∙ 3,14 |
||||||
|
|
|
|
|
|
|
|
|
Bunnan = 2 ∙ 0,99 ∙ 10−8 = 1,98 |
∙ 10−8 . |
|
||||||
Mısal 12. Eger trubanıń uzınlıǵı 0,6 m, basımnıń parqı 100 Pa, aǵıw tezligi 2,04 10-10 m3/s bolǵan maydıń jabısqaqlıǵın anıqlań.
Sheshimi: Puazeyl teńlemesinen paydalamız:
= = ∙ 4∆
8∙η∙ℓ
26

Q – suyıqlıqtıń aǵımınıń tezlik kólemi, ol basım astında R waqıt birligi ishinde kapillyar boylap uzınlıǵı ℓ ǵa hám radiusı r ǵa teń bolǵan suyıqlıqtıń kólemniń V qatnasına teń; η – suyıqlıqtıń dinamikalıq jabısqaqlıǵı.
Teńlemeni suyıqlıqtıń jabısqaqlıǵın anıqlaw ushın túrlendiremiz hám berilgen maǵlıwmatlardıń mánislerin Sİ sistemasında qoyamız:
η = |
∙ 4∆ |
= |
3,14 ∙ (0,0005)4 ∙ 100 |
= 20,04 ∙ 10−3 ∙ |
||
8 ∙ ∙ ℓ |
8 ∙ 2,04 ∙ 10−10 ∙ 0,6 |
|
||||
|
|
|
||||
Mısal 13. Dispers fazasınıń koncentraciyası tómendegishe bolǵan AgCl gidrozoliniń jabısqaqlıǵın esaplań: a) massası boyınsha 10% hám b) kólemi boyınsha 10%. Zoldiń bóleksheleri sfera tárizi, dispers fazanıń hám dispers ortalıqtıń tıǵızlıqları sáykes túrde 5,56 hám 1 g/sm3 ge teń; dispers ortalıqtıń jabısqaqlıǵı η0 = 10−3 ∙.
Sheshimi: Eynshteyn teńlemesin paydalanıp, jabısqaqlıqtı anıqlaymız:
η = η0(1 + 2,5 ),
bul jerde – dispers fazanıń kólemlik muǵdarı; = . / .
a) dı esaplaw ushın zoldıń massasın 100 gr dep alamız, onda dispers fazanıń massası 10 g, al dispers ortalıqtıń massası 90 g boladı. Bunnan:
10/5,561 = 10/5,56 + 90/1 = 0,0196;
hám η1 = 10−3(1 + 2,5 ∙ 0,0196) = 1,05 ∙ 10−3 ∙ ,
b) Bul jaǵdayda osmoslıq basımdı esaplaw ushın diń mánisin túrlendiriw jetkilikli: 2 = 10% = 0,1 hám onda
η2 = 10−3(1 + 2,5 ∙ 0,1) = 1,25 ∙ 10−3 ∙ ,
Mısal 14. Cilindrdegi bentonit suspenziyasınıń 0,1 m biyiklikten shógiw waqtın anıqlań. Ortalıqtıń jabısqaqlıǵı 2 ∙ 10−3 ∙ , bólekshe radiusi 14 ∙ 10−6 , bentonittiń tıǵızlıǵı 2,1 ∙ 103 / 3, suyıqlıqtıń tıǵızlıǵı 1,1 ∙ 103 / .
Sheshimi: Shógiw waqtın anıqlaw ushın tómendegi formuladan paydalanamız:
=
bul jerde – suspenziyanıń stolbasınıń biyikligi; – bóleksheniń shógiw waqtı, – shógiw tezligi, ol Stoks teńlemesi járdeminde esaplanadı:
= 2 ∙ 2( − 0) ∙ 9η
bul jerde, - bólekshe radiusi; , 0 - zattıń hám ortalıqtıń tıǵızlıǵı; - erkin túsiw tezligi; η - ortalıqtıń jabısqaqlıǵı.
27

= 2 ∙ (14 ∙ 10−6)2 ∙ (2,1 ∙ 103 − 1,1 ∙ 103) ∙ 9,81 = 2,1364 ∙ 10−3 / . 9 ∙ 2 ∙ 10−3
Onda bóleksheniń shógiw waqtı:
= |
|
= |
0,1 |
|
= 468,1 = 7,8 boladı. |
|
2,1364∙10 |
−3 |
|||
|
|
|
|
Mısal 15. Sanarinniń qızıl ( = 700 nm) hám kók ( = 436 nm) reńlerdegi jaqtılıqtı jayılıw intensivligin salıstırıń. Nefelometriyada qaysı reńdegi jaqtılıqtı paydalanıw qolaylı ekenligi boyınsha juwmaq shıǵarıń.
|
|
2 |
− 2 |
2 |
∙ 2 |
|
||
= 24 ∙ 3 |
∙ ( |
1 |
|
0 |
) ∙ |
|
∙ |
|
2 |
+ 2 2 |
4 |
||||||
|
|
|
0 |
|||||
|
|
1 |
|
0 |
|
|
|
|
Sheshimi: Reley teńlemesine muwapıq jayılǵan jaqtılıqtıń intensivligi túsip atırǵan jaqtılıqtıń tolqın uzınlıǵınıń 4 – dárejesine keri proporcianal. Onda:
|
|
4 |
7004 |
|
2,4 |
∙ 1011 |
|
||
. ó |
= |
|
= |
|
|
= |
|
|
≈ 6,6 . |
|
4 |
436 |
4 |
3,6 |
10 |
||||
|
|
|
|
∙ 10 |
|
||||
. |
|
ó |
|
|
|
|
|
|
|
Solay etip, nefelometriyada kóq reńdegi jaqtılıqtı paydalanǵan maqul boladı.
Mısal 16. Nefelometr járdeminde standart hám izertlenip atırǵan gidrozollardıń tınıqlıǵı (mutnost) salıstırıldı. Jaqtılandırılǵan bóleginiń biyikligi - standart zolda 5 ∙ 10−3 bolǵanda, al izertlenip atırǵan gidrozolda 19 ∙ 10−3 bolǵanda tınıqlıǵı birdey boldı. Standart zoldiń bóleksheleriniń ortasha radiusı 120 ∙ 10−9 . Ekinshi zoldiń bóleksheleriniń radiusın anıqlań.
Sheshimi: Nefelometr járdeminde izertlenip atırǵan bóleksheniń radiusın tabıw tómendegi formula járdeminde esaplanadı:
= √
bul jerde, - standart zoldiń bóleksheleriniń radiusi;
hám - standart hám izertlenip atırǵan zoldiń jaqtılandırılǵan bóleginiń biyikligi
= 120 ∙ 10−9√ 5 ∙ 10−3 = 76,9 ∙ 10−9 . 19 ∙ 10−3
28
Mısal 17. Polivinil spirtiniń xarakteristikalıq jabısqaqlıǵı [ ] = 0,53 ke teń. Mark– Xauvink–Kun teńlemesiniń konstantası járdeminde polivinil spirtiniń ortasha molekulyar massasın esaplań: = 5,9 ∙ 10−4 hám = 0,67.
Sheshimi: Mark–Xauvink–Kun teńlemesindegi [ ] = ∙ ∙ polimerdiń ortasha molekulyar massasın esaplawǵa qolaylı etiw ushın olardı logarifmleymiz: lg[ ] = lg + ∙ lg . Sonda:
|
lg = |
lg[ ] − lg |
= |
−0,2757 − (−3,2291) |
= 4,4081. |
|
|
||||||||||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
0,67 |
|
|
|
|
|
|||||
boladı. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Onda = 104 4081 = 25591,75 ≈ 25592. |
|
|
|
|
|
|
|
||||||||||
Өз бетинше шешиў ушын есаплар |
|
|
|
|
|
|
|
|
|
||||||||
1. |
= |
|
+ 2 |
|
reakciyası ushın ∆ 0 |
, ∆ 0, Go hám A0 |
lardı esaplań. |
||||||||||
4( ) |
( ) |
|
2( ) |
|
|
|
|
|
|
|
|
|
|
|
|
||
Standart jaǵdayda reakciyanıń óz – ózinen júriw múmkinligin anıqlań. |
|
|
|||||||||||||||
2. Metannıń kreking reakciyası tómendegishe boladı: |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
= |
|
+ 2 |
+ ∆ |
|
|
|
||||
|
|
|
|
|
|
|
4( ) |
( ) |
|
2( ) |
|
|
|
|
|
||
Qosımshadaǵı |
keltirilgen |
|
maǵlıwmatlardan |
paydalanıp |
G0 |
hám |
A0 |
lardı |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
298 |
|
298 |
|
esaplań. 298 K temperaturada bul reakciya óz – ózinen júriw múmkinshiligin anıqlań.
3. |
2CO2(g) = 2CO (g) + O2 (g) |
reakciyasında zatlardıń standart |
janıw |
|||||||
jıllılıqlarınan paydalanıp ∆ ti esaplań. |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
4. |
Metannıń janıw reakciyasınıń teńlemesin jazıń. Eger metannıń standart janıw |
|||||||||
jıllılıǵı ∆ 0 |
= −870,31 / ǵa |
teń bolsa, |
metannıń standart |
payda |
bolıw |
|||||
|
|
|
|
|
|
|
|
|
|
|
jıllılıǵın esaplań. |
|
|
|
|
|
|
|
|
||
Janıw ónimleriniń |
standart payda |
bolıw jıllılıqları |
∆ 0 |
= −393,51; ∆ 0 |
|
= |
||||
|
|
|
|
|
|
2 |
|
2 |
|
|
−285,84 ke teń. |
|
|
|
|
|
|
|
|
||
5. |
Onsha úlken bolmaǵan temperatura intervalı ushın Kirxgoff teńlemesinen |
|||||||||
paydalanıp, |
450 |
K temperatura |
hám 1,0133 ∙ 105 |
basımda |
|
+ |
||||
|
|
|
|
|
|
|
|
3 |
( ) |
|
3⁄2 2 ( ) → 2 ( ) + 2 2 ( ) reakciyasınıń jıllılıq effektin esaplań.
6. CH3COOH(g) + C2H5OH(g) = CH3COOC2H5(g) + H2O(g)
Reakciyanıń standart Gibbs energiyasınıń G0 |
mánisi: 3,50 kDj/mol ge teń. |
hám |
|
|
|
lardıń teppe – teńlik konstantasın esaplań. Eger reakciyaǵa 1 mol kislota hám 2 mol spirt kirse, reakciya aralaspasınıń teppe – teńlik quramı qanday boladı?
7. 90 ml (g) suwda 20 g erigendegi eritpeniń koncentraciyasın ózlerińizge belgili bolǵan usıllarda kórsetiń. Koncentraciyanı kórsetiw usılı retinde tómendegilerdi paydalanıń:
a)molyarlıq massalıq koncentraciya (molyallıq);
b)molyarlıq kólemlik koncentraciya (molyarlıq);
29
c)normallıq (ekvivalenttiń molyarlıq koncentraciyası) ;
d)molyallıq (molyarlıq) muǵdarı;
e)titr;
f)massalıq procent;
g)90 g eritkishke tuwra keliwshi erigen zattıń grammı (sol jaǵdaydaǵı eriwsheńlik koefficienti).
8.95 g suwda 1,40 g glicerin eridi. 298 K de suw parlarınıń basımı 3050,2 / 2 ge teń. Esaplań: a) eritpe ústindegi par basımınıń tómenlewin; b) eritpeniń qaynaw temperaturasın; v) muzlaw temperaturasın; g) onıń osmoslıq basımın.
9.400C temperaturada koncentraciyası 0,04 mol/l bolǵan kalciy xloridiniń suwlı
eritpesiniń osmoslıq basımın esaplań. CaCl2 niń dissociaciya (ionlanıw) dárejesi 96% ke teń. Bul eritpe qannıń plazmasına qanday: gipo-, giperyamasa izotonikalıq tásir jasaydı?
10.0,5 g iod tutqan 1 l suwlı eritpede iod kúkirtli uglerodtı ekstrakciyalaydı. İodtıń suw menen kúkirtli uglerod arasında bólistiriw koefficenti 0,0020 teń bolsa:
a) Kólemi 30 ml ekstragentti bir márte ekstrakciyalaw ámelinen soń suwlı eritpede qalǵan iodtıń massasın;
b) Kólemi 5 ml bolǵan kúkirtli uglerodtı 4 márte ekstrakciyalawdan soń suwlı eritpede qalǵan iodtıń massasın
v) (a) hám (b) jaǵdayında kúkirtli uglerod arqalı bólinip shıqqan iod massasın; g) (a) hám (b) jaǵdayında bólingen iodtıń bólinip shıǵıw dárejesin esaplań;
d) Suwlı eritpeden 95% iodtı ajıratıp alıw ushın zárúr bolǵan kólemi 10 ml kúkirtli uglerodtı bólip-bólip ekstrakciyalaw sanın anıqlań
11. Suwdıń muzlaw temperaturasın 1,50 ǵa túsiriw ushın kerek bolatuǵın basımdı hám 1,5 atm ǵa basımdı kótergende muzdıń júziwin támiyinlewshi temperaturanı esaplań. 00C daǵı muzdıń júziwiniń salıstırmalı jıllılıǵı 333,5 ∙ 103 Dj/kg ǵa teń, suwdıń tıǵızlıǵı 0,9998 ∙ 103 kg/ 3, muzdıń tıǵızlıǵı 0,9168 ∙ 103 kg/ 3.
12. Eger anilinniń suw menen aralaspası atmosferalıq basımda 95,40C da qaynaytuǵın bolsa, 11 kg anilindi aydap alıw (peregonka) ushın kerek bolatuǵın suw puwınıń muǵdarın esaplań. Bul temperaturada suw puwınıń basımı 94605 Pa ǵa teń.
13. Ózinde 0,90 mol/l qant tutqan eritpe T = 288K temperaturada 0,5 mol/l NaCl eritpesi penen izotonikalıq bolıp esaplanadı. a) natriy xloridiniń izotonikalıq hám osmoslıq basımın; b) emeski dissociaciya dárejesin (kajushuyusya stepen ego dissociacii) esaplap tabıń.
14. Dárilik zatlardı qaynatılǵan suwda aydap alıw processinde onıń bir bóleginiń tarqalıwınıń aldın alıw maqsetinde qaynaw temperaturasın 180C ǵa tómenletiw kerek. Bunıń ushın aydaw qurılmasındaǵı basım qansha bolıw kerek ekenligin esaplań. Suwdıń puwlanıw jıllılıǵı 41330 Dj/mol.
30
15.= 5 ke teń bolǵan 25 ml acetatlı buferli eritpe tayarlaw ushın kerek bolatuǵın 0,1 M uksus kislotanıń hám natriy acetatınıń kólemin esaplań.
16.0,19 M ammiak eripesiniń salıstırmalı elektr ótkiziwsheńligi 4,76 ∙
10−4 −1 −1 ge teń. 230C daǵı 4+ hám − ionlarınıń qozǵalıwshańlıǵı sáykes túrde 73,5 hám 198,3 ∙ 10−4 −1 −1 ge teń. Eritpeniń ın, eritpedegi vodorod ionlarınıń koncentraciyasın, onıń , ammiaktiń ionlanıw konstantasın hám dárejesin, molyar ótkiziwsheńligin esaplań.
17.Mıs elektrodtan turıwshı 0,02 M aktivlikke iye bolǵan mıs sulfatı eritpesine hám 0,03 M aktivlikke iye bolǵan cink xloridi eritpesine túsilgen galvanikalıq elementtiń formulasın jazıń.
18.(–)Zn|ZnSO4 (c=0,6M)||CuSO4 (c=1,1M)|Cu(+) formulasına iye galvanikalıq elementtiń elektrodlıq potencialın, elektr qozǵawshı kúshin, Gibbs energiyasınıń
ózgeriwin Go hám reakciyanıń (reakciya T=230C da alıp barıladı) teppe – teńlik konstantasın esaplań.
19. 250C daǵı cink sulfidiniń eriwsheńligin hám eriwsheńlik kóbeymesin esaplań.
Koncentrlengen galvanikalıq elementiń: |
|
1 |
2 |
| ZnS || |
4 | Zn |
= |
= 0,6 |
elektr qozǵawshı kúshi (e.q.k.) 0,276 V ǵa teń.
20.25°C da toyınǵan hám vodorodlı kalomel elektrodlı E elementiniń e.q.k. 0,3985 V ǵa teń. Vodorodlı elektrod kontaktlesetuǵın eritpeniń hám ondaǵı vodorod ionlarınıń aktivligi neshege teń?
21.150C da etilacetattıń natriy gidrooksidi menen sabınlanıw reakciyasınıń tezliginiń
konstantası 2,51 min–1 ǵa teń bolsa, 95% li etilacetattıń sabınlanıw reakciyasınıń waqtın anıqlań. Reakciya aralaspası 1 l 0,05 n. etilacetat eritpesi menen: 1) 1 l 0,05N.eritpesi; 2) 1 l 0,1 N. eritpesi menen aralastırılıp alınǵan.
22. Fosgenniń dissociaciya tezliginiń konstantası:
|
2 = + 2 |
3860C da 0,6 ∙ 10−2 −1 |
ǵa teń, al 464oC temperaturada 62,4 ∙ 10−2 −1. |
Esaplań: a) reakciyanıń aktivleniw energiyasın; b) 4100C temperaturadaǵı reakciyanıń tezlik konstantasın; v) 3780C temperaturada tarqalıw reakciyanıń baslanıwınan 95 minutdan sońǵı fosgenniń muǵdarın (fosgenniń dáslepki muǵdarı 1 mol/l).
23.Temperatura 30 dan 900C ǵa arttırılsa natriy sulfacildiń tarqalıw tezligi neshe ese artadı? Reakciyanıń temperaturalıq tezlik koefficienti 3 ge teń.
24.300C da tiykarǵı tásir etiwshi zattıń (furacilin) tarqalıw tezligi 1,5 ∙ 10−5 −1 bolsa, «Kamfomen» aerozolli preperattınıń 15% ge buzılıw (razrushenie) waqtın anıqlań.
31
