
Методы / Метода к курсачу 2020 года
.pdf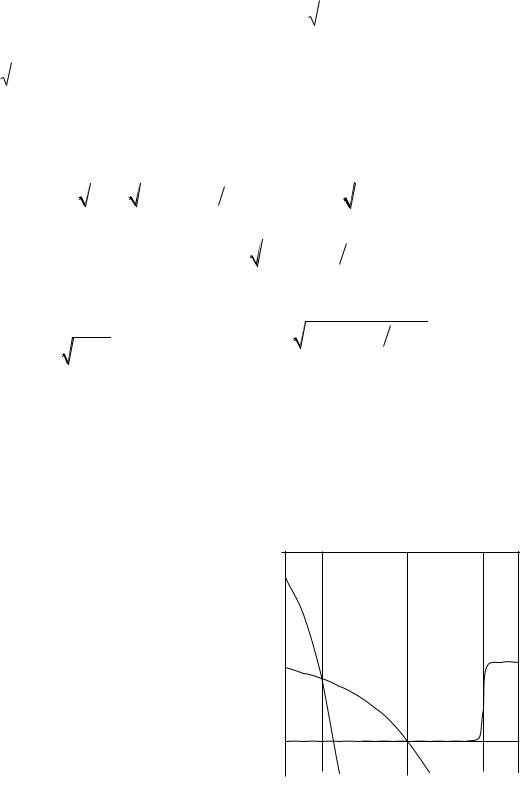
Если Dа tа Da*tд , то можно использовать формулу
|
|
|
|
|
|
|
|
x |
2 |
|
|
|
|
|
|
x |
|
|
|
|
|
|
С ( x, t ) C |
|
exp |
|
|
|
|
С |
|
erfc |
|
|
|
|
С |
|
|||||
|
0а |
|
|
|
|
0д |
|
|
|
|
|
B , |
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
4 D |
t |
|
|
|
2 D |
t |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
д |
|
||||||||||
|
|
|
|
|
|
|
|
|
а |
|
а |
|
|
|
|
д |
|
||||
где C0a |
|
N a |
|
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Da ta |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2. Для рационального выбора шага по оси x при построении распределения определяется глубина залегания коллекторного и эмиттерного переходов:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
x jк 2 |
|
Dа tа |
|
|
|
2, 3 lg(C0а С В ) и x jэ0 6 |
|
Dдtд ; |
||||||||||||||||||||||||
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
1 |
|
|
1/ 2 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
x jэ1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2, 3 lg(C0д |
С0а ) ; |
|||||||||
|
4 D |
|
t |
|
|
4 D |
t |
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
д |
д |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
а |
а |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
1 |
|
|
|
|
|
|
0, 3 |
|
2 |
|
|
1 |
|
1/ 2 |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
x jэ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2, 3 lg(C0 д С0а ) . |
||||||||
|
|
|
|
|
|
|
|
x |
|
|
|
4D |
t |
|
||||||||||||||||||
2 D |
|
t |
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
д |
д |
|
|
|
|
jэ1 |
|
|
|
|
|
|
a |
a |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3. Следующей операцией является построение распределения, показанного на рис. 3.3. Концентрация примеси изменяется по глубине диффузионного слоя, при этом изменяется и плотность дислокаций. Обычно область дислокаций не достигает p-n-переходов.
Диффузанты, у которых различие в атомных радиусах меньше, чем у бора и кремния или у фосфора и кремния, будут образовывать более совершенные p-n- переходы. К таким диффузантам относятся мышьяк, галлий и алюминий. Сильнолегированный бездислокационный слой можно получить, если провести одновременно диффузию двух примесей, имеющих противоположное различие в атомных радиусах.
C ( x, t ), см 3
1E+22
1E+21 |
|
|
n |
|
|
p |
|
|
|
n |
|
n+ |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1E+20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
10 |
|
|
|
|
xjэ |
|
|
xjк |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||||
1E+19 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cк |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1E+18 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1E+1017 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CB |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
16 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1E+1610 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
1 |
2 |
3 |
4 |
5 x,6мкм |
||||||||||
Рис. 3.3
21

|
ЗАДАНИЯ |
|
|
1. |
Вычислить для заданной пары «металл–окисел» зависимости GT0 в |
||
интервале температур Т = 1000…1500 К для реакций |
(1.1)–(1.3) |
по |
|
трем приближениям, используя формулы (1.16)–(1.18) и прил. 1 и 2. |
|
||
2. |
Определить температурные зависимости отношения |
pCO pCO 2 |
для |
всех трех приближений в интервале Т = 1000…1500 К, используя результаты задания 1 и формулы (1.6) и (1.8).
3. Построить графики температурных зависимостей pCO  pCO 2 и
pCO 2 и
K p1.3 (T ) для трех приближений и по знаку G (1.19) сделать вывод об окис-
ляемости заданного металла.
4. Используя термодинамические данные из таблиц прил. 3 и 4 и формулы (2.5) и (2.6), рассчитать температурные зависимости K p 2.1 (T ) , K p 2.4 (T )
иK p 2.6 (T ) в интервале температур Т = 800…1300 К.
5.Вычислить по формуле (2.9) зависимость степени превращения (T, x) для интервала температур T = 800 … 1300 К, интервала относительной влажности водорода x = 0,002…0,03 и заданного индивидуально суммарного давления p .
6.Рассчитать по формулам (2.8) и построить зависимости p H 2O (T , x) и
pAs 2 (T , x) pGa 2O (T , x) для заданных значений влажности х.
7.Используя выражения (2.10) и (2.11), рассчитать и построить зависимости G2 (T , x) и G3 (T , x) для выбранных значений х.
8. Графически вычислить |
корни уравнений G2 (T , x) 0 и |
G3 (T , x) 0; результаты решения |
изобразить графически в координатах |
«температура–влажность» (Т, х); указать границы области стехиометричности газовой фазы.
22
ПРИЛОЖЕНИЯ
1. Термодинамические свойства металлов и соединений
|
H 2980 , |
|
S 2980 , |
|
|
С 0p 298 , |
|
С p (T ) a bT cT 2 |
||||
Вещество |
|
ккал |
|
кал |
|
|
кал |
|
a |
b 103 |
c 10−5 |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
моль |
|
моль К |
|
|
моль К |
|||||
|
|
|
|
|
|
|
|
|
||||
ВаСО3 |
−287,06 |
|
26,80 |
|
20,40 |
|
21,50 |
11,06 |
−3,91 |
|||
ВаО |
−128,60 |
|
16,80 |
|
11,34 |
|
11,79 |
1,88 |
−0,88 |
|||
|
|
|
|
|
|
|
|
|
|
|||
CaCO3 |
−288,44 |
|
21,92 |
|
19,95 |
|
24,98 |
5,24 |
−6,20 |
|||
CaO |
−151,79 |
|
9,50 |
|
10,24 |
|
11,67 |
1,08 |
−1,56 |
|||
|
|
|
|
|
|
|
|
|
|
|
||
C |
0 |
|
|
1,37 |
|
2,04 |
|
4,03 |
1,14 |
−2,04 |
||
|
|
|
|
|
|
|
|
|
|
|||
CO (газ) |
−26,41 |
|
47,22 |
|
6,96 |
|
6,79 |
–0,98 |
−0,11 |
|||
|
|
|
|
|
|
|
|
|
|
|||
CO2 (газ) |
−94,05 |
|
51,06 |
|
8,87 |
|
10,57 |
2,10 |
−2,06 |
|||
Mg |
0 |
|
|
7,81 |
|
5,92 |
|
4,97 |
3,04 |
0,04 |
||
|
|
|
|
|
|
|
|
|
|
|||
MgO |
−143,81 |
|
6,45 |
|
9,03 |
|
10,18 |
1,74 |
–1,48 |
|||
|
|
|
|
|
|
|
|
|
|
|||
MgCO3 |
−261,90 |
|
15,70 |
|
18,05 |
|
18,62 |
13,80 |
–4,16 |
|||
SrCO3 |
−294,60 |
|
23,20 |
|
19,46 |
|
23,52 |
6,32 |
−5,08 |
|||
SrO |
−144,44 |
|
13,10 |
|
10,64 |
|
12,34 |
1,12 |
−1,81 |
|||
|
|
|
|
|
|
|
|
|||||
|
|
Оксиды металлов, входящих в состав кернов |
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||
Ag |
0 |
|
|
10,20 |
|
6,09 |
|
5,09 |
2,04 |
−0,36 |
||
|
|
|
|
|
|
|
|
|
|
|||
Ag2O |
−7,42 |
|
29,00 |
|
15,75 |
|
11,13 |
15,48 |
– |
|||
Al |
0 |
|
|
6,77 |
|
5,82 |
|
4,94 |
2,96 |
– |
||
|
|
|
|
|
|
|
|
|
|
|||
Al2O3 |
−400,48 |
|
12,17 |
|
18,89 |
|
27,43 |
3,06 |
−8,47 |
|||
Cd |
0 |
|
|
12,37 |
|
6,21 |
|
5,31 |
2,94 |
– |
||
|
|
|
|
|
|
|
|
|
|
|||
CdO |
−61,67 |
|
13,10 |
|
10,38 |
|
9,78 |
2,02 |
– |
|||
|
|
|
|
|
|
|
|
|
|
|
||
Cr |
0 |
|
|
5,68 |
|
5,58 |
|
4,16 |
3,62 |
−0,30 |
||
|
|
|
|
|
|
|
|
|
|
|
||
СrO3 |
−139,60 |
|
15,90 |
|
|
– |
|
– |
– |
– |
||
Сr2O3 |
−272,70 |
|
19,40 |
|
28,38 |
|
28,53 |
2,20 |
−3,74 |
|||
Сu |
0 |
|
|
7,97 |
|
5,86 |
|
5,41 |
1,50 |
– |
||
|
|
|
|
|
|
|
|
|
|
|||
СuО |
−37,23 |
|
10,19 |
|
10,11 |
|
11,53 |
1,88 |
–1,76 |
|||
|
|
|
|
|
|
|
|
|
|
|||
Сu2О |
−40,83 |
|
22,08 |
|
14,96 |
|
14,08 |
5,88 |
–0,76 |
|||
Fe |
0 |
|
|
6,49 |
|
5,97 |
|
3,04 |
7,58 |
–0,60 |
||
|
|
|
|
|
|
|
|
|
|
|||
FeO |
−63,64 |
|
13,74 |
|
11,50 |
|
11,66 |
2,00 |
−0,67 |
|||
|
|
|
|
|
|
|
|
|
|
|||
Fe2O3 |
−197,00 |
|
20,89 |
|
24,80 |
|
23,49 |
18,60 |
−3,55 |
|||
Fe3O4 |
−267,13 |
|
36,20 |
|
34,27 |
|
39,92 |
18,86 |
−10,01 |
|||
Mo |
0 |
|
|
6,82 |
|
5,71 |
|
5,18 |
1,66 |
– |
||
|
|
|
|
|
|
|
|
|
|
|||
MoO2 |
−140,80 |
|
11,06 |
|
13,38 |
|
14,11 |
5,82 |
–2,18 |
|||
Nb |
0 |
|
|
8,70 |
|
5,88 |
|
5,89 |
0,81 |
–0,22 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
23 |
|
|
|
|
||
Окончание таблицы
|
H 2980 , |
|
S 2980 , |
|
|
С 0p 298 , |
|
С p (T ) a bT cT 2 |
||||
Вещество |
|
ккал |
|
кал |
|
|
кал |
|
а |
b 103 |
c 10−5 |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
моль |
|
моль К |
|
|
моль К |
|||||
|
|
|
|
|
|
|
|
|
||||
NbO |
−97,03 |
|
11,99 |
|
9,87 |
|
– |
– |
– |
|||
|
|
|
|
|
|
|
|
|
|
|||
NbO2 |
−190,10 |
|
13,03 |
|
13,74 |
|
11,70 |
9,56 |
–0,72 |
|||
Nb2O5 |
−453,50 |
|
32,80 |
|
31,57 |
|
36,90 |
5,12 |
–6,10 |
|||
Ni |
0 |
|
|
7,14 |
|
6,23 |
|
4,06 |
7,04 |
– |
||
|
|
|
|
|
|
|
|
|
|
|||
NiO |
−57,30 |
|
9,08 |
|
10,59 |
|
−4,99 |
37,85 |
3,89 |
|||
|
|
|
|
|
|
|
|
|
|
|
||
Ta |
0 |
|
|
9,92 |
|
6,06 |
|
6,31 |
0,40 |
–0,32 |
||
|
|
|
|
|
|
|
|
|
|
|||
Ta2O5 |
−489,40 |
|
34,20 |
|
32,30 |
|
37,00 |
6,56 |
–5,92 |
|||
Ti |
0 |
|
|
7,33 |
|
5,98 |
|
5,25 |
2,52 |
– |
||
|
|
|
|
|
|
|
|
|
|
|||
TiO |
−124,15 |
|
8,31 |
|
9,55 |
|
10,57 |
3,60 |
–1,86 |
|||
|
|
|
|
|
|
|
|
|
|
|||
Ti2O3 |
−363,40 |
|
18,83 |
|
23,27 |
|
7,31 |
53,52 |
– |
|||
TiO2 |
−225,75 |
|
12,04 |
|
13,16 |
|
17,97 |
0,28 |
−4,35 |
|||
Ti3O5 |
−587,60 |
|
30,92 |
|
37,00 |
|
35,47 |
29,50 |
– |
|||
W |
0 |
|
|
7,80 |
|
5,84 |
|
10,70 |
–1,32 |
–4,64 |
||
|
|
|
|
|
|
|
|
|
|
|||
WO2 |
−140,94 |
|
12,09 |
|
13,32 |
|
15,49 |
3,58 |
–2,80 |
|||
WO3 |
−201,46 |
|
18,15 |
|
17,60 |
|
21,26 |
3,38 |
–4,42 |
|||
Zr |
0 |
|
|
9,29 |
|
6,01 |
|
6,65 |
1,11 |
−0,86 |
||
|
|
|
|
|
|
|
|
|
|
|||
ZrO2 |
−263,04 |
|
12,12 |
|
13,40 |
|
16,64 |
1,80 |
−3,36 |
|||
2.Коэффициенты для расчета теплоемкости в приближении Улиха
иметодом Темкина–Шварцмана
Т, К |
Tf(T) |
М0 |
М1 10 3 |
М 2 10 5 |
500 |
56,65 |
0,1133 |
0,0407 |
0,0916 |
600 |
117,74 |
0,1962 |
0,0759 |
0,1423 |
700 |
195,58 |
0,2794 |
0,1153 |
0,1853 |
800 |
287,76 |
0,3597 |
0,1574 |
0,2213 |
900 |
392,46 |
0,4361 |
0,2012 |
0,2521 |
1000 |
508,30 |
0,5038 |
0,2463 |
0,2783 |
1100 |
634,16 |
0,5765 |
0,2922 |
0,2988 |
1200 |
769,12 |
0,6410 |
0,3389 |
0,3176 |
1300 |
912,42 |
0,7019 |
0,3860 |
0,3340 |
1400 |
1063,43 |
0,7595 |
0,4336 |
0,3484 |
1500 |
1221,58 |
0,8141 |
0,4814 |
0,3610 |
1600 |
1386,40 |
0,8665 |
0,5296 |
0,3723 |
1700 |
1557,48 |
0,9162 |
0,5780 |
0,3824 |
1800 |
1734,45 |
0,9635 |
0,6265 |
0,3915 |
1900 |
1916,97 |
1,0090 |
0,6752 |
0,3998 |
2000 |
2104,76 |
1,0525 |
0,7240 |
0,4072 |
|
|
24 |
|
|
3. Термодинамические данные системы GaAs–H2O–H2
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вещество (состояние) |
|
|
|
|
|
|
|
|
||||||||
|
Функция |
|
T, К |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
Н2 |
|
|
|
Н2О |
|
|
As2 |
|
As4 |
|
Ga2O |
|
Ga2O3 |
|
Ga |
|
GaAs |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
(газ) |
|
|
|
(газ) |
|
(газ) |
|
(газ) |
|
(газ) |
|
(тв) |
|
|
(ж) |
|
(тв) |
||||||||||
|
|
|
|
|
|
|
700 |
|
33,15 |
|
|
47,41 |
|
59,60 |
|
|
80,34 |
|
73,03 |
|
25,63 |
|
|
19,90 |
|
16,27 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
800 |
|
33,72 |
|
|
48,09 |
|
60,29 |
|
|
81,88 |
|
74,07 |
|
27,38 |
|
|
20,79 |
|
16,76 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
ΦT , |
|
900 |
|
34,25 |
|
|
48,75 |
|
60,95 |
|
|
83,34 |
|
75,08 |
|
29,07 |
|
|
21,57 |
|
17,20 |
|
||||||||||||||
|
|
|
кал |
|
1000 |
|
34,76 |
|
|
49,38 |
|
61,58 |
|
|
84,76 |
|
76,04 |
|
30,71 |
|
|
22,27 |
|
17,65 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
моль К |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
1100 |
|
35,24 |
|
|
49,99 |
|
62,17 |
|
|
86,11 |
|
76,96 |
|
32,30 |
|
|
22,90 |
|
18,10 |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
1200 |
|
35,69 |
|
|
50,58 |
|
62,74 |
|
|
87,35 |
|
77,83 |
|
33,82 |
|
|
23,48 |
|
18,43 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
1300 |
|
36,13 |
|
|
51,14 |
|
63,28 |
|
|
88,36 |
|
78,66 |
|
35,24 |
|
|
24,01 |
|
18,88 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
H 2980 , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
ккал |
|
298 |
|
0 |
|
|
|
−57,8 |
|
|
48,0 |
|
|
34,5 |
|
−19,7 |
|
−240 |
|
|
1,34 |
|
−17,7 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
моль |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
4. Термодинамические данные некоторых материалов |
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
0 |
|
|
|
|
|
|
0 |
|
|
|
|
H фаз. переход (кДж/моль) |
|
||||||||||||
|
|
Вещество |
|
H 298 , |
|
S |
298 |
, |
|
|
|
С |
p 298 , |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
кДж |
|
|
|
|
Дж |
|
|
|
|
|
Дж |
Tпл , С |
|
H тв-ж |
Tисп , С |
|
H ж-газ |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
моль К |
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
моль |
|
|
|
|
|
моль К |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
Al (тв) |
|
0 |
|
|
|
28,31 |
|
|
24,34 |
|
|
660 |
|
|
2,60 |
|
|
2520 |
|
69,80 |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
Ga (тв) |
|
0 |
|
|
|
41,09 |
|
|
26,10 |
|
|
30 |
|
|
1,30 |
|
|
2205 |
|
60,90 |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
Ga (газ) |
|
273,00 |
|
168,90 |
|
|
25,35 |
|
|
– |
|
– |
|
|
|
– |
|
|
– |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
GaP |
|
−102,60 |
|
51,90 |
|
|
44,00 |
|
|
1467 |
|
– |
|
|
|
– |
|
|
– |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
H2 |
|
0 |
|
|
|
130,52 |
|
|
28,83 |
|
|
–259,1 |
|
–0,117 |
–252,8 |
|
–0,916 |
|
||||||||||||||||||
|
|
|
H2O |
|
−241,84 |
|
188,74 |
|
|
|
|
– |
– |
|
– |
|
|
|
– |
|
|
– |
|
||||||||||||||||
|
|
|
In (тв) |
|
0 |
|
|
|
57,80 |
|
|
26.70 |
|
|
156 |
|
|
3,30 |
|
|
2024 |
|
228 |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
In (газ) |
|
238,00 |
|
173,70 |
|
|
20,80 |
|
|
– |
|
– |
|
|
|
– |
|
|
– |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
In2O (газ) |
|
−55,00 |
|
298,00 |
|
|
50,00 |
|
|
325 |
|
|
– |
|
|
|
750 |
|
|
– |
|
||||||||||||||||
|
|
In2O3 (тв) |
|
−926,41 |
|
104,25 |
|
|
92,11 |
|
|
1910 |
|
– |
|
|
3300 |
|
|
– |
|
||||||||||||||||||
|
|
|
InAs |
|
−15,50 |
|
18,01 |
|
|
11,42 |
|
|
943 |
|
|
– |
|
|
|
– |
|
|
– |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
Nb |
|
0 |
|
|
|
36,42 |
|
|
24,62 |
|
|
– |
|
– |
|
|
|
– |
|
|
– |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
P (тв) |
|
0 |
|
|
|
41,11 |
|
|
23,86 |
|
|
566 |
|
|
0,16 |
|
|
|
460 |
|
3,10 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
P4 (газ) |
|
59,05 |
|
280,05 |
|
|
67,20 |
|
|
– |
|
– |
|
|
|
– |
|
|
– |
|
||||||||||||||||
|
|
|
Ta |
|
0 |
|
|
|
41,53 |
|
|
25,37 |
|
|
– |
|
31,50 |
|
|
– |
|
|
– |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
25 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
5. Теплофизические характеристики некоторых веществ
Примесь |
D0, см2/c |
Eа, эВ |
Сmax, см 3 |
Тmax, °C |
Проводимость |
|
|
|
Кремний Si (Tпл = 1420 °С) |
|
|
||
B |
1,6 10−9 |
4,6 |
1 1020 |
1200 |
p |
|
Al |
0,05 |
2,7 |
2 1021 |
1150 |
p |
|
Ga |
36,0 |
2,5…3,4 |
7 1020 |
1250 |
p |
|
In |
0,03…0,45 |
2,41 |
3 1019 |
1250 |
p |
|
Tl |
0,06 |
2,5 |
1 1018 |
1250 |
p |
|
As |
6,3…12,7 |
2,42 |
1 1020 |
1150 |
n |
|
Sb |
5,6 |
2,4 |
1 1019 |
1300 |
n |
|
Bi |
6,9 |
2,4 |
1 1017 |
1300 |
n |
|
Li |
2,3 10−3 |
0,5 |
3 1019 |
1100 |
n |
|
Au |
1,1 10−3 |
2,5 |
5 1016 |
1300 |
амфотерная |
|
P |
10,5 |
3,7 |
1,3 1021 |
1200 |
n |
|
Ag |
2 10−3 |
1,6 |
2,0 1017 |
1300 |
n |
|
Cu |
0,04 |
1,0 |
1,5 1018 |
1300 |
p |
|
Zn |
0,1 |
1,4 |
1,6 1016 |
1325 |
p |
|
Sn |
2,16 10−5 |
5,39 |
5,0 1019 |
1200 |
n |
|
Fe |
6,2 10−3 |
0,87 |
3,0 1016 |
1325 |
n |
|
|
|
Германий Ge (Тпл = 937 °С) |
|
|
||
B |
1,8 109 |
4,55 |
1 1018 |
|
800 |
p |
Al |
1,6 102 |
3,24 |
4,3 1020 |
|
700 |
p |
Ga |
40,0 |
3,15 |
5 1020 |
|
650 |
p |
In |
20,0 |
3,0 |
4 1018 |
|
800 |
p |
Ta |
15,0 |
2,9 |
1 1017 |
|
800 |
p |
P |
4,4 10−2 |
1,0 |
2 1020 |
|
560 |
n |
Bi |
3,3 |
2,47 |
6 1016 |
|
910 |
n |
Li |
1,3 10−3 |
0,46 |
7,5 1018 |
|
825 |
n |
Cu |
1,9 10−4 |
0,18 |
6,8 1016 |
|
875 |
p |
Zn |
5,0 |
2,7 |
2,5 1018 |
|
750 |
p |
Au |
2,25 |
2,5 |
3,0 1016 |
|
900 |
амфотерная |
Sb |
10,0 |
2,5 |
1,2 1019 |
|
800 |
n |
As |
1,5 |
2,39 |
7 1019 |
|
800 |
n |
|
|
|
26 |
|
|
|

6. Теплофизические характеристики для расчета коэффициентов диффузии в бинарных полупроводниках
Примесь |
D0, см2/c |
Eа, эВ |
Проводимость |
|
Антимонид алюминия AlSb (Tпл = 1065 C) |
|
|
Zn |
0,33 |
1,93 |
p |
|
|
|
|
Cu |
3,5 10−3 |
0,36 |
p |
|
Арсенид индия InAs (Tпл = 942 С) |
|
|
Cu |
0,036 |
0,52 |
n |
|
|
|
|
Mg |
1,98 10−6 |
1,17 |
p |
Zn |
3,11 10−3 |
1,17 |
p |
Cd |
4,35 10−4 |
1,17 |
p |
Ge |
3,7 10−6 |
1,17 |
n |
Sn |
1,49 10−6 |
1,17 |
n |
S |
6,76 |
2,2 |
n |
|
|
|
|
Se |
12,55 |
2,2 |
n |
|
|
|
|
Te |
3,43 10−5 |
1,28 |
n |
|
Антимонид галлия GaSb (Tпл = 706 С) |
|
|
Sn |
2,4 10−5 |
0,8 |
p |
Te |
3,8 10−4 |
1,2 |
n |
Cd |
1,5 10−6 |
0,72 |
p |
Li |
0,12 |
0,7 |
n |
|
|
|
|
|
Фосфид индия InP (Tпл = 1062 С) |
|
|
Cu |
3,8 10−3 |
0,69 |
p |
Cd |
1 10−7 |
0,72 |
p |
Zn |
1,6 108 |
0,3 |
p |
|
Фосфид галлия GaP (Tпл = 1465 С) |
|
|
Zn |
1,0 |
2,1 |
p |
|
|
|
|
S |
3,0 10−3 |
4,7 |
n |
|
Антимонид индия InSb (Tпл = 530 С) |
|
|
Cu |
3,5 10−5 |
0,37 |
p |
Ag |
1 10−7 |
0,25 |
p |
Li |
7 10−4 |
0,28 |
n |
Cd |
1 10−5 |
1,1 |
p |
Zn |
2,6 10−2 |
1,36 |
p |
Sn |
1,3 10−6 |
0,65 |
n |
Ge |
5 10−6 |
0,95 |
p |
S |
4 10−5 |
1,05 |
n |
Se |
1,6 10−2 |
1,3 |
n |
|
|
27 |
|

|
|
|
Продолжение таблицы |
|
|
|
|
|
|
Примесь |
D0, см2/c |
Eа, эВ |
|
Проводимость |
Co |
1 10−7 |
0,25 |
|
p |
Fe |
1 10−7 |
0,25 |
|
p |
Te |
6,6 10−5 |
1,19 |
|
n |
|
Арсенид галлия GaAs (Tпл = 1238 С) |
|
|
|
Li |
0,53 |
1,0 |
|
n |
|
|
|
|
|
Mg |
4 10−5 |
1,22 |
|
p |
Cd |
0,05 |
2,43 |
|
p |
|
|
|
|
|
Zn |
8 10−5 |
1,5 |
|
p |
Ge |
3 10−5 |
1,8 |
|
n |
Sn |
6 10−4 |
2,5 |
|
n |
S |
1,6 |
2,8 |
|
n |
|
|
|
|
|
Se |
3 103 |
4,16 |
|
n |
Mn |
0,65 |
2,49 |
|
p |
|
|
|
|
|
Te |
2,6 10−5 |
2,0 |
|
n |
Be |
7,3 10−6 |
1,2 |
|
p |
|
Селенид кадмия CdSe (Tпл = 1341 С) |
|
|
|
P |
0,7 |
2,1 |
|
p |
|
|
|
|
|
S |
0,12 |
0,65 |
|
n |
|
|
|
|
|
Te |
16,0 |
2,47 |
|
n |
|
|
|
|
|
|
Теллурид ртути HgTe (Tпл = 670 С) |
|
|
|
Cd |
3,1 10−4 |
0,69 |
|
нейтральная |
In |
1 10−5 |
0,5 |
|
n |
Ag |
6 10−4 |
0,8 |
|
p |
|
Cульфид кадмия CdS (Tпл = 670 С) |
|
|
|
Cu |
1,5 10−3 |
0,76 |
|
p |
Ag |
0,24 |
1,2 |
|
n |
|
|
|
|
|
Au |
200,0 |
1,8 |
|
нейтральная |
|
|
|
|
|
Li |
3 10−6 |
0,68 |
|
p |
|
Теллурид кадмия CdTe (Tпл = 819 С) |
|
|
|
Se |
1,17 10−14 |
1,35 |
|
n |
In |
4,1 10−2 |
1,6 |
|
n |
Ag |
10,0 |
0,61 |
|
p |
|
|
|
|
|
Cu |
3,7 10−4 |
0,67 |
|
p |
O |
6 10−16 |
0,29 |
|
n |
Bi |
10−10 |
0,35 |
|
p |
|
Сульфид цинка ZnS (Tпл = 830 С) |
|
|
|
Mn |
2,33 |
2,46 |
|
p |
|
|
28 |
|
|
|
|
|
Окончание таблицы |
|
|
|
|
Примесь |
D0, см2/c |
Eа, эВ |
Проводимость |
Cu |
2,6 10−3 |
0,73 |
p |
In |
30,0 |
2,2 |
n |
|
|
|
|
Au |
1,75 10−4 |
1,16 |
p |
|
Селенид цинка ZnSe (Tпл = 1520 С) |
|
|
Al |
0,3 |
2 |
n |
|
|
|
|
Cu |
1,7 10−5 |
0,56 |
p |
|
Теллурид цинка ZnTe (Tпл = 1295 С) |
|
|
Li |
2,3 10−2 |
1,22 |
p |
In |
4,0 |
1,95 |
n |
|
|
|
|
29
|
Список рекомендуемой литературы |
|
||
Барыбин А. А. |
Электроника |
и |
микроэлектроника. |
Физико- |
технологические основы. М.: ФИЗМАТЛИТ, 2008.
Барыбин А. А., Сидоров В. Г. Физико-технологические основы электроники. СПб.: Лань, 2001.
Китель Ч. Введение в физику твердого тела / пер. с англ. М.: Мир, 1980. Крапухин В. В., Соколов И. А., Кузнецов Г. Д. Теория процессов полу-
проводниковой технологии. Электронные и микроэлектронные материалы и компоненты твердотельной электроники. М.: МИСИС, 1995.
Свойства неорганических соединений: справ. / сост. А. И. Ефимов и др. Л.: Химия, 1983.
30
