
- •1 Вопрос:
- •2 Вопрос:
- •3 Вопрос:
- •4 Вопрос:
- •5 Вопрос:
- •6 Вопрос:
- •7 Вопрос:
- •8 Вопрос:
- •9 Вопрос:
- •10 Вопрос:
- •11 Вопрос:
- •12 Вопрос:
- •13 Вопрос:
- •14 Вопрос:
- •15 Вопрос:
- •16 Вопрос:
- •17 Вопрос:
- •18. Связь между силой потенциального поля и потенциальной энергией.
- •19. Полная механическая энергия частицы в силовом поле. Законы ее изменения и сохранения.
- •20. Механическая энергия системы частиц. Законы изменения и сохранения механической энергии системы.
- •21. Момент импульса частицы и момент силы относительно некоторой точки. Уравнение моментов.
- •22. Момент импульса системы. Законы изменения и сохранения момента импульса системы.
- •23. Число степеней свободы твердого тела. Уравнения движения твердого тела.
- •24. Момент импульса тела относительно точки. Момент инерции тела относительно оси. Теорема Штейнера.
- •25. Уравнение динамики твердого тела, вращающегося вокруг неподвижной оси.
- •26. Кинетическая энергия вращающегося твердого тела. Работа внешних сил при вращении твердого тела.
- •27. Гироскоп. Гироскопический эффект. Прецессия гироскопа.
- •28. Уравнения динамики твердого тела, совершающего плоское движение. Кинетическая энергия твердого тела при плоском движении.
- •29. Уравнение свободных колебаний под действием квазиупругой силы и его общее решение
- •30. Гармонический осциллятор. Энергия гармонического осциллятора.
- •31. Сложение гармонических колебаний
- •32. Физический и математический маятник(малые колебания без затухания)
- •33. Затухающие колебания. Уравнение затухающих колебаний и его решение.
- •34. Вынужденные колебания и его решение.
- •35. Явление резонанса, определение его характеристик
- •36. Основные характеристики напряжений в упругих средах. Распространение волн в упругой среде. Продольные и поперечные волны. Фронт волны и волновая поверхность
- •37. Фазовая скорость волны. Длина волны
- •38. Плоские, сферические и цилиндрические волны. Уравнение плоской и сферической волн.
- •43. Уравнение состояние системы. Идеальный газ. Уравнение состояния идеального газа.
- •44. Внутренняя энергия идеального газа. Теплообмен и количество теплоты. Работа сил давления газа. Первое начало термодинамики.
- •45. Теплоемкость как функция термодинамического процесса. Уравнение Майера
- •46. Адиабатический процесс. Уравнение Пуассона
- •47. Термодинамический цикл. Кпд цикла
- •52. Распределение молекул идеального газа по координатам во внешнем поле (распределение Больцмана).
- •53. Распределение Максвелла-Больцмана
- •54. Закон равнораспределения энергии по степеням свободы. Статистический смысл температуры.
- •55. Статистический смысл макросостояния. Статистический смысл энтропии. Энтропия системы.
- •56. Второй закон термодинамики. Неравенство Клаузиуса. Закон возрастания энтропии. Энтропия и необратимость.
- •57. Электрический заряд и его свойства. Закон сохранения электрического заряда. Закон Кулона. Принцип суперпозиции сил.
- •58. Электростатическое поле. Напряженность е электростатического поля. Напряженность электростатического поля е точечного заряда и системы зарядов.
- •59. Поток векторного поля е через поверхность. Теорема Гаусса для поля вектора е электростатического поля.
- •60. Теорема о циркуляции вектора напряженности электростатического поля.
- •61. Потенциал электростатического поля. Потенциал поля точечного заряда и системы зарядов.
- •№62 Связь между потенциалом и напряженностью
- •№63 Электрическое поле диполя в дальней зоне
- •№64 Момент сил, действующих на диполь в электрическом поле.
- •№65 Плотность и сила тока. Основные теории Друде для классической электропроводности металлов.
- •67. Вектор магнитной индукции. Магнитное поле равномерно движущегося заряда
- •68.Стационарное магнитное поле. Закон Био-Савара-Лапласа
- •69. Магнитный поток
- •70. Теорема о циркуляции вектора магнитной индукции
- •71. Контур с током в магнитном поле, момент сил. Сила, действующая на контур в неоднородном магнитном осесимметричном поле. Работа сил магнитного поля при перемещении проводника с током.
- •72. Проводники в электростатическом поле. Поле внутри проводника и у его поверхности. Распределение заряда проводнике.
- •73. Электроемкость уединенного проводника. Емкость системы проводников. Энергия электрического поля.
- •74. Полярные и неполярные молекулы. Поляризация диэлектриков. Поляризованность. Поле внутри диэлектрика. Связанные и сторонние заряды. Диэлектрическая восприимчивость.
- •75. Теорема Гаусса для вектора поляризованности.
- •76. Вектор электрического смещения. Диэлектрическая проницаемось. Теорема гауса для вектора электрического смещения.
- •77. Условия на границе двух диэлектриков.
- •78 Сегнетоэлектрики.
- •79 Магнитный момент атомов.
- •80 Намагниченность. Ток намагничивания.
- •81 Теорема о циркуляции вектора намагниченности.
- •82 Теорема о циркуляции вектора напряженности.
- •83 Диамагнетики. Ферромагнетизм.
44. Внутренняя энергия идеального газа. Теплообмен и количество теплоты. Работа сил давления газа. Первое начало термодинамики.
Внутренняя энергия идеального газа – это сумма кинетических энергий движения молекул. Потенциальные энергии не учитываются, потому что газ является идеальным (не учитывается взаимодействие молекул).
Внутренняя энергия U одного моля идеального одноатомного газа равна:
![]()
![]()
Теплопередача (теплообмен) - процесс изменения внутренней энергии без совершения работы. Количественная характеристика - количество теплоты - часть изменения внутренней энергии, происходящего в процессе теплопередачи. Обозначается Q. Единицы измерения: Дж
Работе силы давления газа соответствует площадь под графиком процесса. При расширении газа сила давления совершает положительную работу, а внешняя сила — отрицательную. При сжатии газа наоборот: сила давления совершает отрицательную работу, а внешняя сила — положительную.
А=p (V2-V1)
45. Теплоемкость как функция термодинамического процесса. Уравнение Майера
Теплоёмкость тела характеризуется количеством теплоты, необходимой для нагревания этого тела на один градус
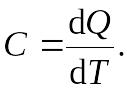
Удельная теплоёмкость (Суд) – есть количество теплоты, необходимое для нагревания единицы массы вещества на 1 градус
Теплоёмкость термодинамической системы зависит от того, как изменяется состояние системы при нагревании.
Если газ нагревать при постоянном объёме, то всё подводимое тепло идёт на нагревание газа, то есть изменение его внутренней энергии. Теплоёмкость при этом обозначается СV.
Уравнение Майера:

![]() Это
уравнение
Майера
для одного моля газа. Из него следует
физический смысл универсальной газовой
постоянной R
– численно равна работе, совершаемой
одним молем газа при нагревании на один
градус при изобарическом процессе.
Это
уравнение
Майера
для одного моля газа. Из него следует
физический смысл универсальной газовой
постоянной R
– численно равна работе, совершаемой
одним молем газа при нагревании на один
градус при изобарическом процессе.
46. Адиабатический процесс. Уравнение Пуассона
Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой.
Уравнение
Пуассона описывает
адиабатный процесс, протекающий
в идеальном
газе.
Адиабатным называют такой процесс, при
котором отсутствует теплообмен между
рассматриваемой системой и окружающей
средой: ![]()
Уравнение
Пуассона имеет вид:
![]()
Здесь V – объем, занимаемый газом, P – его давление, а величина k называется показателем адиабаты.

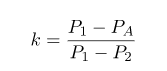
47. Термодинамический цикл. Кпд цикла
Тепловые двигатели работают таким образом, что газ (рабочее тело) расширяется в результате получения теплоты 1 Q от источника, имеющего высокую температуру. Для того чтобы вернуться в первоначальное состояние, можно снова сжать рабочее тело, но при этом полезная работа получена не будет. Для получения полезной работы необходимо в процессе расширения понизить давление газа путем отвода от него части теплоты Q к 2 источнику с более низкой температурой.
Прямой цикл реализуется в тепловом двигателе − периодически действующем устройстве, которое совершает работу за счет полученной от нагревателя теплоты Q. Обратный цикл используется в холодильных установках − периодически действующих устройствах, в которых за счет работы А внешних сил теплота переносится от более холодного тела к телу с более высокой температурой.
Рассмотрим принцип действия теплового двигателя (рис. 12.8.1). В тепловом двигателе от нагревателя с температурой Т1 за цикл отнимается количество теплоты Q1 , а холодильнику с более низкой температурой (T2 < T1) за цикл передается количество теплоты Q2 . При этом совершается работа. Поскольку термодинамическая система (тепловая машина) за цикл возвращается в исходное состояние (внутренняя энергия оказывается прежней), то на основании первого начала термодинамики получим значение работы теплового двигателя за цикл:
![]()
Термический
коэффициент полезного действия (КПД)
определяется отношением:
 Рассмотрим принцип действия холодильной
установки (рис. 12.8.1). В холодильной
установке за счет совершения внешними
силами работы А от более холодного тела
с температурой T2 за цикл отнимается
количество теплоты Q2 и отдается во
внешнюю среду с температурой (Т1 > Т2)
количество теплоты, равное Q1 . Для оценки
эффективности работы холодильной
установки используют отношение
количества теплоты, отнятого за цикл
от холодильной камеры, к работе А внешних
сил. Эта величина называется показателем
цикла k, или холодильным коэффициентом:
Рассмотрим принцип действия холодильной
установки (рис. 12.8.1). В холодильной
установке за счет совершения внешними
силами работы А от более холодного тела
с температурой T2 за цикл отнимается
количество теплоты Q2 и отдается во
внешнюю среду с температурой (Т1 > Т2)
количество теплоты, равное Q1 . Для оценки
эффективности работы холодильной
установки используют отношение
количества теплоты, отнятого за цикл
от холодильной камеры, к работе А внешних
сил. Эта величина называется показателем
цикла k, или холодильным коэффициентом:
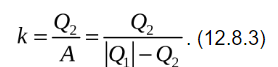
48. Цикл Карно. КПД цикла Карно
Цикл Карно – идеальный круговой процесс, состоящий из двух адиабатных и двух изотермических процессов.
КПД машины Карно равен отношению разности абсолютных температур нагревателя и холодильника к абсолютной температуре нагревателя. Площадь, ограниченная изотермами и адиабатами, численно равна работе цикла Карно.
49. Понятие функции распределения плотности вероятности случайной величины.
Это
функция характеризующая распределение
случайной величины или случайного
вектора. (![]() она
же интегральная функция распределения
вероятностей) – это вероятность того,
что случайная величина (назовем ее ξ)
примет значение меньшее, чем конкретное
числовое значение X:
она
же интегральная функция распределения
вероятностей) – это вероятность того,
что случайная величина (назовем ее ξ)
примет значение меньшее, чем конкретное
числовое значение X:
 5
5 0.
Распределение Максвелла
0.
Распределение Максвелла

51. Средняя, среднеквадратичная и наиболее вероятная скорости молекул
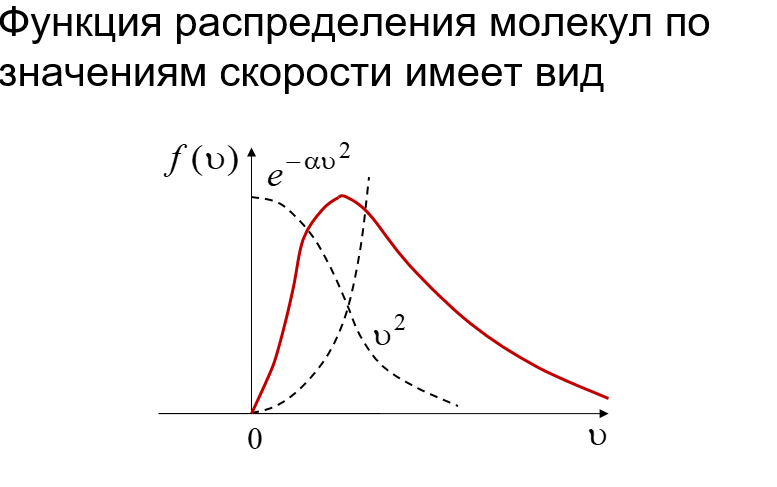
Функция
распределения молекул по скоростям
(функция распределения Максвелла) имеет
вид:![]()
 Где
Где
![]() это величина А, называющаяся нормированным
множителем. Тогда формула распределения
Максвелла принимает вид:
это величина А, называющаяся нормированным
множителем. Тогда формула распределения
Максвелла принимает вид:![]()
При ее помощи получим значения средней, среднеквадратичной и наиболее вероятной скоростей молекул.
Наиболее вероятная скорость
Наиболее вероятной в данном случае будет максимальная скорость. Следовательно, найдя максимум функции f(v) найдем наиболее вероятную скорость.
Продифференцируем
выражение по скорости и приравняем к
нулю:
Значение v, обращающее в нуль выражение в скобках и будет искомой скоростью.
Средняя скорость молекул
Разобьем
ось скоростей на малые интервалы.
Каждому интервалу соответствует
количество молекул:![]()
Скорость каждой из Ni молекул будем считать приближенно равной v, так как интервал vi бесконечно мал. Тогда сумму всех скоростей можно представить в виде интеграла суммы
Ч тобы
получить среднюю скорость, разделим
сумму скоростей на число молекул N.
Тогда
тобы
получить среднюю скорость, разделим
сумму скоростей на число молекул N.
Тогда
Перейдем к интегралу:
Подставим нашу функцию f(v) в полученный интеграл. Получим формулу вычисления средней скорости:
Средняя квадратичная скорость молекул
Аналогичным
образом получаем значения для среднего
значения квадрата скорости. Получаем:![]()
