
- •Получение стали
- •Сравнение основных свойств железа, меди, алюминия, титана.
- •Атомно-кристаллическое строение металлов. Кристаллизация металлов. Типы кристаллических решеток, Полиморфизм. Анизотропия. Аморфное состояние.
- •Анизотропия свойств металлов.
- •Аморфное состояние металлов
- •Дефекты кристаллических решеток. Влияние плотности дислокаций на прочность . Влияние пластической деформации на структуру и свойства металлов. Дефекты кристаллического строения
- •Влияние пластической деформации на структуру и механические свойства металлов и сплавов
- •Превращения в наклепанном металле при нагреве. Изменения его структуры и свойств
- •Виды изломов. Методы исследования структуры материалов. Строение металлического слитка . Дефекты структуры.
- •Методы исследования структуры материалов
- •Металлографические методы Макроскопический анализ
- •Микроскопический анализ
- •Строение слитка.
- •Классификация дефектов
- •Методы исследования структуры металлов: макроскопический анализ. Макроскопический анализ
- •Методы исследования структуры металлов: микроскопический анализ. Микроскопический анализ
- •Методы исследования структуры и дефектов металлов: рентгеноструктурный анализ, пэм, сэм, узи и магнитопорошковый метод.
- •Методы определения твердости материалов. Понятие «твердость материала», «индентор».
- •Определение твердости материалов по методу Бринеля .Обозначение твердости по Бринелю на машиностроительных чертежах.
- •Определение твердости материалов по методу Роквелла .Обозначение твердости по Роквеллу на машиностроительных чертежах.
- •Определение твердости материалов по методу Викерса .Обозначение твердости по Викерсу на машиностроительных чертежах.
- •Порог хладноломкости
- •Понятие металлического сплава. Понятие «компонент», «фаза», «структура». Типы структур сплавов.
- •Строение металлического сплава: твердые растворы, механические смеси и химические соединения.
- •Диаграмма состояния эвтектического типа. Диаграммы состояния сплавов с ограниченной растворимостью. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии, с эвтектикой
- •4.5. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии, с перитектикой
- •Диаграммы эвтектического типа
- •Диаграмма состояния системы, в которой компоненты образуют непрерывный ряд твердых растворов.
- •Связь между свойствами сплавов и типом диаграммы состояния
- •Диаграмма состояния железо-углерода.
- •Фаза и структуры в системе железо-углерод, их краткие характеристики
- •2. Фазы и структуры в железоуглеродистых сплавах.
- •Стали обыкновенного качества. Маркировка. Автоматные стали.
- •Конструкционные
- •Инструментальные;
- •С особыми физико-химическими характеристиками.
- •Углеродистые инструментальные стали . Характеристика и маркировка. Углеродистые инструментальные стали Основные характеристики:
- •Применение
- •Маркировка
- •Углеродистые качественные конструкционные стали. Классификация качественных углеродистых сталей
- •Общая характеристика качественных углеродистых сталей
- •Применение качественной конструкционной углеродистой стали
- •Особенности маркировки
- •Чугун. Влияние формы углерода на свойства чугуна. Структуры чугунов. Маркировка чугунов.
- •Белый чугун, его состав, структура, свойства, область применения.
- •Марки чугунов. Специальные чугуны (антифрикционный, жаростойкий и жаропрочный чугун). Специальные чугуны
- •Антифрикционные чугуны
- •Классификация легированных сталей.
- •Инструментальные легированные стали. Штампованные стали. Быстрорежущие стали.
- •Штампованные стали
- •Быстрорежущие стали
- •Быстрорежущие стали. Свойства и маркировка.
- •Расшифровка обозначения марок сталей
- •Легированные стали с особыми свойствами. Коррозионностойкие, жаростойкие , жаропрочные, износостойкие. Влияние легирующих элементов на свойства. Примеры марок.
- •Хладостойкие стали и сплавы
- •Твердые инструментальные сплавы. Классификация, маркировка. Сравнение с инструментальными сталями . Твердые сплавы и их маркировка
- •Краткое сравнение твердых сплавов с другими инструментальными материалами
- •Упрочняющая и разупрочняющая термическая обработка металлов. Критические точки . Превращение аустенита при охлаждении.
- •Отжиг и нормализация, как виды термической обработки стали.
- •Объемная закалка стали. Охлаждающие среды. Закаливаемость и прокаливаемость сталей. Поверхностная закалка.
- •Способы объемной закалки
- •Этапы закалки стали
- •Способы охлаждения при закаливании стали
- •Поверхностная закалка
- •Внутренние напряжения в закаленной стали. Отпуск стали. Закалка сталей. Внутренние напряжения при закалке.
- •Закалочные среды. Способы закалки.
- •Отпуск стали.
- •Виды хто стали. Диффузионное насыщение поверхности металлами и неметаллами.
- •Цементация стали.
- •Азотирование стали.
- •Нитроцементация и цианирование стали.
- •Медь и ее сплавы. Свойства. Маркировка.
- •Алюминий и его сплавы. Свойства. Маркировка.
- •Неметаллические машиностроительные материалы. Композиционные материалы.
- •1. Классификация композиционных материалов
- •2. Состав, строение и свойства композиционных материалов
Классификация металлов, применяемых в машиностроении. Основные свойства черных и цветных металлов. Получение чугуна и стали .Сравнение основных свойств железа, меди, алюминия, титана.
Металлы и сплавы, применяемые в машиностроении.
Основными материалами, применяемыми в машиностроении при изготовлении деталей, узлов машин и различных металлических конструкций, являются металлы и сплавы.
Металлами называются химические элементы, обладающие следующими характерными признаками: непрозрачностью, хорошей проводимостью тепла и электрического тока, характерным «металлическим» блеском в изломе, а также способностью поддаваться ковке, прокатке, волочению, литью и обработке резанием.
Сплавами называются сложные по составу металлические тела, образовавшиеся в результате затвердевания жидкого раствора, состоящие из двух или нескольких металлов и металлоидов.
Широкое применение в промышленности получило железо, которое в сплавах с углеродом и другими элементами образует группу черных металлов. В эту группу входят различные марки стали и чугуна. Из цветных металлов широко используются медь (обычно в виде сплавов), магний, алюминий, свинец, олово и др.
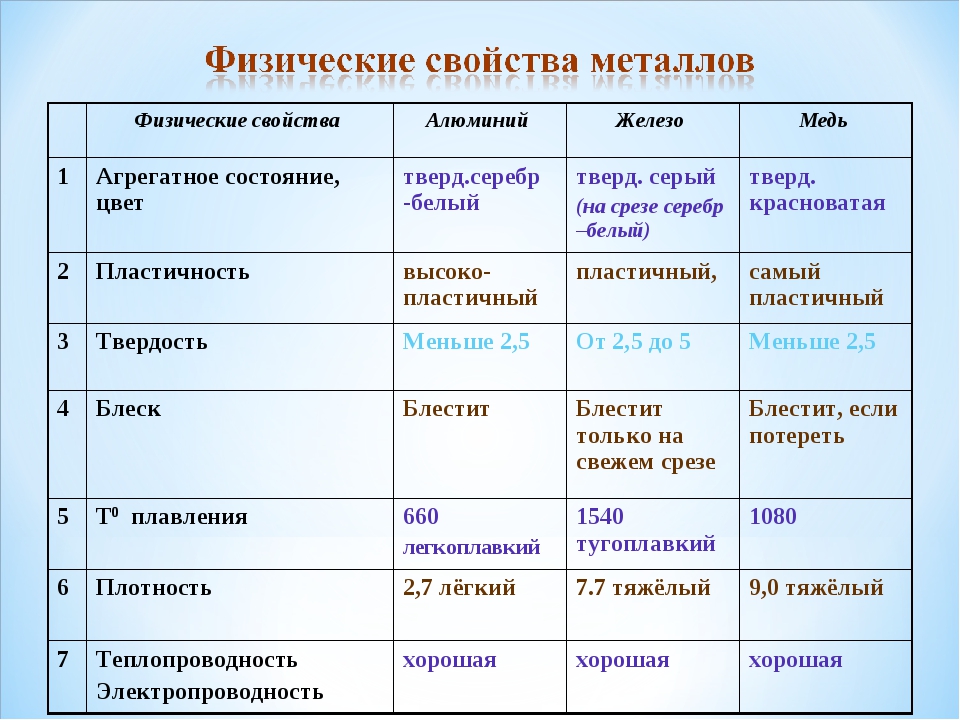
Металлы и сплавы имеют различные физические, механические, химические и технологические свойства.
К физическим свойствам относятся: цвет, плотность, температура плавления (плавкость), теплопроводность, теплоемкость, тепловое расширение, электропроводность, способность намагничиваться.
Температура плавления - температура, при которой металл при нагревании переходит из твердого состояния в жидкое.
Плавкость металлов используют для получения отливок при разливке расплавленного металла в формы. Легкоплавкие металлы (например, свинец) применяют в качестве закалочной среды для стали.
Теплопроводность - это свойство металла проводить тепло. Знание теплопроводности металлов важно для обработки их давлением, для термической обработки и т. п. Лучшие проводники электрического тока являются вместе с тем и лучшими проводниками тепла и наоборот.
Электропроводность - способность металлов и сплавов проводить электрический ток. Металлы с высокой электропроводностью (медь, алюминий) применяют в электромашиностроении, для устройства линий электропередач, а сплавы с высоким электросопротивлением - для ламп накаливания, нагревательных приборов и т. п.
Магнитные свойства металлов особенно важное значение имеют в электромашиностроении (электродвигатели, динамомашины, трансформаторы), для приборов связи (телефонные и телеграфные аппараты), в автоматике и телемеханике (реле), радиоаппаратуре и т. п. Магнитными свойствами обладают только железо и его сплавы и в небольшой степени никель и кобальт. Остальные металлы практически немагнитны.
К механическим свойствам металлов и сплавов относятся прочность, пластичность, упругость, твердость, вязкость, хрупкость, износостойкость.
Прочность - это способность металла или сплава сопротивляться разрушению под действием внешних сил.
Пластичность - свойство металла или сплава изменять свою форму под действием нагрузки не разрушаясь и сохранять принятую форму после прекращения действия нагрузки. Пластичность металлов дает возможность обрабатывать их давлением (ковать, прокатывать, гнуть, вытягивать).
Упругость отличается от пластичности тем, что после снятия нагрузки материал принимает первоначальную форму.
Твердость - свойство металла или сплава сопротивляться проникновению в него другого, более твердого материала.
Ударная вязкость - способность металла выдерживать ударную нагрузку, не разрушаясь.
Хрупкость - способность металла или сплава разрушаться под действием ударной нагрузки без пластической деформации.
Износостойкость - способность поверхностного слоя материала противостоять истиранию под влиянием трения.
К химическим свойствам металлов относятся жаростойкость, жароупорность и коррозионная стойкость.
Из химических свойств металлов коррозионная стойкость особенно важна для изделий, работающих в сильно окислительных средах (детали химических машин и приборов). Высокой коррозионной стойкостью обладают специальные нержавеющие, кислотостойкие и жаропрочные стали.
К технологическим свойствам металлов и сплавов относятся обрабатываемость резанием, свариваемость, ковкость, прокаливаемость, жидкотекучесть.
Обрабатываемость - свойство металла или сплава, характеризующее его способность подвергаться обработке резанием (определяется по скорости резания, усилию резания и по чистоте обработки).
Свариваемость - свойство металла давать доброкачественное соединение при сварке, характеризующееся отсутствием трещин и других пороков металла в швах и прилегающих к шву зонах.
Ковкость - способность металла или сплава без разрушения изменять свою форму при обработке давлением.
Прокаливаемость - способность сплава воспринимать закалку на определенную глубину от поверхности.
Жидкотекучесть - способность металла или сплава в расплавленном состоянии заполнять литейную форму.
Чтобы определить строение, состав и свойства металла, его подвергают испытанию (механические испытания, химический, спектральный, металлографический и рентгенографический анализ, технические пробы и дефектоскопия).
Перечень свойств черных металлов:
Прочный
Высокая прочность на разрыв
Обычно магнитный
Низкая устойчивость к коррозии
Серебристый цвет
Пригодный для вторичной переработки
Хорошие проводники электричества
Ключевыми свойствами цветных металлов являются:
устойчивость к коррозии
отличная электропроводность
высокий показатель пластичности и гибкости
малый вес (по отношению к чермету)
наличие уникальных свойств и прочее
Получение стали
Сталь является важнейшим продуктом чёрной металлургии. Так как без стали не могла бы работать практически ни одна отрасль промышленности, то уровень производства стали может служить одной из характеристик общего технико-экономического уровня развития государства.
Сталь получают главным образом из смеси чугуна, выплавляемого в доменных печах, со стальным ломом. Основные агрегаты для получения стали - конверторы, мартеновские и электрические печи; полученная в них сталь называется соответственно конверторной, мартеновской и электросталью. Наиболее прогрессивным в наши дни считается кислородно-конверторный способ производства стали. В то же время развиваются такие перспективные способы получения сталей, как прямое восстановление стали из руды,
Получение стали из чугуна - то есть материала, значительно более богатого углеродом, кремнием, марганцем и фосфором, чем сталь перед её раскислением, - представляет собой ряд окислительных процессов, в результате которых уменьшаются концентрации углерода, кремния, марганца и вредных элементов, отрицательно влияющих на качество стали. Все процессы получения стали выплавкой происходят при участии шлаковых расплавов, выполняющих сразу несколько функций (удаление вредных примесей, защита от вторичного окисления и др.) Подробно основные теории процессов получения стали изложены в работе .
Чугун получают в ходе доменного процесса, основанного на восстановлении железа из его природных оксидов, содержащихся в железных рудах, коксом при высокой температуре. Кокс, сгорая, образует углекислый газ. При прохождении через раскаленный кокс он превращается в оксид углерода, который и восстанавливает железо в верней части печи. Опускаясь в нижнюю горячую часть печи, железо плавится в взаимодействии с коксом и частично растворяя его, превращается в чугун.
Сравнение основных свойств железа, меди, алюминия, титана.
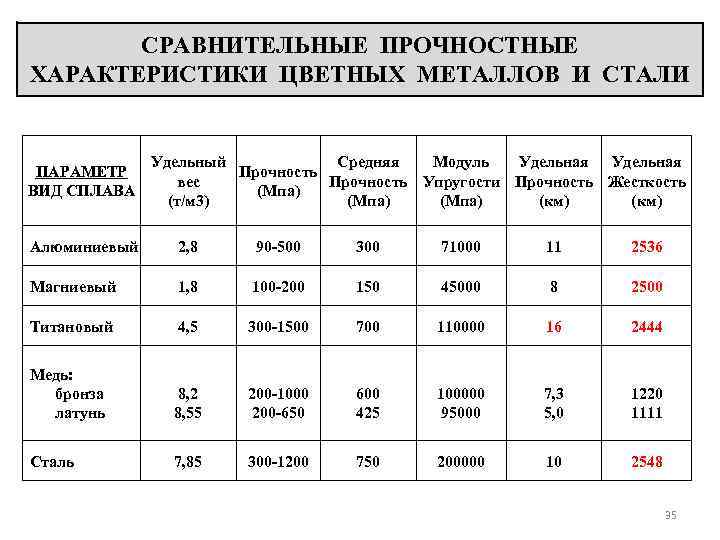
Атомно-кристаллическое строение металлов. Кристаллизация металлов. Типы кристаллических решеток, Полиморфизм. Анизотропия. Аморфное состояние.
Под атомно-кристаллической структурой понимают взаимное расположение атомов, существующее в кристалле. Атомы в кристалле расположены в определенном порядке, который периодически повторяется в трех измерениях.
Для описания атомно-кристаллической структуры пользуются понятием пространственной или кристаллической решетки.
Кристаллическая решетка представляет собой воображаемую пространственную сетку, в узле которой располагаются атомы (ионы), образующие металл.
 Наименьший
объем кристалла, дающий представление
об атомной структуре металла во всем
объеме, получил название элементарной
кристаллической ячейки
(решетки).
Наименьший
объем кристалла, дающий представление
об атомной структуре металла во всем
объеме, получил название элементарной
кристаллической ячейки
(решетки).
Для характеристики элементарной ячейки задают шесть величин: три ребра ячейки a, b, c и три угла между ними α, β, γ. Эти величины называют параметрами кристаллической решетки.
Кристаллические решетки бывают простыми (атомы только в вершинах решетки) и сложными.
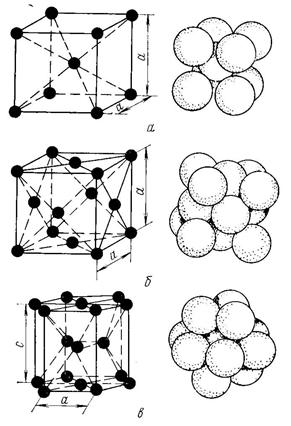
Металлы образуют одну из следующих высокосимметричных сложных решеток с плотной упаковкой атомов: кубическую объемноцентрированную (ОЦК), кубическую гранецентрированную (ГЦК) и гексагональную (ГПУ).
ОЦК: Rb, K, Na, Li, Tiβ, Tlβ, Zrβ, Ta, W, V, Feα, Cr, Nb, Ba, и др.
ГЦК: Cu, Al, Pt, Pb, Ni, Ag, Au, Pd, Rh, Ir, Feγ, Coα, Caα, Ce, Srα, Th, Sc и др.
ГПУ: Mg, Cd, Re, Os, Ru, Zn, Be, Coβ, Caα, Zrα, Laα, Tiα и др.
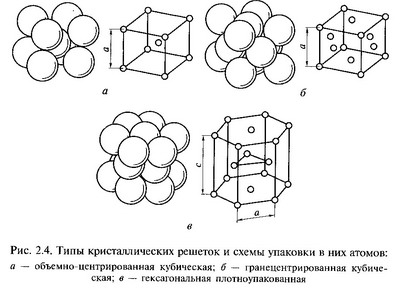
2.Для большинства металлов характерны следующие типы кристаллических решеток: объемно-центрированная кубическая (ОЦК); гранецентрированная кубическая (ГЦК); гексагональная плотноупакованная (ГПУ). Основные типы кристаллических решеток представлены на рис. 2.4.
В объемно-центрированной кубической решетке (рис. 2.4, а) атомы расположены в углах и центре куба. Период решетки равен а, координационное число К= 8, базис решетки равен 2; 8 атомов расположены в углах куба, 1 атом в центре куба принадлежит только одной ячейке). Данный тип решетки имеют металлы К, Na, Li, Та, W, Mo, Fea, Cr, Nb и др.
В гранецентрированной кубической решетке (рис. 2.4, б) атомы расположены в углах куба и центрах его граней. Эта решетка характеризуется периодом а, координационном числом К= 12, базисом, равным 4: (1/8) • 8 + ½ • 6 = 4; 8 атомов в углах куба и 6 атомов в центрах граней, каждый из которых принадлежит двум элементарным ячейкам. Кубическую гранецентрированную решетку имеют следующие металлы: Са, Pb, Ni, Ag, Au, Pt, FeY и др.
В гексагональной плотноупакованной решетке (рис. 2.4, в) атомы расположены в вершинах и центрах шестигранных оснований призмы, кроме того, три атома находятся в средней плоскости призмы. Периоды решетки — а и с, причем с/а > 1 .
1.Переход из жидкого состояния в твердое (кристаллическое) называют кристаллизацией. Процессы кристаллизации зависят от температуры и протекают во времени, поэтому кривые ох-лаждения строятся в координатах температу-ра - время (рис. 3). Теоретический, т. е. идеаль-ный процесс кристаллизации металла без пере-охлаждения протекает при температуре Т 5 (рис. 3). При достижении идеальной температу-ры затвердевания Т 5 падение температуры пре-кращается. Это объясняется тем, что перегруп-пировка атомов при формировании кристаллической решетки идет с выделением тепла (выде-ляется скрытая теплота кристаллизации). Каждый чистый металл (не сплав) кристаллизуется при строго индивидуальной постоянной темпера-туре. По окончании затвердевания металла тем-пература его снова понижается.
Практически кристаллизация протекает при более низкой температуре, т. е. при переохлаждении металла до температур Tn, Tn 1, Tn 2 (напри-мер, кривые 1, 2). Степень переохлаждения (ДT=T s --Tn) зависит от природы и чистоты ме-талла к скорости охлаждения. Чем чище жидкий металл, тем он более склонен к переохлаждению. При увеличении скорости охлаждения степень переохлаждения возрастает, а зерна металла ста-новятся мельче, что улучшает его качество. Для большинства металлов степень переохлаждения при кристаллизации в производственных усло-виях составляет от 10 до 30°С. При больших скоростях охлаждения она может достигать со-тен градусов.
Процесс кристаллизации состоит из двух ста-дий: зарождения - кристаллов (зародышей или центров кристаллизации) и роста кристаллов из этих центров. При переохлаждении сплава ниже Tn на многих участках жидкого металла (рис. 4, а, б) образуются способные к росту кри-сталлические зародыши.
Сначала образовавшие-ся кристаллы растут свободно и имеют более или менее правильную геометрическую форму (рис. 4, в, г, д). Затем при соприкосновении рас-тущих кристаллов их правильная форма нару-шается, так как в этих участках рост граней пре-кращается. Рост кристалла продолжается только в тех направлениях, где есть свободный доступ жидкого металла. В результате кристаллы, имев-шие сначала геометрически правильную форму, после затвердевания получают неправильную форму, их называют кристаллитами или зернами (рис. 4,е).
Величина зерен зависит от числа центров кристаллизации и скорости роста кристаллов. Чем больше центров кристаллизации, тем мельче зерно металла.
Величина зерен, образующихся при кристаллизации, зависит не только от количества самопроизвольно зарождающихся центров кристаллизации, но также и от количества нерастворимых примесей, всегда имеющихся в жидком металле. Такие нерастворимые примеси являются готовы-ми центрами кристаллизации. Ими являются окислы (например, Al2O3), нитриды, сульфиды и другие соединения. Центрами кристаллизации в данном металле или сплаве могут быть только такие твердые частицы, которые соизмеримы с размерами атомов основного металла. Кристал-лическая решетка таких твердых частиц должна быть близка по своему строению и параметрам решетке кристаллизующегося металла. Чем боль-ше таких частичек, тем мельче будут зерна за-кристаллизовавшегося металла.
На образование центров кристаллизации вли-яет и скорость охлаждения. Чем выше скорость охлаждения, тем больше возникает центров кри-сталлизации и, следовательно, мельче зерно ме-талла.
Чтобы получить мелкое зерно, создают искусственные центры кристаллизации. Для этого в расплавленный металл (расплав) вводят специальные вещества, называемые модификаторами. Модифицирование отливок проводят введением в расплав добавок, которые образуют тугоплавкие соединения (карбиды, окислы). При модифицировании, например, ста-ли применяют алюминий, титан, ванадий; алюминиевых сплавов -- марганец, титан, ванадий.
Полиморфизм. Для ряда металлов характерно явление полиморфизма. Этим термином называют способность вещества формировать различные типы кристаллических решеток. Так, при разных температурах железо может иметь ОЦК или ГЦК решетку, кобальт — ГЦК или ГПУ решетку. Полиморфизм характерен и для других металлов. Различные кристаллические формы одного и того же вещества называются полиморфными или аллотропными модификациями.
Превращение одной модификации в другую с изменением кристаллической решетки называется полиморфным превращением.
Полиморфное превращение происходит в результате нагрева или охлаждения: в чистых металлах при постоянной температуре, а в сплавах — в интервале температур.
Полиморфизмом обладают железо, кобальт, титан олово, марганец, ванадий, стронций, кальций, цирконий и др.
Физическая суть полиморфного превращения заключается в том, что кристаллическое вещество при разных температурах переходит в состояние с меньшим запасом свободной энергии. Например, полиморфное равновесие титана наблюдается при 880 °С, а олова - при 13,2 °С.
