
- •2.Характеристика белковых веществ. Элементарный состав белка. Значение белков для организма: белки – ферменты, белки – гормоны, структурные белки, белки – рецепторы, транспортные белки, антитела.
- •3. Аминокислоты как структурные элементы белка. Классификация аминокислот. Физико-химические свойства аминокислот. Общность строения, оптическая изомерия, амфотерность, сродство радикалов к воде.
- •4. Структурная организация белков. Типы связей, участвующие в формировании первичной, вторичной, третичной и четвертичной структур.
- •5. Физико-химические свойства белков. Денатурация белка. Использование процесса денатурации в медицине.
- •1)Белки –коллоидные растворы.
- •2) Суммарный заряд белка.
- •3)Растворимость
- •4)Амфотерность (за счёт аминокислот, см. 2 вопрос)
- •6. Белки как амфотерные электролиты. Поведение белков в электрическом поле. Электрофорез. Применение его во врачебной практике. Изометрическая точка белков. Определение суммарного заряда белка.
- •7. Классификация белков. Важнейшие представители протеинов и протеидов. Биологические функции белков.
- •8. Нуклеопротеиды. Химический состав белковой и простетической группы. Структурные компоненты нуклеиновых кислот. Номенклатура нуклеотидов, нуклеозидов, азотистых оснований. Их химическое строение.
- •9. Гемоглобин. Строение и свойства. Окси-, карбокси-,карб- метгемоглобин. Вариации первичной структуры и свойства гемоглобина. Гемоглобинопатии.
- •10. Хромопротеиды. Гемоглобин, миоглобин, каталаза, цитохромоксидаза, цитохромы. Их химическая природа и значение для организма.
- •12. Фосфопротеиды. Способ связи простетической группы с белковым компонентом. Значение в обмене веществ. Металлопротеиды и их биологическая роль в тканевом дыхании.
- •13. Липопротеиды. Химическое строение, представители, роль в обмене веществ. Состав и строение транспортных липопротеидов крови.
- •15. Роль и значение ферментов в процессе жизнедеятельности. Ферменты как биологические катализаторы. Химическая природа ферментов. Ферменты простые и сложные. Апофермент и кофермент.
- •Особенности ферментов как биологических катализаторов
- •16. Понятие об изоферментах. Лактатдегидрогеназа. Определение изоферментов с целью диагностики болезней.
- •17. Ингибиторы ферментов. Типы ингибирования. Конкурентное, неконкурентное,аллостерическое ингибирование. Использование ингибиторов ферментов в качестве лекарств.
- •Необратимое ингибирование
- •Механизм необратимого ингибирования ацетилхолинэстеразы
- •Механизм необратимого ингибирования циклооксигеназы
- •Обратимое ингибирование
- •Конкурентное ингибирование
- •Конкурентное ингибирование сукцинатдегидрогеназы
- •Смешанное ингибирование
- •1)Действие многих лекарственных средств
- •18. Изменение активности ферментов при заболеваниях. Наследственные энзимопатии. Определение активности ферментов в плазме с целью диагностики болезней.
- •19. Ферменты пищеварительной системы, гидролизующие углеводы, липиды, белки.
- •20. Особенности ферментативного катализа. Специфичность действия ферментов. Особенности ферментативного катализа.
- •21. Кинетика ферментативных реакций. Факторы, определяющие скорость ферментативных реакций. Кинетика ферментативных реакций –
- •22. Активный центр и механизм действия ферментов, специфичность.
- •23. Кофакторы ферментов и их роль в катализе. Витамины - как предшественники коферментов. Гиповитаминозы, их причины и проявления.
- •24. Современная классификация ферментов. Номенклатура. Тип катализируемых реакций. Примеры.
- •Изменение активности фермента при фосфорилировании-дефосфорилировании
- •26. Регуляция активности ферментов путем ассоциации/диссоциации протомеров.
- •27. Применение ферментов в медицине. Энзимодиагностика и энзимотерапия.
- •29. Биосинтез днк (репликация). Принцип комплементарности азотистых оснований. Биологический генетический код.
- •30. Биосинтез рнк (транскрипция), рнк-полимеразы. Типы рнк и их биологическая роль.
- •31. Современные представления о синтезе белка. Регуляция биосинтеза белка.
- •32. Витамины. Понятие о гипо- и гипервитаминозах. Механизм действия витаминов. Классификация витаминов. Важнейшие представители витаминов. Их биологическое значение.
- •33. Жирорастворимые витамины. Витамин а. Химическая природа, свойства, распространение, потребность, роль в обмене веществ. Авитаминозы.
- •34. Витамины группы д. Химическая природа и свойства. Роль в обмене веществ. Биохимическая характеристика патогенеза рахита.
- •35. Витамин е. Химическое строение, свойства, роль в обмене веществ.
- •36. Витамин к. Химическое строение, свойства, роль в обмене веществ.
- •37. Водорастворимые витамины. Витамин в1 . Химическая природа нарушений в обмене веществ при в1 -авитаминозе. Распространение, потребность.
- •38. Витамин в2 . Химическое строение, распространение, суточная потребность, участие в построении флавиновых ферментов. Авитаминоз.
- •39. Витамин в6 , его производные. Химическое строение, распространение, суточная потребность, симптомы авитаминозов. Коферментная роль витамина в6 .
- •41. Пантотеновая кислота. П-аминобензойная кислота. Химическая природа, свойства, роль в обмене веществ. Авитаминозы.
- •42. Витамин н (биотин). Биологическая роль, участие в обмене веществ. Химическая природа, авитаминоз.
- •43. Фолиевая кислота. Тетрагидрофолиевая кислота. Синтез одноуглеродистых радикалов. Химическая природа, биологическая роль. Авитаминозы. Участие в обмене веществ.
- •44. Витамин с. Авитаминоз. Химическая природа, содержание в пищевых продуктах, потребность, роль в обмене веществ.
- •45. Гомоны. Химическая природа,механизм действия,их роль в регуляции обмена веществ.
- •47. Гормоны панкреатической(поджелудочной) железы.
- •48. Гормоны мозгового вещества надпочечников.
- •49. Гормоны коры надпочесников.
- •50. Гормоны передней доли гипофиза.
- •51. Гормоны задней доли гипофиза.
- •52. Механизм действия гормонов.Мембранный и внутриклеточный типы гормоныльной регуляции.
- •53. Аденилатциклазная система передачи сигналов,роль g-белков в трансдукции сигнала.
- •55. Окислительное декарбоксилирование пирувата.
- •56. Окисление ацетил-КоА в цикле Кребса. Связь между общими путями катаболизма и цепью переноса электронов и протонов. Цикл трикарбоновых кислот
- •Образование цитрата
- •Превращение цитрата в изоцитрат
- •Окислительное декарбоксилирование изоцитрата
- •Превращение сукцинил-КоА в сукцинат
- •Дегидрирование сукцината
- •Образование малата из фумарата
- •Дегидрирование малата
- •57. Механизм образования атф. Окислительное фосфорилирование. Отличие от субстратного фосфорилирования.
- •58. Углеводы пищи: строение, переваривание. Механизмы трансмембранного переноса глюкозы. Примеры нарушения переваривания углеводов.
- •59. Метаболизм глюкозы в клетках.
- •61. Аэробное окисление углеводов. Ферменты, участвующие в этих процессах.
- •62. Анаэробное расщепление глюкозы в тканях. Гликолиз и гликогенолиз. Ферменты, роль этого процесса.
- •63. Глюконеогенез. Взаимосвязь гликолиза и глюконеогенеза (цикл Кори).
- •64. Апотомический распад углеводов. Биологическое значение пентозофосфатного цикла.
- •Значение пентозофосфатного пути
- •65. Энергетический выход окисления одной молекулы глюкозы при гликолизе, аэробном окислении и прямом окислении. Регуляция углеводного обмена
- •67.Значение белков в питании. Азотистый баланс и азотистое равновесие. Заменимые и незаменимые аминокислоты.
- •69. Катаболизм аминокислот (реакция дезаминирования).
- •71. Обмен аммиака. Механизм токсического действия аммиака. Связывание (обезвреживание) аммиака.
- •72. Орнитиновый цикл (цикл мочевины). Наследственные нарушения орнитинового цикла и их основные проявления.
- •73. Заменимые и незаменимые а/к. Биосинтез заменимых.
- •74. Обмен серина и глицина. Роль фолиевой кислоты в обмене аминокислот. Участие глицина в синтезе креатина и глутатиона.
- •75. Особенности обмена метионина. Синтез фосфатидилхолина. Синтез карнитина. Синтез креатина и креатинфосфата.Образование цистеина из метионина.
- •79. Структура, классификация и свойства основных липидов организма человека. Химическое строение и биологическая роль. Фосфолипиды, сфинголипиды, цереброзиды, гликолипиды
- •80. Переваривание и всасывание липидов в жкт. Роль желчных кислот. Механизм всасывания жиров. Нарушения в переваривании липидов. Транспорт жиров из кишечника.
- •81. Современная теория окисления жирных кислот с четным и нечетным числом углеродных атомов. Общий выход энергии при окислении жирных кислот до со2 и н2о.
- •82. Пути образования и использования ацетоуксусной кислоты в организме. Нарушение и регуляция липидного обмена.
- •83. Биосинтез триацилглицеридов и фосфолипидов. Функции фосфолипидов. Регуляция и патология липидного обмена.
- •84. Обмен стероидов. Биосинтез холестерина. Холестерин как предшественник ряда других стероидов. Нарушение обмена холестерина.
- •85. Биосинтез жирных кислот. Регуляция синтеза жирных кислот. Источники цитоплазматического ацетил-КоА. Роль биотина, надфн2, апб в синтезе жирных кислот.
- •86. Синтез желчных кислот, регуляция процесса. Их роль в переваривании и всасывании липидов. Желчно-каменная болезнь.
- •87. Гиперхолестеролемия. Механизм развития атеросклероза и основные подходы к лечению.
- •88. Регуляция обмена углеводов, липидов и аминокислот.
- •89. Биохимические представления о сахарном диабете: важнейшие изменения гормонального статуса и метаболизма при сахарном диабете.
- •90. Регуляция водно-солевого обмена гормонами. Вазопрессин и альдостерон: строение и механизм действия.
- •91. Ренин-альдостерон-ангиотензиновая система. Биохимические механизмы развития почечной гипертонии. Нарушения водно-солевого обмена.
- •92. Паратгормон и кальцитонин: химическая природа, механизм действия, влияние на обмен кальция и фосфатов. Гипо- и гиперкальциемия.
- •95. Механизмы обезвреживания токсических веществ в печени. Микросомальное окисление. Реакции конъюгации.
- •96. Биотрансформация лекарств в печени.
- •98. Ферменты крови их диагностическое значение.
- •99. Структурная организация и основные компоненты мембран. Строение и функции липидов мембран
- •Характеристика мембранных белков
- •Липидный состав мембран
- •100. Избирательная проницаемость мембран. Механизмы переноса веществ через мембраны (примеры).
75. Особенности обмена метионина. Синтез фосфатидилхолина. Синтез карнитина. Синтез креатина и креатинфосфата.Образование цистеина из метионина.
МЕТИОНИН:
Метильная группа метионина — мобильный одноуглеродный фрагмент, используемый для синтеза ряда соединений. Перенос метальной группы метионина на соответствующий акцептор называют реакцией трансметилирования, имеющей важное метаболическое значение.
Метальная группа в молекуле метионина прочно связана с атомом серы, поэтому непосредственным донором этого одноуглеродного фрагмента служит активная форма аминокислоты.
Реакция активации метионина
Активной формой метионина является S-аденозилметионин (SAM) — сульфониевая форма аминокислоты, образующаяся в результате присоединения метионина к молекуле аденозина. Аденозин образуется при гидролизе АТФ (см. схему А).
Схема А
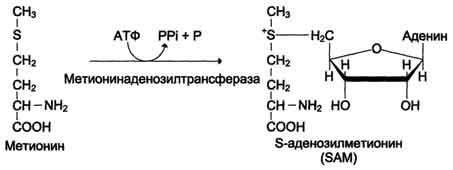

Эту реакцию катализирует фермент метионин аденозилтрансфераза, присутствующий во всех типах клеток. Структура (-S+-CH3) в SAM — нестабильная группировка, определяющая высокую активность метильной группы (отсюда термин «активный метионин»). Эта реакция уникальна для биологических систем, так как, по-видимому, является единственной известной реакцией, в результате которой освобождаются все три фосфатных остатка АТФ.
Отщепление метильной группы от SAM и перенос её на соединение-акцептор катализируют ферменты метилтрансферазы. SAM в ходе реакции превращается в S-аденозилгомоцистеин (SAT).
Регенерация метионина
+Реакции метилирования играют важную роль в организме и протекают очень интенсивно. Это вызывает большой расход метионина, так как он является незаменимой аминокислотой (в клетках метионин синтезироваться не может). В связи с этим большое значение приобретает возможность регенерации метионина с участием заменимых аминокислот (Сер, Гли). В результате отщепления метильной группы SAM превращается в S-аденозилгомоцистеин (SAT), который при действии гидролазы расщепляется на аденозин и гомоцистеин.
S-аденозилгомоцистеин + Н2О → Аденозин + Гомоцистеин
Гомоцистеин может снова превращаться в ме тионин под действием гомоцистеинметилтранс феразы.
Промежуточным переносчиком метильной группы в этой реакции служит производное витамина В12 - метилкобаламин, выполняющий роль кофермента.
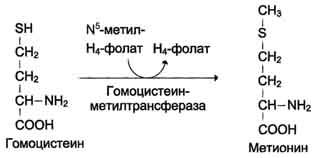
ФОСФАТИДИЛХОЛИН:
Фосфатидилхолины (лецитины) — наиболее распространённая группа глицерофосфолипидов, участвующих в образовании мембран клеток и липопротеинов, в составе которых осуществляется транспорт липидов (см. схему Б)
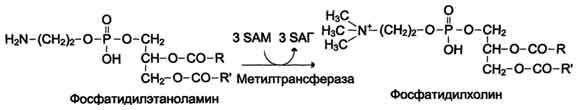
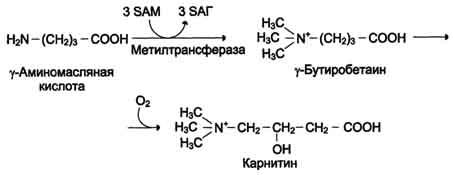
Синтез карнитина
Карнитин - переносчик жирных кислот через мембрану митохондрий
Синтез креатина
Креатин необходим для образования в мышцах высокоэнергетического соединения - креатинфосфата. Синтез креатина идёт в 2 стадии с участием 3 аминокислот: аргинина, глицина и метионина. В почках образуется гуанидинацетат при действии глицинамидинотрансферазы.
Затем гуанидинацетат транспортируется в печень, где происходит реакция его метилирования.
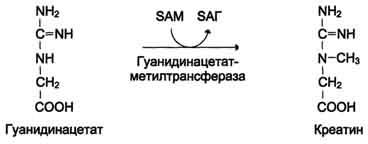
Креатин с кровотоком переносится в мышцы и клетки мозга, где из него образуется высокоэнергетическое соединение - креатинфосфат. (см. схему А на с. 502).
Эта реакция легко обратима и катализируется ферментом креатинкиназой. Фермент локализован в цитозоле и митохондриях клеток, обладает органоспецифичностью. В норме активность его в крови очень мала. Обнаружено три изоферментные формы креатинкиназы
Креатинфосфат играет важную роль в обеспечении энергией работающей мышцы в начальный период. В результате неферментативного дефосфорилирования, главным образом в мышцах, креатинфосфат превращается в креатинин, выводимый с мочой.
Для синтеза цистеина необходимы 2 аминокислоты:
Серин - источник углеродного скелета;
Метионин - первичный источник атома S (см. схему А).
Синтез цистеина из гомоцистеина происходит в 2 стадии под действием пиридоксальзависимых ферментов цистатионинсинтазы и цистатионинлиазы (см. схему Б на с. 504).
При нарушении использования гомоцистеина в организме из него образуется гомоцистин:
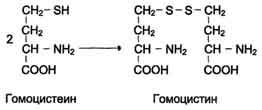
Гомоцистин может накапливаться в крови и тканях" выделяться с мочой, вызывая гомоцистинурию. Возможной причиной является наследственное нарушение обмена гомоцистеина либо гиповитаминоз фолиевой кислоты, а также витаминов В12 и В6. Из других биохимических нарушений можно отметить цистатионинурию, также часто возникающую при недостаточности витаминов группы В.
Биологические функции цистеина разнообразны и очень важны для организма. Так, цистеин, входящий в состав белков, играет необычайно важную роль в их фолдинге, поскольку тиогруппы цис способны образовывать прочную дисульфидную связь. При этом 2 остатка цистеина формируют молекулу цистина (см. схему В на с. 504).
Окислительная реакция протекает либо с участием кофермента NAD+ под действием фермента цистеинредуктазы, либо неферментативно. Дисульфидные связи стабилизируют пространственную структуру полипептидной цепи или связывают между собой 2 цепи (например, А- и В-цепи гормона инсулина). Очень многие белки и ферменты в активном центре содержат SH-группы, участвующие в катализе. При их окислении ферментативная активность падает (см. разделы 1, 2). Восстановление SH-групп часто
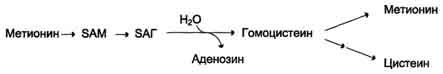
Схема А
503
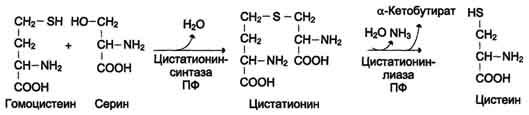
Схема Б
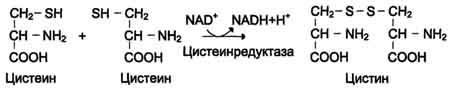
Схема В
происходит с использованием глутатиона - атипичного трипептида, содержащего γ-глутаминовую кислоту, цистеин и глицин (см. схему Г).
76. Метаболизм фенилаланина и тирозина.Заболевания,связанные с нар-м метаболизма фенилаланина и тирозина. Фенилаланин - незаменимая аминокислота, так как в клетках животных не синтезируется её бензольное кольцо. Тирозин - условно заменимая аминокислота, поскольку образуется из фенилаланина. Содержание этих аминокислот в пищевых белках (в том числе и растительных) достаточно велико. Фенилаланин и тирозин используются для синтеза многих биологически активных соединений. Фенилаланин используется в организме только в 2 процессах: включается в белки и превращается в тирозин.Превращение фенилаланина в тирозин прежде всего необходимо для удаления избытка фенилаланина, так как высокие концентрации его токсичны для клеток. Основной путь метаболизма фенилаланина начинается с его гидроксилирования, в результате чего образуется тирозин. Эта реакция катализируется специфической монооксигеназой - фенилаланингидроксилазой, коферментом которой служит тетрагидробиоптерин (Н4БП). Активность фермента зависит также от наличия Fe2+. Реакция необратима. Н4БП в результате реакции окисляется в дигидробиоптерин (Н2БП). Регенерация последнего происходит при участии дигидроптеридинредуктазы с использованием NADPH + H+. Обмен тирозина значительно сложнее, чем обмен фенилаланина. Кроме использования в синтезе белков, тирозин в разных тканях выступает предшественником таких соединений, как катехоламины, тироксин, меланины. В печени происходит катаболизм тирозина до конечных продуктов:фумарата и ацетоацетата. Фумарат включается в ЦТК, превращается в оксалоацетат и может использоваться в процессе глюконеогенеза. В пигментных клетках (меланоцитах) тирозин выступает предшественником тёмных пигментов - меланинов. Среди них преобладают 2 типа: эумеланины и феомеланины. Эумеланины – пигменты чёрного и коричневого цвета, феомеланины - жёлтые или красновато-коричневые полимеры.Заболевания: -фенилкетонурия(сопровождается накоплением фенилаланина и его токсических продуктов, что приводит к тяжёлому поражению ЦНС, проявляющемуся, в частности, в виде нарушения умственного развития; связано с резким снижением или полным отсутствием активности печёночного фермента фенилаланин-4-гидроксилазы, который в норме катализирует превращение фенилаланина в тирозин; -тирозинемия(1тип- дефект фермента фумарилацетоацетатгидролазы, катализирующего расщепление фумарилацетоацетата на фумарат и ацетоацетат;2тип- дефект фермента тирозинаминотрансферазы); -альбинизм(врождённый дефект тирозиназы. Этот фермент катализирует превращение тирозина в ДОФА в меланоцитах); -болезнь Паркенсона(развивается при недостаточности дофамина в чёрной субстанции мозга; снижена активность тирозингидроксилазы, ДОФА-декарбоксилазы).
77. Биосинтез пуриновых нуклеотидов.Синтез АМФ и ГМФ из ИМФ.«Запасные пути» синтеза.Катаболизм пуриновых нуклеотидов. Было установлено, что в формировании пуринового кольца принимают участие аминокислоты Асп, Гли, Глн, СО2 и два одноуглеродных производных тетрагидрофолата: метенил-Н4-фолат и формил-Н4-фолат. Центральное место в синтезе пуриновых и пиримидиновых нуклеотидов занимает 5-фосфорибозил-1-дифосфат (ФРДФ) или фосфорибозилпирофосфат (ФРПФ), который образуется из рибозо-5-фосфата и АТФ в реакции, которая катализируется ФРДФ-синтетазой. Он образуется за счёт переноса β,γ-пирофосфатного остатка АТФ на рибозо-5-фосфат в реакции, катализируемой ФРДФ-синтетазой. Источниками рибозо-5-фосфата могут быть: пентозофосфатный путь превращения глюкозы или катаболизм нуклеозидов, в ходе которого под действием нуклеозидфосфорилазы первоначально образуется рибозо-1-фосфат, а затем с помощью соответствующей мутазы фосфатный остаток переносится в 5-положение. Биосинтез пуриновых нуклеотидов происходит путем сборки пуринового гетероциклического основания на остатке рибозо-5-фосфата при участии простых предшественников: глицина, СО2, амидного азота глутамина, α-аминогруппы аспартата и одноуглеродных производных Н4-фолата. Первая специфическая реакция образования пуриновых нуклеотидов - перенос амидной группы Глн на ФРДФ с образованием 5-фосфорибозил-1 -амина. Эту реакцию катализирует фермент амидофосфорибозилтрансфераза. При этом формируется β-N-гликозидная связь. Затем к аминогруппе 5-фосфорибозил-1-амина присоединяются остаток глицина, N5,N10-метенил-Н4-фолата ещё одна амидная группа глутамина, диоксид углерода, аминогруппа аспартата и формильный остаток N10-формил Н4-фолата. Результатом этой десятистадийной серии реакций является образование первого пуринового нуклеотида - инозин-5'-монофосфата (ИМФ), на синтез которого затрачивается не менее шести молекул АТФ. Все реакции протекают в цитозоле клетки. Остальные пуриновые нуклеотиды – АМФ и ГМФ образуются из ИМФ. Синтез АМФ и ГМФ из ИМФ. АМФ синтезируется при участии аденилосукцинатсинтетазы и аденилосукциназы, ГМФ - при участии ИМФ-дегидрогеназы и ГМФ-синтетазы. Аденилосукцинатсинтетаза, используя энергию ГТФ, присоединяет аспартат к ИМФ с образованием аденилосукцината, который в реакции, катализируемой аденилосукциназой, отщепляет фумарат и превращается в АМФ. Второй пуриновый нуклеотид (ГМФ) образуется также в 2 стадии. Сначала ИМФ окисляется NAD+-зависимой ИМФ-дегидрогеназой с образованием ксантозин-5'-монофосфата (КМФ). Последующее трансамидирование гидроксильной группы при С2-пуринового кольца КМФ катализирует ГМФ-синтетаза с использованием амидной группы Глн и энергии АТФ. При образовании пуриновых нуклеотидов ГТФ расходуется на синтез АМФ, а АТФ - на синтез ГМФ, что помогает поддерживать в клетках баланс адениловых и гуаниловых нуклеотидов. Печень - основное место образования пуриновых нуклеотидов, откуда они могут поступать в ткани, не способные к их синтезу: эритроциты и мозг. В периоды активного роста тканей синтез пуриновых нуклеотидов из простых предшественников не способен полностью обеспечить нуклеиновые кислоты субстратами. Заметную роль в этих условиях играют ферменты "запасных" путей синтеза этих молекул. Наибольшее значение в этом процессе имеют ферменты, осуществляющие превращение пуринов в мононуклеотиды с использованием ФРДФ как донора остатка фосфорибозы. ФРДФ-зависимое фосфорибозилирование пуринов катализируют 2 фермента: -аденинфосфорибозилтрансфераза, обеспечивающая образование АМФ из аденина и ФРДФ; -гипоксантин-гуанинфосфорибозилтрансфераза, катализирующая превращение азотистых оснований гипоксантина и гуанина в ИМФ и ГМФ с использованием ФРДФ в качестве донора фосфорибозы; У человека основной продукт катаболизма пуриновых нуклеотидов - мочевая кислота. Её образование идёт путём гидролитического отщепления фосфатного остатка от нуклеотидов с помощью нуклеотидаз или фосфатаз. От АМФ и аденозина аминогруппа удаляется гидролитически аденозиндезаминазой с образованием ИМФ или инозина. ИМФ и ГМФ превращаются в соответствующие нуклеозиды: инозин и гуанозин под действием 5´-нуклеотидазы. Пуриннуклеозидфосфорилаза катализирует расщепление N-гликозидной связи в инозине и гуанозине с образованием рибозо-1-фосфата и азотистых оснований: гуанина и гипоксантина. Гуанин дезаминируется и превращается в ксантин, а гипоксантин окисляется в ксантин с помощью ксантиноксидазы, которая катализирует и дальнейшее окисление ксантина в мочевую кислоту. Ксантиноксидаза - аэробная оксидоредуктаза, простетическая группа которой включает ион молибдена, железа (Fe3+) и FAD. Аллопуринол-противоподагрическое средство, ограничивающее синтез мочевой кислоты. Ингибирует фермент ксантиноксидазу и окисление эндогенных пуринов, в результате чего уменьшается концентрация мочевой кислоты и ее солей в плазме крови и моче. Пода́гра-гетерогенное по происхождению заболевание, которое характеризуется отложением в различных тканях организма кристаллов уратов в форме моноурата натрия или мочевой кислоты. В основе возникновения лежит накопление мочевой кислоты и уменьшение её выделения почками, что приводит к повышению концентрации последней в крови (гиперурикемия).Ксантинурия-выделение с мочой аномально большого количества производной пурина ксантина; обычно развивается в результате врожденного нарушения обмена веществ, вследствие недостаточности ксантин дегидрогеназы.
78. Синтез пиримидиновых нуклеотидов.Образование УМФ.«Запасные пути»,катаболизм. Пиримидиновое кольцо синтезируется из простых предшественников: глутамина, СО2 и аспарагиновой кислоты и затем связывается с рибозо-5-фосфатом, полученным от ФРДФ. Процесс протекает в цитозоле клеток. Синтез ключевого пиримидинового нуклеотида - УМФ идёт с участием 3 ферментов, 2 из которых полифункциональны.Ключевой, регуляторной реакцией в синтезе пиримидиновых нуклеотидов является синтез карбамоилфосфата из глутамина, СО2 и АТФ, в реакции катализируемой карбамоилфосфатсинтетазой II (КФС II), которая протекает в цитозоле клеток. В реакции NH2-гpyппa карбамоилфосфата образуется за счёт амидной группы глутамина, что отличает эту реакцию от реакции синтеза карбамоилфосфата в митохондриях в процессе синтеза мочевины из СО2, NH3 и АТФ с участием КФС I. Карбамоилфосфат, использующийся на образование пиримидиновых нуклеотидов, является продуктом полифункционального фермента, который наряду с активностью КФС II содержит каталитические центры аспартаттранскарбамоилазы и дигидрооротазы. Этот фермент назвали "КАД-фермент".Почти весь синтезированный в первой реакции карбамоилфосфат взаимодействует с аспартатом и образование карбамоиласпартата, от которого отщепляется вода и образуется циклический продукт - дигидрооротат. Отщепляясь от КАД-фермента, дигидрооротат подвергается дегидрированию NAD-зависимой дигидрооротатдегидрогеназой и превращается в свободное пиримидиновое основание - оротовую кислоту, или оротат. В цитозоле оротат становится субстратом бифункционального фермента - УМФ-синтазы, которая обнаруживает оротатфосфорибозилтрансферазную и ОМФ-декарбоксилазную активности. Первоначально фосфорибозильный остаток от ФРДФ переносится на оротат и образуется нуклеотид - оротидин-5'-монофосфат (ОМФ), декарбоксилирование которого даёт уридин-5-монофосфат (УМФ). Часть ЦМФ может превращаться в УМФ под действием цитидиндезаминазы и пополнять запасы уридиловых нуклеотидов. Цитидиловые нуклеотиды могут гидролитически терять аминогруппу и превращаться в УМФ. Когда от УМФ при участии нуклеотидазы (или фосфатазы) и уридинфосфорилазы отщепляются неорганический фосфат и рибоза, то остаётся азотистое основание - урацил. Пиримидиновые основания при участии дигидропиримидиндегидрогеназы присоединяют 2 атома водорода по двойной связи кольца с образованием дигидроурацила или дигидротимина. Оба гетероцикла могут взаимодействовать с водой в реакции, катализируемой дигидропиримидинциклогидролазой, и дигидроурацил превращается в β-уреидопропионовую кислоту, а дигидротимин - в β-уреидоизомасляную кислоту. Оба β-уреидопроизводных под действием общего для них фермента уреидопропионазы расщепляются с образованием СО2, NH4+ и β-аланина или β-аминоизомасляной кислоты соответственно. β-Аланин обнаруживают в плазме крови и многих тканях. Он используется в мышцах на образование дипептидов: карнозина и анзерина. Под действием бактериальной микрофлоры кишечника β-аланин включается в пантотеновую кислоту, которая всасывается и используется на образование КоА.
