
- •7. Биосинтез пиримидиновых мононуклеотидов.
- •8. Биосинтез нуклеозидтрифосфатов.
- •9. Биосинтез дезоксирибонуклеотидов.
- •10. Синтез нуклеиновых кислот.
- •11. Структура и биологическая роль нуклеотидов и нуклеиновых кислот.
- •12. Биосинтез днк (репликация); условия, этапы, репарация.
- •13. Биосинтез рнк (транскрипция); условия, этапы, обратная транскрипция.
- •3 Этапа процесса:
- •14. Созревание и синтез транскрипта.
- •15. Процессинг тРнк и р рнк.
- •16. Биосинтез белка (трансляция); этапы, регуляция , и генетический код.
- •17. Нарушение процесса трансляции.
- •18. Факторы, определяющие состояние белкового обмена. Синтез аммонийных солей.
- •19. Общие пути обмена аминокислот. Биосинтез аминокислот.
- •20. Реакции трансаминирования, Дезаминирование. Синтез мочевины.
- •21. Метаболизм глюкозы.
- •22. Расчет выхода атф при анаэробном окислении глюкозы.
- •23. Расчет выхода атф при аэробном окислении.
- •24. Биологическое значение и классификация липидов.
- •26. Биосинтез жирных кислот, химизм, ферменты.
- •27. Биосинтез жирных кислот с длинной цепью углеродных атомов и непредельных.
- •28. Биосинтез триглицеридов, фосфолипидов и холестерина.
- •29. Синтез и распад кетоновых тел.
- •30. Этапы энергетического обмена.
- •31. Цикл Кребса.
- •32. Энергетический баланс одного оборота цтк.
- •33. Тканевое дыхание и окислительное фосфорилирование.
- •3 4. Компоненты системы синтеза атф в митохондриях
- •35. Хемиосмотическая теория окислительного фосфорилирования.
- •36. Механизм окислительного фосфорилирования. Короткий вариант 36 вопроса
- •Подробный вариант 36 вопроса
- •37. Регуляция энергетического обмена.
- •38. Другие пути использования кислорода.
- •39. Пути использования кислорода в реакциях биологического окисления.
- •40. Сравнительная характеристика путей синтеза пуриновых и пиримидиновых нуклеотидов.
3 4. Компоненты системы синтеза атф в митохондриях
35. Хемиосмотическая теория окислительного фосфорилирования.
Для объяснения механизма окислительного фосфорилирования в 1961 г. П. Митчеллом была предложена хемиосмотическая теория. В обобщенном виде суть хемиосмотической теории можно представить следующим образом: внутренняя мембрана митохондрий разделяет потоки ē и Н+ – первые транспортируются вдоль мембраны, вторые – поперек, при этом создается трансмембранный электрохимический потенциал, обусловленный разностью зарядов и концентраций протонов в матриксе и межмембранном пространстве митохондрий. Энергия этого электрохимического потенциала используется АТФ-синтазой для синтеза АТФ из АДФ и фосфата, т. е. для фосфорилирования. Согласно концепции П. Митчелла тканевое дыхание и окислительное фосфорилирование сопряжены, а сопрягающим звеном между ними служит электрохимический потенциал: дыхание создает его, а фосфорилирование расходует.
При переносе Н+ из матрикса в межмембранное пространство на внутренней мембране создается осмотический градиент протонов (химический потенциал) рН = 60 мВ (при рН = 1) (в матриксе рН выше, чем в межмембранном пространстве). Так как каждый Н+ несет положительный заряд, на внутренней мембране также появляется разность электрических потенциалов V= 160 мВ, внутренняя сторона мембраны заряжается отрицательно, внешняя – положительно. В сумме осмотический градиент протонов и разность потенциалов образуют электрохимический потенциал, который составляет около 220 мВ.
Энергия образовавшегося на внутренней мембране митохондрий электрохимического потенциала может использоваться для фосфорилирования АДФ в АТФ, транспорта веществ через мембрану митохондрий и теплопродукции.
36. Механизм окислительного фосфорилирования. Короткий вариант 36 вопроса
На основании строения и функций компонентов дыхательной цепи предложен механизм окислительного фосфорилирования:
1. Ферменты дыхательной цепи расположены в строго определенной последовательности: каждый последующий белок обладает большим сродством к электронам, чем предыдущий (он более электроположителен, т.е. обладает более положительным окислительно-восстановительным потенциалом). Это обеспечивает однонаправленное движение электронов.
2. Все атомы водорода, отщепленные дегидрогеназами от субстратов в аэробных условиях, достигают внутренней мембраны митохондрий в составе НАДН или ФАДН2.
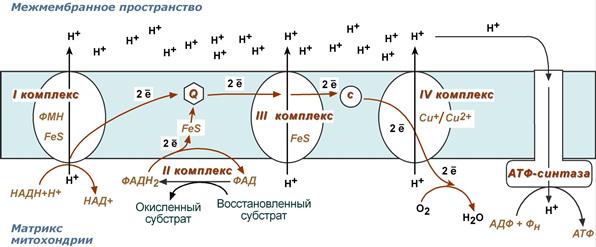
3. Здесь атомы водорода (от НАДН и ФАДН2) передают свои электроны в дыхательную ферментативную цепь, по которой электроны движутся (50-200 шт/сек) к своему конечному акцептору – кислороду. В результате образуется вода.
4. Поступающие в дыхательную цепь электроны богаты свободной энергией. По мере их продвижения по цепи они теряют энергию.
Часть энергии электронов используется I, III, IV комплексами дыхательных ферментов для перемещения ионов водорода через мембрану в межмембранное пространство. Другая часть рассеивается в виде тепла. Упрощенно сказанное можно представить в виде равенства:

5. Перенос ионов водорода через мембрану (выкачивание) происходит не случайно, а в строго определенных участках мембраны. Эти участки называются участки сопряжения (или, не совсем точно, пункты фосфорилирования). Они представлены I, III, IV комплексами дыхательных ферментов. В результате работы этих комплексов формируется градиент ионов водорода между внутренней и наружной поверхностями внутренней митохондриальной мембраны. Такой градиент обладает потенциальной энергией.
6. Как завершение всех предыдущих событий и необходимый их результат происходит наработка АТФ: ионы H+ теряют свою энергию, проходя через АТФ-синтазу (Н+-транспортирующая АТФ-аза, КФ 3.6.3.14.). Часть этой энергии тратится на синтез АТФ. Другая часть рассеивается в виде тепла:
![]()
Механизм работы АТФ-синтазы получил название вращательный катализ.
