
- •Силикаты – это соли кремниевых кислот. Они твердые тугоплавкие вещества, не имеющие окраски.
- •Общие химические свойства металлов
- •2. Реакции металлов с кислотами:
- •3. Взаимодействие металлов с водой:
- •4. Вытеснение более активными металлами менее активных металлов из растворов их солей:
- •Область применения
- •В реакциях присоединения полярных молекул типа НХ к несимметричным алкенам водород присоединяется к более гидрогенизированному атому углерода при двойной связи (т.е. атому углерода, связанному с наибольшим числом атомов водорода).
- •Реакции окисления алкенов
- •4. Окисление в присутствии солей палладия:
- •Классификация, номенклатура, изомерия
- •1. Кумулированные:
- •Номенклатура
- •2. Международная
- •В присутствии солей меди (I) и кислоты ацетилен легко димеризуется и далее тримеризуется:
- •Образование дисульфидов и их роль в биохимических процессах
- •Жиры
- •СЛОЖНЫЕ ЛИПИДЫ
- •1. Взаимодействие внутри молекулы – образование внутренних солей (биполярных ионов)
- •2. Взаимодействие с основаниями и кислотами
- •5. Качественные реакции!
- •5.1.1 Основный понятия и постулаты термодинамики
- •Исходные постулаты (положения) термодинамики. Пусть дан изолированный сосуд (рисунок 5.1.2), который разделен полупроницаемой перегородкой. В первой части сосуда температура Т1, во второй – температура Т2; Т1 > Т2.
- •5.1.2 Первый закон термодинамики, его формулировки
- •5.1.3 Термохимия
- •5.2.1 Второй закон термодинамики
- •5.2.2 Фундаментальные уравнения термодинамики
- •5.4.1 Предмет химической кинетики.
- •5.4.2 Основные понятия химической кинетики.
- •5.4.3 Кинетический закон действия масс – основной постулат химической кинетики.
- •5.4.4 Кинетические особенности протекания простых реакций.
- •5.4.5 Методы определения порядка реакции и константы скорости по экспериментальным данным.
- •5.4.6 Кинетические особенности протекания сложных реакций.
- •5.4.7 Зависимость скорости реакции от температуры.
- •5.4.8 Кинетика цепных реакций.
- •5.4.9 Кинетика фотохимических реакций.
- •5.4.10 Основы кинетики гетерогенных процессов.
- •5.4.11 Катализ.
- •5.4.1 Предмет химической кинетики
- •Химическая кинетика решает следующие задачи, перечисленные в порядке сложности их решения:
- •5.4.2 Основные понятия химической кинетики
- •АНАЛИЗ СМЕСИ АНИОНОВ
- •МЕТОДЫ КОЛИЧЕСТВЕННОГО АНАЛИЗА
- •Титриметрические методы анализа
- •Кислотно-основное титрование
- •Окислительно-восстановительное титрование
- •Перманганатометрия. Стандартизация рабочего раствора перманганата калия
- •Комплексонометрическое титрование
- •Определение общей жесткости воды
- •1. Предмет аналитической химии.
- •2. Краткая история развития аналитической химии.
- •3. Методы аналитической химии.
- •4. Основные стадии химического анализа.
- •5. Статистическая обработка результатов измерений.
- •6. Отбор проб.
- •7. Потери и загрязнения при отборе пробы. Хранение пробы.
- •8. Подготовка пробы к анализу.
- •9. Аналитическая реакция и её характеристики.
- •10. Дробный и систематический анализ.
- •37. Сущность гравиметрического анализа.
- •38. Типы гравиметрических определений.
- •39. Теория осаждения.
- •40. Операции гравиметрического анализа.
- •41. Расчеты в гравиметрическом анализе.

545
водорода или галогена. Обе кислоты, присоединяя водород, переходят в стеариновую кислоту.
Жиры
Жиры являются сложными эфирами глицерина и высших алифатических кислот, то есть триацилглицеринами, или триглицеридами.
Общая формула :
CH2 – O–COR
CH – O–COR
CH2 – O–COR
В состав жиров и масел обычно входят кислоты: предельные – пальмитиновая и стеариновая, непредельные – олеиновая, линолевая, линоленовая и др. Могут входить в состав жиров и высшие оксикислоты,
например рицинолевая СН3(СН2)5СНОН – СН = СН(СН2)7СООН
(касторовое масло).
Триацилглицерины бывают простыми и смешанными: простые включают остатки одинаковых кислот, смешанные — разных. Встречаются жиры, триглицериды которых состоят одновременно из насыщенных и ненасыщенных кислот. Например, свиной жир (сало) состоит в основном из триглицеридов олеиновой, пальмитиновой и стеариновой кислот, а коровье масло — из триглицеридов олеиновой, пальмитиновой, масляной, миристиновой и стеариновой кислот.
По консистенции жиры могут быть твердыми и жидкими. Твердые жиры содержат преимущественно остатки насыщенных высших жирных кислот. В состав жидких жиров, обычно называемых маслами, входят в основном остатки ненасыщенных кислот. Чем длиннее цепь остатка непредельных кислоты и чем она более насыщенна, тем вше температура плавления жира, так что по последней можно судить о содержании непредельных кислот. Жиры животного происхождения, как правило, — твердые вещества, растительные жиры — жидкие. Исключения составляют рыбий жир, являющийся жидкостью, и масло какао — твердое вещество (при обычных условиях). В молекулах как растительных, так и животных жиров (за исключением свиного) чаще всего остатки непредельных кислот занимают положение 2.
Жиры являются необходимой и весьма ценной составной частью пищи. С жирами организм получает значительно большое количество энергии, чем с таким же количеством белков и углеводов (по массе и объему). При усвоении 1 г жира выделяется 38,9 кДж.
Кислоты с несколькими двойными связями (линолевая, линоленовая) синтезируются только растениями и поэтому являются незаменимыми компонентами пищи.

546
Номенклатура и изомерия жиров. По систематической номенклатуре IUPAC родоначальной структурой в молекуле жира является глицерин. Ацильные остатки жирных кислот перечисляют в начале названия в алфавитном порядке, если необходимо, употребляют множительные приставки ди- и три-. Тривиальные названия жиров образуют из приставок, построенных из названий соответствующих жирных кислот путем опускания части названия кислоты -иновая кислота и добавления суффикса -ин:
CH2 – O – CO – C17H35 |
CH2 – O – CO – C17H23 |
||
|
|
|
|
CH – O – CO – C17H35 |
CH – O – CO – C15H31 |
||
CH2 – O – CO – C17H35 |
CH2 – O – CO – C17H35 |
||
Тристеароилглицерин; |
1-лауроил-2-палмитоил-3- |
||
|
тристеарин |
|
стеароил-глицерин; |
|
|
1-лауро-2-палмитостеарин |
|
Примеры смешанных триглецеридов – пальмитоолеостеарин, содержащий остатки пальмитиновой, олеиновой и стеариновой кислот, и диолеостеарин с двумя остатками олеиновой и одним остатком стеариновой кислот:
α СН2—O—CО—С15Н31 |
СН2—O—CО—С17Н33 |
| |
| |
β CH —O—CО—С17Н33 |
СН2—O—CО—С17Н35 |
| |
| |
α' CH2—O—CО—С17Н35 |
СН2—O—CО—С17Н33 |
α-пальмито-β-олео- |
α, α' –диолео-β-стеарин |
-α'-стеарин |
|
Изомерия жиров связана в основном с различным взаимным расположением ацильных остатков в структуре триацилглицерина
(структурная изомерия).
Молекулы смешанных триглицеридов, содержащие асимметрический атом углерода, существуют в виде двух оптических изомеров. Для жиров, молекулы которых содержат остатки непредельных кислот, характерна
геометрическая изомерия.
Физические свойства жиров
Физические свойства жиров определяются строением жирных кислот, образующих их молекулы. Так, температуры плавления жиров, содержащих остатки ненасыщенных кислот, значительно ниже, чем у насыщенных жиров с тем же числом атомов углерода. С увеличением длины углеродных цепей жирных кислот температуры плавления жиров повышаются. Большинство
547
жиров плавится при температуре 22–55 °С.
Жиры легкорастворимы в углеводородах и их хлорпроизводных, эфирах, кетонах, малорастворимы в этиловом спирте (исключение составляет касторовое масло, растворимое в этаноле), нерастворимы в воде, однако в присутствии поверхностно-активных веществ (ПАВ), называемых эмульгаторами, жиры образуют высокодисперсные гетерогенные системы типа эмульсий. В частности, эмульгирующее действие белков придает стабильность эмульсии молочного жира в воде — молоку.
Химические свойства жиров.
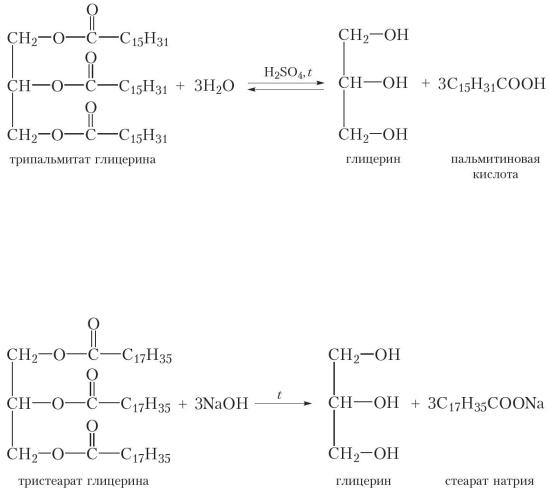
1. Гидролиз (щелочной гидролиз называют омылением):
Приведём уравнение реакции кислотного гидролиза на примере триглицерида пальмитиновой кислоты:
Практически гидролиз жиров производят или перегретым паром, или же нагреванием в присутствии серной кислоты или щелочей. Например, при гидролизе триглицерида стеариновой кислоты раствором гидроксида натрия образуется натриевая соль стеариновой кислоты — стеарат натрия:
В семенах клещевины находится особый фермент – липаза, ускорающий гидролиз жиров. Липаза широко применяется в технике каталитического гидролиза жиров.
2. Реакции присоединения.
Двойные связи непредельных кислот, входящих в состав жира, могут быть прогидрированы каталитическим путем, они присоединяют бром и иод.
3. Прогоркание. Многие жиры при стоянии на воздухе прогоркают – приобретают неприятный вкус и запах. Различают два типа прогоркания –
