
- •Разделение гомогенных систем
- •Основное уравнение массопередачи. Уравнения движущей силы. Коэффициент массопередачи.
- •Уравнения массоотдачи. Коэффициент массоотдачи.
- •Соотношение коэффициентов массопередачи и массоотдачи. Лимитирование сопротивления массопереоноса.
- •Теоретическая ступень разделения (теоретическая тарелка).
- •Критерий Шервуда.
- •Критерий Шмидта
- •С редняя движущая сила массопередачи при линейных рабочей и равновесных линиях.
- •Кпд по Мэрфи.
- •Кинетическая кривая. Определение высоты массообменных аппаратов со ступенчатым контактом фаз.
- •Минимальный и оптимальных расход поглотителя при абсорбции.
- •Работа насадочных колонн в различных гидродинамических режимах.
- •Построение рабочих линий непрерывной ректификации
- •Флегмовое число. Влияние на размер колонны и расход пара.
- •Основные допущения расчета непрерывной ректификации.
- •Сопоставление тарельчатых и насадочных колонных аппаратов:
- •Принцип устройства и схема действия насадочного абсорбера. Сравнение с тарельчатым.
- •Насадочная ректификационная колонна. Типы, конструкции и требования к насадкам.
- •А бсорбционная колонна с провальными тарелками.
- •А бсорбер с ситчатыми тарелками с переточными устройствами.
- •А бсорбер с клапанными тарелками.
- •Абсорбер с колпачковыми тарелками.
- •Р аспылительный абсорбер.
- •У становка для простой перегонки.
- •Установка непрерывной ректификации.
- •Ректификационная колонна с клапанными тарелками.
- •Ректификационная колонна с провальными ситчатыми тарелками.
- •Гидромеханические процессы
- •Критерий Архимеда для осаждения.
- •Гидродинамические режимы обтекания тел.
- •Зависимость состояния зернистого слоя от скорости восходящего потока.
- •Расчет диаметра аппарата с зернистым слоем.
- •Приведите последовательность расчета диаметра и гидравлического сопротивления аппарата с псевдоожиженным слоем.
- •Приведите уравнение фильтрования в дифференциальной форме. Охарактеризуйте входящие величины. Какие возможны способы проведения процесса фильтрования?
- •Основные способы разделения суспензий. Охарактеризуйте каждый из способов, укажите области применения.
- •Основные способы очистки газов от пыли. Охарактеризуйте каждый из способов, укажите области применения.
- •Нутч-фильтры.
- •Барабанный вакуум-фильтр.
- •Фильтрующая центрифуга.
- •Рукавный фильтр.
- •Одноярусный гребковый отстойник.
- •Циклон.
- •Батарейный циклон.
- •Г идроциклон.
- •Электрофильтр.
- •Барботажный пылеуловитель.
Разделение гомогенных систем

Вторые вопросы
Основное уравнение массопередачи. Уравнения движущей силы. Коэффициент массопередачи.
Массопередача — перенос вещества внутри одной фазы к границе раздела, через границу раздела и перенос вещества внутри другой фазы.
M![]() =Ky*Δуср*F
=Ky*Δуср*F
M=Ky*Δхср*F – основные уравнения массопередачи,
Где: М – кол-во переносимых компонентов;
F – поверхность соприкосновения;
Δу/х – средняя движущая сила
K![]() у/Kх
- коэффициенты массопередачи, определяют
массу распределяемого вещества,
переходящего из одной фазы в другую за
единицу времени через единицу поверхности
контакта фаз при движущей силе равной
единице. (характеризует скорость процесса
переноса вещества из одной фазы в другую)
Размерность зависит от размерности
движущей силы.
у/Kх
- коэффициенты массопередачи, определяют
массу распределяемого вещества,
переходящего из одной фазы в другую за
единицу времени через единицу поверхности
контакта фаз при движущей силе равной
единице. (характеризует скорость процесса
переноса вещества из одной фазы в другую)
Размерность зависит от размерности
движущей силы.

Средняя
движущая сила массопередачи:
![]()
(при кривой линии равновесия)
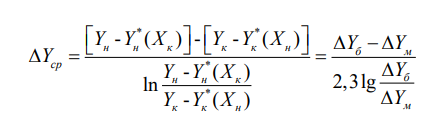
Для прямой линии равновесия:
Уравнения массоотдачи. Коэффициент массоотдачи.
Массоотдача — процесс переноса вещества внутри одной фазы к границе раздела или от нее.
П ри
переносе вещества из газовой фазы в
жидкую:
ри
переносе вещества из газовой фазы в
жидкую:
Где: М – кол-во переносимых компонентов;
F – поверхность соприкосновения;
β у и βх - коэффициенты массоотдачи по фазам, характеризуют количество вещества, передаваемого совместно диффузией и конвекцией через единицу поверхности в единицу времени при разности концентраций внутри фазы и на границе раздела равной единице. (Размерность такая же, как и коэффициента массопередачи - зависит от размерности движущей силы).
Соотношение коэффициентов массопередачи и массоотдачи. Лимитирование сопротивления массопереоноса.
С оотношение
коэффициентов выводится из дифференциальной
формы уравнений массопереноса.
оотношение
коэффициентов выводится из дифференциальной
формы уравнений массопереноса.
Э то
- уравнение аддитивности фазовых
диффузионных сопротивлений. Это уравнение
свидетельствует, что общее сопротивление
массопередаче складывается из частных
сопротивлений в фазах.
то
- уравнение аддитивности фазовых
диффузионных сопротивлений. Это уравнение
свидетельствует, что общее сопротивление
массопередаче складывается из частных
сопротивлений в фазах.
m – коэффициент распределения (тангенс угла касательной к равновесной линии).
r![]()
 —
фазовые диффузионные сопротивления;
—
фазовые диффузионные сопротивления;
R — общее диффузионное сопротивление, выраженное в единицах газовой фазы.
П оложение
линий равновесия:
оложение
линий равновесия:
1. Хорошо растворимый газ. Например, аммиак в воде (NH3-H2O) ; хлористый
водород в воде (HCl-H2O). В этом случае m-мало, rx – очень мало. Все сопротивление массопередаче сосредоточено в газовой фазе Ky≈βу. Процесс переноса определяется скоростью диффузии вещества в газовой фазе (лимитируется газовой фазой). Процесс в жидкости идет очень быстро. Для увеличения массопереноса надо турбулизировать поток газа.
2. Плохо растворимые газы. Например, N2; O2; CO2 в воде.
В этом случае m-велико; тогда ry- очень мало.
Тогда: Kx≈βx. Все сопротивление сосредоточено в жидкой фазе и именно ее необходимо турбулизировать.
Теоретическая ступень разделения (теоретическая тарелка).
Т![]() еоретическая
ступень разделения — аппарат или часть
аппарата, из которого выходят фазы,
находящиеся в состоянии равновесия.
(Изменение состава пара в объеме тарелки)
еоретическая
ступень разделения — аппарат или часть
аппарата, из которого выходят фазы,
находящиеся в состоянии равновесия.
(Изменение состава пара в объеме тарелки)
Состояние равновесия для n-го участка:
Расчет можно выполнить графически:


Чем больше теоретических тарелок доступно в колонке, тем больше уравновешивания между неподвижной и подвижной фазами и тем лучше качество разделения. Условием эффективного разделения является высокое значение числа теоретических тарелок (N) и низкое значение высоты теоретической тарелки (H).
Расчёт массообменного процесса сводится к определению минимально необходимого (при заданных материальных потоках) числа теоретических тарелок (теоретических ступеней разделения), после чего определяется необходимое количество реальных массообменных устройств с учётом их КПД.
