
- •1. Предмет патологической анатомии и методы исследования.
- •3. Уровни морфологического исследования в патанатомии.
- •4. Роль патологической анатомии в системе подготовки будущего врача и задачи патологической анатомии в практическом здравоохранении.
- •2. История развития патологической анатомии.
- •3. Патология клетки. Патология ядра, цитоплазмы.
- •1. Патология клетки как структурная основа болезней. Неспецифическая и специфическая патология клетки.
- •2. Патология митоза; хромосомные аберрации.
- •4. Дегенеративные процессы. Дистрофии. 1. Классификация дегенеративных процессов, взаимосвязь их разных форм. 2. Дистрофии, определение понятия, причины развития.
- •4. Классификация дистрофических процессов.
- •5. Исходы дистрофий.
- •5. Паренхиматозные белковые дистрофии.
- •2. Паренхиматозные белковые дистрофии: виды, механизмы развития.
- •6. Паренхиматозные жировые дистрофии.
- •2. Гистохимические методы выявления жира в тканях.
- •7. Паренхиматозные углеводные дистрофии.
- •5. Морфология нарушения обмена гликопротеидов.
- •8. Стромально - сосудистые дистрофии.
- •9. Гиалиноз.
- •3. Гиалиноз сосудов, клинические примеры.
- •10. Амилоидоз.
- •2. Морфогенетические механизмы образования alи aa-форм амилоида.
- •2. Основные гистохимические методы выявления в тканях амилоида.
- •3. Клинико-анатомическая классификация амилоидоза.
- •4. Вторичный амилоидоз, типичные органные поражения.
- •11. Стромально - сосудистые жировые дистрофии.
- •2) Местное ожирение - причины развития, клинические примеры.
- •4) Типы общего ожирения.
- •5) Связь общего ожирения с другими болезнями; клиническое значение ожирения, причины смерти
- •12. Смешанные дистрофии.
- •2. Гемоглобиногенные пигменты: виды, локализация, свойства.
- •5. Первичный гемохроматоз, морфологические изменения, причины смерти.
- •13. Патология обмена билирубина.
- •1. Желтухи - определение понятия и пигменты, их обусловливающие.
- •2. Надпеченочная желтуха, механизм развития, изменения мочи и стула.
- •14. Нарушение обмена меланина и липидогенных пигментов.
- •15. Нарушения обмена нуклеопротеидов и соединений кальция.
- •25. Стаз. 1. Определение понятия. 2-3. Причины возникновения, стадийность развития; виды стаза. 4. Сладж-феномен; обратимость стаза. 5. Вторичные расстройства кровообращения; связь стаза с шоком.
- •37. Иммунопатологические процессы. Аутоиммунные болезни.
- •38. Иммунопатологические процессы. Иммунодефициты.
- •39. Регенерация.
- •2. Уровни регенерации, примеры.
- •Физиологическая и репаративная регенерация, примеры.
- •40. Заживление повреждений. Склероз. Патологическая регенерация.
- •41. Процессы адаптации (приспособления) и компенсации.
- •3. Виды компенсаторных процессов.
- •5. Морфологические основы быстро и постепенно развиваюшщейся декомпенсации. Морфология сердца в стадии декомпенсации.
- •42. Компенсаторные процессы. Перестройка.
- •2. Виды гипертрофии.
- •43. Атрофия.
- •3. Виды местной атрофии.
- •4. Общая атрофия - причины развития, морфология.
- •44. Опухоли. Теории развития. Морфология опухолевой клетки и ткани.
- •2. Теории развития опухолей: теория онкогенов, теория эмбриональных зачатков Конгейма.
- •3. Морфологические проявления опухолевой трансформации клетки. Понятие об атипизме.
- •4. Виды морфологического атипизма.
- •3.Ультраструктурный атипизм
- •5. Атипизм в доброкачественных и злокачественных опухолях.
- •45. Морфогенез опухолей.
- •4. Макроскопические формы опухолей.
- •5. Механизмы противоопухолевой резистентности
- •46. Гистологическая классификация опухолей. Доброкачественные и злокачественные опухоли.
- •1. Гистологическая классификации опухолей.
- •Клинико-морфологические отличия доброкачественных и злокачественных опухолей.
- •3. Метастазирование и его виды.
- •47. Доброкачественные и злокачественные эпителиальные опухоли.
- •4. Органоспецифические эпителиальные опухоли - локализация, клинические проявления.
- •48. Доброкачественные и злокачественные опухоли из мезенхимальной ткани.
- •1. Опухоли соединительной ткани. Фиброматозы.
- •2. Опухоли мышечной и жировой ткани.
- •3. Опухоли сосудов.
- •4. Опухоли костной и хрящевой ткани.
- •49. Опухоли меланинообразующей ткани. Опухоли из апуд-системы.
- •5. Терминология опухолей из апуд-системы и клинические примеры наиболее частых их локализаций.
- •50. Опухоли нервной ткани и оболочек мозга.
- •1. Нейроэктодермальные опухоли цнс: классификация.
- •2. Олигодендроглиальные опухоли
- •3.Эпендимальные опухоли и опухоли хориоидного эпителия
- •4. Нейрональные опухоли
- •5.Низкодифференцированные и эмбриональные опухоли
- •4. Терминология опухолей вегетативной и периферической нервной системы.
- •5. Особенности опухолей у детей. Реверсия опухолей.
- •51. Нозология. Понятие о болезни. Диагноз.
- •3. Критика "функциональных" и "структурных" болезней.
- •4. Классификации болезней.
- •52. Рак желудка.
- •2. Топография ракового процесса в желудке.
- •3. Классификация по внешнему виду и гистологические типы.
- •4. Закономерности лимфогенного и гематогенного метастазирования.
- •5. Осложнения и причины смерти.
- •53. Рак лёгкого.
- •54. Рак молочной железы.
- •2. Макроскопическая характеристика различных типов рака.
- •3. Гистологические типы раков. Рак Педжета.
- •55. Рак матки.
- •56. Опухолевые заболевания кроветворной ткани.
- •2. Основные виды гематосарком и их типичная локализация.
- •57. Патанатомия острых форм лейкозов.
- •4. Особенности острого лейкоза у детей.
- •58. Хронические лейкозы.
- •59. Злокачественные лимфомы.
- •4. Гистологические формы лимфогранулематоза и прогноз заболевания.
- •72. Острый бронхит. Бронхопневмония.
- •5. "Болезнь легионеров" - возбудитель, эпидемиология, характерные морфологические изменения легких.
- •73. Крупозная пневмония.
- •74. Хронические неспецифические заболевания лёгких.
- •75. Альвеолярная эмфизема лёгких. Интерстициальные болезни легких.
- •76. Пневмокониозы. Пневмофиброзы.
- •5. Пневмофиброзы - классификация, морфологические изменения легких. Понятие о циррозе легкого.
- •85. Гломерулонефрит.
- •2. Этиология и патогенез. Роль иммунопатологических реакций.
- •3. Топография воспаления в клубочках.
- •4. Патоморфология острого и подострого гломерулонефрита.
- •5. Хронический гломерулонефрит, морфология его типов. Исходы и причины смерти.
- •86. Первичный нефротический синдром.
- •1. Первичный нефротический синдром - определение понятия, классификация.
- •5. Осложнения и причины смерти при первичном нефротическом синдроме.
- •87. Острый тубулярный некроз (острая почечная недостаточность).
- •5. Подагрическая нефропатия и поражение почек при множественной миеломе.
- •88. Интерстициальные болезни почек.
- •3. Пиелонефрит - определение понятия, классификация, пути проникновения инфекции в почку.
- •4. Патоморфология почек при остром пиелонефрите, его варианты.
- •5. Патоморфология почек при хроническом пиелонефрите.
- •89. Нефролитиаз.
- •1. Определение понятия. Причины образования камней и их химический состав.
- •2. Клиническое значение камней в мочевыводящей системе.
- •3. Гидронефроз - определение понятия, причины развития, исходы, осложнения.
- •4. Нефросклероз - классификация, патоморфология почек.
- •5. Патологическая анатомия уремии (хронической почечной недостаточности).
- •90. Болезни желёз внутренней секреции.
- •1. Патология аденогипофиза - врожденный и приобретенный гипопитуитаризм. Синдром Симмондса-Шихана.
- •91. Болезни желёз внутренней секреции.
- •1. Аддисонова болезнь - изменения надпочечников, клинические симптомы.
- •2. Зоб (струма) - макро- и микроскопические изменения.
- •3. Эндемический и спорадический зоб, причины развития.
- •4. Диффузный токсический зоб (Базедова болезнь) - патоморфология.
- •92. Сахарный диабет.
- •1. Определение понятия.
- •2. Основные типы сахарного диабета, их этиология и патогенез.
- •3. Морфологические изменения островкового аппарата поджелудочной железы.
- •4. Диабетические микроангиопатии - причина развития, основные поражаемые органы.
- •5. Диабетическая макроангиопатия и связанные с ней осложнения.
- •93. Сахарный диабет.
- •3. Поражение почек при диабете.
- •4. Диабетическая стопа и диабетические нейропатии.
- •5) Вторичные иммунодефициты при сахарном диабете - механизмы развития, следствия.
- •94. Болезни мужских и женских половых органов.
- •1. Нодулярная доброкачественная гиперплазия предстательной железы - причины развития, патоморфология, осложнения.
- •2. Эндоцервикоз - причины развития, морфологические изменения шейки матки, осложнения.
- •3. Полипы шейки матки клинико-морфологическая картина.
- •4. Железисто-кистозная гиперплазия эндометрия - причины развития, кинико-морфологическая картина, исходы.
- •5. Железистые полипы эндометрия, клинико-морфологическая картина.
- •95. Болезни беременности и послеродового периода.
- •1. Понятие о гестозе, этиология и патогенез.
- •96. Болезни центральной нервной системы.
- •97. Болезни костно-мышечной системы.
- •98. Инфекционные болезни - общая характеристика.
- •1. Определение понятия инфекционного процесса. Виды сосуществования микробов и макроорганизма.
- •2. Пути распространения возбудителей в организме; формы протекания инфекционных заболеваний.
- •99. Вирусные болезни. Грипп.
- •1. Варианты взаимоотношения вирусов с клетками - мишенями.
- •2. Морфологические особенности воспалительной реакции при вирусных инфекциях.
- •3. Грипп - этиология, патогенез.
- •4. Клинико-морфологические формы гриппа и их патоморфологическая картина.
- •5. Парагрипп, аденовирусная и рс-инфекции - общая клинико-морфологическая характеристика.
- •100. Патологическая анатомия вич-инфекции.
- •1. Возбудитель и пути его проникновения в организм.
- •2. Механизмы цитопатического действия вируса.
- •3. Характер развивающихся нарушений иммунной системы.
- •4. Клиникоморфологические стадии вич-инфекции.
- •5. Спид-ассоциированные инфекции и спидиндикаторные болезни.
- •101. Патологическая анатомия спида.
- •1. Морфология поражения лёгких.
- •2. Морфология поражения головного мозга.
- •3. Морфология поражения желудочно - кишечного тракта.
- •4. Морфология поражения кожи.
- •5. Причины смерти больных вич-инфекцией.
- •102. Менингококковая инфекция.
- •1. Возбудители и входные ворота инфекции.
- •2. Классификация форм инфекции.
- •3. Патоморфология менингококкового цереброспинального менингита.
- •4. Патоморфология молниеносной менингококцемии. Роль иммунных комплексов в ее патогенезе.
- •5. Осложнения и причины смерти при менингококковой инфекции.
- •103. Сепсис.
- •1.Сепсис - определение понятия.
- •2. Особенности бактериемии при сепсисе и тип иммунодефицита.
- •3. Патоморфология первичного септического очага.
- •4. Клиникоанатомические формы сепсиса (септикопиемия и септицемия), их морфологические особенности.
- •5. Причины смерти при сепсисе.
- •104. Септические эндокардиты.
- •1.Клинико-анатомические формы септического эндокардита и микробы - возбудители.
- •4. Особенности септического эндокардита у инъекционных нарко-манов. Ятрогенный септический эндокардит.
- •5. Осложнения и причины смерти при септических эндокардитах.
- •105. Туберкулёз, основные клинико-морфологические формы. Первичный туберкулёз: патоморфология и формы прогрессирования.
- •1. Определение понятия, этиология и патогенез туберкулеза. Основные клиникоанатомические формы.
- •2. Морфология первичного туберкулёзного комплекса в лёгких.
- •3. Морфология первичного комплекса в кишечнике.
- •4. Морфология заживления первичного туберкулезного комплекса в легких.
- •5. Формы прогрессирования первичного туберкулёза.
- •106. Гематогенный туберкулёз.
- •1. Определение понятия. Связь гематогенного туберкулеза с первичным туберкулезом.
- •2. Клинико-анатомические формы.
- •3. Патоморфология острого общего гематогенного туберкулёза.
- •4. Патоморфология гематогенного туберкулёза лёгких.
- •5. Основные формы внелегочного гематогенного туберкулеза.
- •107. Вторичный туберкулёз.
- •1. Определение понятия вторичного туберкулеза. Механизмы заражения и пути распространения инфекции в организме.
- •2. Клинико-анатомические формы.
- •5. Инфильтративный туберкулёз.
- •108. Вторичный туберкулёз.
- •1. Казеозная пневмония.
- •4. Строение стенок острой и хронической каверн.
- •5. Морфология цирротического туберкулёза.
- •109. Возрастные особенности туберкулёза. Патоморфоз туберкулёза.
- •1. Особенности детского туберкулеза.
- •2. Особенности старческого туберкулёза.
- •3. Особенности течения туберкулеза у алкоголиков и вич-инфицированных.
- •4. Патоморфоз туберкулёза.
- •5. Осложнения туберкулёза и причины смерти.
- •110. Патологоанатомическая служба – организационная структура и задачи.
- •3. Клинико-анатомические сопоставления.
- •111. Понятие о диагнозе. Сличение клинического и патологоанатомического диагнозов.
- •1. Виды диагнозов и их основные рубрики.
- •5. Причины расхождения диагнозов и категории расхождения.
- •112. Медицинское свидетельство о смерти и его рубрики.
- •3. Международная классификация болезней и проблем, связанных со здоровьем х пересмотра: ее структура и цели.
- •4. Кодировка рубрик диагноза согласно мкб-10.
- •5. Особенности оформления медицинского свидетельства о перинатальной смерти.
- •113. Деонтологические аспекты патолого-анатомической практики. Этика патологоанатомических вскрытий.
- •1. Действия лечащего врача при смерти больного.
- •2. Общение лечащего врача и патологоанатома с родственниками умершего.
- •5. Когда возможна выдача трупа родственникам без патологоанатомического вскрытия? в каких случаях отмена патологоанатомического вскрытия не возможна?
- •114. Ятрогении. Патология реанимации
- •1. Ятрогении, связанные с диагностическими исследованиями:
- •2. Ятрогении, связанные с лечением (самая обширная группа):
- •3. Ятрогении, связанные с профилактическими мероприятиями, главным образом прививками.
- •4. Информационные ятрогении
- •5. Ятрогенные псевдоболезни (гипердиагностика различных болезней, например, острого аппендицита при аппендикулярной колике и последовавшей аппендэктомии).
- •6. Прочие ятрогении
15. Нарушения обмена нуклеопротеидов и соединений кальция.
1.Подагра, сущность процесса, органопатология. При нарушении обмена нуклеопротеидов и избыточном образовании мочевой кислоты ее соли могут выпадать в тканях, что наблюдается при подагре, мочекаменной болезни и мочекислом инфаркте.
Подагра — заболевание, при котором периодически в суставах выпадают соли мочекислого натрия, что сопровождается болевым приступом. Различают первичную и вторичную подагру.
Первичная подагра обусловлена врожденными нарушениями пуринового обмена. Об этом свидетельствует ее семейный характер и сочетание подагры с другими нарушениями обмена веществ (ожирение, диабет, желчекаменная болезнь). Велика роль в развитии заболевания особенностей питания, употребления больших количеств животных белков, сухих вин, шампанского, пива (!), неподвижного образа жизни. Соли обычно выпадают в синовии и хрящах мелких суставов, в сухожилиях и суставных сумках, в хряще ушных раковин. Ткани вокруг отложений солей некротизируются. Перифокально развивается воспалительная гранулематозная реакция со скоплением гигантских клеток. По мере увеличения отложений солей и разрастания вокруг них соединительной ткани образуются подагрические шишки (tophi urici), суставы деформируются. В почках отмечается накопление мочевой кислоты и солей мочекислого натрия в канальцах с обтурацией их просвета, развитие вторичных воспалительных и атрофических изменений (подагрические почки).
Вторичная подагра является осложнением:
1) опухолей кроветворной ткани (при усиленном распаде опухолевых клеток);
2) эндокринных заболеваний;
3) болезней почек различной этиологии с исходом в нефроцирроз.
2. Мочекаменная болезнь - патоморфология, осложнения, исходы. Почечнокаменная болезнь (нефролитиаз) - заболевание, при котором в почечных чашечках, лоханках и мочеточниках образуются камни разной величины, структуры и химического состава (фосфаты, ураты, оксалаты, карбонаты и др.). Заболевание имеет хроническое течение; в процесс вовлекаются одна или обе почки.
Факторы образования камней: генетическая предрасположенность, преобладание в пище белков животного происхождения и углеводов (чрезмерное закисление мочи), низкое потребление витамина А, высокая концентрация солей. Хронические воспалительные процессы в почках и мочевыводящем тракте, хронический уростаз, приводящий к повышенной солей в моче, нарушению рн и коллоидному дисбалансу мочи. Химический состав: ураты, оксалаты, кальциевые и фосфатные камни
Клин значение. Почечные камни вызывают обструкцию устья уретры, что приводит к препятствию для оттока мочи с последующим формированием гидронефроза и возникновением атрофии почечной ткани.
Гидронефроз - это расширение анатомических полостей почек из-за хронической задержки оттока мочи от почек. Гидронефроз может осложниться гидропионефрозом, который характеризуется накоплением большого количества гноя в полостях почки. Под действием повышенного внутрилоханочного давления чашечки становятся круглыми. Стенка лоханки истончается; атрофируются нервные окончания, облитерируются кровеносные сосуды лоханки. В конечной стадии лоханка - тонкостенный мешок.
Растягивающаяся лоханка оттесняет почечную паренхиму к периферии; паренхима оказывается сжатой между фиброзной капсулой и лоханкой.
Возможные осложнения по степени нарастания тяжести
Пиелит
Гидронефроз
Гидроуретеронефроз - когда камень, обтурирующий мочеточник, вызывает расширение как лоханки, так и просвета мочеточника выше обтурации
Уретерит воспаление стенки мочеточника, которое может повести к стриктурам; редко образуется пролежень с перфорацией мочеточника в месте его закупорки.
Пионефроз (пиоуретеронефроз)
Инфекция ведет к развитию пиелита, пиелонефрита, апостематозного (гнойничкового) нефрита, к гнойному расплавлению паренхимы.
Воспаление нередко переходит на околопочечную клетчатку, что ведет к хроническому паранефриту.Почка в таких случаях оказывается замурованной в толстой капсуле из грануляционной, жировой и фиброзной ткани (панцирный паранефрит), а иногда и полностью замещается склерозированной жировой клетчаткой (жировое замещение почки).
ОПН и ХПН
Смерть больных нефролитиазом чаще всего наступает от уремии и осложнений в связи с гнойным расплавлением почки.
3-5. Дистрофическое, метастатическое и метаболическое обызвествление: причины развития, патоморфология.
1. Метастатическая кальцификация (метастатическое обызвествление) возникает при увеличении концентрации кальция или фосфора в крови (гиперкальциемия). Кальцификация происходит наиболее часто в стенках артерий, альвеолярных перегородках легких, в слизистой оболочке желудка, в миокарде левого желудочка и в почках. Легкие, желудок и почки выделяют кислые продукты и их ткани вследствие большей щелочности менее способны удерживать соли кальция в растворе, чем ткани других органов. В миокарде и стенке артерий соли кальция откладываются в связи с тем, что их ткани омываются артериальной кровью и относительно бедны углекислотой.
Причины метастатического обызвествления:
А) связанные с усиленным выходом солей кальция из депо:
— гиперпродукция паратгормона (гиперплазия или опухоли паращитовидных желез);
— недостаток кальцитонина (некоторые заболевания щитовидной железы);
— остеомаляции (миеломная болезнь, туберкулез костей, многооскольчатые переломы, метастазы опухолей, патология беременности).
Б) связанные с пониженным выведением солей кальция из организма:
— поражения толстой кишки (отравление сулемой, хроническая дизентерия);
— болезни почек (поликистоз, хронический нефрит, отравление сулемой);
— гипервитаминоз витамина D.
Накопление кальция в тканях можно определить рентгенологически. При микроскопии кальций окрашивается в интенсивно фиолетовый цвет (базофильно). В ранних стадиях кальцификации очаги скопления кальция кажутся гранулярными, большие очаги – аморфные. Гистохимически кальций выявляют методом серебрения Косса. В миокарде и почках первичные отложения извести находят в митохондриях и фаголизосомах, обладающих высокой активностью фосфотаз. В интерстициуме соли кальция первично выпадают по ходу мембран сосудов и волокнистых структур. Вокруг отложений извести наблюдается воспалительная реакция, иногда отмечаются скопления макрофагов, гигантских клеток, образование гранулемы. Внешний вид органов и тканей мало изменен.
Исход. Неблагоприятен: выпавшие соли практически не рассасываются.
Значение. При кальцификации почечного интерстициума (нефрокальциноз) может возникать ХПН. Обширная кальцификация кровеносных сосудов может приводить к ишемии, особенно в коже. Редко при обширном повреждении легочных альвеол возникают нарушения диффузии газов. Кроме этих случаев, кальцификация не нарушает функции паренхиматозных клеток в тканях.
2.При дистрофическом обызвествлении (петрификации) или дистрофической кальцификации метаболизм кальция и фосфора не нарушен. Их уровень концентрации в сыворотке крови нормальный. Кальцификация происходит в результате местных нарушений в тканях. Отложения солей кальция имеют местный характер и обычно обнаруживаются в тканях омертвевших или находящихся в состоянии глубокой дистрофии, то есть в тканях с пониженным уровнем жизнедеятельности.
Основная причина дистрофического обызвествления — физико-химические изменения тканей, сопровождающиеся ощелачиванием среды в связи с усиленным потреблением кислорода и выделением углекислоты, изменением свойств белковых коллоидов (коагуляцией белка) и усилением активности фосфатаз. В таких тканях появляются разных размеров очаги каменистой плотности — петрификаты. Дистрофическому обызвествлению подвергаются:
1. Некротизированные ткани организма (казеозный некроз в гранулемах (при туберкулезе, сифилисе)
2. Тромбы.
3. Экссудат (чаще фибринозный, например, панцирное сердце).
4. Очаги старых кровоизлияний (гематома).
5. Погибшие паразиты (цистицеркоз, эхинококкоз, трихинеллез, шистосомиаз, филяриоз).
6. Мертвый плод при замершей беременности (литопедион)
7. Некоторые новообразования (псаммомные тельца).
3.Метаболическое обызвествление (интерстициальный кальциноз). Механизм его развития до конца не ясен. Главное значение придают нестойкости буферных систем (ph и белковые коллоиды) крови и тканевой жидкости, в связи с чем кальций не удерживается в них даже при его невысокой концентрации, часто играет роль наследственная предрасположенность.
Примером интерстициального системного кальциноза служит опухолеподобный кальциноз (формирование неопухолевых узелковых кальцифицированных масс в подкожной клетчатке, по ходу сухожилий, фасций и апоневрозов в мышцах, нервах и сосудах). Интерстициальный ограниченный кальциноз, или известковая подагра, характеризуется отложением солей кальция в виде пластинок в коже рук, реже ног.
Значение кальциноза. Имеют значение распространенность, локализация и характер обызвествления. Так, отложение извести в стенке сосуда ведет к структурно-функциональным нарушениям и может явиться причиной ряда осложнений (например, тромбоза). Наряду с этим, отложение извести в очагах казеозного некроза при туберкулезе свидетельствует о его заживлениии.
16. Образование камней. 1. Причины и патогенез камнеобразования. 2. Виды камней. 3. Места образования камней в организме. 4. Камни желчевыводящей и мочевыводящей систем, их виды. 5. Последствия камнеобразования.
Камни, или конкременты (от лат. Concrementum - сросток) — очень плотные образования, свободно лежащие в полостных органах или выводных протоках желез.
Причины и факторы, способствующие камнеобразованию:
Общий фактор: нарушения обмена веществ приобретенного или наследственного характера. Пример: связь ЖКБ с общим ожирением и атеросклерозом, МКБ - с подагрой, оксалурией.
Местный фактор: нарушение секреции и застой секрета → ↑ концентрации веществ, из которых строятся камни, и осаждению их из раствора, чему способствует усиление реабсорбции и сгущение секрета. + воспаление в органе → появление белковых веществ, что создает органическую матрицу, в которую откладываются соли и на которой строится камень. Впоследствии камень и воспаление нередко становятся дополняющими друг друга факторами, определяющими прогрессирование камнеобразования.
Механизм образования камня складывается из двух процессов: образования органической матрицы и кристаллизации солей, причем каждый из этих процессов в определенных ситуациях может быть первичным.
Виды камней (форма, величина, цвет, структура на распиле) различен:
По величине: макро и микролиты.
Форма камня нередко повторяет полость, которую он заполняет: круглые или овальные камни находятся в мочевом и желчном пузырях, отростчатые - в лоханках и чашечках почек, цилиндрические - в протоках желез.
Камни могут быть одиночными и множественными (имеют граненые притертые друг к другу поверхности - фасетированные камни).
Поверхность камней бывает гладкой, шероховатой (оксалаты, напоминают тутовую ягоду), что травмирует слизистую оболочку, вызывает ее воспаление.
Цвет камней различный, что определяется их разным химическим составом: белый (фосфаты), желтый (ураты), темнокоричневый или темно-зеленый (пигментные).
На распиле камни имеют радиарное строение (кристаллоидные), слоистое (коллоидные), слоисто-радиарное (коллоидно-кристаллоидные).
Химический состав. Желчные камни могут быть холестериновыми, пигментными, известковыми или холестериново-пигментно-известковыми (сложные, или комбинированные, камни). Мочевые камни могут состоять из мочевой кислоты и ее солей (ураты), фосфата кальция (фосфаты), оксалата кальция (оксалаты), цистина и ксантина. Бронхиальные камни состоят обычно из инкрустированной известью слизи.
Локализация камней: чаще - желчные и мочевые пути (ЖКБ и МКБ), также: выводные протоки поджелудочной железы и слюнных желез, бронхи и бронхоэктазы, крипты миндалин, вены (флеболиты - отделившиеся от стенки сосуда петрифицированные тромбы), кишечник (копролиты - уплотнившееся содержимое кишечника).
По составу конкременты при ЖКБ делятся на:
Холестериновые – образуются в результате нарушения обмена холестерина и желчных кислот. Они имеют желтоватый, золотистый или зеленоватый оттенок. Чаще встречаются у людей, страдающих лишним весом. Образование таких камней редко сопровождается воспалительным процессом, поэтому их наличие долго остается незамеченным.
Билирубиновые – образуются из-за изменения состава крови. Чаще это округлые единичные конкременты темного цвета, но встречаются и множественные конкременты небольших размеров.
Кальциевые – образуются как следствие воспалительных процессов в желчном пузыре. Имеют белесый оттенок, помимо кальция содержат отмершие эпителиальные клетки, а также холестерин.
Смешанные – встречаются наиболее часто. Имеют слоистую структуру, состоят из разных элементов – холестерина, гликопротеина, желчных кислот и т. Д. Смешанные конкременты нередко становятся причиной желчной колики.
По составу конкременты при МКБ делятся на:
Кальциевые камни (80%) образуются в любом возрасте, но наиболее часто они наблюдаются у мужчин в возрасте старше 50 лет. Кальциевые камни могут быть оксалатными, фосфатными или карбонатными. В большинстве случаев конкременты состоят из кальциевых оксалатов с незначительным включением кальциевых фосфатов.
Уратные камни (6-10%) образуются из солей мочевой кислоты.
Струвитные камни (10%) — конкременты, образовавшиеся в результате инфекций мочевыделительной системы и состоящие из магнезио-аммониевых фосфатов, которые являются отходами жизнедеятельности патогенных микроорганизмов. Струвиты чаще встречаются у женщин, так как они более подвержены инфекционным заболеваниям мочевыделительной системы, особенно почек.
Цистиновые камни (1%) образуются у пациентов с редкой генетической аномалией, характеризующейся нарушением выведения аминокислоты цистина. При этом повышается содержание цистина в моче.
Последствия. В результате давления камней на ткань может возникнуть ее омертвение (почечные лоханки, мочеточники, желчный пузырь и желчные протоки, червеобразный отросток) → образование пролежней, перфорации, спайки, свищи. Камни бывают причиной воспаления полостных органов (пиелоцистит, холецистит) и протоков (холангит, холангиолит). Нарушая отделение секрета, они ведут к тяжелым осложнениям общего (желтуха при закупорке общего желчного протока) или местного (гидронефроз при обтурации мочеточника) характера.
17. Некроз. 1. Определение понятия. 2. Причины развития и морфогенез некроза. 3. Прямой и непрямой некроз. 4. Микроскопические признаки некроза. 5. Апоптоз: определение понятия, морфология, биологическое значение. Морфологические отличия апоптоза от обычного некроза.
НЕКРОЗ - местная гибель клеток в живом организме. От апоптоза некроз отличается причинами своего развития, а также массивностью и одномоментностью гибели клеток, что всегда сопровождается ответной воспалительной реакцией.
В зависимости от причины некроза:
Травматический некроз является результатом прямого действия на ткань физических или химических факторов. Такой некроз возникает при воздействии радиации, низких (отморожение) и высоких (ожог) температур, в краях раневого канала, при электротравме.
Токсический некроз развивается в результате действия на ткани токсинов как бактериального, так и небактериального происхождения, химических соединений различной природы (кислоты, щелочи, лекарственные препараты, этиловый спирт и др.). Таков, например, некроз эпителия проксимального отдела нефрона при отравлении сулемой, некроз кардиомиоцитов при воздействии дифтерийного экзотоксина.
Трофоневротический некроз возникает при нарушениях нервной трофики тканей. В результате этих нарушений развиваются циркуляторные расстройства, дистрофические и некробиотические изменения, завершающиеся некрозом. Таковы некрозы при заболеваниях и травмах центральной и периферической нервной системы (незаживающие язвы при повреждении периферических нервов). Примером трофоневротического некроза являются пролежни.
Аллергический некроз ткани наступает в сенсибилизированном организме и является, как правило, выражением реакций гиперчувствительности немедленного типа. Обычно это фибриноидный некроз, часто встречающийся при инфекционно-аллергических и аутоиммунных заболеваниях. Классическим примером аллергического некроза может служить феномен Артюса.
Сосудистый некроз, который называют инфарктом, возникает при нарушении или прекращении кровотока в артериях вследствие тромбоза, эмболии, длительного спазма (антиогенный некроз). Недостаточный приток крови вызывает ишемию, гипоксию и гибель ткани вследствие прекращения окислительно-восстановительных процессов (ишемический некроз). Таковы, например, ишемические некрозы миокарда в условиях функциональной нагрузки при стенозирующем атеросклерозе венечных (коронарных) артерий сердца.
Морфогенез некроза - стадии:
1) паранекроз - подобные некротическим, но обратимые изменения;
2) некробиоз - необратимые дистрофические изменения, характеризующиеся преобладанием катаболических реакций над анаболическими;
3) смерть клетки, время наступления которой установить трудно;
4) аутолиз - разложение мертвого субстрата под действием гидролитических ферментов погибших клеток и макрофагов. В морфологическом выражении некроз равнозначен аутолизу.
В зависимости от механизма действия:
Прямой некроз, обусловленный непосредственным воздействием (травматический и токсический некрозы)
Непрямой некроз, возникающий опосредованно через сосудистую и нервноэндокринную системы (трофоневротический, аллергический, сосудистый некрозы).
Во внутриутробном периоде и в детском возрасте преобладает прямой некроз, связанный с непосредственным воздействием инфекционного агента или токсического вещества на ткани (множественные ареактивные некрозы внутренних органов и слизистых оболочек у плодов, новорожденных и недоношенных при генерализованной ветряной оспе, генерализованной оспенной вакцине, сепсисе, токсоплазмозе) или вследствие побочного токсического воздействия некоторых лекарственных препаратов (цитостатические средства, аминазин и др.). Непрямые некрозы, часто встречающиеся у взрослых, наблюдаются у детей в виде исключения при пороках развития сосудистого русла того или иного органа или нарушениях обмена электролитов.
Микроскопические признаки некроза.
Ядро сморщивается, при этом происходит конденсация хроматина - кариопикноз, распадается на глыбки - кариорексис и растворяется - кариолизис. Пикноз, рексис и лизис ядра являются последовательными стадиями процесса и отражают динамику активации гидролаз - рибонуклеазы и дезоксирибонуклеазы, что ведет к отщеплению от нуклеотидов фосфатных групп и высвобождению нуклеиновых кислот, которые подвергаются деполимеризации.
В цитоплазме происходят денатурация и коагуляция белков. Изменения могут охватывать часть клетки (фокальный коагуляционный некроз), которая отторгается, или всю клетку (коагуляция цитоплазмы). Коагуляция завершается плазморексисом - распадом цитоплазмы на глыбки. На заключительном этапе разрушение мембранных структур клетки ведет к ее гидратации, наступает гидролитическое расплавление цитоплазмы - плазмолиз. Расплавление в одних случаях охватывает всю клетку (цитолиз), в других - лишь часть ее (фокальный колликвационный некроз, или баллонная дистрофия).
Изменения цитоплазмы (коагуляция, плазморексис, плазмолиз), так же как и изменения ядра клетки, являются морфологическим выражением ферментативного процесса, в основе которого лежит активация гидролитических ферментов лизосом.
Промежуточное вещество вследствие деполимеризации его гликозаминогликанов и пропитывания белками плазмы крови набухает и расплавляется.
Коллагеновые волокна также набухают, пропитываются белками плазмы (фибрин), превращаются в плотные гомогенные массы, распадаются или лизируются. Изменения эластических волокон: набухание, базофилия, распад, расплавление - эластолиз. Ретикулярные волокна нередко сохраняются в очагах некроза длительное время, но затем подвергаются фрагментации и глыбчатому распаду; аналогичны изменения и нервных волокон. Распад волокнистых структур связан с активацией специфических ферментов - коллагеназы и эластазы.
А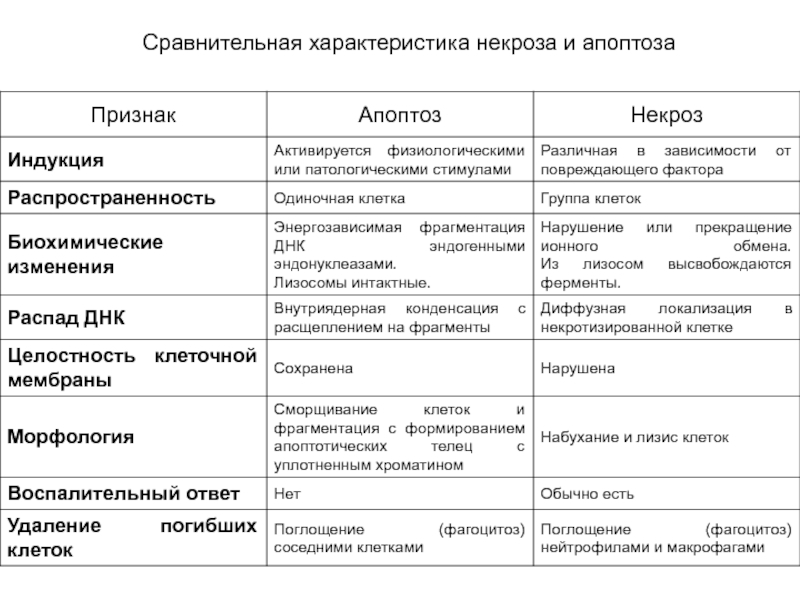 ПОПТОЗ
- разновидность коагуляционного некроза
клеток, вызванного активацией специфических
генов апоптоза в ядре клетки («гены
смерти»). Эта активация может происходить
под влиянием гормонов, интерлейкинов
(особенно фактора некроза опухоли) или
спонтанно при физиологическом старении
клетки.
ПОПТОЗ
- разновидность коагуляционного некроза
клеток, вызванного активацией специфических
генов апоптоза в ядре клетки («гены
смерти»). Эта активация может происходить
под влиянием гормонов, интерлейкинов
(особенно фактора некроза опухоли) или
спонтанно при физиологическом старении
клетки.
Морфология: сморщивание ядра, конденсация и фрагментация хроматина, образование цитоплазматических выпячиваний и апоптотических телец, фагоцитоз апоптозных клеток или телец.
Биологическое значение: играет важную роль в морфообразовательных процессах в эмбриогенезе, в обновлении тканей, в противоопухолевой резистентности (апоптоз образующихся опухолевых клеток), при ВИЧ-инфекции, увеличивая количество гибнущих Т-хелперов.
18. Некроз. 1. Клинико - морфологические формы некроза. 2. Сухая и влажная гангрены - их причина и морфология. 3. Инфаркт, виды, причины развития. 4. Морфология инфаркта сердца, головного мозга, лёгких. 5. Исходы некроза.
Клинико-морфологические формы некроза:
1. Коагуляционный (сухой) некроз характеризуется тем, что возникающие при нем мертвые участки сухие, плотные, серо-желтого цвета. В основе сухого некроза лежат процессы денатурации белков с образованием труднорастворимых соединений, которые могут длительное время не подвергаться гидролитическому расщеплению, ткани при этом обезвоживаются. Условия для развития сухого некроза имеются прежде всего в тканях, богатых белками и бедных жидкостями. Примером могут служить восковидный, или ценкеровский (описан Ценкером), некроз мышц при инфекциях (брюшной и сыпной тифы), травме; творожистый некроз при туберкулезе, сифилисе, лепре, лимфогранулематозе; фибриноидный некроз при аллергических и аутоиммунных заболеваниях.
2. Колликвационный (влажный) некроз характеризуется расплавлением мертвой ткани, образованием кист. Развивается он в тканях, относительно бедных белками и богатых жидкостью, где существуют благоприятные условия для гидролитических процессов. Типичным влажным некрозом является очаг серого размягчения (ишемический инфаркт) головного мозга. При расплавлении масс сухого некроза говорят о вторичной колликвации.
3. Гангрена - некроз тканей, соприкасающихся с внешней средой, при этом ткани становятся серо-бурыми или черными, что связано с превращением кровяных пигментов в сульфид железа.
При сухой гангрене мертвая ткань под воздействием воздуха высыхает, уплотняется, сморщивается, становится похожей на ткань мумий. Поэтому сухую гангрену называют также мумификацией. Сухая гангрена возникает в тканях, бедных влагой. Таковы сухая гангрена конечностей при атеросклерозе и тромбозе ее артерии (атеросклеротическая гангрена), при отморожении или ожоге, пальцев - при болезни Рейно или вибрационной болезни, кожи - при инфекциях (сыпной тиф), сопровождающихся глубокими нарушениями трофики, и т.д.
При влажной гангрене мертвая ткань подвергается действию, гнилостных микроорганизмов (Вас. Perfringens, fusiformis, putrificans, histolyticus, proteus и др.), набухает, становится отечной, издает зловонный запах. Влажная гангрена развивается чаще в тканях, богатых влагой. Ее возникновению способствуют расстройства кровообращения (венозный застой) и лимфообращения (лимфостаз, отек). Влажная гангрена встречается в легких, осложняя воспалительные процессы (пневмонии), в кишечнике при непроходимости брыжеечных артерий (тромбоз, эмболия). У ослабленных инфекционным заболеванием (чаще корь) детей может развиться влажная гангрена мягких тканей щек, промежности, которую называют номой.
От сухой и влажной гангрены следует отличать анаэробную гангрену, представляющую собой самостоятельное инфекционное заболевание, которое вызывается группой определенных микроорганизмов (прежде всего Вас. Perfringens). Она возникает чаще при огнестрельных и других ранениях, сопровождающихся массивной деструкцией мышц и размозжением костей.
Пролежни - омертвение поверхностных участков тела (кожа, мягкие ткани), подвергающихся давлению. Поэтому пролежни чаще появляются в области крестца, остистых отростков позвонков, большого вертела бедренной кости. По своему генезу это трофоневротический некроз, который возникает обычно у тяжелобольных, страдающих сердечно-сосудистыми, онкологическими, инфекционными или нервными болезнями.
4. Секвестр - участок мертвой ткани, который не подвергается аутолизу, не замещается соединительной тканью и свободно располагается среди живых тканей. Секвестры обычно возникают в костях при воспалении костного мозга - остеомиелите. Вокруг такого секвестра образуются секвестральная капсула и полость, заполненная гноем. Нередко секвестр выходит из полости через свищи, которые закрываются лишь после полного его выделения. Секвестрируются и мягкие ткани (например, участки некроза легкого, пролежня); такие секвестры, как правило, быстро расплавляются.
5. Инфаркт - это сосудистый (ишемический) некроз, следствие и крайнее выражение ишемии. Инфаркт - самый частый вид некроза.
Виды инфаркта:
— клиновидные, основание клина обращено к капсуле, а острие - к воротам органа (образуются в селезенке, почках, легких, что определяется характером ангиомагистральным типом ветвления их артерий).
— неправильной формы (в сердце, мозге, кишечнике, т.е. В тех органах, где преобладает не магистральный, а рассыпной или смешанный тип ветвления артерий).
Инфаркт может охватывать большую часть или весь орган (субтотальный или тотальный инфаркт) или обнаруживается лишь под микроскопом (микроинфаркт).
Если инфаркт развивается по типу коагуляционного некроза, то ткань в области омертвения уплотняется, становится суховатой (инфаркт миокарда, почек, селезенки); если же инфаркт образуется по типу колликвационного некроза, она размягчается и разжижается (инфаркт мозга, кишки).
Цвет инфаркта:
1. Белый (ишемический) инфаркт представляет собой участок бело-желтого цвета, хорошо отграниченный от окружающей ткани. Обычно он возникает в участках с недостаточным коллатеральным кровообращением. Особенно часто встречается в селезенке, почках.
2. Белый инфаркт с геморрагическим венчиком представлен участком беложелтого цвета, но этот участок окружен зоной кровоизлияний. Она образуется в результате того, что спазм сосудов по периферии инфаркта сменяется паретическим их расширением и развитием кровоизлияний. Такой инфаркт находят в почках, миокарде.
3. При красном (геморрагическом) инфаркте участок омертвения пропитан кровью, он темнокрасный и хорошо отграничен. Благоприятным условием для такого геморрагического пропитывания является венозный застой. Определенное значение для развития красного инфаркта имеют и особенности ангиоархитектоники органа (анастомозы между бронхиальной и легочной артериями). Встречается геморрагический инфаркт, как правил, в легких, редко - в кишечнике, селезенке, почках.
Причины развития инфаркта - длительный спазм, тромбоз или эмболия артерии, а также функциональное напряжение органа в условиях недостаточного его кровоснабжения; недостаточность анастомозов и коллатералей, которая зависит от степени поражения стенок артерий и сужения их просветов (атеросклероз, облитерирующий эндартериит), от степени нарушения кровообращения (например, венозного застоя) и от уровня выключения артерии тромбом или эмболом. Обмен веществ в органах и тканях, в которых возникает инфаркт, как правило, нарушен в связи с гипоксией, обусловленной общими расстройствами кровообращения.
В сердце инфаркт обычно белый с геморрагическим венчиком, имеет неправильную форму, встречается чаще в левом желудочке и межжелудочковой перегородке, крайне редко - в правом желудочке и предсердиях. Омертвение может локализоваться под эндокардом (субэндокардиальный инфаркт), эпикардом (субэпикардиальный инфаркт) или охватывать всю толщу миокарда (трансмуральный инфаркт). В области инфаркта на эндокарде нередко образуются тромботические, а на перикарде - фибринозные наложения, что связано с развитием реактивного воспаления вокруг участков некроза. Чаще всего инфаркт миокарда встречается на фоне атеросклероза и ГБ и рассматривается как самостоятельное заболевание.
В головном мозге чаще возникает белый инфаркт, который быстро размягчается (очаг серого размягчения мозга). Если инфаркт образуется на фоне значительных расстройств кровообращения, венозного застоя, то очаг омертвения мозга пропитывается кровью и становится красным (очаг красного размягчения мозга). Инфаркт локализуется обычно в подкорковых узлах, разрушая проводящие пути мозга, что проявляется параличами. Инфаркт мозга, как и инфаркт миокарда, чаще всего встречается на фоне атеросклероза и гипертонической болезни и является одним из проявлений цереброваскулярных заболеваний.
В легких в подавляющем большинстве случаев образуется геморрагический инфаркт. Он хорошо отграничен, имеет форму конуса, основание которого обращено к плевре. На плевре в области инфаркта появляются наложения фибрина (реактивный плеврит). У острия конуса, обращенного к корню легкого, нередко обнаруживается тромб или эмбол в ветви легочной артерии. Омертвевшая ткань плотна, зерниста, темно-красного цвета. Геморрагический инфаркт легких обычно возникает на фоне венозного застоя, причем развитие его в значительной мере определяется особенностями ангиоархитектоники легких, наличием анастомозов между системами легочной и бронхиальных артерий. В условиях застойного полнокровия и закрытия просвета ветви легочной артерии в область омертвения ткани легкого из бронхиальной артерии поступает кровь, которая разрывает капилляры и изливается в просвет альвеол. Вокруг инфаркта нередко развивается воспаление легочной ткани (периинфарктная пневмония). Массивный геморрагический инфаркт легкого может быть причиной надпеченочной желтухи. Белый инфаркт в легких - исключительная редкость. Возникает он при склерозе и облитерации просвета бронхиальных артерий.
Исходы некроза: отторжение некротических масс по типу мутиляции, отторжение с образованием полости (каверна), рассасывание с полным восстановлением ткани, рассасывание с образованием рубца, рассасывание с образованием полости (кисты), рассасывание или отторжение с образованием эрозии или язвы, частичное краевое рассасывание с образованием секвестра (обычно в костях), инкапсуляция очага некроза.
При благоприятном исходе вокруг омертвевших тканей возникает реактивное воспаление, которое отграничивает мертвую ткань - демаркационная зона → размножаются клетки соединительной ткани, которая замещает или обрастает участок некроза (организация – образуется рубец). Обрастание участка некроза ведет к его инкапсуляции. В мертвые массы при сухом некрозе и в очаг омертвения, подвергшийся организации, могут откладываться соли кальция — петрификация, оссификация. При рассасывании тканевого детрита и формировании капсулы, что встречается обычно при влажном некрозе на месте омертвения появляется полость - киста.
Неблагоприятный исход некроза - гнойное расплавление очага омертвения - гнойное расплавление инфарктов при сепсисе (такие инфаркты называют септическими). В исходе некроза на ранних этапах внутриутробного развития возникает порок органа, части тела.
19. Общая смерть. 1. Определение понятия общей смерти. 2. Стадии развития. 3. Клинико-морфологические критерии разграничения стадий общей смерти. 4. Ранние и поздние морфологические признаки необратимой стадии смерти. 5. Этика патологоанатомических вскрытий.
Смерть — необратимое прекращение жизнедеятельности организма. С наступлением смерти человек превращается в мертвое тело, труп (cadaver).
Стадии развития умирания:
Предагональное состояние, характеризующееся выраженными расстройствами кровообращения и дыхания. Длительность этого состояния может быть различной — от нескольких часов до нескольких дней.
Терминальная пауза. Она характеризуется внезапной остановкой дыхания, резким угнетением деятельности сердца, угасанием биоэлектрической активности головного мозга, угасанием роговичных и других рефлексов. Продолжительность терминальной паузы от нескольких секунд до 4 минут.
Агония — вспышка борьбы организма за жизнь. Её может и не быть, или они могут следовать одна за другой. Агония начинается обычно с кратковременных задержек дыхания. Затем наступает ослабление сердечной деятельности и функциональные расстройства различных систем. Она отражает некоординированную деятельность гомеостатических систем в терминальном периоде (аритмии, паралич сфинктеров, судороги, отек легких). Продолжительность агонии может быть различной, что зависит от вида и механизма смерти. Она может быть кратковременной (несколько минут) и продолжительной (несколько часов и дней). В ряде случаев она отсутствует.
Стадия клинической смерти – наступает после остановки дыхания и кровообращения, продолжающаяся 4-6 минут. При искусственном или случайном охлаждении тела этот период может увеличиваться до 10 минут. Агония и период так называемой "клинической смерти", которому она предшествует, может быть обратимой, с полным восстановлением функций организма. В основе клинической смерти лежит своеобразное гипоксическое состояние (прежде всего ЦНС) в связи с прекращением кровообращения и отсутствием центральной его регуляции.
Биологическая смерть — это необратимое состояние и восстановить жизненные функции организма человека в этот период невозможно. Их можно лишь искусственно поддерживать. Раньше всего (5-6 мин) необратимые изменения наступают в коре головного мозга — "смерть мозга". Этот момент, когда нарушается интегрирующая деятельность ЦНС, и следует считать началом биологической смерти.
Посмертные изменения:
1. Охлаждение трупа (algor mortis) развивается в связи с прекращением после смерти выработки в теле тепла и выравниванием температуры мертвого тела и окружающей среды. Если перед смертью у больного была очень высокая температура или в длительном атональном периоде наблюдались судороги, то охлаждение трупа происходит медленно. В ряде случаев (смерть от столбняка, отравления стрихнином) в ближайшие часы после смерти температура трупа может повышаться.
2. Трупное окоченение (rigor mortis) выражается в уплотнении произвольных и непроизвольных мышц. Оно обусловлено исчезновением после смерти из мышц АТФ и накоплением в них молочной кислоты. Трупное окоченение развивается обычно через 2-5 ч после смерти и к концу суток охватывает всю мускулатуру. Сначала окоченению подвергаются жевательные и мимические мышцы лица, затем мышцы шеи, туловища и конечностей. Трупное окоченение сохраняется в течение 2-3 сут, а затем исчезает (разрешается) в той же последовательности, в какой и возникает. Трупное окоченение сильно выражено при судорогах (при столбняке, отравлении стрихнином). Слабо выражено трупное окоченение у стариков и детей, у лиц, истощенных и умерших от сепсиса; у недоношенных плодов трупное окоченение отсутствует. Низкая температура окружающей среды затрудняет наступление трупного окоченения и удлиняет сроки его существования, высокая температура ускоряет разрешение трупного окоченения.
3. Трупное высыхание возникает вследствие испарения влаги с поверхности тела. Оно может ограничиваться отдельными участками, но высыханию может подвергнуться и весь труп (мумификация трупа). Прежде всего высыхание затрагивает кожные покровы, глазные яблоки, слизистые оболочки. С высыханием связано помутнение роговиц, появление на склере при открытой глазной щели сухих буроватых пятен треугольной формы; основание этих пятен обращено к роговице, а вершина - к углу глаза. Слизистые оболочки становятся сухими, плотными, буроватого цвета. На коже сухие, желто-бурые, пергаментного вида пятна появляются прежде всего в местах мацерации или повреждений эпидермиса. Так называемые пергаментные пятна от высыхания могут быть приняты за прижизненные ссадины и ожоги.
4. Перераспределение крови в трупе выражается в переполнении кровью вен, тогда как артерии оказываются почти пустыми. В венах и полостях правой половины сердца происходит посмертное свертывание крови. Образующиеся посмертные сгустки крови имеют желтую или красную окраску, гладкую поверхность, эластическую консистенцию (тянутся) и лежат свободно в просвете или камере сердца, что отличает их от тромбов. При быстром наступлении смерти посмертных сгустков бывает мало, при медленном - много. При смерти в состоянии асфиксии (например, асфиксия новорожденных) кровь в трупе не свертывается. Со временем наступает трупный гемолиз.
5. Трупные пятна возникают в связи с перераспределением крови в трупе и зависят от его положения. В силу того что кровь стекает в вены нижележащих частей тела и там накапливается, через 3-6 ч после наступления смерти образуются трупные гипостазы. Они имеют вид темно-фиолетовых пятен и при надавливании бледнеют. Трупные гипостазы отсутствуют в участках тела, подвергающихся давлению (область крестца, лопаток при положении трупа на спине). Они хорошо выражены при смерти от заболеваний, ведущих к общему венозному застою, и плохо - при малокровии, истощении. В последующем, когда наступает посмертный гемолиз эритроцитов, область трупных гипостазов пропитывается диффундирующей из сосудов и окрашенной гемоглобином плазмой крови. Возникают поздние трупные пятна, или трупная имбибиция. Эти пятна имеют красно-розовую окраску и не исчезают при надавливании.
6. Трупное разложение связано с процессами аутолиза и гниения трупа. Посмертный аутолиз раньше возникает и интенсивнее выражен в железистых органах (печень, поджелудочная железа, желудок). При забрасывании желудочного содержимого в пищевод возможно самопереваривание его стенки (эзофагомаляция), а при аспирации желудочного содержимого в дыхательные пути - «кислое» размягчение легких (pneumomalacia acida). К посмертному аутолизу быстро присоединяются гнилостные процессы в связи с размножением гнилостных бактерий в кишечнике и последующим заселением ими тканей трупа. Газы, образующиеся при гниении трупа, раздувают кишечник, проникают в ткани и органы, которые приобретают пенистый вид, и при ощупывании слышна крепитация (трупная эмфизема).
При вскрытии трупа патологоанатом должен относится с уважением к умершему человеку и соблюдать принципы деонтологии. В частности, все манипуляции, связанные с приобретением практических навыков врачами-клиницистами на трупах - катетеризация подключичной вены, пункции сердца, интубация трахеи, отработка техники пластических операций на лице - должны проводиться с согласия родственников умершего. Патологоанатомические разрезы должны быть максимально косметическими, в частности есть смысл шире применять разрез по Лешке. Не допустимы смех и шутки при вскрытии трупа, а также курение в зале.
20. Нарушения кровообращения. Артериальное полнокровие. 1. Классификация нарушения кровообращения. 2. Виды местного артериального полнокровия. 3-5. Морфологическая характеристика ангионевротической и коллатеральной гиперемии, гиперемии после анемии, вакатной гиперемии.
Расстройства кровообращения можно разделить на 3 группы:
1) нарушения кровонаполнения, представленные полнокровием (артериальным или венозным) и малокровием;
2) нарушения проницаемости стенки сосудов, к которым относят кровотечение (кровоизлияние) и плазморрагию;
3) нарушения течения и состояния (т.е. Реологии) крови в виде стаза, сладжфеномена, тромбоза и эмболии.
Артериальное полнокровие - повышенное кровенаполнение органа, ткани вследствие увеличенного притока артериальной крови.
Общий характер: при ↑ ОЦК или числа эритроцитов, отмечается красная окраска кожных покровов и слизистых оболочек и повышение артериального давления.
Местный характер: возникает чаще; различают физиологическую артериальную гиперемию, возникающую при действии адекватных доз физических и химических факторов, при чувстве стыда и гнева (рефлекторные гиперемии), при усилении функции органов (рабочая гиперемия), и патологическую артериальную гиперемию.
Исходя из особенностей этиологии и механизма развития, различают следующие виды патологической артериальной гиперемии:
1. Ангионевротическая (нейропаралитическая) гиперемия наблюдается как следствие раздражения сосудорасширяющих нервов или паралича сосудосуживающих нервов. Кожа, слизистые оболочки становятся красными, слегка припухшими, на ощупь теплыми или горячими. Этот вид гиперемии может возникать на определенных участках тела при нарушении иннервации, на коже и слизистых оболочках лица при некоторых инфекциях, сопровождающихся поражением узлов симпатической нервной системы. Обычно эта гиперемия быстро проходит и не оставляет следов.
2. Коллатеральная гиперемия возникает в связи с затруднением кровотока по магистральному артериальному стволу, закрытому тромбом или эмболом. В этих случаях кровь устремляется по коллатеральным сосудам. Просвет их рефлекторно расширяется, приток артериальной крови усиливается и ткань получает увеличенное количество крови.
3. Гиперемия после анемии (постанемическая) развивается в тех случаях, когда фактор, ведущий к сдавлению артерии (опухоль, скопление жидкости в полости, лигатура и др.) И малокровию ткани, быстро устраняется. В этих случаях сосуды ранее обескровленной ткани резко расширяются и переполняются кровью, что может привести не только к их разрыву и кровоизлиянию, но и к малокровию других органов, например головного мозга, в связи с резким перераспределением крови. Поэтому такие манипуляции, как извлечение жидкости из полостей тела, удаление больших опухолей, снятие эластического жгута, производят медленно.
4. Вакатная гиперемия (от лат. Vacuus - пустой) развивается в связи с уменьшением барометрического давления. Она может быть общей, например у водолазов и кессонных рабочих при быстром подъеме из области повышенного давления. Возникающая при этом гиперемия сочетается с газовой эмболией, тромбозом сосудов и кровоизлияниями. Местная вакатная гиперемия появляется на коже под действием, например, медицинских банок, создающих над определенным участком ее разреженное пространство.
5. Воспалительная гиперемия - постоянный спутник воспаления.
6. Гиперемия на почве артериовенозного свища возникает в тех случаях, когда, например, при огнестрельном ранении или другой травме образуется соустье между артерией и веной и артериальная кровь устремляется в вену.
Значение определяется главным образом ее видом. Коллатеральная гиперемия, например, является по существу компенсаторной, обеспечивая кровообращение при закрытии артериального ствола. Воспалительная гиперемия - обязательный компонент этой защитно-приспособительной реакции. Однако вакатная гиперемия становится одним из слагаемых кессонной болезни.
21. Венозное полнокровие. 1. Определение понятия. 2-3. Острое (местное и общее) венозное полнокровие, причины развития, морфологические изменения в тканях. 4-5. Хроническое (местное и общее) венозное полнокровие, причины развития, морфологические изменения в тканях.
ВЕНОЗНОЕ ПОЛНОКРОВИЕ (поб) - переполнение кровью венозного отдела сосудистой сети. Венозное полнокровие - повышенное кровенаполнение органа или ткани в связи с уменьшением (затруднением) оттока крови; приток крови при этом не изменен или уменьшен. Застой венозной крови (застойная гиперемия) приводит к расширению вен и капилляров, замедлению в них кровотока, с чем связано развитие гипоксии, повышение проницаемости базальных мембран капилляров.
Венозное полнокровие может быть общим и местным. Общее венозное полнокровие развивается при патологии сердца, ведущей к острой или хронической сердечной (сердечно-сосудистой) недостаточности.
Местное венозное полнокровие:
Обтурационная - закупорка просвета вены тромбом, эмболом (облитерирующий тромбофлебит печеночных вен – болезнь Хиари, при которой также как при общем венозном полнокровии будет развиваться мускатная печень; цианотическая индурация почек при тромбозе почечных вен);
Компрессионная - при сдавлении вены извне воспалительным отеком, опухолью, лигатурой, разрастающейся соединительной тканью;
Коллатеральная - при закрытии крупного магистрального венозного ствола, например, портокавальные анастомозы при затруднении оттока крови по воротной вене (тромбоз воротной вены, цирроз печени). Такие изменения носят название варикозное расширение вен и наблюдаются на нижних конечностях, в семенном канатике (варикоцеле), в широких связках матки, в области уретры, в области заднепроходного отверстия и близлежащей части прямой кишки – геморрой. На передней брюшной стенке переполненные венозной кровью сосуды имеют вид, получивший название “головы медузы». Переполненные кровью коллатеральные вены резко расширяются, а стенка их истончается. При варикозном расширении вен нижних конечностей отмечаются синюшность, отеки, выраженные атрофические процессы: кожа и подкожная клетчатка, особенно нижней трети голени, очень истончаются, а возникающие затем язвы голени поддаются излечению с большим трудом (“варикозные язвы голени”).
Острое венозное полнокровие, является проявлением синдрома острой сердечной недостаточности (при инфаркте миокарда, остром миокардите), в результате гипоксического повреждения гистогематических барьеров и резкого повышения капиллярной проницаемости в тканях наблюдаются плазматическое пропитывание (плазморрагия) и отек, стазы в капиллярах и множественные кровоизлияния диапедезного характера, в паренхиматозных органах появляются дистрофические и некротические изменения.
Структурно-функциональные особенности органа, в котором развивается острый венозный застой, определяют преобладание отечно-плазморрагических, геморрагических либо дистрофических и некротических изменений. В легких гистофизиологические особенности аэрогематического барьера объясняют развитие при остром венозном застое преимущественно отека и геморрагии. В почках вследствие особенностей структуры нефрона и кровообращения возникают в основном дистрофические и некротические изменения, особенно эпителия канальцев. В печени в связи с особенностями архитектоники печеночной дольки и ее кровообращения при остром полнокровии появляются центролобулярные кровоизлияния и некрозы.
Хроническое общее венозное полнокровие развивается при ХСН. Длительно поддерживая состояние тканевой гипоксии, оно определяет развитие не только плазморрагии, отека, стаза и кровоизлияний, дистрофии и некроза, но и атрофических и склеротических изменений. Склеротические изменения связаны с тем, что хроническая гипоксия стимулирует синтез коллагена фибробластами и фибробластоподобными клетками. Соединительная ткань вытесняет паренхиматозные элементы, развивается застойное уплотнение (индурация) органов и тканей. Порочный круг при хроническом венозном полнокровии замыкается развитием капиллярно-паренхиматозного блока в связи с «утолщением» базальных мембран эндотелия и эпителия за счет повышенной продукции коллагена фибробластами, гладкими мышечными клетками и липофибробластами.
• Кожа, особенно нижних конечностей, становится холодной и приобретает синюшную окраску (цианоз). Вены кожи и подкожной клетчатки расширены, переполнены кровью; также расширены и переполнены лимфой лимфатические сосуды. Выражены отек дермы и подкожной клетчатки, разрастание в коже соединительной ткани. В связи с венозным застоем, отеком и склерозом в коже легко возникают воспалительные процессы и изъязвления, которые долгое время не заживают.
• Печень при хроническом венозном застое увеличена, плотная, ее края закруглены, поверхность разреза пестрая, серо-желтая с темно-красным крапом и напоминает мускатный орех, поэтому такую печень называют мускатной.
При микроскопическом исследовании видно, что полнокровны лишь центральные отделы долек, где гепатоциты разрушены; эти отделы на разрезе печени выглядят темно-красными. На периферии долек клетки печени находятся в состоянии дистрофии, нередко жировой, чем объясняется серо-желтый цвет печеночной ткани.
Избирательное полнокровие центра долек связано с тем, что застой печени охватывает прежде всего печеночные вены, распространяясь на собирательные и центральные вены, а затем и на синусоиды. Последние расширяются, но только в центральных и средних отделах дольки, где встречают сопротивление со стороны впадающих в синусоиды капиллярных разветвлений печеночной артерии, давление в которых выше, чем в синусоидах. По мере нарастания полнокровия в центре долек появляются кровоизлияния, гепатоциты здесь подвергаются дистрофии, некрозу и атрофии. Гепатоциты периферии долек компенсаторно гипертрофируются и приобретают сходство с центролобулярными. Разрастание соединительной ткани в зоне кровоизлияний и гибели гепатоцитов связано с пролиферацией клеток синусоидов - липоцитов, которые могут выступать в роли фибробластов, а вблизи центральных и собирательных вен - с пролиферацией фибробластов адвентиции этих вен. В результате разрастания соединительной ткани в синусоидах появляется непрерывная базальная мембрана, т.е. Происходит капилляризация синусоидов, возникает капиллярно-паренхиматозный блок, который, усугубляя гипоксию, ведет к прогрессированию атрофических и склеротических изменений печени.
В финале развивается застойный фиброз (склероз) печени. Развивается застойный (мускатный) цирроз печени, который называют также сердечным, так как он обычно встречается при хронической сердечной недостаточности.
• В легких при хроническом венозном полнокровии развиваются два вида изменений - множественные кровоизлияния, обусловливающие гемосидероз легких, и разрастание соединительной ткани, т.е. Склероз. Легкие становятся большими, бурыми и плотными - бурое уплотнение (индурация) легких. В ответ на гипертензию в малом круге кровообращения происходит гипертрофия мышечно-эластических структур мелких ветвей легочной вены и артерии с перестройкой сосудов по типу замыкающих артерий, что предохраняет капилляры легкого от резкого переполнения кровью. Со временем адаптивные изменения сосудов легкого сменяются склеротическими, развиваются декомпенсация легочного кровообращения, переполнение капилляров межальвеолярных перегородок кровью. Нарастает гипоксия ткани, в связи с чем повышается сосудистая проницаемость, возникают множественные диапедезные кровоизлияния. В альвеолах, бронхах, межальвеолярных перегородках, лимфатических сосудах и узлах легких появляются скопления нагруженных гемосидерином клеток - сидеробластов и сидерофагов и свободнолежащего гемосидерина. Возникает диффузный гемосидероз легких. Гемосидерин и белки плазмы (фибрин) «засоряют» строму и лимфатические дренажи легких, что ведет к резорбционной недостаточности их лимфатической системы, которая сменяется механической. Склероз кровеносных сосудов и недостаточность лимфатической системы усиливают легочную гипоксию, которая становится причиной пролиферации фибробластов, утолщения межальвеолярных перегородок. Возникает капиллярно-паренхиматозный блок, замыкающий порочный круг в морфогенезе индурации легких, развивается застойный склероз легких. Он более значителен в нижних отделах легких, где сильнее выражен венозный застой и больше скоплений кровяных пигментов, фибрина.
• Почки при хроническом общем венозном застое становятся большими, плотными и цианотичными - цианотическая индурация почек. Особенно полнокровны вены мозгового вещества и пограничной зоны. На фоне венозного застоя развивается лимфостаз. В условиях нарастающей гипоксии возникают дистрофия нефроцитов главных отделов нефрона и склероз, который, однако, не бывает резко выраженным.
• Хронический венозный застой в селезенке также ведет к ее цианотической индурации. Она увеличена, плотна, темно-вишневого цвета, отмечаются атрофия фолликулов и склероз пульпы.
• При общем хроническом венозном застое цианотическая индурация свойственна и другим органам.
22. Патоморфология хронической сердечной недостаточности. 1. Причины развития. 2-3. Морфологические изменения внутренних органов (легкие, печень, почки, селезенка). 4. Отечный синдром – механизм развития, клиническое значение. 5. Морфологические основы развития полиорганной недостаточности.
Наиболее частыми причинами развития ХСН являются: АГ и ИБС, реже пороки сердца и миокардиты. Механизмы развития связаны с патологиями миокарда (↓ количества кардиомиоцитов и сократительной активности жизнеспособных кардиомиоцитов), гемодинамической нагрузкой (предшествует гиперфункция и гипертрофия миокарда), токсическим поражением миокарда.
Печень при ХСН увеличена, плотная, ее края закруглены, поверхность разреза пестрая, серо-желтая с темно-красным крапом и напоминает мускатный орех, поэтому такую печень называют мускатной. При микроскопическом исследовании видно, что полнокровны лишь центральные отделы долек, где гепатоциты разрушены; эти отделы на разрезе печени выглядят темно-красными. На периферии долек клетки печени находятся в состоянии дистрофии, нередко жировой, чем объясняется серо-желтый цвет печеночной ткани.
Избирательное полнокровие центра долек связано с тем, что застой печени охватывает прежде всего печеночные вены, распространяясь на собирательные и центральные вены, а затем и на синусоиды. Последние расширяются, но только в центральных и средних отделах дольки, где встречают сопротивление со стороны впадающих в синусоиды капиллярных разветвлений печеночной артерии, давление в которых выше, чем в синусоидах. По мере нарастания полнокровия в центре долек появляются кровоизлияния, гепатоциты здесь подвергаются дистрофии, некрозу и атрофии. Гепатоциты периферии долек компенсаторно гипертрофируются и приобретают сходство с центролобулярными. Разрастание соединительной ткани в зоне кровоизлияний и гибели гепатоцитов связано с пролиферацией клеток синусоидов - липоцитов, которые могут выступать в роли фибробластов, а вблизи центральных и собирательных вен - с пролиферацией фибробластов адвентиции этих вен. В результате разрастания соединительной ткани в синусоидах появляется непрерывная базальная мембрана, т.е. Происходит капилляризация синусоидов, возникает капиллярно-паренхиматозный блок, который, усугубляя гипоксию, ведет к прогрессированию атрофических и склеротических изменений печени.
В финале развивается застойный фиброз (склероз) печени. Развивается застойный (мускатный) цирроз печени, который называют также сердечным, так как он обычно встречается при хронической сердечной недостаточности.
В легких развиваются два вида изменений - множественные кровоизлияния, обусловливающие гемосидероз легких, и разрастание соединительной ткани, т.е. Склероз. Легкие становятся большими, бурыми и плотными - бурое уплотнение (индурация) легких. В ответ на гипертензию в малом круге кровообращения происходит гипертрофия мышечно-эластических структур мелких ветвей легочной вены и артерии с перестройкой сосудов по типу замыкающих артерий, что предохраняет капилляры легкого от резкого переполнения кровью. Со временем адаптивные изменения сосудов легкого сменяются склеротическими, развиваются декомпенсация легочного кровообращения, переполнение капилляров межальвеолярных перегородок кровью. Нарастает гипоксия ткани, в связи с чем повышается сосудистая проницаемость, возникают множественные диапедезные кровоизлияния. В альвеолах, бронхах, межальвеолярных перегородках, лимфатических сосудах и узлах легких появляются скопления нагруженных гемосидерином клеток - сидеробластов и сидерофагов и свободнолежащего гемосидерина. Возникает диффузный гемосидероз легких. Гемосидерин и белки плазмы (фибрин) «засоряют» строму и лимфатические дренажи легких, что ведет к резорбционной недостаточности их лимфатической системы, которая сменяется механической. Склероз кровеносных сосудов и недостаточность лимфатической системы усиливают легочную гипоксию, которая становится причиной пролиферации фибробластов, утолщения межальвеолярных перегородок. Возникает капиллярно-паренхиматозный блок, замыкающий порочный круг в морфогенезе индурации легких, развивается застойный склероз легких. Он более значителен в нижних отделах легких, где сильнее выражен венозный застой и больше скоплений кровяных пигментов, фибрина.
Почки становятся большими, плотными и цианотичными - цианотическая индурация почек. Особенно полнокровны вены мозгового вещества и пограничной зоны. На фоне венозного застоя развивается лимфостаз. В условиях нарастающей гипоксии возникают дистрофия нефроцитов главных отделов нефрона и склероз, который, однако, не бывает резко выраженным.
Хронический венозный застой в селезенке также ведет к ее цианотической индурации. Она увеличена, плотна, темно-вишневого цвета, отмечаются атрофия фолликулов и склероз пульпы.
Отечный синдром при ХСН связан с ↑ ОЦК и задержкой натрия. Данные изменения возникают с одной стороны из-за снижения кровотока в почках и активации РАГ-системы, вследствие которого ↓ диурез и ↑ ОЦК. В то же время вследствие венозного застоя ↑ гидростатическое давление в капилярах и возникает транссудация жидкой части крови в ПЖК. Начальные стадии сердечной недостаточности характеризуются легкой пастозностью, затем локальной отечностью в области стоп и голеней. Больные отмечают появление или усиление отечности преимущественно к вечеру, к концу рабочего дня, к утру отеки полностью исчезают или значительно уменьшаются. Чем тяжелее стадия ХСН, тем выраженнее отеки. По мере прогрессирования отеки становятся более распространенными и могут локализоваться не только в области стоп, лодыжек, голеней, но и в области бедер, мошонки, передней стенки живота, в поясничной области. Крайняя степень отечного синдрома — анасарка. В связи с венозным застоем, отеком и склерозом в коже легко возникают воспалительные процессы и изъязвления, которые долгое время не заживают.
Полиорганная недостаточность связана со снижением сократительной способности сердца и микроциркуляторных нарушений, которые распространяются на весь организм. В итоге во всех органах развивается хронический венозный застой, ведущий к хронической гипоксии.
23. Малокровие. 1. Определение понятия, классификация. 2. Анемия и ишемия - общее и различия. 3. Виды анемии. 4. Причины ишемии. 5. Морфологические изменения тканей при остром и хроническом малокровии.
Малокровие, или ишемия (от греч. Ischo - задерживать) — внезапное или постепенно развивающееся уменьшение притока крови к какому-либо участку органа; уменьшенное кровенаполнение ткани, органа, части тела в результате недостаточного притока крови. Малокровие может быть общим и местным. По продолжительности развития выделяют острую и хроническую ишемию.
Общее малокровие, или анемия, является заболеванием кроветворной системы и характеризуется недостаточным содержанием эритроцитов и гемоглобина. Общее между анемией и ишемией — гипоксия тканей.
В зависимости от этиологии и патогенеза различают основные группы анемий:
1) вследствие кровопотери (постгеморрагические анемии);
2) вследствие нарушенного кровообразования;
3) вследствие повышенного кроворазрушения (гемолитические анемии).
По характеру течения анемии делят на острые и хронические.
В соответствии с морфологическим и функциональным состоянием костного мозга, отражающим его регенераторные возможности, анемия может быть регенераторной, гипорегенераторной, гипопластической, апластической, диспластической.
Изменения ткани, возникающие при малокровии, в конечном счете связаны с гипоксией или аноксией, т.е. Кислородным голоданием. В зависимости от причины, вызвавшей малокровие, момента внезапности ее возникновения, длительности гипоксии и степени чувствительности к ней ткани при малокровии возникают либо тонкие изменения на уровне ультраструктур, либо грубые деструктивные изменения, вплоть до ишемического некроза - инфаркта.
В зависимости от причин и условий возникновения различают следующие виды малокровия:
1. Ангиоспастическое малокровие возникает вследствие спазма артерии в связи с действием различных раздражителей. Например, болевое раздражение может вызвать спазм артерий и малокровие определенных участков тела. Таков же механизм действия сосудосуживающих лекарственных препаратов (например, адреналина). Ангиоспастическая ишемия появляется и при отрицательных эмоциональных аффектах («ангиоспазм неотреагированных эмоций»).
2. Обтурационное малокровие развивается вследствие закрытия просвета артерии тромбом или эмболом, в результате разрастания соединительной ткани в просвете артерии при воспалении ее стенки (облитерирующий эндартериит), сужения просвета артерии атеросклеротической бляшкой. Обтурационная ишемия, обусловленная тромбозом артерии, нередко завершает ангиоспазм, и наоборот, ангиоспазм дополняет обтурацию артерии тромбом или эмболом.
3. Компрессионное малокровие появляется при сдавлении артерии опухолью, выпотом, жгутом, лигатурой.
4. Ишемия в результате перераспределения крови наблюдается в случаях гиперемии после анемии. Такова, например, ишемия головного мозга при извлечении жидкости из брюшной полости, куда устремляется большая масса крови.
При остром малокровии обычно возникают дистрофические и некробиотические изменения. Им предшествуют гистохимические и ультраструктурные изменения - исчезновение из ткани гликогена, ↓ активности окислительно-восстановительных ферментов и деструкция митохондрий. Для макроскопической диагностики применяют различные соли тетразолия, теллурит калия, которые вне участков ишемии (где активность дегидрогеназ высокая) восстанавливаются и окрашивают ткань в серый или черный цвет, а участки ишемии (где активность ферментов снижена или отсутствует) остаются неокрашенными. На основании результатов электронно-гистохимического изучения тканевых изменений при остром малокровии и при инфаркте острую ишемию следует рассматривать как преднекротическое (предынфарктное) состояние.
При длительном малокровии развиваются атрофия паренхиматозных элементов и склероз в результате повышения коллагенсинтезирующей активности фибробластов.
Значение и последствия малокровия зависят от особенностей причины и продолжительности ее действия. Малокровие вследствие спазма артерий обычно непродолжительно и не вызывает особых расстройств. Однако при длительных спазмах возможно развитие дистрофических изменений и даже ишемического некроза (инфаркт). Острое обтурационное малокровие особенно опасно, так как нередко ведет к инфаркту. Если закрытие просвета артерии развивается медленно, то кровообращение может быть восстановлено с помощью коллатералей и последствия такой анемии могут быть незначительными. Однако длительно существующее малокровие рано или поздно ведет к атрофии и склерозу.
24. Инфаркт. 1. Определение. 2. Причины развития инфарктов. 3-4. Морфологические разновидности инфарктов. Морфологические особенности инфарктов в сердце, головном мозге, почках, лёгких, селезёнке. 5. Исходы и причины смерти.
Инфаркт (от лат. Infarcire - начинять, набивать) - разновидность некроза в каком-либо органе при острой ишемии; сосудистый (ишемический) некроз, следствие и крайнее выражение ишемии.
Причины развития инфаркта - длительный спазм, тромбоз или эмболия артерии, а также функциональное напряжение органа в условиях недостаточного его кровоснабжения; недостаточность анастомозов и коллатералей, которая зависит от степени поражения стенок артерий и сужения их просветов (атеросклероз, облитерирующий эндартериит), от степени нарушения кровообращения (например, венозного застоя) и от уровня выключения артерии тромбом или эмболом. Обмен веществ в органах и тканях, в которых возникает инфаркт, как правило, нарушен в связи с гипоксией, обусловленной общими расстройствами кровообращения.
Виды инфаркта:
— клиновидные, основание клина обращено к капсуле, а острие - к воротам органа (образуются в селезенке, почках, легких, что определяется характером ангиомагистральным типом ветвления их артерий).
— неправильной формы (в сердце, мозге, кишечнике, т.е. В тех органах, где преобладает не магистральный, а рассыпной или смешанный тип ветвления артерий).
Инфаркт может охватывать большую часть или весь орган (субтотальный или тотальный инфаркт) или обнаруживается лишь под микроскопом (микроинфаркт).
Если инфаркт развивается по типу коагуляционного некроза, то ткань в области омертвения уплотняется, становится суховатой (инфаркт миокарда, почек, селезенки); если же инфаркт образуется по типу колликвационного некроза, она размягчается и разжижается (инфаркт мозга, кишки).
Цвет инфаркта:
1. Белый (ишемический) инфаркт представляет собой участок бело-желтого цвета, хорошо отграниченный от окружающей ткани. Обычно он возникает в участках с недостаточным коллатеральным кровообращением. Особенно часто встречается в селезенке, почках.
2. Белый инфаркт с геморрагическим венчиком представлен участком беложелтого цвета, но этот участок окружен зоной кровоизлияний. Она образуется в результате того, что спазм сосудов по периферии инфаркта сменяется паретическим их расширением и развитием кровоизлияний. Такой инфаркт находят в почках, миокарде.
3. При красном (геморрагическом) инфаркте участок омертвения пропитан кровью, он темнокрасный и хорошо отграничен. Благоприятным условием для такого геморрагического пропитывания является венозный застой. Определенное значение для развития красного инфаркта имеют и особенности ангиоархитектоники органа (анастомозы между бронхиальной и легочной артериями). Встречается геморрагический инфаркт, как правил, в легких, редко - в кишечнике, селезенке, почках.
В сердце инфаркт обычно белый с геморрагическим венчиком, имеет неправильную форму, встречается чаще в левом желудочке и межжелудочковой перегородке, крайне редко - в правом желудочке и предсердиях. Омертвение может локализоваться под эндокардом (субэндокардиальный инфаркт), эпикардом (субэпикардиальный инфаркт) или охватывать всю толщу миокарда (трансмуральный инфаркт). В области инфаркта на эндокарде нередко образуются тромботические, а на перикарде - фибринозные наложения, что связано с развитием реактивного воспаления вокруг участков некроза. Чаще всего инфаркт миокарда встречается на фоне атеросклероза и гипертонической болезни и рассматривается как самостоятельное заболевание.
В головном мозге чаще возникает белый инфаркт, который быстро размягчается (очаг серого размягчения мозга). Если инфаркт образуется на фоне значительных расстройств кровообращения, венозного застоя, то очаг омертвения мозга пропитывается кровью и становится красным (очаг красного размягчения мозга). Инфаркт локализуется обычно в подкорковых узлах, разрушая проводящие пути мозга, что проявляется параличами. Инфаркт мозга, как и инфаркт миокарда, чаще всего встречается на фоне атеросклероза и гипертонической болезни и является одним из проявлений цереброваскулярных заболеваний.
В легких в подавляющем большинстве случаев образуется геморрагический инфаркт. Он хорошо отграничен, имеет форму конуса, основание которого обращено к плевре. На плевре в области инфаркта появляются наложения фибрина (реактивный плеврит). У острия конуса, обращенного к корню легкого, нередко обнаруживается тромб или эмбол в ветви легочной артерии. Омертвевшая ткань плотна, зерниста, темно-красного цвета. Геморрагический инфаркт легких обычно возникает на фоне венозного застоя, причем развитие его в значительной мере определяется особенностями ангиоархитектоники легких, наличием анастомозов между системами легочной и бронхиальных артерий. В условиях застойного полнокровия и закрытия просвета ветви легочной артерии в область омертвения ткани легкого из бронхиальной артерии поступает кровь, которая разрывает капилляры и изливается в просвет альвеол. Вокруг инфаркта нередко развивается воспаление легочной ткани (периинфарктная пневмония). Массивный геморрагический инфаркт легкого может быть причиной надпеченочной желтухи. Белый инфаркт в легких - исключительная редкость. Возникает он при склерозе и облитерации просвета бронхиальных артерий.
В почках инфаркт, как правило, белый с геморрагическим венчиком, конусовидный участок некроза охватывает либо корковое вещество, либо всю толщу паренхимы. При закрытии основного артериального ствола развивается тотальный или субтотальный инфаркт почки. Своеобразной разновидностью инфарктов являются симметричные некрозы коркового вещества почек, ведущие к острой почечной недостаточности. Развитие ишемических инфарктов почек связано обычно с тромбоэмболией, реже - с тромбозом ветвей почечной артерии, осложняющим ревматизм, затяжной септический эндокардит, гипертоническую болезнь, ишемическую болезнь сердца. Редко при тромбозе почечных вен возникает венозный инфаркт почек.
В селезенке встречаются белые инфаркты, нередко с реактивным фибринозным воспалением капсулы и последующим образованием спаек с диафрагмой, париетальным листком брюшины, петлями кишечника. Ишемические инфаркты селезенки связаны с тромбозом и эмболией. При тромбозе селезеночной вены иногда образуются венозные инфаркты.
Исходы некроза: отторжение некротических масс по типу мутиляции, отторжение с образованием полости (каверна), рассасывание с полным восстановлением ткани, рассасывание с образованием рубца, рассасывание с образованием полости (кисты), рассасывание или отторжение с образованием эрозии или язвы, частичное краевое рассасывание с образованием секвестра (обычно в костях), инкапсуляция очага некроза.
При благоприятном исходе вокруг омертвевших тканей возникает реактивное воспаление, которое отграничивает мертвую ткань - демаркационная зона → размножаются клетки соединительной ткани, которая замещает или обрастает участок некроза (организация – образуется рубец). Обрастание участка некроза ведет к его инкапсуляции. В мертвые массы при сухом некрозе и в очаг омертвения, подвергшийся организации, могут откладываться соли кальция — петрификация, оссификация. При рассасывании тканевого детрита и формировании капсулы, что встречается обычно при влажном некрозе на месте омертвения появляется полость - киста.
Неблагоприятный исход некроза - гнойное расплавление очага омертвения - гнойное расплавление инфарктов при сепсисе (такие инфаркты называют септическими). В исходе некроза на ранних этапах внутриутробного развития возникает порок органа, части тела.
При инфаркте миокарда смерть может наступить от ОСН, кардиогенного шока, фибриляции желудочков, асистолии, разрыва сердца. При остальных ??? Органная недостаточность.
