
Опера о чуме (учебник)

Тибета лечение, выжили, тогда как на Тибете летальность оказалась абсолютной (штаммы имели различные мутации в гене rpsL)1.
Конечно, проблема антибиотикорезистентности у чумного микроба не стоит так остро, как у других бактерий, однако существование штаммов с резистентностью к антибиотикам (Табл. 25.1) является тревожным «звонком», грозящим сильно затруднить как борьбу с инфекцией, так и её лечение. Не следует забывать и об искусственно созданных штаммах (например, Y. pestis KM219, КМ244, КМ245 и КМ258), имеющих устойчивость к канамицину, которые представляют угрозу как возможный объект биотерроризма. С другой стороны, по сведениям Игоря Валериановича Домарадского, им (с коллегами) был получен антибиотикорезистентный штамм Y. pestis EV, на основе которого была создана вакцина, преимуществом которой стала возможность применения «одновременно с экстренной профилактикой с помощью антибиотиков (обычная же вакцина при этом погибает)»2.
Для решения проблемы антибитикорезистентности, уже ставшей актуальной и для чумы, разрабатываются альтернативные методы лечения, среди которых важную роль играет применение бактериофагов или фаготерапия. Ранее мы уже говорили о литических фагах – бактериальных вирусах с высокой специфичностью, чей жизненный цикл заканчивается лизисом клеточной стенки бактерии (соответственно, с её гибелью) и «выходом» новых бактериофагов.
История бактериофагов началась в 1895 году, когда Пéрси Фарадéй Фр нкленд3 проводил опыты4 по сокультивированию брю-
шнотифозной (Salmonella typhi) и кишечной (Escherichia coli) палочек
1Это свидетельствует в пользу того, что резистентность к стрептомицину не явилась причиной смерти паицентов из Тибета.
2Создан в рамках «пятой» проблемы (бактериологической защиты) примерно 1970–1973 года, данные не публиковались; цит. по: Домарадский И.В. Перевёртыш
(рассказ «неудобного человека»). М.: [б. и.], 1995. 176 с.
3Percy Faraday Frankland, 1858–1946; британский химик. Член Королевского общетсва Лондона (1891). Вместе со своей женой Грейс Франкленд выделил первую
чистую культуру нитрифицирующих (т. е. окисляющих аммиак) бактерий.
4 Frankland P. Ueber das Verhalten des Typhusbacillus und des Bacillus coli communis im Trinkwasser. Zeitschrift für Hygiene und Infektionskrankheiten 1895; 19(1):393–407; DOI: 10.1007/bf02216789.
290

Табл. 25.1. Штаммы чумного микроба с резистентностью к антибиотикам
Год |
Место |
Хозяин |
Меха- |
Резистент- |
Штамм |
|
низм |
ность |
Y. pestis |
||||
|
|
|
||||
1987 |
Андапа |
человек |
мутация |
стрептомицин |
12/87 |
|
(Мадагаскар) |
гена rpsL |
|||||
|
|
|
|
|||
1995 |
Амбалавао |
человек |
плазмида |
множествен- |
17/95 |
|
(Мадагаскар) |
IP1202 |
ная1 |
(IP275) |
|||
|
|
|||||
1995 |
Ампитана |
человек |
плазмида |
стрептомицин |
16/95 |
|
(Мадагаскар) |
IP1203 |
|||||
|
|
|
|
|||
1996 |
Кайю |
человек |
мутация |
стрептомицин |
S19960127 |
|
(Тибет) |
гена rpsL |
|||||
|
|
|
|
|||
|
Антанана- |
|
плазмида |
|
|
|
1998 |
риву (Мада- |
крыса |
доксициклин |
IP2180Н |
||
рIP2180Н |
||||||
|
гаскар) |
|
|
|
||
|
|
|
|
|
||
1999 |
Казахстан |
человек |
? |
левомицетин |
? |
|
2013 |
Фарацихо |
человек |
мутация |
стрептомицин |
56/13 |
|
(Мадагаскар) |
гена rpsL |
|||||
|
|
|
|
|||
2013 |
Фарацихо |
человек |
мутация |
стрептомицин |
59/13 |
|
(Мадагаскар) |
гена rpsL |
|||||
|
|
|
|
|||
1960- |
Монголия |
сурок |
? |
множествен- |
MNG3122 |
|
2007 |
ная2 |
|||||
|
|
|
|
Примечание:
1 стрептомицин, ампициллин, канамицин, спектиномицин, сульфаниламид, тетрациклин, миноциклин и хлорамфеникол (чувствителен к котримоксазолу).
2 гентамицин, тетрациклин, доксициклин, хлорамфеникол
в воде, обнаружив, что в случае культивирования в воде из английской реки Темзы первые стремительно погибают, чему он не смог найти объяснение. В 1896 году Эрнéст Хэ нбери Хэ нкин1, желая изучить количество содержащихся в индийской реке Ганг холерных вибрионов (Vibrio cholerae), обнаружил2, что в 1 мл воды на месте
1 Ernest Hanbury Hankin, 1865–1939; британский врач, бактериолог. Автор работ по холере и малярии, а также свойствам опиума и яда кобры. Изучал фауну Индии
(в основном птиц) и архитектуру Великих Моголов.
2 Hankin E. H. L'action bactericide des eaux de la Jumna et du Gange sur le vibrion du cholera. Annales de l'Institut Pasteur. 1896; 10:511–523.
291

входа в город Агру содержится 100 000 бактериальных клеток, тогда как на выходе – только 90 клеток. Это явление также тогда не нашло объяснения и было названо «феноменом Хэнкина». Похожее явление через два года наблюдал Николай Фёдорович Гамалéя1, когда культивируемый в дистиллированной воде сибиреязвенный микроб (Bacillus anthracis) стремительно погибал, а жидкость приобретала способность лизировать другие культуры сибиреязвенного микроба. Увиденное он объяснил2 действием бактериолизина, образующегося при распаде бактерий. Многие учёные опишут схожие явления, и только в 1915 году Фредерик Туóрт3 сообщит4 о неком агенте, способном заражать стафилококки, уже определив его как вирус, а два года спустя Фéликс д’Эрéлль5, обнаружив вирус возбудителя дизентерии (Shigella spp.)6, назвёт его «бактериофагом» (греч. φ γω – «пожираю»; Рис. 25.1). Он же успешно применит бактериофаги во время эпидемий чумы и холеры в Египте (1921) и предложит их использовать для лечения инфекционных болезней.
Примерно в это же время Феликс д’Эрелль знакомится с Георгием Григорьевичем Эли вой7, найдя в его лице соратника, благодаря
1 1859–1949; украинский и советский врач, бактериолог, эпидемиолог. Членкорреспондент (1939) и почётный член (1940) Академии наук СССР, академик Академии медицинских наук СССР (1945). Лауреат Сталинской премии (1943). Автор работ по инфекционным болезням, внёс значительный вклад в иммунологию и разработал учение об иммунитете. Научный руководитель (1930–1938) Центрального института эпидемиологии и микробиологии (ныне – НИЦ эпидемиологии и микробиологии им. Н. Ф. Гамалеи).
2Гамалея Н. Ф. Бактериолизины – ферменты, разрушающие бактерии. Русский архив патологии, клинической медицины и бактериологии. 1898; 6:148–161 (цит. по D.
Bardell [1982]: «N. F. Gamaleya, ‘Bacteriolysins – ferments destroying bacteria’, Russian Archives of Pathology, Clinical Medicine, and Bacteriology, 1898, 6, 607–613 [in Russian]»).
3Frederik Twort; 1877–1950; британский врач, бактериолог, автор работ по ин-
фекционным болезням. Член Королевского общества Лондона (1929)
4 Twort F. W. An investigation on the nature of ultra-microscopic viruses. Lancet. 1915; 186(4814):1241–1243; DOI: 10.1016/S0140-6736(0)20383-3.
5 Félix d’Hérelle, 1873–1949; французский и канадский энтузиаст, не имевший ни-
какого специального образования, но ставший отцом фагологии.
6 D’Hérelles F. Sur un microbe invisible antagoniste des bacilles dysentériques.
Comptes Rendus Academie des Sciences Paris. 1917; 165:373–375.
7 , 1892–1937; советский (грузинский) врач, бактериолог, основоположник фаготерапии в СССР и основатель Института бактериофага (ныне – Институт бактериофага, микробиологии и вирусологии им. Г. Элиавы). Как враг народа расстрелян 09.07.1937; реабилитирован Военной коллегией Верховного суда СССР
22.08.1957 «за отсутствием состава преступления».
292
чему в 1923 году в городе Тбилиси (Грузия, СССР) появляется Институт бактериофага (сам Феликс д’Эрелль несколько лет жил в городе Тбилиси, но на фоне репрессий 1930-х годов спешно покинул СССР).
Появление антибиотиков, однако, предало забвению идею фаготеропии, а её изучением продолжили заниматься только в СССР, что сыграло важную роль во время Второй мировой войны, когда Магдалина Петровна Покрóвская1 успешно применяла бактериофаги для лечения ран у солдат.
Вместе с тем для лечения чумы, за исключением опыта Феликса д’Эрелля, приведшего к выздоровлению четырёх пациентов с бубонной формой2 , бактериофаги не использовались 3 . Опыты 4 , проведён-
ные на животных, показали, что независимо от формы чумы и способа введения бактериофага (интраназально, внутрибрюшинно, внутривенно), даже в случае коктейля (т. е. смеси бактериофагов), фаготерапия не предотвращает бактериемию, а только отсрочивает гибель животных, при том, что бактериофаг аккумулируется в ор-
1 1901–1980; советский (российский) врач, бактериолог, эпидемиолог. Заслуженный деятель науки РСФСР. Заместитель директора по научной работе Научноисследовательского противочумного института Кавказа и Закавказья (ныне – Ставропольский научно-исследовательский противочумный институт). Автор знаменитой книги «Лечение ран бактериофагом» (1941), в которой изложен опыт применения бактериофагов при лечении ран (в том числе гнойных) во время войны. Выделила противочумный бактериофаг, названный в её честь.
2D’Herelle F. Essai de traitement de la peste bubonique par le bacteriophage. Press. Med. 1925; 33:1393–1394.
3Противочумный бактериофаг Покровской примеянется только для диагности-
ческих целей.
4 Filippov A. A., Sergueev K. V., et al. Bacteriophage therapy of experimental bubonic plague in mice. Adv Exp Med Biol. 2012; 954:337–348; DOI: 10.1007/978-1-4614-3561-7_41; Vagima Y., Gur D., et al. Phage Therapy Potentiates Second-Line Antibiotic Treatment against Pneumonic Plague. Viruses. 2022; 14(4):688; DOI: 10.3390/v14040688.
293
ганах и крови животного уже через 30 минут. Вероятно, кровь ингибирует его литические свойства.
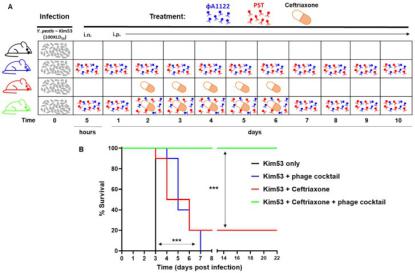
С другой стороны, сочетание фаговой терапии и антибиотиков (в дозировке, недостаточной для лечения) обеспечивает выживание при лёгочной форме чумы (Рис. 25.2), что особенно показательно ввиду сложности лечения данной формы заболевания. Кроме того, такая комбинированная терапия возможна с препаратами второй линии (в частности, цефтриаксоном).
Рис. 25.2. Схема лечения (А) и кривые выживаемости (В) мышей при аэрогенном инфицировании штаммом Y. pestis KIM53. Контрольные мыши (чёрный цвет), не получавшие лечения, умерли на 3 день. Мыши, получавшие лечение, к пятому дню обнаруживали лучшую выживаемость при фаготерапии (синий цвет), однако, к 7 дню все погибали, тогда как 20 % мышей при антибиотикотерапии (красный цвет) выживали. Мыши, получавшие комбинированное лечение, выживали в 100% случаев. В качестве антибиотикотерапии применялось подкожное введение цефтриаксона, в качестве фаготерапии – интраназальное или внутрибрюшинное
введение коктейля фагов ϕА1122 и PST (по Vagima Y., 2022)
294

26 |
ПРОФИЛАКТИКА |
|
|
Не бывает пророк без чести, разве только в отечестве своём и у родственников, и в доме своём…
Мк. 6:4
Эффективным способом борьбы с инфекционными заболеваниями является профилактика (специфическая и неспецифическая). Как мудро отмечал Китасато Сибасабуро: «В борьбе с чумой нельзя полагаться только на карантин».
К неспецифической профилактике относят комплекс мер, направленных на ограничение контакта человека с чумным микробом (Рис. 26.1). К ним, с одной стороны, относят просветительскую работу с населением, ограничительные мероприятия, специальную подготовку ветеринарных и медицинских работников. На приведённых примерах мы видели, что люди, живущие на территории природных очагов, могут употреблять в пищу сырые органы сурков, а врачи далеко не всегда способны распознать чуму, причём как у человека, так и животного (особенно когда речь идёт о таком редком явлении, как первичная лёгочная чума у собак). С другой стороны, важным компонентом неспецифической профилактики является эпидемиологический надзор за очагом (Рис. 26.2 и Рис. 26.3), который включает в себя наблюдение за течением эпизоотий – идентификация возбудителя, а также учёт и своевременная регуляция численности носителей и переносчиков 1 . Наблюдение осуществляется специальными бригадами, которые производят забор проб окружающей среды и отлов животных (носителей и переносчиков). В экстренных случаях проводят дезинфекцию (т. е. уничтожение возбудителя), дезинсекцию (т. е. уничтожение пере-
1 В случае возникновения антропургических очагов проводят экстренные дезинфекционные мероприятия, включающие умерщвление носителей и их исследование
(Рис. 26.4).
295

Рис. 26.1. Плакат в деревне Еа-Ви (провинция Даклак), призывающий к уничтожению крыс для борьбы с чумой (слева) и плакат на дороге
Хошимин – Далат, предупреждающий об очаге чумы (справа), Вьетнам, 2004 год (любезно предоставлено Виктором Васильевичем Сунцовым)
носчиков1) и дератизацию (т. е. уничтожение носителей2). Для дезинфекции применяют физические и химические методы. К первым относятся сжигание, кипячение, паровая и ультрафиолетовая обработки (и др.), ко вторым – применение хлорсодержащих (хлорная известь) и кислородсодержащих (перекись водорода) препаратов, альдегидов (глутаровый альдегид) и спиртов (этиловый спирт), а также любых веществ, активных в отношении возбудителя3. При осуществлении дезинсекционных и дератизационных
мероприятий первостепенное значение имеют предотвращение
загрязнения природы и сохранение биологического разнообразия.
1Интересно, что ещё в Древнем Египте населению рекомендовалось покрывать тело маслом моринги масличной (Moringa oleifera) для защиты от укусов клещей, блох и комаров (Папирус Эберса, ок. 1550 года до н. э.).
2В данном случае грызунов.
3Следует помнить, что даже истребление основного носителя не может привести к ликвидации очага, примером чего является истребление малого суслика на территории Прикаспийского Северо-Западного степного очага к 1960 году. Уже в 1972 году эпизоотическая активность очага возобновилась.
296

Рис. 26.2. Полевая работа в очаге чумы (1954). На фотографии, любезно предоставленной Андреем Павловичем Анисимовым, запечатлён его отец, Павел Иванович Анисимов1, подкармливающий местного верблюда во время одной из «верблюжьих экспедиций»2. Как мы помним, верблюды являются носителями чумы, но заразиться можно только от их мяса и молока, не прошедших термической обработки. Обратите внимание на одежду специалиста (так называемую пижаму), о ней подробнее поговорим в Главе 28.
11929–2019; советский (российский) врач, бактериолог. Директор Российского противочумного института «Микроб» (1973–1988). Один из основоположников отечественной генетики особо опасных инфекций, создатель (с колл.) диагностических и профилактических препаратов, в частности, вакцины холерной бивалентной химической таблетированной (патент RU 2080121 C1, 27.05.1997).
2целью экспедиций, проводимых силами сотрудников Небит – Дагского отделения Туркменской противочумной станции (ныне – Балканабадское отделение Центра профилактики особо опасных инфекций), было определение роли верблюдов в эпидемиологии чумы, изучение их восприимчивости к чуме, механизма заражения
вприродных и экспериментальных условиях, уточнение патогенеза и клиники.
297

Рис. 26.3. Исследование популяции гималайских сусликов
(Marmota himalayana) в природном очаге чумы провинции Сычуань (Китай)
Рис. 26.4. Массовое исследование умерщвлённых портовых крыс в Японии во время третьей пандемии чумы. Подобные меры позволили выявить чумной микроб до заболевания первого человека во время завоза в город Йокогама в 1902 году
(по Shibasaburo K., 1906; публикуется с разрешения Мемориального музея Образовательной корпорации Института Китасато)
298
Оценку эпидемиологического потенциала природного очага (т. е. показателя опасности заражения людей) осуществляют по формуле:
П |
, |
где S – площадь эпизоотии, Y – интенсивность эпизоотии, К – доля участка очага, занятая поселениями основного носителя, Р – плотность грызунов или их поселений на 1 км2, М – запас блох на 1 км2, V – вирулентность штаммов возбудителя, В1 – контакт человека с блохами носителей, В2 – наличие блох и грызунов в жилье, В3 – наличие верблюдов и их численость, В4 – охота на основных и случайных носителей, В5 – близость людских поселений к местам обитания носителей и контакт детей с ними, В6 – наличие в жилье человека кошек и собак.
На современном этапе данная формула лежит в основе компьютерных программ для оценки эпидемиологического потенциала природного очага, а критерии Bi включают в себя множество уточнений, например, контакт с большой песчанкой (В11) или браконьерство (В42).
Следует понимать, что случай заражения даже одного человека является чрезвычайной ситуацией в области общественного здравоохранения, однако в зависимости от развития инфраструктуры территории и напряжённости эпидемиологической обстановки, сложившейся в природных очагах, чрезвычайная ситуация может иметь различное значение (Табл. 26.1).
Конечную оценку проводят по величине итогового показателя, равного сумме всех критериев (в долях от единицы), делённой на их количество (т. е. 5). Таким образом получают, что величина итогового показтеля для локального уровня ≤1, для регионального – от 1,1 до 3, для национального – от 3,1 до 4, а для международного – от
4,1 до 5.
299
