
- •Перелік питань до семінару Загальні шляхи метаболізму
- •2 Семестр
- •7. Обмін сірковмісних амінокислот метіоніну та цистеїну. Біосинтез та біологічна роль креатину і креатинфосфату.
- •8. Спеціалізовані шляхи метаболізму циклічних амінокислот – фенілаланіну, тирозину, триптофану.
- •15. Глюкозо-лактатний цикл, схема взаємозв’язку гліколізу та глюконеогенезу. Роль лдг у м’язах та печінці. Гормональна регуляція процесів.
- •16. Глюкозо-аланіновий цикл, схема взаємозв’язку гліколізу та глюконеогенезу. Роль алт у м’язах та печінці. Гормональна регуляція процесів.
- •20. Біосинтез пуринових нуклеотидів: схема реакцій синтезу імф; утворення амф та гмф; механізми регуляції. Роль амінокислот.
- •21. Біосинтез піримідинових нуклеотидів: схема реакцій; регуляція синтезу. Біосинтез дезоксирибонуклеотидів. Утворення тимідилових нуклеотидів; інгібітори біосинтезу дТмф як протипухлинні засоби.
- •22. Обмін порфіринів. Роль цтк та амінокислот в синтезі гему. Регуляція процесу. Катаболізм гемоглобіну, утворення та детоксикація білірубіну.
- •Ситуаційні завдання
20. Біосинтез пуринових нуклеотидів: схема реакцій синтезу імф; утворення амф та гмф; механізми регуляції. Роль амінокислот.
схема реакцій синтезу ІМФ:
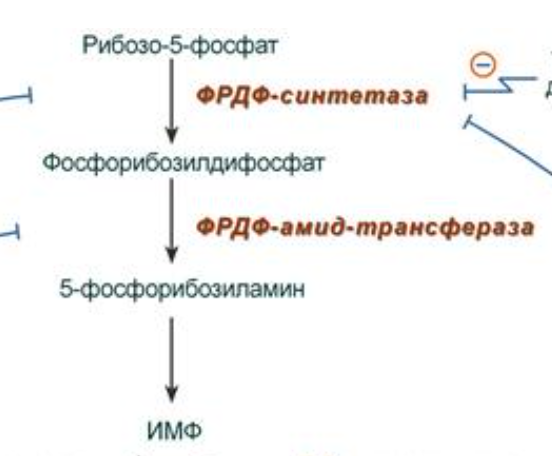
утворення АМФ та ГМФ

Регуляция синтеза пуринов (пуриновых нуклеотидов) происходит по механизму обратной отрицательной связи, т.е. продукт реакции (или совокупности реакций) ингибирует начальные этапы процесса. Для синтеза пуринов такими ингибиторами являются АМФ и ГМФ:
ГМФ блокирует первые две реакции синтеза ИМФ, а также ИМФ-дегидрогеназную реакцию,
АМФ блокирует первую реакцию синтеза ИМФ и аденилосукцинатсинтетазную реакцию.
Кроме этого, имеется положительная перекрестная регуляция со стороны АТФ и ГТФ, а именно – как участник реакций каждый из них оказывает стимулирующее влияние на синтез другого нуклеотида. Это заключается в том, что АТФ, принимая участие в ГМФ-синтетазной реакции, облегчает синтез ГМФ. В свою очередь, ГТФ является донором энергии для синтеза АМФ, участвуя в аденилосукцинат-синтетазной реакции.
Аминокислоты играют важную роль в биосинтезе пуринов, поскольку они являются составными частями некоторых межпродуктов и ковалентно связаны с пуриновыми основами на разных этапах синтеза. К примеру, аспартат, глютамат и глицин используются для формирования различных интермедиатов в биосинтезе пуринов. Таким образом, наличие и концентрация подходящих аминокислот может влиять на эффективность этого биохимического пути.
21. Біосинтез піримідинових нуклеотидів: схема реакцій; регуляція синтезу. Біосинтез дезоксирибонуклеотидів. Утворення тимідилових нуклеотидів; інгібітори біосинтезу дТмф як протипухлинні засоби.
Біосинтез піримідинових нуклеотидів:
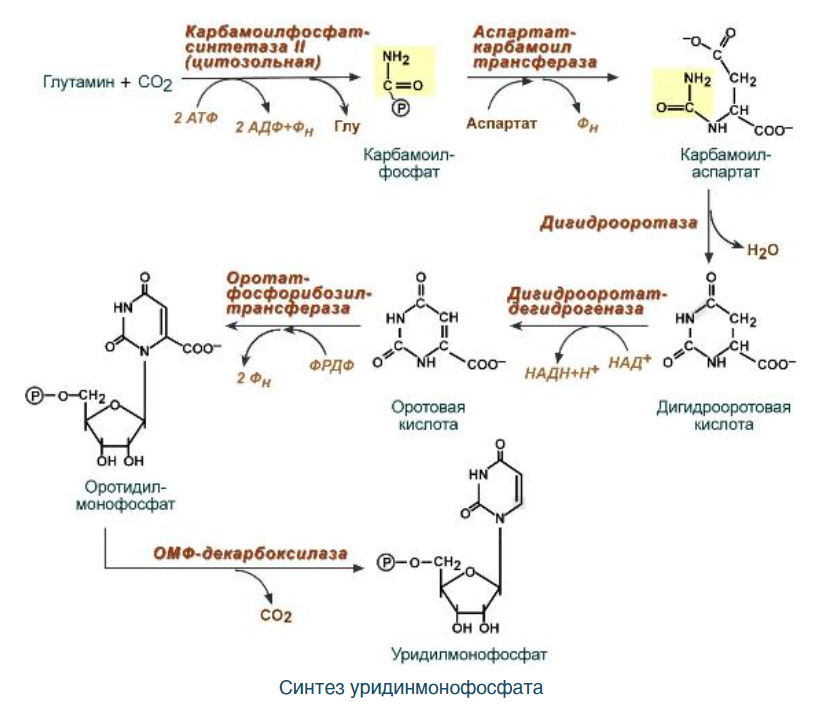
Регуляция синтеза пиримидиновых нуклеотидов. Контроль скорости биосинтеза пиримидиновых нуклеотидов обеспечивается на уровне двух регуляторных ферментов:
1) карбамоилфосфатсинтетазы, которая обеспечивает снабжение биосинтетического пути одним из первых субстратов — карбамоилфосфатом (этот пункт регуляции является основным у высших животных (млекопитающих), включая организм человека); аллостерическим ингибитором фермента является УТФ - конечный продукт биосинтетического пути; вместе с тем ФРПФ — интермедиат пуринового синтеза — увеличивает активность фермента, являющегося одним из механизмов обеспечения координированного синтеза пуринов и пиримидинов;
2) аспартаткарбамоилтрансферазы, катализирующей синтез уреидоянтарной кислоты; аллостерическим ингибитором фермента является ЦТФ, активатором - АТФ.
УТФ присоединяет аминогруппу от глутамина, превращаясь в цитидинтрифосфат. Эту реакцию провоцирует ГТФ. Помимо указанной цепи реакций может иметь место прямое включение свободных пиримидиновых оснований в состав нуклеотидов по аналогичному механизму, как для пуриновых нуклеотидов.
Наследственное нарушение синтеза пиримидинов, известное как оротацидурия, характеризуется образованием избытка оротовой кислоты и выведением ее с мочой. Причиной является низкая активность ферментов оротат-фосфорибозилтрансферазы и декарбоксилазы, катализирующих две последние реакции синтеза УМФ.
Недостаток пиримидиновых нуклеотидов будет способствовать повышенному образованию оротовой кислоты, поскольку не будет происходить торможение синтеза пиримидинов конечным продуктом. Наблюдаются задержка роста и умственного развития детей в раннем возрасте, мегалобластическая анемия. Указанные нарушения развиваются в результате недостатка пиримидиновых нуклеотидов, необходимых для синтеза нуклеиновых кислот.
Прием уридина или цитидина приводит к снижению образования и экскреции оротовой кислоты, восстанавливает нормальный рост и развитие. Такое лечение должно продолжаться на протяжении всей жизни людей с наследственным дефектом.
Синтез дезоксирибонуклеотидов происходит в три реакции

синтез ТТФ идет особым образом

Ингибиторы синтеза дТМФ как противоопухолевые препараты. Ряд структурных аналогов пуринов и пиримидинов, а также фолиевой кислоты являются ингибиторами синтеза дезоксирибонуклеотидов, они блокируют репликацию ДНК. Механизм противоопухолевого действия соединений, блокирующих синтез дТМФ: Е1-тимидилатсинтаза; Е2-дигидрофолатредуктаза; Н4F-тетрагидрофолат (ТГФК); H2F-дигидрофолат ФК
