
- •Ответы Ферменты Общие сведенья
- •Свойства витаминов
- •Ферментопатии
- •Класификация
- •Строение ферментов
- •Изоферменты
- •Специфичность
- •Кинетика ферментативных реакций
- •Механизм действия ферментов
- •Энергетический барьер реакции и энергия активации
- •Влияние активаторов и ингибиторов на скорость ферментативных реакций
- •Углеводы анаэробное окисление глюкозы
- •Аэробное окисление глюкозы
- •Гормональная регуляция глюкозы
- •Челночные механизмы
- •Глицеролфосфатный челночный механизм:
- •Малат-аспартатный челночный механизм
- •Глюконеогенез общие сведенья
- •Глюконеогенез
- •Цикл Кори (Глюкозо-Лактатный цикл)
- •Глюкозо-аланиновый цикл
- •Пентозофосфатный путь
- •Агликогенозы
- •Метаболизм Понятие о метаболизме
- •Окислительное декарбоксилирование пирувата
- •Регуляция пируватдегидрогеназного комплекса
- •Цикл трикарбоновых кислот (цикл Кребса, лимоннокислый цикл).
- •Последовательность реакций цитратного цикла:
- •Пути утилизации энергии в организме
- •Механизмы синтеза атф
- •Биологическое окисление
- •Пиридиновые дегидрогеназы
- •2. Флавиновые дегидрогеназы
- •3. СоQ или убихинон;
- •4. Цитохромная система
- •5. Железо-серные белки (железо-серные комплексы)
- •Структурно-функциональная организация компонентов дыхательной цепи в митохондриях
- •Механизм окислительного фосфорилирования и дыхательной цепи
- •Роль о2
- •Окислительное фосфорилирование и его теория.
- •Разобщение окисления и фосфорилирования
- •Ингибирование ферментов дыхательной цепи
- •Липиды Липиды в крации
- •Переваривание липидов
- •Ресинтез таг
- •Ресинтез фосфолипидов
- •Нарушение синтезу фосфоліпідів та його можливі наслідки.
- •Дисфункция клеточных мембран:
- •Воспалительные процессы:
- •Заболевания печени:
- •Катаболизм таг
- •Гормональная регуляция таг
- •Липотропные факторы
- •Окисление жирных кислот (β-окисление)
- •Расчет энергии бета-окисления
- •Глицерол и его энергия
- •Кетогенез
- •Синтез жк
- •Синтеза жирных кислот
- •Холестерин: строение и биороль
- •Синтез холестерола
- •Регуляция синтеза холестерина
- •Липопротеиды
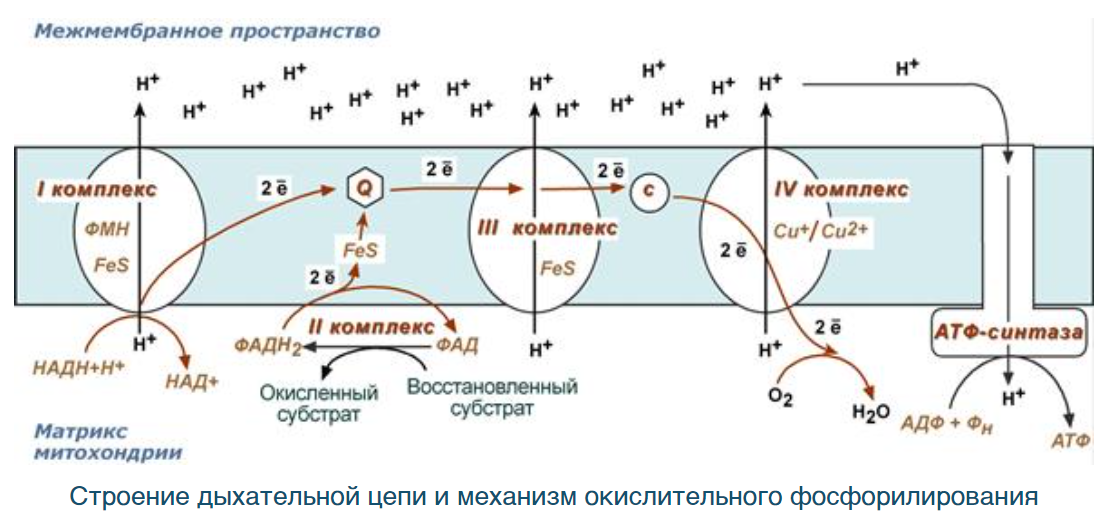
Механизм окислительного фосфорилирования и дыхательной цепи
Окислительное фосфорилирование – это многоэтапный процесс, происходящий во внутренней мембране митохондрий и заключающийся в окислении восстановленных эквивалентов (НАДН и ФАДН2) ферментами дыхательной цепи и сопровождающийся синтезом АТФ.
Пиридиновые дегидрогеназы содержат в качестве кофермента НАД. Субстраты малат, изоцитрат, пируват, глутамат окисляются НАД-зависимой дегидрогеназой, которая содержит кофермент НАД. Водороды от этих субстратов передаются на НАД, восстанавливая ее до НАДН2. Эта молекула идет к первому комплексу -- НАД-Н – дегидрогеназа, FMN которой забирает 1Н от НАДН2 и 1Н из воды в матриксе митохондрии, восстанавливаясь до FMNН2. Электроны от FMNН2 идут на FeS, а с него на убихинон, а протоны в межклеточное пространство с помощью СЭ. Перенос ионов водорода через мембрану (выкачивание) происходит в участках сопряжения. Они представлены I, III, IV комплексами дыхательных ферментов. В результате работы этих комплексов формируется градиент ионов водорода между внутренней и наружной поверхностями внутренней митохондриальной мембраны. Такой градиент обладает потенциальной энергией.
Второй комплекс (сукцинат-дегидрогеназа) содержит ФАД-зависимые дегидрогеназы, содержащие кофермент ФАД, и окисляющие сукцинат, оксалоацитат, ацил-КоА. Водороды от них переходят к ФАД = ФАДН2. Атомы отсюда сразу идут на убихинон.
Убихинон (отдельная структура) восстанавливается, превращаясь в убихинол. Электроны от него перейдут на 3 комплекс – убихинолдегидрогеназа.
С убихинола электроны передаются на 3 комплекс КоQ-цитохром c-оксидоредуктаза: б1, потом на б2, на FeS и наконец на с1. В каждом цитохроме происходит восстановление Fe3+ до Fe2+. Электроны передаются на цитохром с (отдельная структура), переносящий электроны на 4 комплекс -- цитохромоксидазный комплекс (цитохром а1 и а3, содержат гем и медь)
Электроны с него переноситься на О2, который связывается с протонами Н из матрикса митохондрии, образовывая метаболическую воду.
Свободная энергия с помощью, которой выбрасывались протоны, образовала электрохимический градиент; в матриксе -, снаружи +. Этот градиент нам нужен, чтобы протоны передались на АТФ-синтазу.
АТФ-синтаза содержит 2 части: F0 (канал, передающий протоны) и F1 (каталитическая -- синтез). Протоны тащат за собой энергию и градиент, запуская процесс превращения АДФ в АТФ, которая выброситься вон с помощью фермента транслоказа.

Роль о2
Роль кислорода: Кислород выступает в качестве акцептора электронов в реакции образования воды. В митохондриях кислород взаимодействует с электронами, возникающими во время электронного транспорта во время клеточного дыхания.
Окислительное фосфорилирование и его теория.
При прохождении электронов по дыхательной цепи происходит освобождение энергии. Однако благодаря большому количеству переносчиков выделение свободной энергии, которым сопровождается перенос одной пары электронов от НАДН2 на кислород, происходит не одномоментно, а разбивается на ряд относительно небольших порций. Поэтому дыхательную цепь можно рассматривать как каскад, при помощи которого клетка получает свободную энергию, извлекаемую из питательных веществ, в «расфасованном виде».
Коэффициент фосфорилирования это количество молекул АТФ, которое может быть синтезировано на одну молекулу NADH или FADH2 в процессе дыхательной цепи (окислительного фосфорилирования). Зависит от того, через какой комплекс дыхательной цепи электроны прошли
Общепризнанной теорией ОФ является хемиосмотическая (протондвижущая) теория П.Митчелла, по которой движущей силой ОФ является протонный потенциал (μН + ). Он возникает за счет того, что компоненты дыхательной цепи, присоединяя электроны, одновременно переносят протоны водорода в межмембранное пространство.
Таким образом в межмембранном пространстве на наружной поверхности внутренней мембраны митохондрии создается протонный (концентрационный) градиент. Градиент заставляет протоны двигаться из мембранного пространства внутрь в матрикс. Однако так как внутренняя мембрана митохондрий непроницаема для протонов, их движение в обратном направлении возможно только через особые каналы митохондриального белка F0 АТФсинтазы. Проходя через канал они изменяют конформацию белка F в результате чего фермент приобратает АТФсинтазную активность.

