
книги2 / монография 5
.pdfграмму обработки результатов измерения давления в аноректальной зоне и толстой кишке.
В процессе исследования определяются следующие параметры и характеристики: максимальное и среднее давление сжатия наружного сфинктера ануса; асимметрия сжатия сфинктера; ингибирующий аноректальный рефлекс; векторный объём; длина сфинктера; профиль давления в прямой кишке с шагом в 1 см.
Использование катетера с баллоном позволяет определить: порог ректальной чувствительности (минимальный объём, необходимый для появления ощущения заполнения кишечника – меньше или равно 25 мл); минимальный объём для расслабления внутреннего анального сфинктера (объём, при котором возникает первый позыв на дефекацию; в норме составляет 1020 мл); порог для постоянного позыва на дефекацию (объём, необходимый для появления постоянного позыва; в норме меньше или равен 220 мл) и максимально переносимый объём (в норме – 110-280 мл).
Эндоскопия. Поскольку аноректальная злокачественность или проктит могут быть причиной недержания кала, все такие пациенты, в зависимости от возраста, семейного анамнеза и предыдущего эндоскопического исследования, могут рассматриваться для гибкой сигмоскопии или колоноскопии. Исследование также может быть показано для оценки выпадающего геморроя, пролапса прямой кишки и ректоцеле.
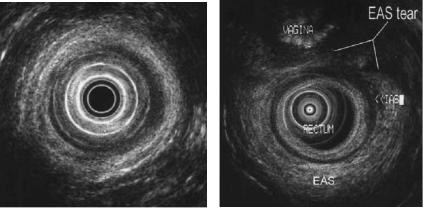
У пациентов с пониженным тонусом сфинктера для оценки целостности сфинктеров и исключения родовой травмы или другого повреждения, оценки стенки прямой кишки может быть показано анальная ЭУС (Рисунок 100) или МРТ. Анальная эндосонография менее инвазивная и в руках опытного оператора ценный диагностический метод. Данные ЭУС подтверждают, что многие пациенты с диагнозом «идиопатическое недержание кала» имеют хирургически устранимый дефект сфинктера. Также показано, что повреждение сфинктера во время родов происходит намного чаще, чем принято считать. Несмотря на то, что истинная распространенность разрывов сфинктера ниже, чем изначально полагали исследователи, у многих женщин во время и после родов происходят существенные морфологические изменения сфинктера. Преимущества в диагностике и точной оценке распространенности повреждения наружного сфинктера подтверждены путем сравнения результатов с данными электромиографических исследований и интраоперационного осмотра. Дифференциальная диагностика с учетом результатов анального ЭУС превосходит простые манометрические и векторные объемные исследования в случаях идиопатического недержания кала и дефекта сфинктера. Эндосонография дополняет физиологические исследования и является идеальным инструментом скрининга при недержании кала, позволяющим выявить пациентов с повреждением сфинктера, которым показано хирургическое вмешательство.
401
А |
Б |
Рисунок 100. А, ЭУС изображение (радиальное сканирование) нормального анального сфинктера. Внутренний гипоэхогенный слой – внутренний анальный сфинктер. Наружный гиперэхогенный слой представляет наружный анальный сфинктер. Б, ЭУС изображение (секторальное сканирование) разрыва наружного сфинктера (EAS). IAS – внутренний анальный сфинктер.
Проспективное исследование выявило, что анальная ЭУС превосходит МРТ для диагностики повреждения наружного и внутреннего сфинктера (Malouf A.J. et al., 2000). В другом проспективном исследовании было выявлена незначительная разница в чувствительности ЭУС против МРТ (90% против 81%) в диагностике дефекта наружного анального сфинктера и его атрофии (Dobben A.C. et al., 2007). Будущее исследование новых технологий ЭУС (к примеру, 3D изображение, высокочастотный датчик) и МРТ (к примеру, внутривлагалищный подход) поможет определить роль таких дополнительных методов визуализации при недержании кала.
Техника анальной ЭУС. Гибкая сигмоскопия выполняется до ЭУС. Этим преследуется несколько целей, включающих оценку воспаления ректальной слизистой оболочки, выявление опухолей, если присутствуют, и оценку адекватности подготовки. Затем вводится радиальной сканирующий эхоэндоскоп. Для пациентов, подвергающихся исследованию по поводу ректального рака, для оценки подвздошной лимфаденопатии, эхоэндоскоп вводится, примерно, на 30 см. Для пациентов, обследуемых по поводу недержания кала или перианальных заболеваний, вероятно, достаточно обследования до ректосигмоидного соединения. Для исследования анального канала баллон раздувается минимально. Рукой эхоэндоскоп стабилизируется в анальном канале. При необходимости (к примеру, ректальный рак с аденопатией), затем вводится линейный сканирующий эхоэндоскоп и патология (опухоль/аденопатия) визуализируется прицельно. Поскольку прямая кишка с нестерильной средой, до выполнения тонкоигольной аспирационной биопсии, с целью профилактики инфекции, внутривенно вводится антибиотик. Для дальнейшего уменьшения риска инфекции профилактическое лечение должно быть продолжено с оральным применением квинолона 48 часов по-
402
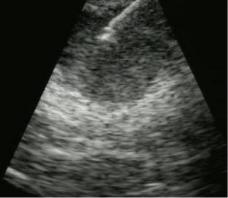
сле процедуры. Полезна умеренная седация, особенно, когда выполняется под контролем ЭУС тонкоигольная аспирационная биопсия (Рисунок 101).
Рисунок 101. Аспирационная игла в опухоли.
ЭУС также показала успешность в предсказании исхода сфинктеропластики (Ternent C.A. et al., 1997). У 31 пациента, которым была проведена сфинктеропластика, по поводу недержания кала, была выполнена ЭУС (Savoye-Collet C. et al., 1999). У 21 пациента, у которых ЭУС документировано закрытие дефекта наружного анального сфинктера, 86% пациентов отметили улучшение в недержании кала. В тоже время у пациентов, которые имели оставшийся дефект после сфинктеропластики, все еще имели значительное недержание кала.
Роль декографии в оценке недержания кала ограничена и успешна у отдельных пациентов (к примеру, у пациентов с клинически предполагаемым ректоцеле). Декография с мягкой бариевой пастой может также дать полезную информацию об аноректальном угле, ослаблении угла таза и выпадении прямой кишки, которые могут способствовать недержанию кала.
Анальная электромиография с применением игольчатых электродов успешна только для выявления нейрогенных или миопатических повреждений анального сфинктера.
Лечение.
Подходы включают медикаментозное лечение, биологическую обратную связь и операцию.
Улучшение консистенции стула. Усилия должны быть направлены для улучшения консистенции стула и уменьшения частоты стула при диарее. Консистенция стула может быть повышена с использованием наполнителя, к примеру, метилцеллюлозы, антидиарейных агентов, таких как лоперамид или дифеноксилат (хотя лоперамид лучше) и антихолинергических агентов, таких как гиосциамин, принимаемых до еды. Опиаты могут быть необходимы в трудных случаях в дополнение к лоперамиду. Некоторые эксперты возражают против применения такой комбинации. Лекарственные препараты второй линии, такие как клонидин, октреотид и холестирамин менее эффективны и не хорошо переносятся.
403
Ректальные свечи или клизмы могут быть полезными у пациентов с неполной дефекацией. Пациенты с недержание кала в следствие переполнения прямой кишки, связанной с копростазом, мегаректумом или с притуплением ректальной чувствительности (диабет, множественный склероз), могут иметь пользу от клизм. Пациенты с недостаточностью резервуарной функции, вызванной воспалением, операцией или опухолью получат облегчение от бесшлаковой диеты, антидиарейных препаратов и лечения воспаления. Разовые, специальные анальные пробки могут быть применены у пациентов с нарушенной чувствительностью в результате неврологических расстройств, деменции. При идиопатическом недержании кала могут быть применены низкие дозы трициклических антидепрессантов.
Биологическая обратная связь (от греческого bio – жизнь + logos –
учение) – процедуры, которые позволяют с минимальной временной задержкой информировать человека о состоянии его телесных функций, за счет чего возникает возможность их сознательной регуляции. Есть опыт использования ее для изменения температуры тела, глубокой мышечной релаксации, снижения артериального давления, изменения кислотности желудочного сока и т.д.
Биологическая обратная связь часто применяется для улучшения ректальной чувствительности у пациентов с такой патологией и структурно неповрежденным внутренним сфинктером. Она не подходит для пациентов с когнитивными проблемами, отсутствием иннервации прямой кишки, полным повреждением спинного мозга и большими дефектами сфинктеров. В тоже время предполагается, что до 75-90% тщательно отобранных пациентов будут иметь пользу (улучшение или разрешение проблемы) от такой терапии. Хотя другие эксперты не показали превосходства биологически обратной связи над консервативной терапией, включающей диету, жидкости и применение антидиарейных агентов.
Методика биологической обратной связи практикуется в мире уже более 30 лет, но в России пока еще не стала популярной. Зарубежные коллеги отмечают, что этот метод, по сравнению с другими, даёт не только самые положительные результаты, но и самые стойкие. Этой методике хочется уделить особое внимание. Осуществляется она с применением медицинских приборов биологически обратной связи. Принцип действия аппарата заключается в том, что для пациента устанавливается задача по сокращению и способности задерживать напряжение наружного сфинктера в заданном режиме. При помощи ректального датчика регистрируется электромиограмма, а информация выводится на компьютер в виде графиков. Пациент при получении информации о том, насколько правильно выполняется поставленная задача, может сознательно контролировать и корректировать длительность и силу сокращения мышц сфинктера. Это, в свою очередь, значительно увеличивает эффективность тренировок наружного сфинктера, и способствует восстановлению кортико-висцеральных путей, которые отвечают за функ-
404
цию удержания содержимого кишечника. При использовании данного метода удается достичь положительных результатов в 60% случаев.
Оперативный подход включает пластику сфинктера у пациентов с его повреждением, ректопексию при полном ректальном пролапсе и пластику тазового дна при неврологическом недержании. Однако в некоторых случаях только колостомия может быть реальной процедурой. За исключением лечения выпадения прямой кишки и острой травмы анальных сфинктеров, роль хирургии вследствие сомнительной эффективности и высокой частоты осложнений, противоречива. Антеградные промывания – процедура, часто применяемая у детей с расщелиной позвоночника (spina bifida). Это позволяет через аппендикостому или специальное приспособление проводить антеградное клизмирование.
Эндоскопическая радиочастотная (тепловая) терапия – новая процедура, использующая тепловую энергию для образования такого фиброза (похожего на рубцовую ткань), который как уплотнительное кольцо формирует анальный сфинктер, и помогает в контроле содержимого кишки. Процедура менее инвазивная, чем другие виды оперативного лечения. Выполняется под седацией или местной анестезией.
Заключение.
Недержание кала – это обычно мультифакторное расстройство. Роль операции ограничена отдельными пациентами. Методика биологической обратной связи опорожнения кишечника помогает большинству пациентов. Лечение недержания кала должно фокусироваться на оценке пациента, определении подлежащей патологии и выборе соответствующей терапии. Для пациентов с диарей, употребление пищевых волокон и добавок для уплотнения стула может помочь формировать плотный стул. Медикаменты, такие как лоперамид и дифеноксилат, замедляют время гастроинтестинального транзита, уменьшают частоту стула, замедляют перистальтику и повышают тонус сфинктера и давление в покое, благотворны для лечения диареи. Для пациентов с недержание кала, вследствие переполнения прямой кишки, применение средств, размягчающих каловые массы и увеличивающие объем стула, а также средств, стимулирующих перистальтику, и солевых слабительных может помочь в размягчении консистенции стула, повышении объема стула и уменьшении времени транзита и, следовательно, в снижении риска копростаза.
405
19. ХРОНИЧЕСКАЯ РЕКТАЛЬНАЯ БОЛЬ
Хроническая или часто рецидивирующая боль в анальном канале, прямой кишке или тазе – частый симптом, который поражает 6,6% популяции (Drossman D.A. et al, 1993). Хотя только треть людей с такими болями консультируется врачами, заболевание значительно влияет на качество жизни, является причиной невыхода на работу и вызывает психологический дистресс. Однако, несмотря на частоту, относительно мало опубликовано исследований, которые адресованы эпидемиологии, патофизиологии и лечению хронической ректальной боли. Целью этого раздела является обзор известной диагностики и лечения наиболее частых форм аноректальной и тазовой боли, называемых хронической прокталгией, хронической тазовой болью, кокцигодинией и невралгией срамного нерва. Обзор больше направлен на хроническую прокталгию и дифференциальную диагностику с другими синдромами тазовой боли. Органические заболевания, которые наиболее часто встречаются при хронической аноректальной и тазовой боли – криптиты, трещины, абсцессы, геморрой, солитарные ректальные язвы, ВЗК и ректальная ишемия. Также хронический простатит и тазовый эндометриоз потенциальные причины хронической тазовой боли (Wald A. et al., 2006). Хотя дифференциальная диагностика обширная и, к сожалению, плохо стандартизированная, у, примерно, 85% пациентов, обращающихся к гастроэнтерологу или проктологу, не обнаруживается органического заболевания, объясняющего причину хронической или тазовой боли (Chiarioni G. et al., 2011).
Хроническая прокталгия – обобщающий термин для хронической или рецидивирующей боли в анальном канале или прямой кишке (Wald A. et al., 2006). Другие названия, такие как синдром мышцы, поднимающей задний проход, пуборектальный синдром, хроническая идиопатическая перианальная боль, пириформис-синдром и синдром хронической невоспалительной боли, являются синонимами. Римские критерии III определяют хроническую прокталгию как хроническую или рецидивирующую ректальную боль, длящуюся, по крайней мере, 20 минут, при отсутствии структурных или системных заболеваний, объясняющих такие симптомы (Wald A. et al., 2006). Боль, длящаяся 20 минут и более, является ключевым признаком. Эпизоды боли длительностью менее 20 минут, предполагают скоротечную прокталгию (proctalgia fugax), при которой сильная боль в аноректальном регионе длится менее 20 минут и исчезает полностью (Wald A. et al., 2006). Скоротечная прокталгия может рецидивировать, но эпизоды редкие. Считается, что скоротечная прокталгия имеет другую, чем хроническая прокталгия, хотя нет согласию какую, этиологию. В Римских критериях III хроническая прокталгия, на основании наличия или отсутствия напряжения, когда мышца, поднимающая задний проход, во время пальцевого ректального исследования напряжена, разделяется на два подтипа: синдром мышцы, поднимаю-
406
щей задний проход, и неспецифическая функциональная аноректальная боль.
Патофизиология. Хотя нет точного доказательства этой гипотезы, хроническое напряжение или спазм поперечнополосатых мышц дна таза часто считается патофизиологической основой хронической прокталгии (Wald A. et al., 2006). Воспаление сухожилия или мышцы, поднимающей задний проход, также предполагается как причина хронической прокталгии. Однако локальное введение стероидов не показало эффективности лечения хронической прокталгии (Park D.H. et al., 2005). В ретроспективных исследованиях показано, что многие пациенты ранее перенесли операции на тазу, прямой кишке и даже на позвоночнике (Gilliland R. et al., 1997; Salvati E.P., 1987).
Деторождение может быть другим вызывающим беспокойство фактором (Salvati E.P., 1987). Кроме этого, высокая частота беспокойства, депрессии и стресса, часто докладываемых при хронической прокталгии, может быть значительным вызывающим фактором у некоторых пациентов (Renzi C., Pescatori M., 2000). За исключением органических заболеваний, тесты аноректальной физиологии и визуализации традиционно считаются как имеющие малую диагностическую ценность (Christiansen J. et al., 2001).
Клиника. Хроническая прокталгия часто описывается пациентами как тупая боль или ощущение давления в прямой кишке, которая провоцируется длительным сидением и облегчается стоянием или лежанием (Wald A. et al., 2006). Боль редко возникает ночью, она обычно начинается утром и усиливается по тяжести днем. Боль может быть вызвана длительной ездой в автомобиле, стрессом, сексуальным сношением и дефекацией (Wald A., 2001).
Диагностика хронической прокталгии все еще базируется на (1) клинических симптомах рецидивирующей хронической боли в анальном канале или прямой кишке, длящейся 20 минут или дольше (Wald A. et al., 2006) и (2) исключении альтернативных заболеваний, объясняющих такие симптомы множественными диагностическими тестами и консультациями специалистов. Кроме этого выполняется пальцевое исследование прямой кишки для определения напряжения, когда применяется тракция на мышцу, поднимающую задний проход. Этот диагностический признак весомый предсказатель будет ли пациент иметь пользу от лечения, расслабляющего мышцы дна таза.
Нет одного вида лечения эффективного при хронической прокталгии (Wald A. et al., 2006), а лечение может быть тщетной попыткой для пациентов и врача (Ger G.C. et al., 1993). Необходимо убедиться, что боль доброкачественного происхождения и не предполагается злокачественность (Salvati E.P., 1987). Первое лечение, предложенное для лечения хронической прокталгии – пальцевой массаж (Salvati E.P., 1987). Массаж лобковоректальной мышцы проводится интенсивным манером, в зависимости от переносимости пациента, массируя пораженные стороны до 50 раз. Некоторые авторы утверждают, что если массаж у пациента вызывает дискомфорт, он может быть неэффективным (Salvati E.P., 1987). Массаж редко выполняется как единст-
407
венное лечение, а дополняется горячими сидячими ваннами и коротким курсом диазепама, которые имеют миорелаксирующее действие. Ранние исследования предполагали, что пальцевой массаж в сочетании с горячими сидячими ваннами и/или диазепамом были эффективны в избавлении от боли у 68% пациентов с хронической прокталгией (Grant S.R. et al., 1974). Однако при длительном наблюдении польза оказалась сомнительной, а длительный прием диазепама приводил к зависимости (Wald A. et al., 2006). Электрогальваническая стимуляция, традиционно применяемая психиатрами для лечения мышечной спастичности (Salvati E.P., 1987), рекомендуется для лечения синдрома мышцы, поднимающей задний проход, когда консервативное лечение неэффективное. Лечебные протоколы широко колеблются в количестве и длительности сеансов. Лечение по принципу обратной связи было впервые описано в 1991 году Gilliland R. с соавторами. Они пролечили 12 пациентов с данной методикой, направленной на волевое расслабление тонуса наружного анального сфинктера. Боль исчезла у всех пациентов после, в среднем, восьми сеансов. Последующие исследования не смогли воспроизвести такие результаты, и частота успеха колебалась от 35% до 87,5%
(Gilliland R. et al., 1991; Ger G.C. et al., 1993; Heah S.M. et al., 1997). Ботули-
нический токсин (BoTox A) был тестирован в рандоминизированном исследовании у 12 пациентов и не было разницы в ректальной боли, наблюдаемой между пациентами, получивших инъекции BoTox или физраствор (Rao S.S., 2003). Гипотеза тендинита (воспаления) была проверена блокадой смеси триамциналона и лидокаина с отрицательными результатами (Park D.H. et al., 2005; Ger G.C. et al., 1993). Стимуляция крестцового нерва также доложена как успешная процедура в исследовании 27 пациентов с хронической прокталгией. Однако окончательное избавление от боли было у менее 50% лиц (Falletto E. et al., 2009). Главный недостаток в оценке лечения хронической прокталгии в литературе – большие вариации в критериях включения в исследование, критериях исхода и интервалах наблюдения. Дополнительные недостатки – малые группы пациентов и контрольных групп.
Кокцигодиния определена как боль, возникающая в области копчика после длительного сидения на твердой поверхности (Mazza L. et al., 2004). Боль считается хронической, когда она длится более двух месяцев, и наиболее часто возникает после повторных травм или деторождения (Andromanakos N.P. et al., 2011). Кокцигодиния также может быть идиопатического происхождения или вторичной к дегенерации поясничного диска (Traycoff R.B. et al., 1989). Она также доложена редко как осложнение епидуральной инфекции при анестезии или различных ректальных или спиналь-
ных операций (Traycoff R.B. et al., 1989).
Патофизиология. Заболевание встречается в 5 раз чаще у женщин, чем у мужчин, а ожирение, кажется, предрасполагающий фактор, вызывающий ротации таза (Andromanakos N.P. et al., 2011). Анатомия женского таза также предрасполагает к кокцигодинии, оставляя копчик более подверженным травматическим повреждениям. Точный этиологический механизм/ы, ассо-
408
циированные с кокцигодинией, все еще неясные. Хронический спазм дна таза, вызывающий болезненное напряжение копчика, традиционно считается этиологическим фактором, а случайная травма действует как пусковой механизм (Andromanakos N.P. et al., 2011). В большом проценте случаев рентгенологически была выявлена нестабильность копчика, потенциально коррелирующая с тяжестью симптомов (Maigne J.Y. et al., 2000).
Клиника. Боль в копчике и в рядом расположенных структурах (крестец, промежность, прямая кишка) – главный симптом. Эпидемиологических данных о распространенности кокцигодинии в общей популяции недостаточно, но кокцигодиния считается редким расстройством. Ретроспективные данные предполагают, что кокцигодиния насчитывает менее чем 1% всех случаев болей в нижней части спины (Andromanakos N.P. et al., 2011). Боль ухудшается длительным сидением, сгибанием, подъемом тяжестей, длительной вынужденной позой. Некоторые пациенты отмечают появление боли при вставании из положения сидя.
Диагноз кокцигодинии основывается на анамнезе и клиническом исследовании. Опрос пациента о предыдущей травме копчика или родовой травме является основным, так как согласно Salvati E.P. (1987), отсутствие предыдущей травмы делает диагноз маловероятным. Ключом к диагнозу является воспроизведение боли давлением или манипуляцией на копчике (Mazza L. et al., 2004). Ненормальные смещения копчика при пальпации – дополнительный признак для подтверждения клинического подозрения кокцигодинии (Traycoff R.B. et al., 1989). Динамическая рентгенография может поддержать диагноз. Стандартное боковое рентгенологическое исследование копчика в положении стоя дополняется снимком в положении сидя на твердой поверхности (Maigne J.Y. et al., 2000). Более чем 50% пациентов показывают признаки нестабильности копчика (или чрезмерное сгибание, или чрезмерная подвижность), которые, кажется, коррелируют с тяжестью боли и предыдущей травмы. Кроме этого, 15% пациентов с кокцигодинией имеют шип на конце копчика (так называемая спикула) (Maigne J.Y. et al., 2000). Для исключения опухоли или заболевания диска должна быть выполнена МРТ, но кажется, она значительно диагностику не дополняет (Traycoff R.B. et al, 1989).
Изначальное лечение кокцигодинии фокусируется на исключении провоцирующих факторов и (для уменьшения давления) включает сидение на кольцевидной подушке или подкладке с гелем, сидячие ванны и НПВП (Andromanakos N.P. et al., 2011). Лечение часто продолжается 6-8 недель. Нет исследований о терапевтическом исходе таких простых мер. Если такие рекомендации недостаточные, большинство авторов рекомендуют пальцевые манипуляции на связках копчика и интраректальных манипуляциях на мышцах дна таза. Различные методы массажа и манипуляций, особенно в сочетании с локальными инъекциями стероидов или психотерапией, позволяют уменьшить боль у до 85% пациентов (Wray C.C. et al., 1991). Оперативное лечение кокцигодинии – лечебный подход у небольшого числа пациентов
409
(примерно, у 19%), но средняя частота избавления от боли высокая (более 80% пациентов). Операцией выбора является полное или частичное удаление копчика.
Невралгия срамного нерва – это хроническая боль в промежности, вторичная к ущемлению и повреждению срамного нерва в мышечно-остео- апоневротическом тоннеле, между крестцово-бугорной и крестцовоостистой связками, при отсутствии органических заболеваний, которые могут объяснить этом симптом (Mazza L. et al., 2004). Невралгия срамного нерва редко описана как вторичная к герпетической нейропатии, нейропатии от растяжения и послелучевой нейропатии, но ущемление срамного нерва – наиболее частая этиология (Benson J.T. et al., 2005). Невралгия срамного нерва также называется синдромом канала Alcock’s или синдромом срамно-
го канала (Mazza L. et al., 2004).
Клинические проявления невралгии срамного нерва описываются как поверхностная боль, ощущение жжения, онемение или парестезии в ягодичной, промежностной и/или генитальной областях (Mazza L. et al., 2004). Боль может быть односторонней или двухсторонней, радировать в таз и ноги и быть ассоциированной с дискомфортом в глубине таза (Benson J.T. et al., 2005). Боль может возникать после полового сношения, а первоначально может быть принята за ишиас. Эпидемиология невралгии срамного нерва в общей популяции неизвестна, но считается редким заболеванием.
Диагностика. Считается, что невралгия срамного нерва может быть просто диагностирована на основании наличия боли в тазу, промежности и ягодицах без доказательств органического заболевания в процессе диагностического поиска (Labat J.J. et al., 2008). Особенно спорна ассоциация с ректальной болью, наличие которой требует дифференциальной диагностики с хронической прокталгией (Mazza L. et al., 2004).
В 2006 году мультидисциплинарная рабочая группа по невралгии срамного нерва в г. Нант, Франция, пришла к выводу, что только оперативные данные ущемления нерва и послеоперационное избавление от боли могут формально подтвердить диагноз (Labat J.J. et al., 2008). Также идентифицировано 4 диагностических критериев для невралгии срамного нерва: (А) необходимые критерии, (В) дополнительные диагностические критерии, (С) исключающие критерии, (D) ассоциированные признаки, не исключающие диагноз. Необходимые критерии обсуждены в деталях.
(1)боль должна быть ограничена областью иннервации срамного нерва. Это исключает любую боль, которая ограничена копчиком, областью таза или ягодиц;
(2)боль, согласно гипотезе сдавления, преимущественно испытывается во время сидения. При долголетнем расстройстве боль может стать постоянной, но все еще ухудшается в сидячем положении;
(3)боль редко беспокоит пациента ночью;
(4)при клиническом исследовании нет объективных нарушений чувствительности, даже при наличии парестезии. При наличии дефекта чувстви-
410
