
6 курс / Медицинская реабилитация, ЛФК, Спортивная медицина / Физиотерапия, лазерная терапия / Лазерная_терапия_в_онкологии_Москвин_С_В_,_Стражев
.pdf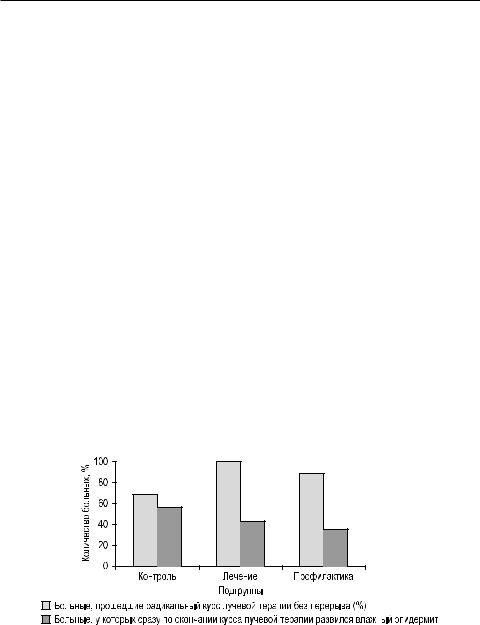
Лазерная терапия в онкологии
больных (15 человек). В лечебной подгруппе (n = 7) все больные получили дозы 50–70 Гр без перерыва под «защитой» лазера. В результате уже после первой процедуры лазерного воздействия значительно уменьшались боли, отёчность и гиперемия, эрозии подсыхали, а в процессе ЛТ (лечение), даже на фоне продолжающейся лучевой терапии, начиналась эпителизация в зонах влажного эпидермита. В контроле из всего количества больных, закончивших лучевую терапию без перерыва, у 81,8% (9 человек) сразу же по окончании курса описан влажный эпидермит в зонах облучения разной степени выраженности. В профилактической подгруппе только у 40% больных (6 человек), закончивших лучевую терапию без перерыва, развился влажный эпидермит.
Влечебной подгруппе эта цифра составляет 42,9% (3 человека). При этом в профилактическойподгруппепослепоявления элементоввлажногоэпидермита под «защитой» лазера удалось подвести дополнительно 8,6 ± 1,5 Гр (n = 3), а в лечебной – 13,7 ± 1,5 Гр (n = 7) до запланированной дозы, не прерывая лечения. В результате доза, подведённая без перерыва в лечении, в контрольной подгруппе составила 56,1 ± 0,9 Гр (n = 11), в профилактической – 60,5 ± 0,2 Гр (n = 15), в лечебной – 58,5 ± 2,5 Гр (n = 7). При сравнении контрольной и профилактической подгрупп (рис. 65) результаты достоверны (р < 0,001).
Влечебной подгруппе больные получили в среднем 9,8 ± 2,3 процедуры лазерной терапии; в профилактической – 23 ± 1,6 процедуры. У двух больных из профилактической подгруппы в лучевом лечении был стандартный двухнедельный перерыв на СОД 40 Гр, причиной которого послужили посторонние обстоятельства, не связанные с развитием лучевой реакции [Курсова Л.В., 2000].
Рис. 65. Эффективность лазерной терапии у больных РМЖ (Курсова Л.В., 2000)
С целью профилактики послеоперационной инфекции у больных РМЖ рекомендуется проводить послеоперационное освечивание НИЛИ, оказывая бактерицидное и стимулирующее действие на процессы репарации в ране, вследствие чего уменьшается количество послеоперационных ГСО почти в
440

Лазерная терапия в комплексном лечении онкологических больных
2 раза [Шамилов А.К., 1992; Шамилов А.К. и др., 1991]. Лазерная терапия у больныхРМЖпредотвращаетпослеоперационноеснижениечисламоноцитов, В-лимфоцитов, общей фракции Т-лимфоцитов (CD3+), CD4+Т-хелперов и активированных Т-лимфоцитов (CD3+HLADR+), скорости внутриклеточного лизиса фагоцитированных нейтрофилами бактерий и способствует активации цитотоксических CD8+Т-лимфоцитов. У пациентов с повышенным уровнем низкомолекулярных циркулирующих иммунных комплексов после курса ЛТ происходит снижение их концентрации и одновременно увеличивается активность естественных киллеров, наблюдается увеличение фагоцитарного числа относительно уровня после операции [Зимин А.А., 2010; Зимин А.А.
и др., 2010].
Неоадъювантная аутогемохимиотерапия, модифицированная НИЛИ и постоянным магнитным полем [Пат. 2420328 RU], в комплексном лечении больных местно-распространённым раком молочной железы позволяет улучшить непосредственные результаты лечения за счёт увеличения общего регрессионного эффекта относительно стандартной ПХТ и аутогемохимиотерапии, соответственно, на 20 и 14% (p < 0,05), снижение случаев прогрессирования процесса в 3,5 и 1,5 раза соответственно, общих токсических реакций, в том числе лейкопении II и III степени, и обеспечивает 3-летнюю общую и бессобытийную выживаемость у 93 и 97% больных, что на 30% выше, чем при аутогемохимиотерапии (p < 0,001) [Кечеджиева С.М., 2011].
При изучении лечебного патоморфоза в опухолях молочной железы под влиянием аутогемохимиотерапии, усиленной фотомагнитным воздействием, отмечено увеличение количества дистрофических изменённых клеток (227 ± 11,2 против 189 ± 8,4 и 109,7 ± 9,4% в группе сравнения и контроле, p < 0,05), уменьшение площади паренхимы (17,1 ± 0,9 против 20,4 ± 1,1 и 30,5 ± 1,2% соответственно, p < 0,05), увеличение площади стромы опухоли (82,3 ± 4,5 против 75,6 ± 4,2 и 66,9 ± 3,2%, p < 0,05), что подтверждается аппаратными методами объективизации.
Неоадъювантнаяфотомодифицированнаяаутогемохимиотерапияоказывает положительное влияние на клеточный метаболизм, увеличивая энергообеспечение лимфоцитов периферической крови за счёт усиления активности СДГ в 2,4 раза относительно контроля, а также на системообразующие свойства бесклеточнойсреды–сывороткикрови,увеличиваяв12разморфотипыфаций с радиальной и частично-радиальной симметрией, в 2,5 раза снижая уровень маркеров интоксикации и в 2,2 раза – маркеров склерозирования.
После фотомодифицированной аутогемохимиотерапии отмечено повышение в ткани опухоли и её перифокальной зоне активности каталазы в 1,6 и 1,4 раза соответственно по сравнению с показателями без лечения и активности СОД в ткани опухоли – 24,5%, что указывало на донорно-акцепторное взаимодействие с рецепторами биологических мембран клеток организма, а также непосредственное влияние на ряд ферментативных систем, включая гемм-содержащие ферменты.
441
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

Лазерная терапия в онкологии
Важным звеном противоопухолевого действия фотомодифицированной аутогемохимиотерапии является изменение гормонов, секретируемых гипофизом: исходно повышенная секреция пролактина нормализовалась в 43% случаев, отмечена нормализация ФСГ у всех пролеченных больных раком молочной железы, как с его исходно повышенным, так и сниженным уровнем, что свидетельствует о включении центральных механизмов регуляции гомеостазаорганизма.Установленопролонгированноебиоадаптивноевлияние методики, характеризующееся выраженным преобладанием антистрессорных реакций над стрессом и возрастанием коэффициента их соотношения в 1,4–1,8разанавсехэтапахнеоадъювантноголечения[КечеджиеваС.М.,2011].
Лазерную акупунктуру благодаря универсальности и простоте метода достаточно часто применяют врачи самых различных специальностей. Посколькулазерноеосвечиваниеточекакупунктурывызываетименносистемныереакции организма, это крайне важно для онкологической практики. В частности, Yang Fu-Shou et al. (1988) сообщают, что именно они первыми (с 1976 г.) стали применять с очень хорошими результатами лазерную акупунктуру (азотный лазер, длина волны 337 нм) при лечении онкологических больных (102 случая на момент публикации), предполагая, что подавление раковой опухоли происходит опосредованно, через стимуляцию иммунной системы. А.В. Алясовой (1999) опубликованы неплохие результаты светолечения больных злокачественными лимфомами с дисфункцией Т-клеточного иммунитета, проходивших курс ПХТ (нормализация содержания CD4+, CD8+ и уровня ЦИК), которые полностью нивелируются отсутствием описания методики: «Коррекция … осуществлялась с помощью серийного прибора … действующего подобно инфракрасномулазеру».Всё!Идажеуказаниенарефлексотерапиюнеспасает, хотя параметры освечивания ТА достаточно стандартизированы, но рецепт выбора ТА и последовательность воздействия на них не приводятся.
Известна общность ряда факторов, влияющих на развитие рака молочной железы и многих доброкачественных заболеваний: при фиброзно-кистозных изменениях–в89,5%,прифиброаденомах –в71%,присолитарныхкистах –в 57%. Вероятность малигнизации кистозных изменений молочных желёз составляет7,2%,априналичиитолстостенныхкистспапилломатознымиразрастаниями она увеличивается до 18,7%. Лечение больных фиброзно-кистозной болезнью с помощью лазерной терапии оказалось достаточно эффективным и переносимым. По субъективным данным, происходит быстрое нарастание эффекта уже по завершении первого курса лазерной терапии. На протяжении 3 мес. после начала лечения число больных с полной регрессией симптомов составляет 80%. После проведения повторного курса ЛТ к 12 мес. число больных с регрессией первоначальных симптомов достигает 90%. Результаты выявленных объективными методами исследований молочных желёз (измерение резистентности, УЗИ, маммографическое и морфологическое) подтверждают нарастающую динамику. Применение сочетанной (лазерной и медикамен-
442

Лазерная терапия в комплексном лечении онкологических больных
тозной) терапии характеризуется частичным суммированием эффектов от каждого из методов [Мустафин Н.К., 2000].
Наоснованииданныхсобственныхисследованийбылразработанметодлазерной адоптивной иммунотерапии. Метод заключается в освечивании непрерывным НИЛИ красного спектра (λ = 633 нм) лимфолейкомассы, выделяемой на сепараторе крови, в процессе сепарирования с последующей реинфузией данному больному. В клинике опухолей молочных желёз ВОНЦ АМН СССР
этот метод был применён с целью ранней профилактики метастазирования у 15 больных РМЖ после радикальной мастэктомии с сохранением большой грудной мышцы. У таких больных, как правило, наблюдаются снижение активности Т-лимфоцитов, нарушения в соотношении субполуляций Т-хел- перов-индукторов/Т-супрессоров-киллеров (в сторону снижения хелперной и повышения супрессорной активности), снижение функциональной активности естественных киллеров, что создаёт условия повышенного риска для возобновления заболевания (рецидивирования, метастазирования) в после операционном периоде, которые могут быть сняты с помощью предложенной методики [Купин В.И. и др., 1989].
Через 2–3 недели после операции больным проводился однократно курс лазерной адоптивной иммунотерапии. Сниженные до процедуры показатели Т-клеточной активности возрастали после её проведения, затем в течение 3–4 недель снижались до нормального уровня и оставались на достаточно высоких значениях в течение последующих 3 лет наблюдения, супрессорная активность после процедуры у большинства больных снижалась, но у некоторых незначительно возрастала, однако на протяжении последующего периодаснижаласьиудерживаласьнапостояннонизкомуровне,исследования
смоноклональными антителами показали увеличение хелперной активности, снижение супрессорной активности, нормализацию активности ЕК-клеток. В течение 3 лет наблюдения у всех больных по клиническим данным и иммунологическим показателям прогрессирования процесса не обнаружено, это свидетельствует о перспективности включения данного метода в комплекс лечебных мероприятий, используемых в настоящее время в онкологии
сцелью профилактики метастазирования злокачественных новообразований
[Купин В.И. и др., 1989].
Частные методики лазерной терапии
Основным методом лазерной терапии является ВЛОК-635 или ВЛОК-525+ ЛУФОК® (табл. 13, 14). Как один из вариантов может рассматриваться НЛОК (табл. 10), например, при отсутствии оборудования или специальных условий для проведения внутривенного лазерного освечивания крови.
Дополнительно к ВЛОК местное воздействие на проекцию иммунокомпетентных органов (табл. 9), до 8–10 процедур. У пациентов, которым проводится курс химиотерапии, с целью детоксикации дополнительно освечи-
443
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

Лазерная терапия в онкологии
вать область проекции печени импульсным ИК НИЛИ (матричная лазерная излучающая головка, длина волны 904 нм, частота 80–150 Гц, ПМ 5–7 Вт/ см2, экспозиция 2 мин), контактно через насадку ПМН, стабильно, на курс 8–10 процедур, периодичность которых определяется схемой лечения.
В качестве профилактики развития послеоперационных осложнений в предоперационный период и плекситов после лучевой терапии до начала облучения проводятся 1–2 процедуры в области локализации опухоли импульснымИКНИЛИ(матричнаяизлучающаяголовка,длинаволны904нм,частота 80–150 Гц, ПМ 5–7 Вт/см2, экспозиция 2 мин), контактно через насадку ПМН, стабильно. На раннем этапе реабилитации рекомендуется по возможности задействовать все методы, на курс 10–12 процедур.
Дополнительно проводится лазерная акупунктура (табл. 5).
Перечень рекомендуемого оборудования для максимально эффективной реализациивсехметодиклазернойтерапиипредставленв табл.91,принеобходимости он всегда может быть дополнен лазерными излучающими головками и насадками.
Таблица 91
Оборудование для лазерной терапии, применяемое в комплексном лечении больных раком молочной железы
Наименование |
|
|
|
|
|
аппарата |
|
Кол-во, |
|
|
|
или лазерной |
Основные параметры |
Методика |
Примечание |
||
шт. |
|||||
излучающей |
|
|
|
||
|
|
|
|
||
головки |
|
|
|
|
|
|
Базовый блок: 2 канала |
|
|
|
|
|
Масса, кг, не более: 1,0 |
|
|
|
|
|
Габаритные размеры, мм, не бо- |
|
|
|
|
|
лее: 280 × 195 × 100 |
|
|
|
|
|
Таймер: фиксированные зна- |
|
|
|
|
|
чения: 2, 5 и «Н» (неограничен- |
|
|
Базовый блок |
|
|
но); диапазон регулирования |
|
|
предназначен |
|
Аппарат лазер- |
произвольной экспозиции: от 1 с |
|
|
для подключе- |
|
до 90 мин |
|
|
ния лазерных |
||
ный физиоте- |
Диапазон частот: фиксирован- |
1 |
– |
излучающих |
|
рапевтический |
|||||
ные частоты: 10, 80, 3000, 10 000 |
|
|
головок, зада- |
||
«Лазмик-01» |
|
|
|||
Диапазон регулирования |
|
|
ния и контроля |
||
|
|
|
|||
|
частоты – от 0,5 до 10 000 |
|
|
параметров |
|
|
Электропитание: напряжение |
|
|
методики ЛТ |
|
|
100–240 В, частота 50–60 Гц |
|
|
|
|
|
Мощность, потребляемая аппа- |
|
|
|
|
|
ратом, не более 14 ВА |
|
|
|
|
|
Возможность внешней модуля- |
|
|
|
|
|
ции лазерного излучения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Применяются |
|
КЛ-ВЛОК-635-2 |
Длина волны 635 нм |
1 |
ВЛОК-635 |
с одноразовыми |
|
Мощность не менее 2 мВт |
стерильными |
||||
|
|
|
|
световодами1 |
444

Лазерная терапия в комплексном лечении онкологических больных
Продолжение табл. 91
Наименование |
|
|
|
|
|
аппарата |
|
Кол-во, |
|
|
|
или лазерной |
Основные параметры |
Методика |
Примечание |
||
шт. |
|||||
излучающей |
|
|
|
||
|
|
|
|
||
головки |
|
|
|
|
|
|
|
|
|
Применяются |
|
КЛ-ВЛОК-525-2 |
Длина волны 525 нм |
1 |
ВЛОК-525 |
с одноразовыми |
|
Мощность не менее 2 мВт |
стерильными |
||||
|
|
|
|
световодами1 |
|
|
|
|
|
Применяются |
|
КЛ-ВЛОК-365-2 |
Длина волны 365 нм |
1 |
ЛУФОК® |
с одноразовыми |
|
|
Мощность не менее 2 мВт |
|
|
стерильными |
|
|
|
|
|
световодами1 |
|
|
Импульсный режим |
|
|
|
|
|
Длина волны 635 нм |
|
|
С насадкой |
|
МЛ-635-402 |
Мощность не менее 35 Вт |
1 |
НЛОК |
||
ПМН3 |
|||||
|
Длительность импульса не менее |
|
|
||
|
|
|
|
||
|
70 нс |
|
|
|
|
|
|
|
Местно, пара- |
|
|
|
Импульсный режим |
|
вертебрально, |
|
|
|
Длина волны 904 нм |
|
в проекцию |
С насадкой |
|
МЛ-904-802 |
Мощность не менее 50 Вт |
1 |
внутренних |
||
ПМН3 |
|||||
|
Длительность импульса не менее |
|
органов, на им- |
||
|
|
|
|||
|
70 нс |
|
мунокомпетент- |
|
|
|
|
|
ные органы |
|
|
|
|
|
Местно, пара- |
|
|
|
Импульсный режим |
|
вертебрально, |
С зеркальной, |
|
|
Длина волны 904 нм |
|
в проекцию |
||
|
|
магнитной |
|||
ЛО-904-20 |
Мощность не менее 15 Вт |
2 |
внутренних |
||
акупунктурной |
|||||
|
Длительность импульса не менее |
|
органов, на им- |
||
|
|
насадкой |
|||
|
70 нс |
|
мунокомпетент- |
||
|
|
|
|||
|
|
|
ные органы |
|
|
|
|
|
Местно |
С зеркальной, |
|
|
Длина волны 635 нм |
|
магнитной |
||
КЛО-635-15 |
1 |
или лазерная |
|||
Мощность не менее 15 мВт |
акупунктурной |
||||
|
|
акупунктура |
|||
|
|
|
насадкой |
||
|
|
|
|
||
Прозрачная |
Насадка выполнена из прозрач- |
|
Обеспечивая |
|
|
насадка для |
ного ударопрочного поликар- |
2 |
контакт лазер- |
– |
|
матричных |
боната, крепится на матричной |
ной головки |
|||
|
|
||||
головок (ПМН) |
лазерной излучающей головке |
|
с кожей |
|
|
Магнитная на- |
Индукция магнитного поля |
|
Для магнитола- |
|
|
в плоскости выходного окна |
1 |
зерной терапии |
– |
||
садка ММ-50 |
|||||
насадки 50 мТл |
|
(МЛТ) |
|
||
|
|
|
|||
Зеркальная |
Диаметр 35 мм |
2 |
– |
– |
|
насадка ЗН-35 |
|||||
|
|
|
|
||
Магнитная на- |
Индукция магнитного поля |
|
|
|
|
в плоскости выходного окна |
2 |
– |
– |
||
садка ЗМ-50 |
|||||
насадки 50 мТл |
|
|
|
||
|
|
|
|
||
Акупунктурная |
Акупунктурная |
1 |
– |
– |
|
насадка А-3 |
|||||
|
|
|
|
445
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/

Лазерная терапия в онкологии
Окончание табл. 91
Наименование |
|
|
|
|
|
аппарата |
|
Кол-во, |
|
|
|
или лазерной |
Основные параметры |
Методика |
Примечание |
||
шт. |
|||||
излучающей |
|
|
|
||
|
|
|
|
||
головки |
|
|
|
|
|
Световод |
|
|
|
|
|
одноразовый |
Стерильный одноразовый |
|
|
|
|
для внутривен- |
|
|
|
||
световод с иглой для ВЛОК |
По коли- |
|
|
||
ного облучения |
|
|
|||
по ТУ 9444-005-72085060-2008 |
честву |
ВЛОК |
– |
||
крови КИВЛ-01 |
Регистрационное удостоверение |
процедур |
|
|
|
к аппаратам |
№ ФСР 2009/04331 от 16.02.2009 |
|
|
|
|
лазерным тера- |
|
|
|
||
певтическим |
|
|
|
|
Примечание. 1 – КИВЛ-01 к аппаратам лазерным терапевтическим по ТУ 9444-005- 72085060-2008 производства Научно-исследовательского центра «Матрикс»; 2 – матрица из 8 лазерных диодов; 3 – прозрачная насадка, в комплекте может поставляться магнитная насадка ММ-50 для МЛТ.
Рак шейки матки
По последним данным, в структуре смертности от злокачественных новообразований в России у женщин в возрастной группе 30–59 лет рак шейки матки занимает 2-е место (10,6%) после рака молочной железы (27,6%) [Злокачественные новообразования в России…, 2019]. Основными методами лечения инвазивных форм рака шейки матки являются хирургический, комбинированный и лучевой, в т. ч. химиолучевой [Архангельская П.А. и др., 2018].
Дистанционное облучение является неотъемлемой частью сочетанной лучевой терапии больных раком шейки матки. Основные задачи дистанционного облучения: воздействие на область первичного очага, на краевые отделы первичной опухоли и на зоны регионарного метастазирования. За последние десятилетия произошло значительное совершенствование методов наружного облучения: использование высокоэнергетических источников, создание новых систем предлучевой подготовки и контроля воспроизведения сеанса облучения и др. В настоящее время разработаны и успешно используются в клинике различные способы направленной центрации фигурных полей статического и подвижного облучения [Крейнина Ю.М., 2011].
Несмотря на появление усовершенствованной техники подведения дозы облучения к мишени, прилежащие здоровые органы и ткани неизбежно испытывают лучевую нагрузку. Развитие лучевых реакций может привести к вынужденному прерыванию курса лучевой терапии, при сочетании с операцией – к нарушению сроков комбинированного лечения, что может негативно повлиять на онкологические результаты лечения. Химиотерапия также сопровождается различными осложнениями, значительно ухудшающими качество жизни пациентов. Химиолучевая терапия может вызвать такие осложнения,
446

Лазерная терапия в комплексном лечении онкологических больных
как эпителииты, эпидермиты, энтериты и др., часто приводящие к нарушению режима облучения или введения цитостатиков и снижению их доз. Таким образом, развитие лучевых реакций – основной лимитирующий фактор для проведения лучевой терапии без перерыва и возможности подведения планируемой дозы облучения. Лучевые реакции со стороны прямой кишки, мочевого пузыря и кишечника составляют основу ранних и поздних лучевых повреждений при проведении лучевой терапии у больных раком шейки матки
иво многом определяют качество жизни излеченных от опухоли пациенток. Частота ранних и поздних лучевых осложнений смежных с маткой органов, по данным различных авторов, составляет от 10 до 50% [Урлова А.Н., 2016].
Лазерная терапия является общепризнанным эффективным методом профилактики ранних лучевых осложнений у онкогинекологических больных. Позволим себе процитировать нормативный документ в части общих рекомендаций с незначительной коррекцией терминологии1, не искажая основной
иверный в целом смысл [Федеральные клинические рекомендации…, 2014].
–Лазерную терапию сопровождения начинают с 1-го дня лучевой терапии.
–Лазерная терапия сопровождения проводится курсом, состоящим из 15 процедур.
–Интервал между процедурами лазернойтерапии сопровождениясоставляет 24 ч (за исключением выходных дней).
–Процедуры лазерной терапии сопровождения проводят через 1–3 ч после сеанса облучения (лучевой терапии).
–Перед началом процедуры лазерной терапии сопровождения пациентку консультирует врач отделения реабилитации; консультация включает сбор жалоб, осмотр кожи передней брюшной стенки, изучение документации.
–Во время процедуры лазерной терапии сопровождения применяется методика полипозиционного воздействия.
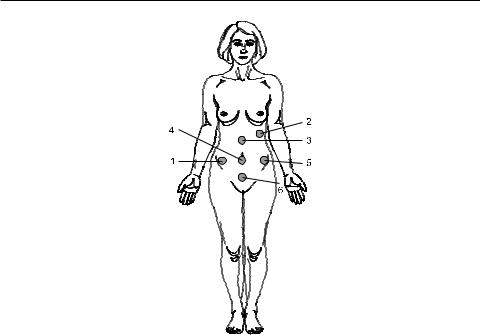
–Лазерную излучающую головку последовательно устанавливают контактно через зеркальную или магнитную насадку на кожу передней брюшной стенки в проекции восходящего отдела ободочной кишки, нисходящего отдела ободочной кишки, поперечной ободочной кишки, желудка, двенадцатиперстной кишки, петель тонкой кишки, сигмовидной кишки и мочевого пузыря (рис. 66).
–Время воздействия в каждой зоне – 4 мин.
1 Термин «магнитолазерная терапия» неактуален, вследствие того что индукция магнитного поля сохраняется не далее чем несколько миллиметров от поверхности кожи, а воздействие в описываемой методике предусмотрено на внутренние органы. Также заменили слово «сеанс», использующееся для лучевой терапии, на термин «процедура», более применимый для лазерной терапии.
447
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Лазерная терапия в онкологии
Рис. 66. Схематическое изображение зон лазерного воздействия в зависимости от проекции внутренних органов на коже передней брюшной стенки:
1 – проекция восходящего отдела ободочной кишки; 2 – проекция нисходящего отдела ободочной кишки, 3 – проекция поперечной ободочной кишки, желудка, двенадцатиперстной кишки; 4 – проекция петель тонкой кишки; 5 – проекция сигмовидной кишки; 6 – проекция мочевого пузыря (Федеральные клинические рекомендации…, 2014)
–Вовремялеченияпациентканаходитсявположениилёжанаспине,руки расположены вдоль тела, коленные суставы разогнуты.
–По окончании процедуры пациентка остаётся в исходном положении в течение 10–15 мин под наблюдением медперсонала кабинета, где проводилась процедура лазерной терапии.
Для достижения эффективного воздействия на глубоко расположенные органы рекомендуется использовать импульсное ИК НИЛИ мощностью не менее 9–12 Вт. Лазерное излучение с частотой 600 Гц оказывает противовоспалительное действие и определяет парасимпатическое состояние освечиваемых биологических тканей. При длительном курсе (более 14–15 процедур) возможно развитие реакции привыкания организма к лечебному фактору.
Применение лазерной терапии сопровождения уменьшает частоту лучевых реакций на 18% и выраженность лучевых реакций. При использовании этой методики не отмечено повышения частоты местных рецидивов и нет ухудшения показателей 3- и 5-летней выживаемости онкологических больных. Разработанная методика лазерной терапии сопровождения является бе-
448

Лазерная терапия в комплексном лечении онкологических больных
зопасной и хорошо переносимой больными, ни у одной пациентки не было зарегистрировано осложнений, связанных с проведением лазерной терапии сопровождения на этапах лучевого лечения. Таким образом, представленный метод профилактики ранних лучевых реакций у онкогинекологических больных позволяет минимизировать частоту и тяжесть осложнений со стороны органов малого таза, не влияя на онкологические результаты лечения и улучшая качествожизнипациенток[Федеральныеклиническиерекомендации…,2014].
Эту методику использовала в своей работе А.Н. Урлова (2016), подтвердив лишнийразданные,представленныевклиническихрекомендациях.Показано, что применение лазерной терапии сопровождения уменьшает:
–частоту лучевых реакций с 48,6 до 31% (р = 0,03), в том числе частоту лучевых циститов с 20 до 4,2% (р = 0,02);
–выраженность лучевых реакций (р = 0,004): частота лучевых реакций I + II ст. в основной и контрольной группе составила 100 и 80% соответственно, III ст. – 0 и 20% соответственно;
–частоту незапланированного перерыва курса лучевого лечения, связанного с развитием лучевых реакций: с 12,5 до 5,1% (р = 0,02) и длительность незапланированного перерыва: с 9,7 до 5,2% при перерыве
3–7 дней и с 2,8 до 0% при перерыве более 7 дней (р = 0,02). Применениелазернойтерапиисопровождениянеухудшаетонкологические
результаты комбинированного и лучевого лечения: кумулятивная 3-летняя общая выживаемость в основной и контрольной группах составила 81,7 и 72,4% соответственно (р = 0,32), кумулятивная 3-летняя безрецидивная выживаемость – 74,9 и 70,5% соответственно (р = 0,97). Разработанная методика лазерной терапии сопровождения является безопасной и хорошо переносимой больными, ни у одной пациентки не было зарегистрировано осложнений, связанных с проведением этой процедуры на этапах лучевого лечения. Лазерная терапия сопровождения по данной методике обоснована и показана для всех онкогинекологических пациентов, проходящих лучевое лечение [Урлова А.Н., 2016].
Основываясь на собственных экспериментальных данных и благоприятных результатах применения ВЛОК при лечении хирургических пациентов, Н.Ф. Гамалея с соавт. (1988) провели ВЛОК-635 (длина волны 633 нм, мощность 5 мВт, экспозиция 5–10 мин) у 25 больных раком шейки матки, которые подвергалисьлучевойтерапииихарактеризовалисьугнетениемкроветворения и иммунного статуса. Несмотря на продолжение лучевой терапии, усиления депрессии кроветворения у больных на фоне лазерной терапии не происходило (табл. 92). Уже после 1–2 процедур наблюдалась стабилизация количества лейкоцитов, постепенное их повышение с максимумом к концу курса терапии. Параллельно повышалось количество эритроцитов и лимфоцитов, показатели СОЭ снижались. При анализе газового состояния крови обнаружено, что насыщение кислородом после каждой процедуры возрастало на 30–40%, парциальное давление углекислого газа снижалось.
449
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
