
4 курс / Общая токсикология (доп.) / Врожденные пороки сердца
.pdf
712 |
Часть 9. ПОРОКИ МИТРАЛЬНОГО КЛАПАНА |
|
|
|
|
а |
|
б |
|
|
|
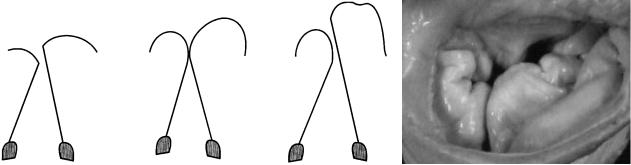
Рис. 5. Парашютный митральный клапан: а ó имеется только одна папиллярная мышца. Стеноз обусловлен облитераци* ей межхордальных пространств; б — препарат сердца с парашютным митральным клапаном
|
клапана сращены или створки настолько дефор |
|
мированы, что комиссуры не идентифицируются. |
|
Иногда вместо одного суженного отверстия может |
|
быть несколько небольших отверстий, которые с |
|
трудом пропускают кровь из увеличенного левого |
|
предсердия. В отдельных случаях над или под кла |
|
паном имеются выраженные соединительноткан |
|
ные образования, частично перекрывающие отве |
|
рстие клапана (1, 13, 14). |
|
ПАТОФИЗИОЛОГИЯ |
|
Функциональная обструкция митрального кла |
|
панного аппарата на любом уровне затрудняет ле |
|
гочный венозный кровоток из левого предсердия в |
|
левый желудочек. В результате повышается давле |
|
ние в левом предсердии, легочных венах и капил |
|
лярном русле. Согласно концепции Starling о |
|
транскапиллярном обмене жидкости, вода проса |
|
чивается в интерстициальное альвеолярное прост |
|
ранство, если гидростатический градиент давле |
|
ния превышает онкотическое давление плазмы. |
|
Застойные бронхиальные ветви сдавливают брон |
Рис. 6. Препарат сердца с аркадой митрального клапана |
хиолы, увеличивая сопротивление дыхательных |
|
путей. Эти и другие факторы отрицательно влияют |
клапана может сочетаться со вторичным и первич |
на механические свойства легких и газообмен, что |
ным ДМПП (27). |
клинически проявляется увеличением дыхатель |
ДИСПЛАЗИЯ |
ных усилий, снижением РаО2, вызывая гипоксе |
мию и гиперкапнию. Одновременно повышается |
|
СТВОРОК МИТРАЛЬНОГО КЛАПАНА |
давление в легочной артерии. Острое повышение |
|
давления в левом предсердии приводит к пассив |
Врожденное изолированное сужение левого |
ному увеличению внутрисосудистого давления, |
AV отверстия без признаков гипоплазии левых от |
растяжению сосудов и компенсаторному сниже |
делов сердца — наиболее редкая аномалия, при |
нию ЛСС (28). Вслед за этим наступает гипокси |
которой створки клапана утолщены, малоподвиж |
ческая легочная вазоконстрикция, развиваются |
ны, неправильной узловатой формы. Комиссуры |
легочная артериальная гипертензия и дисфункция |
Глава 50. СУЖЕНИЕ ПУТЕЙ ПРИТОКА ЛЕВОГО ЖЕЛУДОЧКА |
713 |
|
|
|
|
правого желудочка как результат выраженных структурных изменений резистивных легочных сосудов.
Сопутствующее уменьшение объёма левого же лудочка, ишемия, фиброз и ухудшение его функ ции способствуют снижению сердечного выброса. Падение сердечного выброса и несоответствие доставки кислорода потребностям организма при водят к нарушению обмена веществ, анаэробному метаболизму и системному ацидозу. Вследствие гипоперфузии почек развиваются почечная не достаточность, задержка жидкости и дисбаланс электролитов. В патогенез включаются гормо нальные факторы (29).
КЛИНИКА
Время появления клинических признаков сте ноза митрального клапана зависит от степени обструкции, наличия и характера сопутствующих пороков, физического состояния и адекватности роста младенца. Обструкция митрального клапана заметно не нарушает кровообращение плода, даже при атрезии митрального клапана новорожден ный нормально развит и при рождении отсутству ют признаки внутриутробной сердечной недоста точности.
Проявления выраженного стеноза обнаружи ваются вскоре после рождения и связаны с закры тием артериального протока, снижением систем ного кровотока и возникновением дыхательной недостаточности из за отёка легких. Младенцы с менее тяжелой обструкцией митрального клапана и легкими сопутствующими пороками поступают в клинику после неонатального периода, часто с предшествующей респираторной инфекцией и не достаточной прибавкой массы тела.
Другими признаками являются раздражитель ность, срыгивание при кормлении, профузная пот ливость, одышка и хронический кашель. Плохими прогностическими признаками являются ранний младенческий возраст, малый сердечный выброс и правожелудочковая недостаточность (30).
При тяжелом стенозе отмечаются признаки сниженной периферический перфузии и слабый пульс. При наличии легочной гипертензии увели чен предсердечный толчок правого желудочка. Первый тон сердца ослаблен, тон открытия мит рального клапана обычно отсутствует из за мало подвижности створок клапана. Второй тон сердца расщеплен в большей или меньшей степени, ле гочный компонент акцентуирован при наличии легочной гипертензии. Хотя обструкция притока должна препятствовать наполнению желудочка,
ІІІ и IV сердечные тоны могут выслушиваться. На верхушке определяется низкочастотный негром кий среднедиастолический шум, часто с пресисто лическим усилением. Интенсивность шума может уменьшиться и даже полностью исчезнуть при значительном сниженном сердечном выбросе.
Дополнительные шумы генерируются митраль ной недостаточностью, регургитацией на клапане легочной артерии и сопутствующими пороками.
Электрокардиография
На ЭКГ определяются признаки расширения левого предсердия с широко расщепленным зуб цом Р во II отведении и направленный книзу зубец Р в передних отведениях. Расширение правого же лудочка и предсердия свидетельствует о тяжелом стенозе и легочной гипертензии. Ось QRS откло нена вправо (90–150o), преобладание левого желу дочка может отсутствовать. Однако эти признаки могут варьировать в зависимости от сопутствую щих пороков и развития левого желудочка. При расширении левого предсердия и гипертензии ам булаторные электрокардиографические исследо вания могут выявить предсердные аритмии.
Рентгенография
На рентгенограмме отмечается расширение ле вого предсердия по наличию двойного контура и оттеснению кверху левого главного бронха в пе реднезадней проекции, расширение легочных вен и правых отделов сердца.
Эхокардиография
Одномерная ЭхоКГ более не используется иск лючительно для постановки диагноза, но может быть полезной. Она позволяет оценить открытие митрального клапана, сниженние D Е экскурсии и наклон Е F, аномальное диастолическое движе ние передней створки, увеличение размеров лево го предсердия и уменьшение размеров левого же лудочка.
Двухмерная и цветная Доплер эхокардиогра фия может детализировать большинство анатоми ческих и функциональных признаков митрально го стеноза и, что особенно важно, исключить ле гочную венозную и надклапанную обструкцию.
Парастернальный доступ по длинной оси поз воляет оценить подвижность створок клапана, длину хорд и их прикрепление. Выводной тракт левого желудочка также хорошо виден. Аномалии клапанного кольца и наличие надклапанного мит
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
714 |
Часть 9. ПОРОКИ МИТРАЛЬНОГО КЛАПАНА |
|
|
|
|
рального стенозирующего кольца можно иденти фицировать по парастернальной длинной оси и из четырехкамерного доступа. При тяжелом мит ральном стенозе важно диагностировать тромбоз левых отделов сердца. Парастернальный и субкос тальный доступы по короткой оси хорошо демон стрируют удвоение митрального клапана и анома лии папиллярных мышц (31) (см. рис. 4) .
При цветной допплерографии обнаруживается турбулентный антеградный диастолический ток в левый желудочек. Она может показать локализа цию уровня стеноза (клапан или хордальный ап парат) и оценить выраженность сопутствующей митральной недостаточности. При этом можно оценить другие внутрисердечные пороки. Смеще ние вправо межпредсердной перегородки и оваль ного окна свидетельствуют о повышении давле ния в левом предсердии. С некоторыми ограниче ниями можно количественно оценить объём ре гургитации и степень сужения клапана.
Форма тока при допплерЭхоКГ не нормальна: снижен наклон Е F с ускорением в поздней диас толе. Точное определение размера отверстия кла пана невозможно, так как обструкция может быть на уровне самих створок или дистальнее. Расчет чресклапанного градиента давления производят по модифицированной формуле Bernoulli:
P = 4 v2,
где Р — пик диастолического градиента давле ния на митральном клапане, v — максимальная скорость тока на клапане.
Однако степень стеноза может быть недооцене на, поскольку комплайнс левого предсердия высо кий и значительный градиент давления не может создаться даже при тяжелой обструкции клапана. Площадь митрального отверстия можно рассчи тать, используя допплер сигналы потока (площадь митрального отверстия в см2=220/давление half time (мс)). Давление в левом предсердии можно рассчитать путем прибавления чрезмежпредсерд ного градиента давления через открытое овальное окно к расчетному или известному центральному венозному давлению. И наконец, давление в ле гочной артерии (Рла) рассчитывается по формуле:
Рла=4 (v)2+ЦВД,
где v — пик систолической скорости струи ре гургитации на трехстворчатом клапане (в отсут ствие СЛА).
Периодическое измерение давления в легочной артерии полезно для определения тяжести мит
рального стеноза и времени хирургического вме шательства.
В отдельных случаях показана чреспищеводная ЭхоКГ. Это особенно касается взрослых или пос леоперационных пациентов, у которых наружный доступ ограничен. Исследования могут выпол няться в лаборатории катетеризации, послеопера ционном отделении, во время операции и в амбу латорных условиях у старших пациентов. Интрао перационная ЭхоКГ — важный метод для оценки устранения митрального стеноза и остаточной ре гургитации. Эпикардиальное исследование может быть выполнено с отличным качеством при отсут ствии пищеводного датчика или у очень малень ких детей. Однако это исследование проводится в хирургическом поле. Преимущества чреспище водных исследований состоят в возможности по лучения отличного изображения межпредсердной перегородки, AV клапанов с хордальным аппара том и в отсутствии необходимости внедряться в операционное поле.
Катетеризация сердца
Газы крови отражают умеренную системную де сатурацию и гиперкапнию у пациентов с отёком легких. При тяжелом стенозе оксиметрия позволя ет диагностировать лево правый шунт на предсе рдном уровне через открытое овальное окно. Кате теризация дает возможность произвести прямое измерение давления в легочной артерии и в капил лярном русле и рассчитать ЛСС. Одновременная запись давления в легочном капиллярном русле и левом желудочке демонстрирует увеличенную ле вопредсердную волну а, волну v, среднее давление и диастолический градиент давления между левы ми предсердием и желудочком. Следует отметить, что обструкция легочных вен, трехпредсердное сердце и надклапанное стенозирующее кольцо мо гут имитировать митральный стеноз и сосущество вать с патологией митрального клапана. Сочетание пороков должно быть предварительно диагности ровано неинвазивными методами. Оценка приро ды и тяжести легочной гипертензии усложняется при митральном стенозе. Наличие диастолическо го градиента давления между легочной артерией и средним давлением заклинивания капиллярного ложа свидетельствует о вазоконстрикции или обструктивных изменениях легочных артериаль ных сосудов. Ингаляция кислорода или легочных вазодилататоров может разрешить эту дилемму. Однако иногда требуется открытая биопсия легко го, чтобы определить выраженность легочной со судистой патологии и оценить прогноз. Наконец,
Глава 50. СУЖЕНИЕ ПУТЕЙ ПРИТОКА ЛЕВОГО ЖЕЛУДОЧКА |
715 |
|
|
|
|
если имеется подозрение на обструкцию легочных вен, необходимо сравнить давление заклинивания и давление в левом предсердии.
Киноангиокардиография с контрастированием легочной артерии или левого желудочка в правой передней косой проекции демонстрирует утолще ние и ограниченную подвижность створок мит рального клапана при изолированном стенозе или диастолический дефект заполнения левого желу дочка в виде часового стекла, характерный для па рашютообразного митрального клапана (32). Ан гиография четко выявляет митральную недоста точность. Левая вентрикулография демонстрирует анатомию выводного тракта левого желудочка.
Вредких случаях атрезии митрального клапана
снормально развитым левым желудочком и аор тальным клапаном необходимо селективное конт растирование левого предсердия для уточнения диагноза и выполнения баллонной или ножевой атриосептостомии в целях декомпрессии левого предсердия.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ
Ведение младенцев и детей с невыраженным и умеренным митральным стенозом включает обыч ную терапию сердечной недостаточности и наб людение за возможными осложнениями, такими, как респираторная инфекция, эндокардит, мерца тельная аритмия с угрозой эмболий. При отсут ствии дисфункции правого и левого желудочков назначение дигоксина при сердечной недостаточ ности неэффективно, поскольку повышение дав ления в левом предсердии обусловлено механи ческой обструкцией. Диуретики могут уменьшить легочный венозный застой, однако следует избе гать чрезмерного диуреза, поскольку это может уменьшить выброс левого желудочка из за сниже ния преднагрузки. Если сердечная недостаточ ность устойчива к медикаментозному лечению, необходимо хирургическое устранение обструк ции. Даже в случае временной стабилизации сос тояния ребенка терапевтическое лечение необхо димо рассматривать исключительно как подготов ку к хирургической коррекции порока. В литера туре есть сообщения о единичных случаях успеш ной баллонной ангиопластики митрального сте ноза ревматического или врожденного происхож дения. Однако опыт применения этого метода у младенцев и детей ограничен (33). В настоящее время все усилия должны быть направлены на оп тимальную медикаментозную терапию и сохране ние естественного митрального клапана при хи рургическом вмешательстве.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
При сочетании порока митрального клапана с другими пороками сердца хирургическая тактика должна основываться на наиболее рациональном плане коррекции порока. При умеренно выра женной клинике порока митрального клапана и при наличии других пороков предложено исполь зовать поэтапную коррекцию, например: устра нить хирургическим путем или с помощью кате терной технологии коарктацию аорты, ОАП, кла панный или надклапанный стеноз аорты. Улучше ние состояния ребенка после такой коррекции позволяет отсрочить оперативное вмешательство по поводу митрального стеноза. Взвешенные по казания и время вмешательства являются важной составляющей хирургической тактики.
Вмешательства на митральном клапане целесо образнее выполнять в старшем возрасте, если поз воляет состояние ребенка. Отсрочка дает возмож ность качественнее произвести реконструкцию митрального клапана в большем сердце или вы полнить имплантацию протеза большего размера. Рекомендуется сохранить собственный клапан в период максимального роста ребенка, несмотря на остаточную умеренную некомпетентность мит рального клапана после пластики.
Имплантация митрального клапана в детском возрасте имеет больше отрицательных послед ствий, чем положительных. Наиболее весомым ар гументом против ранних протезирований являет ся необходимость замены протезов по мере увели чения массы тела. Кроме того, постоянный прием ребенком антикоагулянтов создает не меньшую проблему, чем сам искусственный клапан.
Хирургическое лечение врожденного митраль ного стеноза улучшилось с тех пор, как стала более ясной анатомия и функция клапана. Отрицатель ная динамика вторичных изменений и функции левого желудочка, легочной гипертензии и легоч ной функции является показанием для хирурги ческого вмешательства. До настоящего времени мало известно о легочной гипертензии у детей с врожденным митральным стенозом и возможнос ти её уменьшения после длительного естественно го течения (34).
За редкими исключениями, ранние серии вме шательств в 1970 х годах сопровождались неудов летворительными результатами реконструкции или протезирования у детей в возрасте до 1 года (10, 35). В последнее время накопление опыта кла пансохраняющих операций у детей позволило улучшить результаты вальвулопластики и в более старшем возрасте — протезирования клапана
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
716 |
Часть 9. ПОРОКИ МИТРАЛЬНОГО КЛАПАНА |
|
|
|
|
(36–43). Несмотря на улучшение выживаемости, к 8 му году после операции отсутствие необходи мости в повторном вмешательстве составило толь ко 58% (37). Митральная вальвулопластика оста ется паллиативным вмешательством в большин стве случаев. Появление на рынке маленьких низ копрофильных протезов обеспечило возможность раннего протезирования с меньшей обструкцией выводного тракта у отдельных младенцев, состоя ние которых требует замены клапана при неудав шейся попытке его коррекции. Малый диаметр клапанного кольца вынуждает имплантировать клапан в супраанулярную позицию.
Carpentier (44, 45) разделили пациентов с врож денной патологией митрального клапана на две группы: с недостаточностью и стенозом. Методика реконструкции клапана, разработанная Carpentier (46) и основанная на четырех принципах, револю ционизировала хирургию патологии митрального клапана. Эта техника предусматривает:
•ремоделирование кольца;
•резекцию и шовную пластику створок;
•укорочение хорд;
•фенестрацию хордальных сращений.
Коррекция надклапанного стенозирующего кольца
Операция включает иссечение мембраны и коррекцию сопутствующей патологии митрально го клапана. Иногда мембрана настолько прираще на к створкам, что безальтернативным методом остаётся протезирование. Наличие нормального подлежащего митрального клапана дает отличный результат вмешательства.
Врожденный митральный стеноз
Оптимальный возраст пациента для коррекции этой патологии — около 3 лет, хотя операции вы полнялись и в более раннем возрасте. Во время операции следует стремиться получить отверстие, соответствующее среднему нормальному размеру митрального клапана для данной поверхности те ла пациента (см. Приложение, табл. 1). Поскольку врожденный митральный стеноз создается раз личными компонентами клапанного аппарата, важно учесть, являются ли папиллярные мышцы нормальными или патологически уменьшенными.
Нормальные папиллярные мышцы
При гипоплазии клапанного кольца сам клапан может выглядеть нормальным. Компоненты кла
пана и желудочек могут быть гипоплазированны ми, что затрудняет хирургическую коррекцию. В этих случаях следует выбрать один из двух возмож ных вариантов: или клапанный кондуит между ле вым предсердием и левым желудочком (47) или модифицированную операцию Norwood I (48) как первый этап гемодинамической коррекции по Fontan.
При сращении комиссур клапана они обычно слабо дифференцируются, а хорды отсутствуют или плохо развиты. Этот тип сужения устраняют с помощью комиссуротомии и фенестрации папил лярных мышц с удалением вторичных хорд. Хи рург обязан тщательно оценить клапанный аппа рат в области комиссур, так как при врожденном сужении гораздо чаще, чем при приобретенном стенозе, существует вероятность повреждения аномально прикрепленной сухожильной нити или папиллярной мышцы при укорочении хорды. Эф фективная комиссуротомия увеличивает перед нюю створку митрального клапана и не нарушает смыкание створок без необходимости реимплан тации сухожильных нитей. Врожденное сужение митрального клапана часто сопровождается пато логией подклапанного аппарата, в этом случае требуется одновременное расщепление папил лярных мышц.
Необходимость протезирования клапана воз никает редко.
У пациентов с избыточной тканью клапана межхордальные пространства частично или пол ностью облитерированы. Операция предусматри вает иссечение лишних тканей между хордами.
При удвоении митрального клапана с наличи ем фиброзного моста между передней и задней митральными створками имеются два равных кла панных отверстия. Если суммарная площадь двой ного клапана мала, может потребоваться резекция мостика, разделяющего два отверстия. При истин ном удвоении митрального клапана с неравными отверстиями разделять мостик между ними неце лесообразно из за риска развития ятрогенной митральной недостаточности (12).
Аномальные папиллярные мышцы
Эта группа включает три различных варианта врожденного митрального стеноза: парашютооб разный митральный клапан с единственной па пиллярной мышцей, аркаду митрального клапана (гамак) с множеством папиллярных мышц и отсу тствие папиллярных мышц.
При парашютообразном клапане расщепляют папиллярную мышцу и фенестрируют облитери
Глава 50. СУЖЕНИЕ ПУТЕЙ ПРИТОКА ЛЕВОГО ЖЕЛУДОЧКА |
717 |
|
|
|
|
рованные межхордальные пространства. Опера ция часто включает коррекцию сопутствующей обструкции выводного тракта левого желудочка, аортального стеноза и коарктации аорты (комп лекс Shone). Хирургическая летальность зависит от тяжести патологии.
При митральной аркаде (гамаке) стеноз обра зован переплетением хорд и папиллярных мышц, которые заполняют пространство под задней створкой. Такие клапаны часто некомпетентны. Коррекция этого варианта наиболее сложна и, как правило, требует протезирования клапана.
Отсутствие папиллярных мышц как вариант патологии митрального клапана означает прямое прикрепление хорд к стенкам желудочка. При этом межхордальные пространства часто недоста точны. Единственным методом лечения является протезирование клапана.
РЕЗУЛЬТАТЫ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ
Хирургическое лечение врожденного митраль ного стеноза у детей, как показали отдаленные ре зультаты, представленные многими авторами, но сит паллиативный характер. В одном из послед них обзоров авторы (49) сообщают о клиническом
опыте лечения 72 больных, у 13 из которых был изолированный митральный стеноз и у 59 он со четался с другими пороками сердца. Этапному ле чению подвергнуты 23 пациента, одноэтапному — 26. Ранняя летальность составила 12,5%. Факто рами риска были обструкция выводного тракта левого желудочка и этапные вмешательства. В от даленном периоде умерли 8 пациентов. В повтор ных операциях нуждались 24 больных. Десяти па циентам, в том числе оперированным повторно, произведено протезирование клапана. К 15 му году после операции оставались живы 69,6% па циентов, не нуждались в повторных операциях 70,8%, не требовалось протезирование клапана 69,6% пациентам.
Некоторые хирурги являются приверженцами раннего протезирования клапана и размещения его в супраанулярную позицию, однако результаты такого вмешательства неудовлетворительны (50).
Проблемами отдаленного периода являются остаточный митральный стеноз, недостаточность митрального клапана, легочная артериальная ги пертения, левожелудочковая недостаточность, обструкция системного выводного тракта, недос таточность аортального клапана и мерцательная аритмия или трепетание предсердий.
Литература
1.Edmunds H., Wagner H. R. Congenital anomalies of the mitral valve [w:] Arciniegas E. Pediatric Surgery, Year Book Medical Publishers Inc., Chicago, 1985.
2.Ellis H. A history of surgery, Greenwich Medical Media Ltd., London, 2001.
3.Van Mierop LHS, Alley RD, Kausel HW, Stranahan A. The anatomy and embryology of endocardial cushion defect. J Thorac Cardiovasc Surg. 1962; 43: 71–83
4.Gray S. W., Skandalakis J. E. The thoracic aorta, [w:] Embryology for Surgeons, The embryological basic for treatment of congenital defects W. B. Saunders Company, Philadelphia, London, Toronto, 1972.
5.Pansky B. Review of Medical Embriology, Macmillan Publ. Co, New York, Toronto, London, 1982.
6.Magovern JH, Moore GW, Hutchins GM. Development of the atrioven tricular valve region in the human embryo. Anat Rec 1986;215:167–181.
7.Shone J. D., Sellors R. D., Anderson R. C. The development complex of "parachute mitral valve ", supravalvular ring of left atrium, subaortic stenosis and coarctation of the aorta, Am. J. Cardiol. 1963, 11,714.
8.Bharati S., Lev M. Congenital polyvalvular disease, Circulation, 1973, 49, 575.
9.Krovetz L. J., Lorincz A. E., Schiebler G. L. Cardiovascular manifesta tions of the Hurler syndrome, Circulation 1965, 31,132.
10.Ruckman RN, Van Praagh R. Anatomic types of congenital mitral stenosis: report of 49 autopsy cases with consideration of diagnosis and surgical implications. Am J Cardiol 1978;42:592–601.
11.Ascuitto RJ, Ross Ascuitto NT, Kopf GS, et al. Accesory mitral valve tissue causing left ventricular outflow obstruction (two–dimensional .
12.Bano Rodrigo A, Van Praagh S, Trow itzsch E, et al. Double orifice mitral valve: a study of 27 postmortem cases with developmental, diagnostic and surgical considerations. Am J Cardiol 1988;61: 152–160.
13.Davachi R, Moller JH, Edwards JE. Diseases of the mitral valve in infancy: anatomic analysis of 55 cases. Circulation 1971;43:565–579.
14.Ruckman RN, Van Praagh R. Anatomic types of congenital mitral stenosis: report of 49 autopsy cases with consideration of diagnosis and surgical implications. Am J Cardiol 1978;42:592–601.
15.Layman T, Edwards J. Anomalous mitral arcade. Circulation 1967; 35: 389–395.
16.Matsushima A, Park J, Szulc M, et al. Anomalous atrioventricular valve arcade. Am Heart J 1991;121:1824–1826.
17.Carpentier A., Branchini B., Cour J. C. Asfaou E., Villani M., Deloche A., Relland J., D'Allaines C, Blondeau P., Piwnica A., Parenzan L., Brom G. Congenital malformations of the mitral valve in children. Pathology and surgical treatment, J. Thorac. Cardiovasc. Surg. 1976, 72,854.
18.Rosenquist GC. Congenital mitral valve disease associated with coarc tation of the aorta. Circulation 1974;49:985–993.
19.Moller H: Congenital causes of left ventricular inflow obstruction. In: Edwards JE, ed. The heart. Baltimore: Williams & Wilkins, 1974.
20.Glancy DL, Chang MY, Domey ER, et al. Parachute mitral valve: further observations and associated lesions. Am J Cardiol 1971;27:309–317.
21.Celano V, Pieroni DR, Morera JA. et al. Two–dimensional echocardio graphic examination of mitral valve abnormalities associated with coarctation of the aorta. Circulation 1984;69: 924–932.
22.Wernovsky G, Jonas R, Colan S, et al. Results of the arterial switch operation in patients with transposition of the great arteries and abnor
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
718 |
Часть 9. ПОРОКИ МИТРАЛЬНОГО КЛАПАНА |
|
|
|
|
malities of the mitral valve or left ventricular outflow tract. J Am Coll Cardiol 1990;16:1446–1454.
23.Rosenquist GC, Stark J, Taylor JFN. Congenital mitral valve disease in transposition of the great arteries. Circulation 1975;51:731–737
24.Sondheimer HM, Freedom RM, Olley PM. Double outlet right venticle: clinical spectrum and prognosis. Am J Cardiol 1977;39:709–714.
25.De La Cruz MV, Miller BL. Double inlet left ventricle. Circulation 1968;37:249–260.
26.Lieberthson RR, Paul HM, Muster AJ, et al. Straddling and displaced atrioventricular orifices and valves with primitive ventricles. Circulation 1971;43: 213–226.
27.Steinbrunn W, Chon KE, Selzer A. Atrial septal defect associated with mitral stenosis: the Lutembacher syndrome revisited. Am J Med 1970;48:295–302.
28.Snapper JR, Newman JH, Bernard GR, et al. Effects of alveolar hypox ia during partial mitral valve obstruction in anesthetized sheep. Am Rev Resp Dis 1985;131:65–68.
29.Baylen BG, Johnson GJ, Tsang R, et al. The occurrence of hyperaldos teronism in infants with congestive heart failure. Am J Cardiol 1980;305–310.
30.Daoud G, Kaplan S, Perrin EV, et al. Congenital mitral stenosis. Circulation 1963;27:185–196.
31.Trowitzsch E, Bano Rodrigo A, Burger B, et al. Two dimensional echocardiographic findings in double orifice mitral valve. J Am Coll Cardiol 1985;6:383–387.
32.Macartney FJ, Scott O, Ionescu MI, et al. Diagnosis and management of parachute mitral valve and supravalvar ring. Br Heart J 1974;36:641–652.
33.Kveselis DA, Rochini AP, Beekman RB, et al. Balloon angioplasty for congenital and rheumatic mitral stenosis. Am J Cardiol 1986; 57: 348–350.
34.Collins–Nakai RL, Rosenthal A, Castaneda AR, et al. Congenital mitral stenosis: a review of twenty years experience. Circulation 1977; 56: 1039–1047.
35.Klint RB, Cox WD, Agustsson MH, et al. Mitral valve replacement in infancy: a case report. J Thorac Cardiovasc Surg 1976;72:89–93.
36.Benimoun EG, Friedli B, Rutishauser W, et al. Mitral valve replacement in children: comparative study of pre and postoperative hemodynam ics and left ventricular function. Br Heart J 1982;48: 117–124.
37.Coles I, Williams W, Watanabe T, et al. Surgical experience with repar
ative techniques in patients with congenital mitral valvular anomalies. Circulation 1987;76(supplIII):III117–III122.
38.Williams WG, Pollack JC, Geiss DM, et al. Experience with aortic and mitral valve replacement in children. J Thorac Cardiovasc Surg 1981;81:326–333.
39.Antunes MJ. Bioprosthetic valve replacement in children: long term follow up of 135 mitral valve implantations. Eur Heart J 1984;5:913–918.
40.Human DG, Joffe HS, Fraser CB, et al. Mitral valve replacement in chil dren. J Thorac Cardiovasc Surg 1983;83:873–877.
41.Milano A, Vouhe PR, Baillot Vermant F, et al. Late results after left sided cardiac valve replacement in children. J Thorac Cardiovasc Surg 1986;92:218–225.
42.Attie F, Lopez–Soriano F, Ovseyevitz J, et al. Late results of mitral valve replacement with the Bjork Shiley prosthesis in children under 16 years of age. J Thorac Cardiovasc Surg 1986;91:754–758.
43.Schaffer MS, Clarke DR, Campbell DN, et al. The St. Jude medical car diac valve in infants and children: role of anticoagulant therapy. J Am Coll Cardiol 1987;9:235–240.
44.Carpentier A. Congenital malformations of the mitral valve. In: Stark J, de Laval M, eds. Surgery for congenital heart defects. London: Grune & Stratton, 1983: 467–482.
45.Carpentier A, Branchini B, Cour JC, et al. Congenital malformations of the mitral valve in children. J Thorac Cardiovasc Surg 1976; 72: 854–866.
46.Carpentier A. Mitral valve reconstruction in operative surgery. In: Jamieson SW, Shumway NE, eds. Operative surgery. 4th ed. Cardiac surgery. Stoneham, Massachusetts: Butterworth Heinemann 1986;405–414.
47.Corno A, Giannico S, Leibovich S, et al. The hypoplastic mitral valve: when should a left atrial left ventricular extracardiac valve conduit be used? J Thorac Cardiovasc Surg 1986;91: 848–851.
48.Pigott J, Murphy I, Barber G, et al. Palliative reconstructive surgery for hypoplastic left heart syndrome. Ann Thorac Surg 1988;45:122–128.
13. Serraf A, Zoghbi J. Congenital mitral stenosis with or without associ ated defects: an evolving surgical strategy. Circulation 2000;102(19 Suppl 3): III–166–III–171.
50. Adatia I, Moore PM, Jonas RA et al. Clinical course and hemodynam ic observations after supraannular mitral valve replacement in infants and children. / Am Coll Cardiol 1997; 29: 1089–94.
Глава 51
ВРОЖДЕННАЯ НЕДОСТАТОЧНОСТЬ
МИТРАЛЬНОГО КЛАПАНА
Врожденная недостаточность митрального кла пана (ВНМК) обусловлена врожденной аномаль ной структурой компонентов митрального клапа на. Изолированная врожденная недостаточность встречается редко, однако часто сопровождает другие врожденные пороки, заболевания соедини тельной ткани и нарушения обмена веществ. Вто ричная митральная недостаточность возникает вследствие травмы, воспалительных заболеваний, таких, как инфекционные кардиомиопатии, рев матизм, эндокардит, синдром Kawasaki и коллаге новые сосудистые болезни.
ЧАСТОТА
Как изолированный порок развития ВНМК составляет 0,6 % всех ВПС сердца. Патология со четается с другими ВПС в 65–84% случаев (1, 2, 3). Недостаточность митрального клапана, являюща яся специфическим компонентом сложных ВПС (полная форма АВСД, корригированная ТМА, функционально единственный желудочек сердца и др.), в данной главе не рассматривается.
АНАТОМИЧЕСКИЕ ФОРМЫ МИТРАЛЬНОЙ НЕДОСТАТОЧНОСТИ
Пролапс митрального клапана
Частота пролапса митрального клапана состав ляет от 2,5 до 10% всех форм митральной недоста точности (7, 24, 25).
Провисание одной или обеих створок митраль ного клапана происходит за счет того, что свобод ные края створок выступают за края митрального отверстия во время систолы (рис. 1, а). Выбухаю щая в левое предсердие створка (чаще всего зад няя) может иметь истонченные и удлиненные су хожильные нити, кроме того, может отмечаться растяжение фиброзного кольца клапана. Степень пролапса створки бывает различной, поэтому кли ническая симптоматика и тактика хирургического
лечения варьируют. К группе пациентов с этим пороком относятся как пациенты без клиничес кой симптоматики (в основном дети), так и паци енты, нуждающиеся в срочной операции по пово ду выраженной недостаточности митрального клапана (как правило, взрослые).
Этиология «идиопатического», или изолиро ванного, пролапса митрального клапана у детей и взрослых остается неизвестной. Предполагается, что в основе этой патологии лежит миксоматозное перерождение матрикса створок митрального кла пана или коллагеновой структуры хордального ап парата (рис. 1, б, г).
Изолированный пролапс митрального клапана редко приводит к митральной недостаточности и сердечной слабости на первом году жизни. Мик соматозные изменения створок и пролапс отмеча ются при синдроме Marfan уже в раннем возрасте.
Классический пролапс проявляется щелчком, не связанным с выбросом и среднесистолическим шумом.
Легкой формой аномалии створок, при кото рой не показано хирургическое вмешательство в раннем детском возрасте, является волнообраз ный митральный клапан (болезнь Barlow) (30). Особенно часто данная патология обнаруживается у детей пониженного питания. Иногда она сопут ствует синдромам Down, Turner, Klinefelter, синд рому поврежденной Х хромосомы (21), а также синдрому Маrfan (подобная аномалия может об наруживаться при патологии строения грудной клетки — так называемая воронкообразная груд ная клетка (22, 23). Необходимо отличать пролапс митрального клапана от описанного Barlow вол нообразного гипертрофированного клапана (bil lowing valve). При этой аномалии избыток ткани во время систолы перемещается в левое предсердие, в то время как свободные края обеих створок смы каются друг с другом ниже плоскости митрально го клапана. Клапан при синдроме Barlow, несмот ря на нарушение его строения, часто функцио нально сохранен, с хорошим смыканием створок
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
720 |
Часть 9. ПОРОКИ МИТРАЛЬНОГО КЛАПАНА |
|
|
|
|
а |
б |
в |
г |
Рис. 1. Схема створок митрального клапана при различных вариантах их выпадения: а — пролапс створки; б — синдром Barlow без недостаточности митрального клапана; в — синдром Barlow с выпадением створки и недостаточностью мит рального клапана; г — препарат сердца с пролапсом митрального клапана при миксоидной дегенерации
(см. рис. 1, б). Умеренная недостаточность может развиться в детском возрасте. Если же створка клапана будет значительно смещаться по отноше нию к плоскости митрального клапана, возможно развитие выраженной недостаточности. В этом случае пациент подлежит хирургической коррек ции (см. рис. 1, в).
Расщепление створки митрального клапана
Расщепление (cleft) передней створки митраль ного клапана в качестве изолированного порока является наиболее частой аномалией, которая приводит к неполному смыканию его створок (рис. 2) (26, 27). Несмыкание створок может фор мироваться со временем в связи с фиброзом и под ворачиванием створок клапана в месте их расщеп ления (28).
Изолированное расщепление передней створ ки часто сопровождается значительной митраль ной недостаточностью. Реже наблюдается рас щепление задней створки. Изолированное рас щепление митральных створок бывает у людей, не имеющих симптомов. Наиболее частыми сопут ствующими врожденными пороками являются де фекты перегородок и ТМА.
Расщепление передней створки иногда сопро вождается дополнительными хордами, которые аномально крепятся к межжелудочковой перего родке. Они могут создавать препятствие в вывод ном тракте левого желудочка и ограничивать под вижность передней створки, что увеличивает вы раженность митральной недостаточности.
Место расщепления обычно располагается вблизи аортального клапана. Этой аномалии мо жет сопутствовать межжелудочковый дефект. Рас щепление створки клапана является одним из компонентов классического АВСД, который, нес мотря на схожесть отдельных проявлений с изоли рованным расщеплением створки митрального
клапана, представляет собой иной вид патологии
(2). При АВСД леворасположенная, так называе мая митральная, часть общего клапана является не только в анатомическом, но и в функциональном плане многостворчатым клапаном, зачастую с хо рошим смыканием створок. В связи с этим мне ния специалистов разделились: некоторые из них ставят под сомнение необходимость ушивания расщепления створки митрального клапана (или митральной части общего клапана) при полной сохранности его функции. Доводом против рутин ного ушивания расщепления является возмож ность нарушения строения еще незрелого клапана с его ростом или просто вследствие хирургической травмы, приводящей к разрастанию фиброзной ткани. Большая часть хирургов все же рекомен дуют рутинное воссоздание нормальной анатомии митрального клапана, основываясь на том, что ушивание расщепления может препятствовать развитию фиброза в этой области и подворачива нию свободных краев, ведущих к возникновению недостаточности клапана.
Расщепление задней створки митрального кла пана встречается крайне редко (7).
Аркада митрального клапана
При аркаде или гамакоподобном митральном клапане свободные края створок утолщены, зак руглены, хорды укорочены и сращены между со бой и аномальными мышцами. В большинстве случаев недостаточное смыкание створок приво дит к регургитации, которая сочетается с митраль ным стенозом. Известны случаи аномалии Эбш тейна митрального клапана, когда задняя створка смещена книзу (4). Левый желудочек гипоплази рован.
Помимо приведенных выше аномалий сущест вуют также иной анатомический субстрат мит ральной недостаточности, например агенезия

Глава 51. ВРОЖДЕННАЯ НЕДОСТАТОЧНОСТЬ МИТРАЛЬНОГО КЛАПАНА |
721 |
|
|
|
|
Рис. 2. Препарат сердца с изолированным расщеплением пе редней створки митрального клапана
створки либо ее части, врожденная перфорация створки и другие нарушения строения митраль ного клапана (рис. 3).
Вторичная митральная недостаточность
Недостаточность митрального клапана может сопровождаться различными врожденными и приобретенными заболеваниями: дефектом эн докардиальных подушечек, коарктацией аорты, ДМЖП, ДМПП, ОАП, дивертикулом левого же лудочка, отхождением левой коронарной арте рии от легочного ствола, коронарным артери итом (болезнь Kawasaki), дилатационной и гипе ртрофической кардиомиопатиями, опухолью сердца, злокачественной инфильтрацией, рев матическим и вирусным миокардитом, коллаге новыми заболеваниями, метаболическими нару шениями (болезнь Hurler), патологией соедини тельной ткани (синдром Marfan и синдром Ehlers–Danlos) (5–19).
Анатомические нарушения при вторичной митральной недостаточности разнообразны, в патологический процесс вовлечены все элемен ты клапанного аппарата: кольцо, створки, хорды и папиллярные мышцы. Примечательно, что при болезни Kawasaki митральная недостаточность
а |
|
б |
|
в |
г |
|
д |
Рис. 3. Схематическое изображение аномалий митрального клапана: a — нормальное строение; б — частичная аплазия сухожильных нитей; в — изолированное удлинение сухожильных нитей; г — отсутствие (агенезия) папиллярных мышц; д — удлинение одной из папиллярных мышц, приводящее к пролабированию одной из створок
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
