
5 курс / Пульмонология и фтизиатрия / Бронхолегочные_осложнения_хронического_лимфолейкоза_и_множественной
.pdf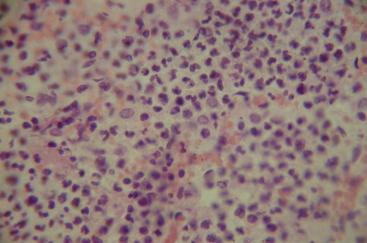
воспалительный фокус, дающий классическую физикальную и рентгенологическую картину. В большинстве случаев пневмонии при агранулоцитозе дебютируют клиникой бактериально-токсического шока. В диагностике пневмонии значительную помощь оказывает компьютерная томография.
3.У больных ММ установлен высокий процент возникновения нозокомиальных пневмоний (39%).
4.Тяжелому, затяжному и атипичному течению пневмоний у больных ММ способствуют гранулоцитопения, вторичный иммунодефицит, значительные нарушения эндобронхиальной микрогемоциркуляции, легочной вентиляции и перфузии, почечная недостаточность, сопутствующая патология.
5.В соответствии с фактом возникновения пневмонии в стационаре или вне стационара, предполагаемым возбудителем, клини- ко-патогенетической ситуацией, наличием осложнений и фоновых заболеваний составлен алгоритм эмпирической антибиотикотерапии пневмоний у больных ММ в период до выявления возбудителя и определения его чувствительности к антибиотикам, а также для тех ситуаций, когда установить этиологический диагноз пневмонии не представляется возможным.
Рис. 47. Пневмония у больного ММ, с количеством лейкоцитов в периферической крови – 5,9×109/л. Окр. гематоксилином и эозином.
Ув. × 240.
231
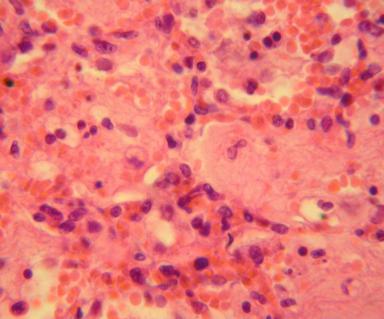
Рис. 48. Пневмония у больного ММ, на фоне агранулоцитоза. Окр. гематоксилином и эозином. Ув. × 240
6.2. Особенности течения хронической обструктивной болезни легких и хронического легочного сердца
при множественной миеломе
Среди 123 обследованных больных с ММ хроническая обструктивная болезнь легких (ХОБЛ) диагнострована у 20 (16,3%), из них 18 мужчин и 2 женщины. Средний возраст – 59,0±2,5 лет. У всех в анамнезе отмечалось длительное курение. Диагноз ХОБЛ 20 пациентам был выставлен до того, как появились первые клинические и лабораторные признаки ММ. Продолжительность ХОБЛ от 5 до 20 лет. В I группе диагностировано 5, во II группе – 13, в III – 2 пациента с ХОБЛ.
Основными клиническими проявлениями ХОБЛ были кашель, выделение мокроты (преимущественно слизисто-гнойного или
232
гнойного характера), одышка, потливость, слабость, быстрая утомляемость. Кашель беспокоил пациентов в течение всех суток, но был более выражен по утрам, часто был приступообразного характера. Мокрота была обильной или скудной, слизисто-гнойной или гнойной. Для всех 20 человек была характерна выраженная одышка с участием вспомогательных дыхательных мышц. Большинство пациентов отмечали усиление одышки при физической нагрузке. Основные клинические проявления ХОБЛ у больных ММ приведены в таблице 67. При этом учитывалось, что такие симптомы как слабость, потливость, повышение температуры тела, утомляемость, одышка могут быть проявлением ММ на поздних этапах опухолевой прогрессии вследствие интоксикации и анемии (II и III группы). Тяжелая одышка развивается у больных с нефрогенным отеком легких. Но на поздних этапах развития ММ, в большинстве случаев, имеют место и другие признаки прогрессирования опухоли. Характерная эмфизематозная деформация грудной клетки в большинстве случаев являлась проявлением ХОБЛ. Но у больных миеломой в III стадии может сформироваться выраженная деформация грудной клетки вследствие остеодеструктивного процесса. Поэтому при диагностике ХОБЛ у этих больных в первую очередь следует учитывать такие клинические проявления как кашель с выделением мокроты и аускультативные данные.
Для больных ММ I группы (IА, IIАстадии) а также для больных в стадии ремиссии и стабильного плато симптомы опухолевой интоксикации и тяжелая анемия не характерны, поэтому в данных ситуациях одышку, слабость, потливость, повышение температуры тела, утомляемость следует объяснять наличием ХОБЛ.
Обострение бронхообструктивного процесса у многих больных ХОБЛ ассоциированной с ММ развивалось после проведения цитостатической терапии, на фоне гранулоцитопении. В 3 случаях у таких больных после проведения цитостатической терапии (протоколы полихимиотерапии, включающие глюкокортикоиды) диагностировали пневмонию с тяжелым и затяжным течением.
При обострении ХОБЛ у больных ММ оценивали тяжесть обоих заболеваний. В большинстве случаев ведущими на этот момент были симптомы бронхообструктивного процесса (за исключением больных с почечной недостаточностью). В подобных ситуациях в начале проводили лечение ХОБЛ и только после достижения ремиссии ХОБЛ назначали цитостатическую терапию.
233
Таблица 67. Основные клинические проявления ХОБЛ у больных ММ.
Симптом |
Количество больных (n=20) |
Кашель |
20 |
Одышка |
20 |
Выделение мокроты: |
20 |
1. Слизисто-гнойная |
13 |
2. Гнойная |
7 |
Слабость |
18 |
Потливость |
16 |
Повышение t˚ |
5 |
Быстрая утомляемость |
20 |
Симптомы интоксикации |
10 |
|
|
Цианоз |
12 |
Хрипы: |
20 |
1. сухие |
16 |
2. влажные |
9 |
Жесткое дыхание |
13 |
|
|
Ослабленное дыхание |
7 |
|
|
Диагностическая бронхоскопия была проведена 15 больным с ХОБЛ протекающей на фоне ММ. У 4 человек был выявлен двухсторонний диффузный эндобронхит I степени, у 6 – II степени и у 5
– III степени.
Средние показатели ФВД, регистрируемые методом спирографии, у больных ХОБЛ и ММ (ЖЕЛ – 53,9±3,0; ОФВ1 – 48,9±3,2;
ИВТ – 50±4,5%Д, ПОСвыд – 34,8±4,0; МОС25 – 32,7±3,6; МОС50 –
30,8±2,6; МОС75 – 38,9±2,8 %Д) не имели достоверных различий с показателями 3-й контрольной группы (больные ХОБЛ без сопутствующего гемобластоза).
В соответствии со спирометрической классификацией тяжести ХОБЛ в зависимости от показателей ОФВ1 и ОФВ1/ФЖЕЛ [262, 322] в основной группе диагностировано 9 больных II (среднетяжелой), 7 больных III (тяжелой) и 4 больных IV (крайне тяжелой) стадий, что в процентном соотношении соответствовало больным 3-й контрольной группы (45, 35 и 20%).
234
Изучение величины бронхиального сопротивления методом пневмотахографии у больных ХОБЛ протекающей на фоне ММ показало значительное увеличение Raw по сравнению с аналогичными показателями в контрольной группе (здоровые) и незначительное увеличение по сравнению с данными больных ХОБЛ без сопутствующего лимфопролиферативного заболевания (таблица 68). Различие показателей величины бронхиального сопротивления у пациентов основной и 3-й контрольной групп объясняется тем, что у больных ММ II и III групп исходно эти показатели несколько выше вследствие специфических бронхолегочных проявлений миеломы и хронической почечной недостаточности (глава 4.2.).
При проведении пикфлоуметрии в среднем в утренние часы показатели ПСВ составляли 46% от должного, в вечернее время 51%. Достоверных различий показателей ПСВ и ее суточных колебаний у больных основной и 3-й контрольной групп не отмечено.
|
|
|
Таблица 68. |
|
|
|
|
|
|
Показатель |
ХОБЛ + ММ |
Контроль |
3-я контрольная |
|
|
(основная группа; |
(n=30) |
группа |
|
|
n=20) |
|
( n=20) |
|
На вдохе |
5,6±0,13; |
2,8±0,1 |
4,8±0,15 |
|
|
Р1<0,001; Р2<0,05 |
|
|
|
На выдохе |
5,8±0,15; |
3,0±0,06 |
5,0±0,2 |
|
|
Р1<0,001; Р2<0,05 |
|
|
|
Показатели бронхиального сопротивления (см.вод.ст/л/сек) у больных ХОБЛ, ассоциированной с ММ.
Примечание: Р1 – достоверность различий между показателями основной и контрольной групп, Р2 – основной и 3-й контрольной группами.
С целью изучения микрогемоциркуляции в проксимальных отделах бронхиального дерева 10 больным ХОБЛ ассоциированной с ММ (2 больных из I, 7 из II, 1 из III групп) выполнена эндобронхиальная ЛДФ на лазерном анализаторе капиллярного кровотока ЛАКК - 02. У всех больных диагностировали значительные нарушения микроциркуляторного кровотока. ПМ, характеризующий состояние перфузии тканей, был значительно снижен (Р<0,001). Значения σ были ниже показателей контроля (Р<0,01). Кv оказался значитель-
235
но выше контроля (Р<0,001). Таблица 69. Выявлены достоверные корреляционные связи между интенсивностью воспаления в бронхах и снижением ПМ (r = - 0,52; Р<0,05), между снижением ОФВ1 и снижением ПМ (r = 0,48; Р<0,05). Но при этом необходимо иметь ввиду, что при ММ выявлены высокие обратные корреляционные связи между уровнем сывороточного парапротеина и снижением ПМ (r = - 0,8, Р<0,01), между длительностью заболевания (ММ) и снижением ПМ (r = - 0,64, Р<0,01), между повышением уровня креатинина крови и снижением ПМ (r = - 0,5, Р<0,05). При ММ важным фактором способствующим нарушению микроциркуляции является гипервискозность крови.
Таблица 69. Характеристика ЛДФ-показателей в проксимальных отделах
бронхов у больных ХОБЛ, ассоциированной с ММ (М±m)
Показа- |
Контроль |
Больные ХОБЛ, |
|
тели |
(n=20) |
ассоциированной с ММ |
|
|
|
|
(n=10) |
|
|
До лечения |
Через месяц после |
|
|
|
лечения |
ПМ, ПЕ |
82,3±5,3 |
30,39±3,2; |
35±3,4 ; |
|
|
Р1<0,001 |
Р1<0,001; Р2>0,05 |
σ, ПЕ |
10,7±0,5 |
8,6±0,4; |
8,8±0,3 ; |
|
|
Р1<0,01 |
Р1<0,01; Р2>0,05 |
Кv, % |
13,8±1,2 |
35,37±4,5; |
29,2±3,0 ; |
|
|
Р1<0,001 |
Р1<0,001; Р2>0,05 |
Аэ, ПЕ |
3,9±0,4 |
2,4±0,13; |
2,6±0,22; |
|
|
Р1<0,05 |
Р1<0,01; Р2>0,05 |
Ан, ПЕ |
3,2±0,7 |
5,5±0,8; |
5,5±0,8; |
|
|
Р1<0,05 |
Р1<0,05; Р2>0,05 |
Ам, ПЕ |
3,6±0,8 |
5,4±0,7; |
5,0±0,6 ; |
|
|
Р1>0,001 |
Р1>0,05; Р2>0,05 |
Ад, ПЕ |
3,7±0,5 |
6,12±0,6; |
5,7±0,5; |
|
|
Р1<0,01 |
Р1<0,01; Р2>0,05 |
Ас, ПЕ |
3,4±0,4 |
2,5±0,13 ; |
2,53±0,1; |
|
|
Р1<0,05 |
Р1<0,05; Р2>0,05 |
Примечание: В таблицах 69 и 70 Р1 – достоверность различий между показателями основной и контрольной групп, Р2 – между показателями основной группы до и после лечения ХОБЛ
236
При проведении амплитудно-частотного анализа допплерограмм выявлено, что амплитуды колебаний в Э-диапазоне, у больных ХОБЛ оказались ниже контрольных значений (Р<0,001). Это можно объяснить исходным снижением колебаний в данном диапазоне у больных II и III групп, вне присоединения БОД. Снижение эндотелиальных колебаний отмечается и у больных с тяжелым течением ХОБЛ, без сопутствующего гемобластоза [238].
Амплитуды колебаний в Н-диапазоне, в отличие от аналогичных у больных ММ, вне присоединения БОД, были повышены, что объясняется их увеличением при ХОБЛ [238]. Амплитуда колебаний в М-диапазоне по сравнению с контролем достоверно не изменялась. Отмечено существенное повышение колебаний в дыхательном диапазоне. Увеличение амплитуды дыхательной волны свидетельствует о снижении микроциркуляторного давления и ухудшении оттока крови из микроциркуляторного русла. Поскольку у больных ММ, вне присоединения БОД, не отмечено повышения нейрогенной и дыхательной амплитуд, их увеличение следует объяснить изменениями бронхиального дерева при ХОБЛ. Амплитуда колебаний в С-диапазоне, приносящихся в микроциркуляторное русло из артерий, была уменьшена по сравнению с контролем. Снижение амплитуды колебаний в данном диапазоне указывает на снижение притока артериальной крови в микроциркуляторное русло. Это может иметь место вследствие гипервискозности плазмы у больных ММ, т.к. в процессе опухолевой прогрессии диагностировано снижение амплитуд колебаний в С-диапазоне (глава 4). У больных ХОБЛ, без сопутствующего гемобластоза амплитуды сердечных колебаний не изменяются [238].
Через 4 недели после начала терапии ХОБЛ, этим больным повторно проводили эндобронхиальную ЛДФ (таблица 69). ПМ оставался значительно сниженным. Значения σ и Кv не претерпевали значительных изменений. Амплитуды колебаний во всех диапазонах достоверно не изменялись. Значительные изменения микроциркуляторного кровотока в слизистой проксимальных бронхов у больных ХОБЛ ассоциированной с ММ сохранялись, даже в случае улучшения бронхоскопической картины (таблица 69). Это может быть обусловлено, в первую очередь, наличием синдрома повышенной вязкости крови, при котором изначально имеют место значительные нарушения микрогемоциркуляции. У больных ММ, без со-
237
путствующего бронхообструктивного процесса, значительно снижены ПМ и Ас.
Исследован газовый состав крови у больных ХОБЛ ассоциированной с ММ. Отмечено увеличение рСО2 (49,6±1,7 мм.рт.ст;
Р<0,001), снижение рО2 (64,2±1,5 мм.рт.ст.; Р<0,001) и рН
(7,365±0,004; Р<0,001) капиллярной крови по сравнению с контролем. Показатели рО2 и рН основной группы были ниже аналогичных показателей в 3 контрольной группе (69,1±0,9; Р<0,05 и 7,38±0,006; Р<0,05 соответственно), что можно объяснить снижением их у больных ММ.
Лечение обострений ХОБЛ у больных ММ проводилось по тем же правилам, что и лечение ХОБЛ при ХЛЛ. Динамика клинических проявлений ХОБЛ в стадию обострения у больных ММ сопоставлялась с динамикой этих показателей у больных ХОБЛ без сопутствующего гемобластоза (3-я контрольная группа). Так как при ММ, в анализах крови имеет место значительное ускорение СОЭ, этот показатель для оценки регрессии проявлений ХОБЛ не учитывали. У больных ХОБЛ и ММ, по сравнению с 3-й контрольной группой, значительно дольше сохранялись слабость, лейкоцитоз и нейтрофиллез (Таблица 70).
Ведущими причинами, способствующими тяжелому и затяжному течению обострений ХОБЛ являются: выраженный вторичный иммунодефицит, в первую очередь «синдром недостаточности антител»; проводимые курсы химиотерапии и глюкокортикоидной терапии, усугубляющие иммунодефицит; наличие бронхолегочных проявлений ММ (плазмоклеточная и лимфоидная инфильтрация легких, бронхов и плевры, парапротеиноз, амилоидоз, пневмофиброз, компенсаторная локализованная эмфизема); нарушение эндобронхиальной микрогемоциркуляции и легочной перфузии; нарушение экскурсии грудной клетки и диафрагмы, вследствие остеодеструктивного процесса.
Из 123 больных ММ у 20 пациентов по данным клинических, рентгенологических, электрокардиографических и эхокардиографических исследований было диагностировано хроническое легочное сердце (ХЛС). Причиной развития ХЛС у них явилось длительное течение хронической обструктивной болезни легких (ХОБЛ). Во всех случаях диагноз ХОБЛ выставлен от 5 до 20 лет назад. При сборе анамнеза удалось выяснить, что первые клинические признаки обструкции легких у большинства этих больных были выявлены за-
238

долго до постановки диагноза ХОБЛ. У 18 пациентов по клиническим и рентгенологическим данным имела место эмфизема легких, у 14 диффузный пневмосклероз.
Таблица 70. Динамика клинических проявлений ХОБЛ у больных основной
и 3-й контрольной групп
Симптом |
Длительность сохранения |
Р |
|
|
симптома (дни) |
|
|
|
3 контр. группа |
Больные ММ |
|
|
(n=25) |
(n=15) |
|
Кашель |
11,9±1,8 |
13,8±1,8 |
>0,05 |
Одышка |
2,7±0,5 |
2,9±0,8 |
>0,05 |
Выделение |
8,5±1,5 |
8,6±1,0 |
>0,05 |
мокроты |
|
|
|
Хрипы |
7,0±1,0 |
7,2±0,9 |
>0,05 |
Слабость |
6,2±0,9 |
10,8±1,1 |
<0,01 |
Потливость |
6,9±1,0 |
7,0±1,1 |
>0,05 |
Повышение |
5,2±0,9 |
6,0±1,0 |
>0,05 |
температуры |
|
|
|
Лейкоцитоз |
7,9±0,8 |
10,8±1,2 |
<0,05 |
Нейтрофиллез |
7,9±0,8 |
10,8±1,2 |
<0,05 |
Компенсированное легочное сердце диагностировано у 14 и декомпенсированное у 6 человек. У больных с компенсированным ХЛС преобладал симптомокомплекс хронической дыхательной недостаточности: одышка, утомляемость при физической нагрузке, цианоз. Важную роль в своевременной диагностике ХЛС у этих пациентов играли данные целенаправленного физикального, лабораторного и инструментального (электрокардиография, ЭХОКГ, ИДКГ, рентгенография) обследования больного. При проведении этих методов исследования выявляли те же характерные проявления ХЛС, что и при диагностике легочного сердца у больных ХЛЛ (глава 5). Клиника декомпенсированного легочного сердца характеризовалась присоединением к дыхательной недостаточности правожелудочковой сердечной недостаточности: отеки, набухание шейных вен, пульсация печени, положительный симптом Плеша. Уве-
239
личение печени при ММ может являться проявлением основного заболевания, поэтому расценивать гепатомегалию только как признак декомпенсации ХЛС в данной ситуации не представляется возможным. Таблица 71.
Таблица 71 Клинические проявления ХЛС у больных ММ
№ |
Клинический симптом |
Количество |
|
|
больных |
1 |
Усиленный разлитой сердечный толчок |
10 |
|
в прекардиальной области |
|
2 |
Тахикардия |
11 |
3 |
Акцент II тона над легочной артерией |
20 |
4 |
Усиленный I тон над трехстворчатым |
18 |
|
клапаном по сравнению с верхушкой сердца |
|
5 |
Усиленный II тон над мечевидным отростком |
14 |
|
в точке прикрепления IV – V ребер к грудине |
|
|
справа по сравнению с основанием сердца |
|
6 |
Эпигастральная пульсация |
8 |
7 |
Цианоз |
20 |
8 |
Расширение правой границы относит. |
6 |
|
тупости сердца |
|
9 |
Смещение кнутри до срединной линии тела |
4 |
|
правой границы абсолютной тупости сердца |
|
10 |
Толчок правого желудочка в IV – V |
4 |
|
межреберьях слева у края грудины |
|
11 |
Пресистолический и протодиастолический |
4 |
|
галоп в зоне аускультации трехстворчатого |
|
|
клапана или правого желудочка |
|
12 |
Одышка |
20 |
13 |
Утомляемость при физической нагрузке |
20 |
14 |
Увеличение печени |
6 |
15 |
Отеки нижних конечностей |
6 |
16 |
Набухание шейных вен |
6 |
17 |
Пульсация печени |
6 |
18 |
Положительный симптом Плеша |
6 |
19 |
Систолический шум у основания грудины |
6 |
20 |
Нарушения со стороны ЦНС |
5 |
21 |
Олигоурия |
3 |
240
