
5 курс / Госпитальная педиатрия / РЛС_Доктор_Неврология_и_психиатрия,_2015
.pdf
|
|
|
|
|
|
Леветинол® |
369 |
|
нение к этому он частично устраня+ |
Фармакокинетические свойства ле+ |
|||||||
ет уменьшение токов по ГАМК+ и |
ветирацетама у пациентов с эпилеп+ |
|||||||
глициновым каналам, |
вызванных |
сией и здоровых добровольцев сопо+ |
||||||
цинком и |
β+карболинами. Более |
ставимы. |
|
|||||
того, в исследованиях in vitro пока+ |
Вследствие полной и линейной аб+ |
|||||||
зано, что леветирацетам связывает+ |
сорбции плазменная концентрация |
|||||||
ся с особыми участками головного |
поддается прогнозированию по вели+ |
|||||||
мозга крыс. Этими участками явля+ |
чине дозы леветирацетама, выражен+ |
|||||||
ется белок 2А синаптических пузы+ |
ной в мг/кг. Поэтому контролировать |
|||||||
рьков, который, как предполагается, |
плазменную концентрацию |
левети+ |
||||||
вовлечен в процесс слияния пузы+ |
рацетама не требуется. |
|
||||||
рьков и экзоцитоз нейротрансмит+ |
У взрослых и детей показана высокая |
|||||||
теров. Леветирацетам и его аналоги, |
корреляция между концентрацией |
|||||||
связывающиеся с белком 2А синап+ |
леветирацетама в плазме и слюне (от+ |
|||||||
тических |
пузырьков, |
проявляют |
ношение слюна/плазма находится в |
|||||
противосудорожную активность на |
пределах 1 для таблеток для приема |
|||||||
аудиогенной модели эпилепсии у |
внутрь). |
|
||||||
мышей, причем чем сильнее связь, |
Взрослые и подростки |
|
||||||
тем выше активность. Эти данные |
Абсорбция. После приема внутрь ле+ |
|||||||
подразумевают, что связывание ле+ |
ветирацетам быстро всасывается. Аб+ |
|||||||
ветирацетама с белком 2А синапти+ |
солютная биодоступность после при+ |
|||||||
ческих |
пузырьков |
реализует |
его |
ема внутрь близка к 100%.Tmax в плаз+ |
||||
противосудорожное действие. |
|
ме — 1,3 ч. Равновесное состояние до+ |
||||||
Фармакодинамические эффекты. Ле+ |
||||||||
стигается через 2 дня при приеме пре+ |
||||||||
ветирацетам оказывает противосудо+ |
парата 2 раза в сутки. |
|
||||||
рожное действие на многих моделях |
Cmax обычно составляет 31 и 43 |
|||||||
парциальных и первично генерализо+ |
мкг/мл соответственно после одно+ |
|||||||
ванных судорог у животных без со+ |
кратного приема 1000 мг и приема |
|||||||
путствующего просудорожного |
эф+ |
1000 мг препарата 2 раза в сутки. Ве+ |
||||||
фекта. Основной метаболит левети+ |
личина абсорбции не зависит от дозы |
|||||||
рацетама неактивен. |
|
|
и от приема пищи. |
|
||||
Леветирацетам проявляет противо+ |
|
|||||||
Распределение. Данные о распределе+ |
||||||||
судорожную активность при |
пар+ |
нии у человека отсутствуют. Левети+ |
||||||
циальной и генерализованной эпи+ |
рацетам и его основной метаболит |
|||||||
лепсии у человека (эпилептиформ+ |
слабо связываются с белками плазмы |
|||||||
ный |
всплеск/фотопароксизмаль+ |
(<10 %).Vd леветирацетама составля+ |
||||||
ный ответ), что подтверждает его |
ет около 0,5–0,7 л/кг, что приблизи+ |
|||||||
широкий |
спектр |
фармакологиче+ |
тельно соответствует объему воды в |
|||||
ского действия. |
|
|
|
организме. |
|
|||
|
|
|
|
|
|
|
||
ФАРМАКОКИНЕТИКА. Леветира+ |
Биотрансформация. Леветирацетам |
|||||||
цетам хорошо проникает через гисто+ |
слабо метаболизируется в организ+ |
|||||||
гематические барьеры. Фармакокине+ |
ме человека. Основным метаболи+ |
|||||||
тический профиль носит линейный |
ческим путем (24% дозы) является |
|||||||
характер с низкой внутри+ и межинди+ |
ферментативный гидролиз |
ацета+ |
||||||
видуальной вариацией. После длите+ |
мидной группы. Изоферменты ци+ |
|||||||
льного применения изменения кли+ |
тохрома Р450 печени не участвуют в |
|||||||
ренса не происходит. Свидетельства о |
образовании основного метаболита |
|||||||
наличии половых, расовых или суточ+ |
(ucb L057). Гидролиз ацетамидной |
|||||||
ных фармакокинетических отличий |
группы происходит во многих тка+ |
|||||||
отсутствуют. |
|
|
|
нях, включая клетки крови. Метабо+ |
||||

370 |
Леветинол® |
|
|
|
Глава 2 |
|||
лит ucb L057 фармакологически не+ |
ние первых 48 ч. Почечный клиренс |
|||||||
активен. |
|
|
|
|
леветирацетама и ucb L057 составля+ |
|||
Также обнаружены два второстепен+ |
ет 0,6 и 4,2 мл/мин/кг соответствен+ |
|||||||
ных метаболита. Первый образуется |
но, что свидетельствует об экскреции |
|||||||
за счет гидроксилирования пирроли+ |
леветирацетама посредством клубоч+ |
|||||||
донового кольца (1,6% дозы), вто+ |
ковой фильтрации с последующей |
|||||||
рой — путем раскрытия пирролидо+ |
канальцевой реабсорбцией, а основ+ |
|||||||
нового кольца (0,9% дозы). Прочие |
ного метаболита — наряду с клубоч+ |
|||||||
неидентифицированные метаболиты |
ковой фильтрацией — путем актив+ |
|||||||
составляют лишь 0,6% дозы. Оптиче+ |
ной канальцевой секреции. Элимина+ |
|||||||
ская изомеризация леветирацетама и |
ция леветирацетама коррелирует с |
|||||||
его основного метаболита in vivo не |
клиренсом креатинина. |
|
|
|||||
выявлена. |
|
|
|
Особые группы пациентов |
|
|||
Леветирацетам и его основной мета+ |
Пожилые пациенты. T1/2 |
у пожилых |
||||||
болит не ингибируют основные изо+ |
увеличивается на 40% (до 10–11 ч), |
|||||||
ферменты |
цитохрома |
Р450 печени |
что обусловлено снижением функции |
|||||
человека (CYP3A4, 2А6, 2С9, 2С19, |
почек у данной группы населения. |
|
||||||
2D6, 2Е1 и 1А2), глюкуронилтранс+ |
Почечная |
недостаточность. Кажу+ |
||||||
феразу (UGT1A1 и UGT1A6) и эпок+ |
щийся клиренс леветирацетама и его |
|||||||
сидгидроксилазу in vitro. Леветираце+ |
основного |
метаболита |
зависит |
от |
||||
там также не влияет на глюкурониро+ |
клиренса креатинина. В связи с этим |
|||||||
вание вальпроевой кислоты in vitro. |
у пациентов со средней и тяжелой |
|||||||
В культуре гепатоцитов человека ле+ |
степенью почечной недостаточности |
|||||||
ветирацетам оказывал слабое влия+ |
рекомендуется корректировать под+ |
|||||||
ние или не влиял на активность изо+ |
держивающую дозу препарата в зави+ |
|||||||
ферментов |
CYP1A2, |
SULT1E1 и |
симости от клиренса креатинина. У |
|||||
UGT1A1. |
|
|
|
взрослых пациентов с терминальной |
||||
Леветирацетам слабо индуцировал |
почечной недостаточностью T1/2 |
со+ |
||||||
активность изоферментов CYP2B6 |
ставляет 25 ч в промежутках между |
|||||||
и CYP3A4. Данные in vitro и данные |
сеансами гемодиализа и 3,1 ч — в те+ |
|||||||
о лекарственном взаимодействии с |
чение самой процедуры. |
|
|
|||||
пероральными |
контрацептивами, |
В течение обычного 4+часового сеан+ |
||||||
дигоксином и варфарином in vivo |
са гемодиализа удаляется около 51% |
|||||||
показывают, что |
значимой индук+ |
леветирацетама. |
|
|
||||
ции ферментов in vivo не ожидается. |
Нарушение функции печени. У паци+ |
|||||||
Поэтому взаимодействие леветира+ |
ентов с легкой и средней степенью пе+ |
|||||||
цетама с другими веществами мало+ |
ченочной |
недостаточности клиренс |
||||||
вероятно. |
|
|
|
леветирацетама меняется незначите+ |
||||
Выведение. T1/2 у взрослых составляет |
льно. У большинства пациентов с тя+ |
|||||||
(7±1) ч и не зависит от дозы, пути |
желой печеночной недостаточностью |
|||||||
введения или длительности примене+ |
клиренс леветирацетама |
снижается |
||||||
ния. Средний общий клиренс состав+ |
более чем на 50%, что обусловлено со+ |
|||||||
ляет 0,96 мл/мин/кг. Основным пу+ |
путствующей почечной недостаточ+ |
|||||||
тем элиминации является выведение |
ностью. |
|
|
|
||||
с мочой (около 95% дозы, из них 93% |
Дети младше 12 лет: дети в возрасте |
|||||||
выводится в течение 48 ч). Выведе+ |
4–12 лет. После однократного прие+ |
|||||||
ние с фекалиями составляет лишь |
ма препарата в дозе 20 мг/кг T1/2 у де+ |
|||||||
0,3% дозы. Общая величина экскре+ |
тей 6–12 лет составляет 6 ч. Скоррек+ |
|||||||
ции леветирацетама и его основного |
тированный по массе тела кажущий+ |
|||||||
метаболита составляет соответствен+ |
ся клиренс на 30% превышает тако+ |
|||||||
но 66 и 24% от принятой дозы в тече+ |
вой у взрослых с эпилепсией. После |
|||||||

|
|
|
Леветинол® |
371 |
|
длительного приема препарата в дозе |
точны. В исследованиях на живот+ |
||||
20–60 мг/кг/сут абсорбция леветира+ |
ных показано наличие репродуктив+ |
||||
цетама у детей 4–12 лет быстрая. Cmax |
ной токсичности. Потенциальный |
||||
достигается в течение 0,5–1 ч. Cmax и |
риск для человека неизвестен. Леве+ |
||||
AUC носят линейный характер и про+ |
тирацетам |
рекомендуется |
приме+ |
||
порциональны дозе. Терминальный |
нять во время беременности, а также |
||||
T1/2 составляет 5 ч. Кажущийся кли+ |
у фертильных женщин, не применя+ |
||||
ренс — 1,1 мл/мин/кг. |
ющих надежные методы контрацеп+ |
||||
ПОКАЗАНИЯ. В качестве моноте+ |
ции, только при наличии веских |
||||
рапии: |
|
оснований. |
|
|
|
|
Как и в отношении других противо+ |
||||
• парциальные судороги с вторичной |
|||||
генерализацией или без нее у паци+ |
судорожных средств, физиологиче+ |
||||
ентов с 16 лет с впервые диагности+ |
ские изменения во время беременно+ |
||||
рованной эпилепсией. |
сти могут влиять на концентрацию |
||||
В качестве вспомогательной терапии |
леветирацетама. Во время беремен+ |
||||
для лечения следующих состояний: |
ности отмечается снижение плазмен+ |
||||
ной концентрации леветирацетама. |
|||||
• парциальные судороги с вторичной |
|||||
генерализацией или без нее у паци+ |
Такое снижение наиболее выражено |
||||
ентов с эпилепсией с 6 лет; |
в течение III триместра (до 60% от ба+ |
||||
зовой концентрации, наблюдавшейся |
|||||
• миоклонические судороги у паци+ |
|||||
ентов с ювенильной миоклониче+ |
до беременности). За беременными, |
||||
ской эпилепсией с 12 лет; |
принимающими леветирацетам, сле+ |
||||
дует установить надлежащее наблю+ |
|||||
• первично генерализованные тони+ |
|||||
ко+клонические судороги у пациен+ |
дение. Отмена противосудорожной |
||||
тов с идиопатической генерализо+ |
терапии может привести к обостре+ |
||||
ванной эпилепсией с 12 лет. |
нию заболевания, что может негатив+ |
||||
ным образом сказаться на состоянии |
|||||
ПРОТИВОПОКАЗАНИЯ |
|||||
матери и плода. |
|
||||
• гиперчувствительность к леветир+ |
|
||||
ацетаму или производным пирро+ |
Леветирацетам проникает в грудное |
||||
молоко. Грудное вскармливание во |
|||||
лидона, другим компонентам пре+ |
|||||
парата; |
|
время приема препарата не рекомен+ |
|||
|
дуется. Однако если терапию левети+ |
||||
• детский возраст до 6 лет (лечение |
|||||
парциальных судорог с вторичной |
рацетамом |
следует продолжить во |
|||
генерализацией или без нее у паци+ |
время грудного вскармливания, сле+ |
||||
ентов с эпилепсией); до 12 лет (ле+ |
дует соотнести ожидаемую пользу и |
||||
чение миоклонических судорог у |
возможный риск лечения и важность |
||||
пациентов с ювенильной миокло+ |
грудного вскармливания. |
|
|||
нической эпилепсией и первично |
В исследования на животных влия+ |
||||
генерализованных тонико+клони+ |
ния на фертильность не обнаружено. |
||||
ческих судорог у пациентов с идио+ |
Клинические данные отсутствуют, |
||||
патической генерализованной эпи+ |
потенциальный риск для человека не |
||||
лепсией); до 16 лет (лечение парци+ |
известен. |
|
|
||
альных судорог с вторичной генера+ |
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ. |
||||
лизацией или без нее у пациентов с |
Внутрь, запивая достаточным коли+ |
||||
впервые |
диагностированной эпи+ |
чеством воды, независимо от приема |
|||
лепсией). |
|
пищи. Суточная доза делится на два |
|||
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕН1 |
равных приема. |
|
|||
НОСТИ И КОРМЛЕНИИ ГРУДЬЮ. |
Монотерапия у взрослых и подрост. |
||||
Данные о применении леветирацета+ |
ков с 16 лет. Рекомендуемая началь+ |
||||
ма во время беременности недоста+ |
ная доза составляет 250 мг 2 раза в |
||||

372 |
Леветинол® |
|
|
|
|
Глава 2 |
||
сутки; |
дозу |
необходимо |
повысить |
Cl креатинина, мл/мин·1,73 м2 = (Cl |
||||
через 2 нед до начальной терапевти+ |
креатинина, мл/мин/ ППТ пациента, |
|||||||
ческой 500 мг 2 раза в сутки. Дозу |
м2) × 1,73. |
|
|
|||||
допускается повышать с шагом 250 |
|
|
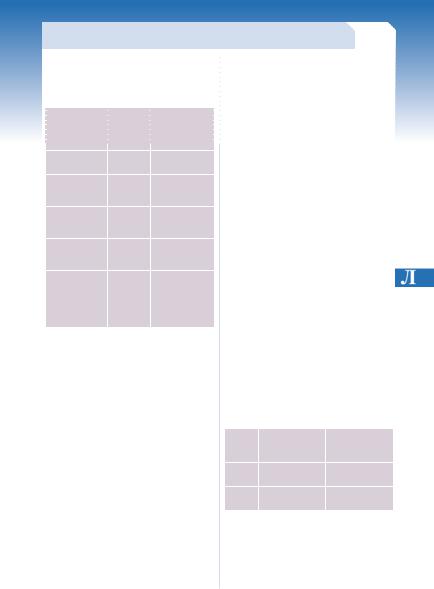
Таблица 1 |
|||||
мг 2 раза в сутки каждые 2 нед, в за+ |
|
|
||||||
Коррекция дозы у взрослых и |
||||||||
висимости от клинического ответа. |
||||||||
Максимальная доза — 1500 мг 1 раз |
подростков с нарушением функции |
|||||||
в сутки. |
|
|
|
почек, масса тела которых >50 кг |
||||
Вспомогательная терапия у взрослых |
Группа |
Cl креати |
Доза и часто |
|||||
и подростков (с 12 лет) с массой тела |
||||||||
|
нина, |
та приема |
||||||
50 кг и более |
|
|
|
|
||||
|
|
|
|
мл/мин/ |
|
|||
Начальная терапевтическая доза со+ |
|
1,73 м2 |
|
|||||
ставляет 500 мг 2 раза в сутки. Такую |
Норма |
>80 |
500–1500 мг 2 |
|||||
дозу допускается применять с 1+го |
|
|
раза в сутки |
|||||
дня лечения. |
|
|
Легкая степень нару |
50–79 |
500–1000 мг 2 |
|||
В зависимости от клинического отве+ |
шения функции почек |
|
раза в сутки |
|||||
та и переносимости суточную дозу |
Средняя степень нару |
30–49 |
250–750 мг 2 |
|||||
допускается повышать до 1500 мг 2 |
шения функции почек |
|
раза в сутки |
|||||
раза в сутки. Дозу допускается повы+ |
Тяжелая степень на |
<30 |
250–500 мг 2 |
|||||
шать или снижать на 500 мг 2 раза в |
||||||||
рушения функции по |
|
раза в сутки |
||||||
сутки каждые 2–4 нед. |
|
|
чек |
|
|
|||
Особые группы пациентов |
|
|
Терминальная стадия |
— |
500–1000 мг 1 |
|||
Пожилые (65 лет и старше). У пожи+ |
почечной недостаточ |
|
раз в сутки2 |
|||||
лых пациентов с нарушенной функ+ |
ности — пациенты, на |
|
|
|||||
ходящиеся на |
|
|
||||||
цией почек рекомендуется корректи+ |
гемодиализе1 |
|
|
|||||
ровать дозу (см. ниже «Почечная не. |
|
|
|
|||||
достаточность»). |
|
|
1 В первый день рекомендуется прием нагрузочной дозы |
|||||
Почечная недостаточность. В зави+ |
750 мг. |
|
|
|||||
2 По завершении гемодиализа рекомендуется прием до |
||||||||
симости от степени нарушения функ+ |
полнительной дозы — 250 или 500 мг. |
|
||||||
ции почек суточную дозу подбирают |
В связи с тем, что клиренс леветира+ |
|||||||
индивидуально. Чтобы воспользова+ |
цетама зависит от функции почек, де+ |
|||||||
ться таблицей коррекции дозы необ+ |
тям с почечной недостаточностью его |
|||||||
ходимо рассчитать Cl креатинина па+ |
дозу подбирают в зависимости от |
|||||||
циента в мл/мин. Его можно опреде+ |
клиренса креатинина. Настоящие ре+ |
|||||||
лить, используя величину |
сыворо+ |
комендации основаны на исследова+ |
||||||
точной |
концентрации креатинина |
ниях у взрослых пациентов. Клиренс |
||||||
(мг/дл) по следующей формуле (для |
креатинина в мл/мин/1,73 м2 у детей |
|||||||
взрослых и подростков с массой тела |
и подростков можно оценить по плаз+ |
|||||||
50 кг и более): |
|
|
менной концентрации креатинина (в |
|||||
Cl креатинина, мл/мин = (140+воз+ |
||||||||
мг/дл) по следующей формуле (фор+ |
||||||||
раст, годы) × |
масса тела, кг)/72 × кон+ |
мула Шварца): |
|
|
||||
центрация |
креатинина |
в |
плазме, |
Cl креатинина (мл/мин/1,73 м2 ) = |
||||
мг/дл. |
|
|
|
|
(рост, см × ks)/ концентрация креати+ |
|||
Для женщин получившуюся величи+ |
||||||||
нина в плазме, мг/дл, |
|
|||||||
ну следует умножить на 0,85. |
|
где ks=0,45 для детей до 1 года; 0,55 — |
||||||
Затем вводится поправка на площадь |
для детей 1–13 лет и подростков+де+ |
|||||||
поверхности тела (ППТ) следующим |
вочек; 0,7 — для подростков+мальчи+ |
|||||||
образом: |
|
|
|
ков. |
|
|
||
|
|
|
|
|
Леветинол® |
373 |
||
|
|
Таблица 2 |
ки, а также при необходимости прие+ |
|||||
Коррекция дозы у детей и |
|
ма дозы <250 мг. |
|
|
||||
|
Монотерапия |
|
|
|||||
подростков с нарушением функции |
|
|
||||||
почек, масса тела которых <50 кг |
Эффективность и безопасность леве+ |
|||||||
тирацетама у детей и подростков |
||||||||
|
|
|
|
|||||
Группа |
Cl креати |
Доза и частота |
младше 16 лет в качестве монотера+ |
|||||
пии не установлена. Данные отсутст+ |
||||||||
|
нина, |
приема |
|
|||||
|
мл/мин/ |
(с 6 лет) |
|
вуют. |
|
|
|
|
|
1,73 м2 |
|
|
Вспомогательная терапия у |
детей |
|||
Норма |
>80 |
10–30 мг/кг 2 раза |
старше 6 лет (парциальные судороги |
|||||
с вторичной генерализацией или без |
||||||||
|
|
в сутки |
|
|||||
Легкая степень |
50–79 |
10–20 мг/кг 2 раза |
нее у пациентов с эпилепсией); стар. |
|||||
ше 12 лет (миоклонические судороги у |
||||||||
нарушения функ |
|
в сутки |
|
пациентов с ювенильной миоклониче. |
||||
ции почек |
|
|
|
|||||
Средняя степень |
30–49 |
5–15 мг/кг 2 раза |
ской эпилепсией и первично генерали. |
|||||
зованные тонико.клонические судоро. |
||||||||
нарушения функ |
|
в сутки |
|
ги у пациентов с идиопатической ге. |
||||
ции почек |
|
|
|
|||||
|
|
|
нерализованной эпилепсией) и с мас. |
|||||
Тяжелая степень |
<30 |
5–10 мг/кг 2 раза |
||||||
сой тела менее 50 кг |
|
|
||||||
нарушения функ |
|
в сутки |
|
Начальная доза составляет 10 мг/кг 2 |
||||
ции почек |
|
|
|
|||||
|
|
|
раза в сутки. |
|
|
|||
стадия почечной |
— |
в сутки1,2 |
|
|
|
|||
|
В зависимости от клинического отве+ |
|||||||
Терминальная |
10–20 мг/кг 1 раз |
|
|
|
|
|||
недостаточно |
|
|
|
та и переносимости, дозу допускается |
||||
|
|
|
повышать до 30 мг/кг 2 раза в сутки. |
|||||
сти — пациенты, |
|
|
|
|||||
находящиеся1 на |
|
|
|
Дозу допускается повышать или сни+ |
||||
гемодиализе |
|
|
|
жать с шагом 10 мг/кг 2 раза в сутки |
||||
1 В первый день рекомендуется прием нагрузочной дозы |
каждые 2 нед. Необходимо приме+ |
|||||||
нять |
наименьшую |
эффективную |
||||||
15 мг/кг. |
|
|
|
дозу. Режим дозирования у детей с |
||||
2 По завершении гемодиализа рекомендуется прием до |
||||||||
полнительной дозы 5–10 мг/кг. |
|
|
массой тела 50 кг и более не отличает+ |
|||||
Нарушение функции печени. У паци+ |
ся от дозирования у взрослых. |
|
||||||
ентов с легкой и средней степенью пе+ |
|
|
Таблица 3 |
|||||
ченочной недостаточности коррек+ |
Рекомендуемые дозы у детей |
|||||||
ция дозы не требуется. У пациентов с |
||||||||
|
с 6 лет |
|
|
|||||
тяжелой печеночной |
недостаточно+ |
|
|
|
||||
|
|
|
|
|||||
стью величина клиренса креатинина |
Масса |
Начальная доза — |
Максимальная |
|||||
может вводить в заблуждение о сте+ |
||||||||
тела, кг |
10 мг/кг 2 раза в |
доза — 30 мг/кг 2 |
||||||
пени почечной недостаточности. |
|
|
сутки |
раза в сутки |
||||
Поэтому при |
Cl креатинина |
<60 |
От 25 250 мг 2 раза в су |
750 мг 2 раза в су |
||||
мл/мин/1,73 м2 следует снизить под+ |
||||||||
|
тки |
тки |
|
|||||
держивающую |
дозу |
препарата |
на |
От 501 |
500 мг 2 раза в су |
1500 мг 2 раза в |
||
50%. |
|
|
|
|||||
Дети |
|
|
|
|
тки |
сутки |
||
|
|
|
|
|
|
|
||
Препарат назначают в дозировке в за+ |
1 Режим дозирования у детей с массой тела 50 кг и более |
|||||||
висимости от возраста, массы тела и |
не отличается от дозирования у взрослых. |
|
||||||
необходимой дозы. Имеющиеся до+ |
ПОБОЧНЫЕ ДЕЙСТВИЯ. Резюме |
|||||||
зировки таблеток не предназначены |
по профилю безопасности |
|
||||||
для начального подбора дозы у детей |
Профиль нежелательных явлений, |
|||||||
с массой тела менее 25 кг, пациентам, |
представленный ниже, составлен по |
|||||||
не способным проглатывать таблет+ |
результатам анализа плацебо+конт+ |
|||||||

374 |
Леветинол® |
|
|
|
Глава 2 |
|||
ролируемых клинических исследо+ |
В плацебо+контролируемых исследо+ |
|||||||
ваний леветирацетама по всем пока+ |
ваниях профиль безопасности леве+ |
|||||||
заниям (общее количество пациен+ |
тирацетама у детей был сопоставим с |
|||||||
тов — 3416). Эти данные дополнены |
таковым у взрослых, за исключением |
|||||||
сведениями о применении левети+ |
поведенческих |
и |
психиатрических |
|||||
рацетама в рамках открытых про+ |
нежелательных реакций, которые у |
|||||||
дленных |
клинических |
исследова+ |
детей возникали чаще, чем у взрос+ |
|||||
ний, а также пострегистрационны+ |
лых. У детей в возрасте 4–16 лет рво+ |
|||||||
ми данными. Наиболее часто сооб+ |
та (очень часто — 11,2%), ажитация |
|||||||
щаемыми нежелательными реакци+ |
(часто — 3,4%), изменения настрое+ |
|||||||
ями являлись назофарингит, сонли+ |
ния (часто — 2,1%), эмоциональная |
|||||||
вость, головная боль, слабость и го+ |
лабильность (часто — 1,7%), агрессия |
|||||||
ловокружение. Профиль безопасно+ |
(часто — 8,2%), нарушение поведения |
|||||||
сти леветирацетама в целом не отли+ |
(часто — 5,6%) и летаргия (часто — |
|||||||
чается в зависимости от возраста (у |
3,9%) отмечались чаще, чем в других |
|||||||
взрослых и детей), а также не зави+ |
возрастных диапазонах. |
|
||||||
сит от одобренных показаний к при+ |
Когнитивные и |
нейропсихологиче+ |
||||||
менению |
(различных |
вариантов |
ские эффекты леветирацетама у де+ |
|||||
эпилепсии). |
|
тей 4–16 лет с парциальными судоро+ |
||||||
Данные о нежелательных реакциях |
||||||||
гами оценивались в двойных слепых |
||||||||
Нежелательные реакции, выявлен+ |
||||||||
плацебо+контролируемых исследова+ |
||||||||
ные в клинических исследованиях и в |
ниях профиля безопасности с испо+ |
|||||||
рамках пострегистрационного мони+ |
льзованием дизайна не меньшей бе+ |
|||||||
торинга (у взрослых, подростков и |
зопасности. Было показано, что леве+ |
|||||||
детей старше 1+го мес), представлены |
тирацетам не отличается (не менее |
|||||||
в таблице 4 по системно+органным |
безопасен) от плацебо по изменениям |
|||||||
классам и частоте. Градация частоты: |
от исходных значений по шкале |
|||||||
очень часто (≥1/10); часто (≥1/100 и |
«Внимание и память Лейтер+Р» (Lei. |
|||||||
<1/10); нечасто (≥1/1000 и <1/100); |
ter.R Attention and Memory), шкале |
|||||||
редко (≥1/10000 и <1/1000) и очень |
«Комплексное наблюдение за памя+ |
|||||||
редко (<1/10000). |
|
тью» (Memory Screen Composite) у па+ |
||||||
Описание отдельных нежелательных |
циентов, подвергнутых анализу |
по |
||||||
реакций |
|
|
|
протоколу. Результаты исследования |
||||
При одновременном применении то+ |
поведенческих |
и |
эмоциональных |
|||||
пирамата и леветирацетама риск раз+ |
функций, подтверждающих, что |
на |
||||||
вития анорексии возрастает. |
фоне применения |
леветирацетама |
||||||
В некоторых случаях алопеции она |
возникает агрессивное поведение, по+ |
|||||||
подвергалась обратному |
развитию |
лучены с помощью стандартизиро+ |
||||||
после отмены леветирацетама. |
ванного метода с использованием ва+ |
|||||||
Дети |
|
|
|
лидированного |
инструмента |
— |
||
В рамках плацебо+контролируемых и |
«Опросник поведения детей Ахенба+ |
|||||||
открытых продленных исследований |
ха» (Achenbach Child Behavior Check. |
|||||||
проходило лечение 645 пациентов в |
list). |
|
|
|
||||
возрасте 4–16 лет, 233 из которых по+ |
Однако у пациентов, принимавших |
|||||||
лучали леветирацетам в рамках пла+ |
леветирацетам долгосрочно, в рамках |
|||||||
цебо+контролируемых исследований. |
открытых исследований, нарушений |
|||||||
Для обоих |
возрастных |
диапазонов |
поведенческих |
и |
эмоциональных |
|||
дополнительно имеются данные по |
функций не возникало, в частности |
|||||||
пострегистрационному опыту приме+ |
уровень агрессивного поведения не |
|||||||
нения леветирацетама. |
|
отличался от исходного. |
|
|||||

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Леветинол® |
|
375 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 4 |
|
||
|
|
|
|
|
|
|
|
|
|
Системно органный |
|
|
Категория частоты |
|
|
|
|
|
класс |
Очень |
Часто |
Нечасто |
Редко |
|
|
|
|
|
|
||||||
|
|
часто |
|
|
|
|
|
|
|
Инфекции и инвазии |
Назофа |
— |
— |
Инфекции |
|
|
|
|
|
|
||||||
|
Со стороны крови и |
рингит |
|
Тромбоцитопения, |
Панцитопения1,2, |
|
||
|
— |
|
|
|||||
|
лимфатической систе |
|
|
лейкопения1 |
нейтропения1 |
|
|
|
|
|
|
|
|
||||
|
мы |
|
|
|
|
|
|
|
|
Нарушения метабо |
— |
Анорексия |
Снижение1 или повышение |
— |
|
|
|
|
лизма и питания |
|
|
массы тела |
|
|
|
|
|
Психические наруше |
— |
Депрессия, враж |
Суицидальные попытки1,суи |
Состоявшийся |
|
|
|
|
ния |
|
дебность или |
цидальные мысли1, психоти |
суицид1, расстрой |
|
||
|
|
|
1 |
ческие расстройства, нару |
ство личности, нару |
|
||
|
|
|
агрессия , наруше |
|
||||
|
|
|
ние сна, нервоз |
шение поведения1, галлюци |
шение мышления |
|
||
|
|
|
ность, раздражи |
нации, озлобление, спутан |
|
|
|
|
|
|
|
тельность |
ность сознания,эмоциональ |
|
|
|
|
|
|
|
|
ная лабильность, изменения |
|
|
|
|
|
|
|
|
настроения, ажитация |
|
|
|
|
|
Со стороны нервной |
Сонли |
Судороги, наруше |
Амнезия, нарушение памяти, |
Хореоатетоз1, дис |
|
||
|
системы |
вость, |
ние равновесия, |
нарушение координации дви |
кинезия, гиперкине |
|
||
|
|
голов |
головокружение, |
жений или атаксия, |
зия |
|
|
|
|
|
ная |
летаргия, тремор |
парестезия1, расстройство |
|
|
|
|
|
|
боль |
|
внимания |
|
|
|
|
|
Со стороны органа |
— |
— |
Диплопия, нарушение зрения |
— |
|
|
|
|
зрения |
|
|
|
|
|
|
|
|
Со стороны органа |
— |
Вертиго |
— |
— |
|
|
|
|
слуха и равновесия |
|
|
|
|
|
|
|
|
Со стороны дыхатель |
— |
Кашель |
— |
— |
|
|
|
|
ной системы, органов |
|
|
|
|
|
|
|
|
грудной клетки и сре |
|
|
|
|
|
|
|
|
достения |
|
|
|
|
|
|
|
|
Со стороны ЖКТ |
— |
Боли в животе, |
— |
Панкреатит1 |
|
|
|
|
|
|
диарея, диспепсия, |
|
|
|
|
|
|
|
|
рвота, тошнота |
|
|
|
|
|
|
Со стороны печени и |
— |
— |
Нарушение функциональных |
Печеночная недос |
|
||
|
желчевыводящих пу |
|
|
проб печени1 |
таточность, гепатит1 |
|
||
|
тей |
|
|
|
|
|
|
|
|
Со стороны кожи и |
— |
Сыпь |
Алопеция1, экзема, зуд |
Токсический эпи |
|
||
|
подкожных тканей |
|
|
|
дермальный |
|
|
|
|
|
|
|
|
некролиз1, синдром |
|
||
|
|
|
|
|
Стивенса Джонсона, |
|
||
|
|
|
|
|
многоформная |
|
||
|
|
|
|
|
эритема1 |
|
|
|
|
Со стороны мышеч |
— |
— |
Мышечная слабость, миалгия |
— |
|
|
|
|
но скелетной и соеди |
|
|
|
|
|
|
|
|
нительной ткани |
|
|
|
|
|
|
|
|
Общие расстройства и |
— |
Астения или утом |
— |
— |
|
|
|
|
расстройства в месте |
|
ляемость |
|
|
|
|
|
|
введения |
|
|
|
|
|
|
|
|
Травмы, отравления и |
— |
— |
Травма |
— |
|
|
|
|
осложнения процедур |
|
|
|
|
|
|
|
1 Нежелательные реакции, выявленные в пострегистрационном периоде.
2 В некоторых случаях установлено угнетение костномозгового кроветворения.

376 |
Леветинол® |
|
|
|
|
|
|
|
Глава 2 |
|||
ВЗАИМОДЕЙСТВИЕ. |
Противосу. |
макокинетику пероральных контра+ |
||||||||||
дорожные средства |
|
|
|
цептивов (этинилэстрадиол и лево+ |
||||||||
Согласно предрегистрационным кли+ |
норгестрел); |
гормональный |
статус |
|||||||||
ническим исследованиям, леветира+ |
(содержание ЛГ и прогестерона) не |
|||||||||||
цетам не влияет на сывороточные |
изменялся. |
Леветирацетам |
в дозе |
|||||||||
концентрации |
других |
противосудо+ |
2000 мг/сут не оказывал влияние на |
|||||||||
рожных средств; фенитоина, карба+ |
фармакокинетику дигоксина и вар+ |
|||||||||||
мазепина, вальпроевой кислоты, фе+ |
фарина, ПВ не изменялось. Одновре+ |
|||||||||||
нобарбитала, |
ламотриджина, |
габа+ |
менное применение дигоксина, перо+ |
|||||||||
пентина и примидона — а эти проти+ |
ральных контрацептивов и варфари+ |
|||||||||||
восудорожные средства не влияют на |
на не оказывало влияние на фармако+ |
|||||||||||
фармакокинетику леветирацетама. |
кинетику леветирацетама. |
|
||||||||||
Аналогично взрослым, у детей в до+ |
Антациды. Данные о влиянии анта+ |
|||||||||||
зах до 60 мг/кг/сут леветирацетам не |
цидов на абсорбцию леветирацетама |
|||||||||||
взаимодействует с другими ЛС. Рет+ |
отсутствуют. |
|
|
|
|
|||||||
роспективная оценка фармакокине+ |
Пища и алкоголь. Пища не влияет на |
|||||||||||
тических взаимодействий у детей и |
степень |
абсорбции |
леветирацетама, |
|||||||||
подростков с эпилепсией (4–17 лет) |
но несколько снижает ее скорость. |
|||||||||||
подтверждает, |
что |
леветирацетам в |
Данные о взаимодействии леветира+ |
|||||||||
качестве вспомогательной терапии не |
цетама с этанолом отсутствуют. |
|||||||||||
влияет на сывороточные Css одновре+ |
ПЕРЕДОЗИРОВКА. |
Симптомы: |
||||||||||
менно применяемых карбамазепина |
||||||||||||
сонливость, ажитация, агрессия, угне+ |
||||||||||||
и вальпроевой кислоты. Однако име+ |
тение сознания, угнетение дыхания и |
|||||||||||
ются данные, что клиренс леветира+ |
кома. |
|
|
|
|
|
||||||
цетама у детей, принимающих проти+ |
Лечение: после острой передозиров+ |
|||||||||||
восудорожные средства — индукторы |
ки — промывание желудка или ин+ |
|||||||||||
микросомальных |
ферментов |
пече+ |
дукция рвоты. Антидот леветираце+ |
|||||||||
ни, — повышается на 20%. Коррекция |
тама не найден. Лечение — симптома+ |
|||||||||||
дозы не требуется. |
|
|
|
тическое, может включать примене+ |
||||||||
Пробенецид. Пробенецид (по 500 мг 4 |
||||||||||||
ние гемодиализа. |
Диализирующая |
|||||||||||
раза в сутки) является блокатором ка+ |
активность в отношении леветираце+ |
|||||||||||
нальцевой секреции в почках, показа+ |
тама равна 60%, в отношении основ+ |
|||||||||||
но, что он ингибирует почечный кли+ |
ного метаболита — 74%. |
|
||||||||||
ренс основного метаболита, но не ле+ |
ОСОБЫЕ УКАЗАНИЯ. Отмена те. |
|||||||||||
ветирацетама. Тем не менее, концент+ |
||||||||||||
рация основного метаболита остается |
рапии |
|
|
|
|
|
||||||
низкой. Ожидается, что другие ЛС, |
Отмену |
препарата |
|
рекомендуется |
||||||||
экскретирующиеся |
посредством ак+ |
проводить постепенно. Например, у |
||||||||||
тивной канальцевой секреции, могут |
взрослых и подростков с массой тела |
|||||||||||
снижать почечный клиренс основного |
более 50 кг: снижение дозы должно |
|||||||||||
метаболита. Влияние леветирацетама |
осуществляться с шагом 500 мг 2 раза |
|||||||||||
на пробенецид не изучалось; влияние |
в сутки не чаще чем каждые 2–4 нед; у |
|||||||||||
леветирацетама на другие лекарствен+ |
детей с 6 лет с массой тела менее 50 кг: |
|||||||||||
ные |
препараты, экскретирующиеся |
снижение дозы должно осуществля+ |
||||||||||
путем активной канальцевой секре+ |
ться с шагом не более 10 мг/кг 2 раза в |
|||||||||||
ции, включая НПВС, сульфонамид и |
сутки не чаще чем каждые 2 нед. |
|||||||||||
метотрексат, неизвестно. |
|
Почечная недостаточность |
|
|||||||||
Пероральные контрацептивы и про. |
Применение леветирацетама у паци+ |
|||||||||||
чие фармакокинетические взаимодей. |
ентов с почечной недостаточностью |
|||||||||||
ствия. Леветирацетам в дозе 1000 |
может потребовать коррекции дозы. |
|||||||||||
мг/сут не оказывал влияние на фар+ |
У пациентов с тяжелой печеночной |
|||||||||||

|
|
|
Лейкопластырь... |
377 |
||
недостаточностью |
рекомендуется |
при управлении транспортными сред+ |
||||
оценивать функцию почек до начала |
ствами и занятии другими видами де+ |
|||||
подбора дозы (см. «Способ примене+ |
ятельности, требующими |
повышен+ |
||||
ния и дозы»). |
|
|
ной концентрации внимания и быст+ |
|||
Суицид |
|
|
роты психомоторных реакций. При |
|||
У пациентов, принимавших противо+ |
возникновении указанных симптомов |
|||||
судорожные средства (включая леве+ |
пациентам следует отказаться от та+ |
|||||
тирацетам), отмечались суицид, по+ |
ких видов деятельности, пока они не |
|||||
пытки суицида, суицидальные мысли |
убедятся, что указанные симптомы не |
|||||
и поведение. |
|
|
оказывают на них значимое влияние. |
|||
Мета+анализ |
рандомизированных |
ФОРМА ВЫПУСКА. Таблетки, по. |
||||
плацебо+контролируемых исследова+ |
крытые пленочной оболочкой, 250 мг, |
|||||
ний противосудорожных ЛС показал |
500 мг, 750 мг, 1000 мг. По 10 табл. в |
|||||
небольшое повышение риска суици+ |
контурной ячейковой упаковке (блис+ |
|||||
дальных мыслей и поведения. Меха+ |
тере) из пленки ПВХ и фольги алю+ |
|||||
низм его реализации неизвестен. |
миниевой. По 3 или 6 блистеров в пач+ |
|||||
В связи с вышеизложенным, необхо+ |
ке картонной. |
|
|
|||
димо осуществлять наблюдение за |
По 30 или по 60 табл. в банке поли+ |
|||||
пациентами с симптомами депрессии |
мерной для ЛС, каждую банку поме+ |
|||||
или суицидальными мыслями и/или |
щают в пачку картонную. |
|
|
|||
поведением и назначать им соответ+ |
УСЛОВИЯ ОТПУСКА ИЗ АПТЕК. |
|||||
ствующую терапию. Пациентов (и |
По рецепту. |
|
|
|||
лиц, ухаживающих за ними) следует |
Леветирацетам* |
|
|
|||
проинформировать о необходимости |
|
|
||||
обращения за медицинской помощью |
37 (Levetiracetam*) |
|
|
|||
при возникновении у них симптомов |
|
|
||||
депрессии и/или суицидальных мыс+ |
Синонимы |
|
|
|||
лей и поведения. |
|
Леветинол®: табл. п.п.о. |
|
|
||
Дети |
|
|
(ГЕРОФАРМ). . . . . . . . . . . . . . . . . . . . . 367 |
|||
Таблетки имеют возрастные ограни+ |
Эпитерра: табл. п.п.о. |
|
|
|||
чения по применению в детском воз+ |
(Teva). . . . . . . . . . . . . . . . . . . . . |
. . . . . . 717 |
||||
расте (см. «Показания»). По имею+ |
ЛЕЙКОПЛАСТЫРЬ МЕДИ1 |
|||||
щимся данным |
|
леветирацетам не |
||||
влияет на рост и половое созревание. |
ЦИНСКИЙ ДОРСАПЛАСТ |
|
||||
Однако долгосрочное влияние на |
(DORSAPLAST) |
|
|
|||
обучение, интеллект, рост, эндокрин+ |
ООО «НаноТек Фарма» (Россия) |
|||||
ную функцию, половое созревание и |
||||||
фертильность детей неизвестно. |
СОСТАВ |
|
|
|||
Влияние на способность управлять |
|
|
||||
Лейкопластырь медицин1 |
|
|||||
транспортными |
средствами, рабо. |
ский . . . . . . . . . . . . . . . . . . . . . 1 шт. |
||||
тать с механизмами. Исследования о |
высококачественный |
мельчай+ |
||||
влиянии на способность управлять |
||||||
ший порошок, продуцирующий |
||||||
транспортными |
средствами и рабо+ |
|||||
излучение в далекой инфракрас+ |
||||||
тать с механизмами не проводились. |
||||||
ной области спектра, магнитный |
||||||
Вследствие индивидуальных разли+ |
||||||
порошок из редкоземельных ме+ |
||||||
чий восприимчивости у некоторых |
||||||
пациентов могут |
возникать сонли+ |
таллов |
|
|
||
вость и другие нарушения со стороны |
ДЕЙСТВИЕ НА ОРГАНИЗМ. Плас+ |
|||||
ЦНС, особенно в начале терапии и по+ |
тырь обладает обезболивающим, про+ |
|||||
сле повышения дозы. Поэтому реко+ |
тивовоспалительным и мышечнорас+ |
|||||
мендуется соблюдать осторожность |
слабляющим действиями, способству+ |
|||||

378 |
Лейкопластырь... |
|
|
|
|
Глава 2 |
|||
|
|
|
|
|
вокружения, |
нарушения чувствите+ |
|||
|
|
|
|
|
льности верхних конечностей; |
||||
|
|
|
|
|
+ грудной остеохондроз; |
|
|||
|
|
|
|
|
+ межреберная невралгия; |
|
|||
|
|
|
|
|
+ поясничный остеохондроз, люмба+ |
||||
|
|
|
|
|
го, ишиас; |
|
|
||
|
|
|
|
|
+ шейно+плечевой, грудной, пояснич+ |
||||
|
|
|
|
|
но+крестцовый радикулит; |
|
|||
|
|
|
|
|
+ заболевания позвоночника, сопро+ |
||||
|
|
|
|
|
вождающиеся локальным |
болевым |
|||
|
|
|
|
|
синдромом; |
|
|
||
|
|
|
|
|
+ боли в шее, спине, поясничной обла+ |
||||
|
|
|
|
|
сти на фоне остеохондроза и ущемле+ |
||||
|
|
|
|
|
ния нервов; |
|
|
||
|
|
|
|
|
+ спондилоартрозы; |
|
|||
|
|
|
|
|
+ |
артриты (остеоартриты), артрозы |
|||
|
|
|
|
|
(остеоартрозы) крупных суставов, в |
||||
|
|
|
|
|
т.ч. коленного, тазобедренного и пле+ |
||||
|
|
|
|
|
чевого суставов; |
|
|||
|
|
|
|
|
+ закрытые травмы мягких тканей — |
||||
|
|
|
|
|
ушибы, растяжения мышц и связок, |
||||
ет восстановлению функции опор+ |
вправленные вывихи суставов, кож+ |
||||||||
ные гематомы и кровоподтеки; |
|||||||||
но+двигательного аппарата (суставов, |
+ спортивные травмы. |
|
|||||||
мышц и связок), в т.ч. позвоночника, а |
ПРОТИВОПОКАЗАНИЯ |
|
|||||||
такжеболеебыстромувосстановлению |
• |
беременность; |
|
||||||
и уменьшению последствий закрытых |
• |
нарушение |
целостности |
кожных |
|||||
травм мягких тканей, опорно+двигате+ |
|
покровов. |
|
|
|||||
льного аппарата (ушибов, растяжений |
|
|
|
||||||
С осторожностью: повышенная чув+ |
|||||||||
связок и мышц, вывихов суставов, кро+ |
|||||||||
воподтеков и кожных гематом). |
|
ствительность. |
|
||||||
|
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ. |
||||||||
СВОЙСТВА КОМПОНЕНТОВ. Со+ |
|||||||||
четанное воздействие инфракрасного |
Наружно. |
|
|
||||||
Пластырь не требует предваритель+ |
|||||||||
(теплового) излучения и магнитного |
|||||||||
поля приводит к улучшению местно+ |
ной обработки. |
|
|||||||
го (локального) крово+ и лимфообра+ |
Снять защитный слой. Зафиксиро+ |
||||||||
щения, уменьшению застоя крови и |
вать пластырь на сухом участке кожи |
||||||||
в беспокоящей области. |
|
||||||||
улучшению венозного оттока, умень+ |
|
||||||||
шению |
|
воспалительной |
реакции |
Пластырь одноразовый. Не подлежит |
|||||
(отека, боли). Улучшает местный ме+ |
повторному |
использованию. Не |
|||||||
таболизм, |
расслабляет |
мышцы |
и |
оставляет следов на коже и одежде, |
|||||
связки. Способствует восстановле+ |
снимается легко и безболезненно, |
||||||||
нию функции опорно+двигательного |
фиксирующий материал имеет телес+ |
||||||||
аппарата, |
уменьшению |
гематом |
и |
ный цвет. |
|
|
|||
кровоподтеков при травмах мягких |
Использование пластыря |
удобно и |
|||||||
тканей и суставов. |
|
|
комфортно, не ограничивает движе+ |
||||||
|
|
ния, не меняет привычный образ жиз+ |
|||||||
РЕКОМЕНДУЕТСЯ. При следую+ |
|||||||||
ни. Для удобства применения, в зави+ |
|||||||||
щих состояниях и заболеваниях: |
|
симости от |
локализации |
беспокоя+ |
|||||
+ шейный остеохондроз, в т.ч. его про+ |
щей области, выпускается пластырь |
||||||||
явления в виде головной боли, голо+ |
двух размеров: 9×12 и 12×18 см. |
||||||||
