
6 курс / Нефрология / Хронический_пиелонефрит_в_детском_возрасте
.pdf101
Таблица 23
Показатели фагоцитоза и уровни цитокинов в сыворотке крови у группы больных первичным хроническим пиелонефритом, получавших общепринятую терапию, и у группы больных первичным хроническим пиелонефритом, получавших лечение в сочетании с полиоксидонием (М±m)
|
|
|
Больные хроническим пиелонефритом: |
|
|
|
|
стадия частичной клинико-лаборатор- |
стадия полной клинико-лабораторной |
||
Показатели |
Здоровые дети, |
ной ремиссии |
ремиссии |
||
|
получавшие лече- |
|
получавшие лече- |
||
n = 183 |
получавшие об- |
получавшие об- |
|||
|
|
щепринятую тера- |
ние в сочетании с |
щепринятую тера- |
ние в сочетании с |
|
|
пию, n = 43 |
полиоксидонием, |
пию, n = 43 |
полиоксидонием, |
|
|
n = 30 |
n = 30 |
||
|
|
|
|
||
ФАН,% |
69,17±1,24 |
57,95±1,83* |
66,27±2,72 |
62,35±1,62* |
72,02±2,28 |
ФИ |
10,67±0,18 |
8,67±0,21* |
9,65±0,36 |
9,37±0,20* |
11,02±0,32 |
НСТ-тест,% |
19,17±0,75 |
13,72±0,37* |
17,38±0,29* |
16,09±0,62* |
18,02±0,32 |
ИФН-α, пкг/мл |
1,83±0,08 |
0,81±0,18* |
1,42±0,33 |
1,29±0,20* |
1,76±0,22 |
ИЛ-1β, пкг/мл |
1,60±0,11 |
40,02±3,06* |
7,82±2,10* |
13,25±2,87* |
3,33±0,68* |
ФНО-α, пкг/мл |
0,50±0,10 |
10,77±2,87* |
4,25±1,22* |
9,26±2,96* |
0,72±0,20 |
|
|
|
|
|
|
Примечание: «*» - р<0,05-0,001 по сравнению с показателями у здоровых детей.
102
казателей ФАН (р<0,001, p<0,01), ФИ (р<0,001, p<0,001) и НСТ-теста (р< 0,001, p<0,01), снижение уровня ИФН-α (р<0,001, p<0,01), значительное повышение уровней ИЛ-1β (р<0,001, p<0,001) и ФНО-α (р<0,001, p<0,01) в сы-
воротке крови. У второй группы больных хроническим пиелонефритом, получавших комплексное лечение в сочетании с полиоксидонием (таблица 23), в стадии частичной клинико-лабораторной ремиссии отмечалось сравнительно небольшое понижение значений НСТ-теста (р<0,05), повышение уровней ИЛ-1β (р<0,01) и ФНО-α (р<0,01) в сыворотке крови, а в периоде полной клинико-лабораторной ремиссии – только небольшое повышение уровня ИЛ1β (р<0,02) в сыворотке крови.
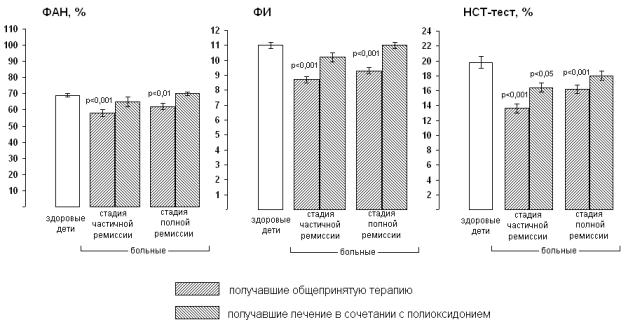
Сдвиги показателей фагоцитоза и уровней цитокинов в сыворотке крови у первой группы больных хроническим пиелонефритом, получавших комплексную общепринятую терапию, и у второй группы больных хроническим пиелонефритом, получавших комплексное лечение в сочетании с полиоксидонием, отражены на рисунках 17 и 18.
Рисунок 17. Показатели фагоцитоза у первой и второй групп больных первичным хроническим пиелонефритом
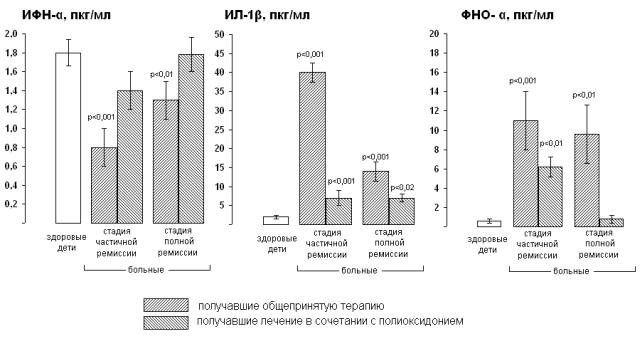
103
Рисунок 18. Уровни цитокинов в сыворотке крови у первой и второй групп больных первичным хроническим пиелонефритом
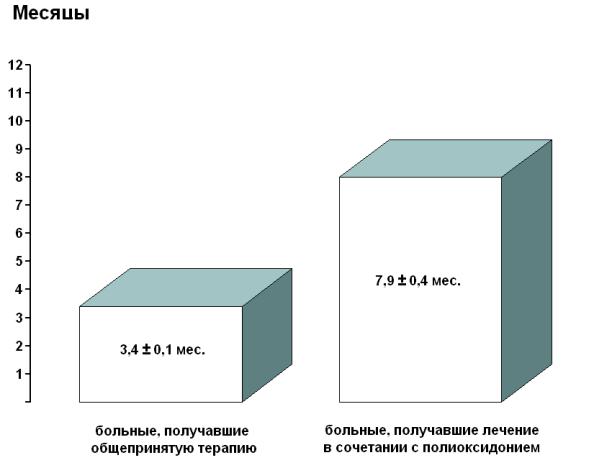
Катамнестическое наблюдение больных первичным хроническим пиелонефритом осуществлялось в течение 1 года. В ходе наблюдения было установлено, что у первой группы больных хроническим пиелонефритом, получавших комплексную общепринятую терапию, продолжительность полной клинико-лабораторной ремиссии составляла 3-4 месяца (в среднем 3,4±0,1 месяца), рецидивы заболевания у пациентов этой группы возникали вследствие острой респираторной инфекции. Продолжительность полной клиниколабораторной ремиссии у второй группы больных хроническим пиелонефритом, получивших во время пребывания в стационаре основной курс инъекций полиоксидония, а также повторный курс лечения полиоксидонием через три месяца после выписки, составляла 6-11 месяцев (в среднем 7,9±0,4 месяца). Таким образом, проведение комплексного лечения в сочетании с двумя курсами инъекций полиоксидония у второй группы детей с рецидивирующим течением первичного хронического пиелонефрита обеспечивало значительное увеличение продолжительности полной клинико-лабораторной ремиссии, которая превышала в два раза (р<0,001) продолжительность полной клинико-лабораторной ремиссии у первой группы детей с рецидивирующим течением первичного хронического пиелонефрита, получавших комплексную общепринятую терапию (рисунок 19).
104
Рисунок 19. Продолжительность клинико-лабораторной ремиссии у первой и второй групп больных первичным хроническим пиелонефритом
Неоднозначные изменения показателей иммунологической реактивности были получены нами и при сопоставлении результатов исследований у наблюдаемых групп детей с вторичным обструктивным хроническим пиелонефритом. Первая группа больных (возраст – 8-15 лет) обструктивным хроническим пиелонефритом (72 пациента) подвергалась во время пребывания в стационаре реконструктивным операциям в сочетании с комплексной консервативной терапией, после выписки из стационара они продолжали получать противорецидивное лечение. Второй группе больных (возраст – 8-15 лет) обструктивным хроническим пиелонефритом (40 пациентов) в раннем послеоперационном периоде на стационарном этапе лечения проводился курс инъекций имунофана (0,005% раствор из расчёта 0,1 мл на год жизни (не более 1,0 мл), подкожно, через два дня на третий, всего – 5 инъекций). Никаких осложнений и побочных реакций у пациентов, получавших лечение имунофаном, не возникало.
105
Исследования показали, что у первой группы больных обструктивным хроническим пиелонефритом, получавших комплексную общепринятую терапию (таблица 24), перед выпиской из стационара и через три месяца после выписки выявлялось уменьшение относительного количества CD3-лим-
фоцитов (р<0,001, р<0,001), СD4-лимфоцитов (р< 0,001, p<0,001) и выражен-
ное увеличение относительного (p<0,001, p<0,001) и абсолютного (p<0,001, p<0,001) количества CD20-лимфоцитов в крови. У второй группы больных обструктивным пиелонефритом, получавших комплексное лечение в сочетании с имунофаном (таблица 24), перед выпиской из стационара и через три месяца после выписки регистрировалось увеличение относительного (р< 0,001, p<0,001) и абсолютного (р<0,001, p<0,001) количества CD3-лимфо-
цитов, а также увеличение относительного (р<0,001, p<0,001) и абсолютного (р<0,001, p<0,001) количества CD20-лимфоцитов при отсутствии существенных сдвигов содержания CD4- и CD8-лимфоцитов в крови.
Перед выпиской из стационара и через три месяца после выписки у первой группы больных обструктивным хроническим пиелонефритом, получавших комплексную общепринятую терапию (таблица 24), констатирова-
лось выраженное повышение уровней IgG (p<0,001, p<0,001), IgA (p<0,001, p<0,05), IgM (p<0,001, p<0,001) и концентрации ЦИК (р<0,001, p<0,05) в сы-
воротке крови. У второй группы больных обструктивным хроническим пиелонефритом, получавших комплексное лечение в сочетании с имунофаном (таблица 24), перед выпиской из стационара и через три месяца после выписки тоже отмечалось, хотя и менее выраженное по сравнению с пациентами первой группы, повышение уровней IgA (p<0,001) и IgM (p< 0,001, 0,001), но отсутствовало повышение уровня IgG и концентрации ЦИК в сыворотке крови.
Упервой группы больных обструктивным хроническим пиелонефритом, получавших комплексную общепринятую терапию (таблица 25), перед выпиской из стационара и через три месяца после выписки регистрировалось значительное снижение показателей ФАН (р<0,001, p<0,001), ФИ (р<0,001, p<0,001) и НСТ-теста (p<0,001, p<0,001). Значительное повышение показателей фагоцитоза констатировалось перед выпиской из стационара и у второй группы больных обструктивным хроническим пиелонефритом (таблица 25), получавших комплексное лечение в сочетании с имунофаном, однако через три месяца после выписки у них выявлялось только повышение показателей ФАН (р<0,001) и НСТ-теста (p<0,001) при отсутствии достоверных изменений показателя ФИ.
Уобеих групп больных обструктивным хроническим пиелонефритом через три месяца после выписки из стационара (таблица 25) отмечалось рез-
106
Таблица 24 Показатели клеточного и гуморального звеньев иммунитета у группы больных обструктивным хроническим пиелонефритом, получавших общепринятую терапию, и у группы больных обструктивным хроническим
пиелонефритом, получавших лечение в сочетании с имунофаном (M±m)
|
|
|
Больные хроническим пиелонефритом: |
|
|
|
Здоровые дети, |
перед выпиской из стационара |
через три месяца после выписки |
||
Показатели |
получавшие об- |
получавшие лече- |
получавшие об- |
получавшие лече- |
|
n = 301 |
ние в сочетании с |
ние в сочетании с |
|||
|
|
щепринятую тера- |
имунофаном, |
щепринятую тера- |
имунофаном, |
|
|
пию, n = 72 |
пию, n = 72 |
||
|
|
n = 40 |
n = 40 |
||
|
|
|
|
||
CD3-лимф.% |
64,10±1,25 |
56,93±0,58* |
74,68±0,57* |
57,16±0,56* |
68,45±0,73* |
CD3-лимф.,109/л |
1,04±0,07 |
1,14±0,03 |
1,52±0,03* |
0,92±0,01 |
1,18±0,02* |
CD4-лимф.% |
49,20±1,32 |
43,25±0,42* |
46,90±0,38* |
43,57±0,43* |
49,17±0,44 |
CD4-лимф.,109/л |
0,59±0,02 |
0,56±0,03 |
0,58±0,02 |
0,56±0,03 |
0,58±0,02 |
CD8-лимф.,% |
25,47±0,96 |
24,05±0,32 |
25,50±0,76 |
23,63±0,30* |
25,12±0,67 |
CD8-лимф.,109/л |
0,31±0,01 |
0,32±0,02 |
0,34±0,01 |
0,27±0,03 |
0,33±0,01 |
СD20-лимф.,% |
9,90±0,77 |
20,10±0,42* |
12,07±0,75* |
20,80±0,39* |
13,40±0,17* |
CD20-лимф.,109/л |
0,17±0,02 |
0,54±0,02* |
0,31±0,02* |
0,57±0,03* |
0,26±0,01* |
IgG,г/л |
9,71±0,15 |
12,01±0,22* |
11,51±0,27* |
11,98±0,14* |
10,11±0,28 |
IgA,г/л |
1,21±0,05 |
1,69±0,04* |
1,55±0,12* |
1,36±0,04* |
1,43±0,09* |
IgM,г/л |
1,22±0,06 |
2,20±0,18* |
1,89±0,06* |
1,79±0,12* |
1,41±0,05* |
ЦИК,ед.опт.пл. |
0,075±0,003 |
0,093±0,002* |
0,071±0,002 |
0,083±0,002* |
0,070±0,002 |
Примечание: «*» - р<0,05-0,001 по сравнению с показателями у здоровых детей.
107
Таблица 25
Показатели фагоцитоза и уровни цитокинов в сыворотке крови у группы больных обструктивным хроническим пиелонефритом, получавших общепринятую терапию, и у группы больных обструктивным хроническим пиелонефритом, получавших лечение в сочетании с имунофаном (М±m)
|
|
|
Больные хроническим пиелонефритом: |
|
|
|
Здоровые дети, |
перед выпиской из стационара |
через три месяца после выписки |
||
Показатели |
получавшие об- |
получавшие лече- |
получавшие об- |
получавшие лече- |
|
|
n = 301 |
щепринятую тера- |
ние в сочетании с |
щепринятую тера- |
ние в сочетании с |
|
|
имунофаном, |
имунофаном, |
||
|
|
пию, n = 72 |
пию, n = 72 |
||
|
|
n = 40 |
n = 40 |
||
|
|
|
|
||
ФАН,% |
69,17±1,24 |
53,73±0,78* |
57,40±0,69* |
57,05±0,69* |
60,63±0,53* |
ФИ |
10,67±0,18 |
7,96±0,12* |
8,90±0,18* |
8,47±0,10* |
10,05±0,07 |
НСТ-тест,% |
19,17±0,75 |
14,06±0,20* |
15,48±1,06* |
13,78±0,18* |
16,13±0,33* |
ИФН-α, пкг/мл |
1,83±0,08 |
- |
- |
<1 |
<1 |
ИЛ-1β, пкг/мл |
1,60±0,11 |
- |
- |
22,28±1,03* |
3,34±0,26* |
ФНО-α, пкг/мл |
0,50±0,10 |
- |
- |
1,67±0,78* |
1,47±0,15* |
|
|
|
|
|
|
Примечание: «*» - р<0,05-0,001 по сравнению с показателями у здоровых детей.
108
ко выраженное снижение уровня ИФН-α в сыворотке крови. Вместе с тем, у первой группы больных обструктивным хроническим пиелонефритом, получавших комплексную общепринятую терапию (таблица 25), через три месяца после выписки из стационара констатировалось резко выраженное повышение уровней ИЛ-1β (р<0,001) и ФНО-α (p<0,001) в сыворотке крови, тогда как у второй группы больных обструктивным хроническим пиелонефритом, получавших комплексное лечение в сочетании с имунофаном (таблица 25), отмечалось сравнительно небольшое повышение (р<0,001, p<0,001) уровней провоспалительных цитокинов в сыворотке крови.
Представленные выше результаты собственных исследований свидетельствуют о том, что включение полиоксидония в комплексное лечение больных первичным хроническим пиелонефритом обеспечивало нормализацию большинства показателей иммунитета и значительное увеличению продолжительности клинической ремиссии, а проведение комплексного лечения с включением имунофана больных обструктивным хроническим пиелонефритом приводило к значительному улучшению состояния иммунологической реактивности.
Коррекция дисбиоза кишечника и системная энзимотерапия
Длительная и повторная антибиотикотерапия при хроническом пиелонефрите оказывает существенное влияние на микробиоценоз кишечника. Поддержание нормального микробиоценоза кишечника, с учётом возможного лимфогенного пути распространения инфекции, является профилактикой рецидивирования микробно-воспалительного процесса в почках и мочевыводящих путях. Коррекция дисбиоза кишечника заключается в организации функционального питания и медикаментозном лечении (Коровина Н.А. с со-
авт., 2007).
Функциональное питание предусматривает систематическое употребление больными хроническим пиелонефритом продуктов естественного происхождения, оказывающих регулирующее влияние на организм. К основным компонентам функционального питания относятся: пищевые волокна (морковь, свёкла, яблочное пюре и др.), олигосахариды (пребиотики), стимулирующие рост нормальной микрофлоры кишечника (бананы и др.), продукты, содержащие живые микроорганизмы (кефир, биокефир, бифилок, Наринэ).
Медикаментозная коррекция дисбиоза кишечника у больных хрониче-
ским пиелонефритом предусматривает элиминацию условно-патогенной (УПФ) и патогенной флоры (ПФ) с последующим восстановлением микро-
109
флоры кишечника с помощью пробиотиков. Элиминация УПФ и ПФ кишечника осуществляется путём применения монокомпетентных и комбинированных бактериофагов (бактериофаги назначаются при упорном высеве однотипного возбудителя из мочи и кала, при стойкой изолированной бактериурии), «биологических нормализаторов» сапрофитной флоры (бактисубтил, споробактерин, биоспорин, энтерол), микробов-антагонистов (препараты на основе лактобактерий – линекс, аципол, биобактон и др.), иммунокорректоров (виферон, ликопид и др.).
После элиминации УПФ и ПФ кишечника больным хроническим пие-
лонефритом назначаются препараты на основе бифидобактерий (бифидум-
бактерин, бифидумбактерин-форте и др.).
В последние годы появились сообщения об использовании полиэнзимных препаратов в комплексном лечении детей с хроническим пиелонефритом Известно, что эти лекарственные средства (вобэнзим, флогэнзим и др.) ограничивают воспалительный процесс и снижают его активность, модулируют физиологические защитные реакции организма.
Исследования показали (Папаян А.В. с соавт., 2001), что вобэнзим хорошо переносится детьми с хроническим пиелонефритом и хорошо сочетается с различными лекарственными средствами. Доза вобэнзима, используемая в комплексной терапии детей с пиелонефритом в активной стадии заболевания, составляет 1 таблетку на 6 кг массы тела в сутки на весь курс антибиотикотерапии. В период частичной и полной клинико-лабораторной ремиссии доза вобэнзима составляет половину от лечебной дозы; в такой дозе препарата назначается в течение 1-1,5-2 месяцев. Установлено, что на фоне лечения вобэнзимом набюдается более быстрое снижение клинико-лабораторной активности, максимальный эффект комплексной терапии с включением вобэнзима у детей с пиелонефритом отмечается через 3-5 недель, использование вобэнзима в комплексной терапии хронического пиелонефрита приводит к более быстрой элиминации микроорганизмов.
Фитотерапия
В комплексном лечении детей с хроническим пиелонефритом уделяют большое внимание фитотерапии. С этой целью применяют сбор лекарственых растений, которые обладают противовоспалительным, антисептическим и регенерирующим действиями (таблица 26). Лечение сбором лекарственных растений начинают после стихания активного микробно-воспалительного процесса в почках и мочевыводящих путях, продолжительность курса фитотерапии составляет 3-6 месяцев.

110
Таблица 26 Сбор лекарственных растений, применяемый при лечении
больных хроническим пиелонефритом
Компоненты |
Количество, г |
Петрушки трава |
5 |
Хвоща трава |
50 |
Буквицы трава |
10 |
Конского щавеля корень |
10 |
Спаржи корень |
30 |
Подорожника лист |
20 |
Земляники лист |
30 |
Крапивы лист |
20 |
Ежевики лист |
15 |
Берёзы лист |
15 |
Льняное семя |
50 |
Кукурузные рыльца |
20 |
|
|
Способ приготовления: 1 столовую ложку сухого измельчённого сбора лекарственных растений заливают 2 стаканами крутого кипятка, томят 10-15 минут, настаивают в течение 2 часов, дают выпить больному в течение 1 дня.
Из готовых к употреблению сборов лекарственных растений следует отметить фитолизин, который выпускается в тубах в виде пасты мягкой консистенции с ароматным запахом и содержит экстракты лекарственных растений (петрушки корень, пырея корневище, полевого хвоща трава, берёзы лист, горца птичьего трава), а также мятное, шалфейное, сосновое и апельсиновое масло, ванилин. Фитолизин оказывает мочегонное, спазмолитическое, антибактериальное и противовоспалительное действия, способствует разрыхлению и удалению конкрементов из мочевых путей. Фитолизин назначают по 1 чайной ложке в ½ стакана подслащенной воды 3 раза в день после еды, в течение 2-3 месяцев.
Готовый фитопрепарат канефрон Н, благодаря своему составу (золототысячник, любисток, розмарин), обладает диуретическим, спазмолитическим, противовоспалительным, антимикробным, антиоксидантным и нефропротекторным действиями. Канефрон Н назначается детям школьного возраста по 1 драже или по 25 капель 3 раза в день, детям старше 14 лет – по 2 драже или по 50 капель, в течение 4-8 недель.
