
6 курс / Неонатология / Неонатология_Н_П_Шабалов_7_е_издание_Том_2_2020
.pdfгде VA - минутный объем альвеолярной вентиляции; ЧД - частота дыхания в минуту; Vt - дыхательный объем; Vd - объем мертвого пространства.
Это положение означает, что альвеолярная вентиляция должна отсутствовать, если ДО меньше объема мертвого пространства. Точный механизм обмена углекислого газа при ВЧ ИВЛ неизвестен, но адекватная вентиляция легких вероятно все-таки достигается.
Взаимоотношения между вентиляцией (выведение СО2) и параметрами ВЧ ИВЛ более сложны для ВЧ ИВЛ, чем для обычной вентиляции. При ВЧ ИВЛ основная элиминация СО2 происходит благодаря чрезвычайно эффективному смешиванию газа в дыхательных путях, иначе говоря, из-за усиленной диффузии. При всех типах ВЧ ИВЛ со всеми аппаратами ВЧ ИВЛ элиминация СО2 примерно пропорциональна произведению частоты ВЧ ИВЛ и ДО ВЧ ИВЛ в квадрате (f × Vt2). Последняя формула была подтверждена в многочисленных исследованиях на животных. В практическом смысле это означает, что маленькое изменение амплитуды ВЧ ИВЛ (ΔP) или ДО серьезно влияют на элиминацию СО2. Следовательно, для большинства пациентов элиминация СО2 не зависит от частоты ВЧ ИВЛ и управляется изменением амплитуды. Важное различие между ВЧ и обычными вентиляторами заключается во взаимоотношении амплитуды давления, измеряемой в центре сечения ЭТТ и достигающей терминальных дыхательных путей и альвеол (рис.
25.16).
При традиционной ИВЛ (ЧД до 60 вдохов в минуту) газообмен происходит почти полностью благодаря основному потоку (конвекция). В этой ситуации
через дыхательные пути подаваемое давление целиком доходит до альвеол. Если частота ИВЛ более высокая (75-150 в минуту) с пропорциональным снижением времени вдоха и выдоха, только недостаточное время дыхательного цикла не позволяет подаваемому давлению полностью достичь альвеол. И тем не менее это прямой путь формирования воздушных ловушек и неконтролируемого РЕЕР, который наблюдается при высокой частоте традиционной ИВЛ. При ВЧ ИВЛ, напротив, наблюдается прогрессивное уменьшение амплитуды давления от верхних дыхательных путей к альвеолам. Газообмен происходит благодаря диффузии и амплитуда давления и объем, достигающие альвеол, значительно ниже, чем измеренные в дыхательных путях. Причем чем выше частота ВЧ ИВЛ, тем более выраженным становится это снижение давления. Вот почему при увеличении частоты ВЧ ИВЛ и сопутствующем укорочении времени вдоха и выдоха происходит снижение амплитуды давления в альвеолах и уменьшение элиминации СО2.
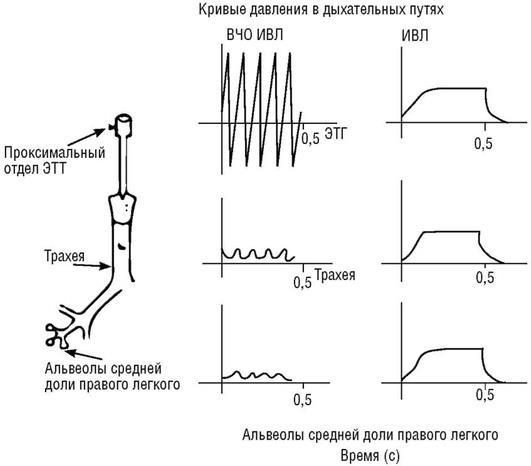
Рис. 25.16. Кривые давления в дыхательных путях на разных уровнях дыхательных путей при ВЧ ИВЛ и традиционной ИВЛ (Mammel M., Boros S., 1996)
Очень важно для каждого пациента выбрать адекватную частоту ВЧ ИВЛ, которая приведет к оптимальному газообмену без воздушных ловушек (при использовании аппарата SensorMedics 3100А Tвд устанавливается 33%, таким образом, Твд/Твыд = 1:2, и за счет активной фазы выдоха воздушных ловушек не формируется). Значение частоты ВЧ ИВЛ зависит от массы тела пациента и особенностей его легочной механики. При этом чем меньше
масса тела пациента, тем выше рекомендуемая для него частота ВЧ ИВЛ, и наоборот. Необходимо помнить, что важнейшим показателем, позволяющим установить оптимальную частоту, является константа времени. Константа времени - это произведение динамического комплайенса и сопротивления дыхательных путей (Cdyn × Raw). Закономерно, что пациенты, имеющие короткую константу времени (низкий легочный комплайенс или низкий резистенс дыхательных путей), нуждаются в более высокой частоте вентиляции, чем дети с более длинной константой времени (высокий легочный комплайенс или высокое аэродинамическое сопротивление дыхательных путей).
В середине 1980-х - начале 1990-х годов, когда ВЧ ИВЛ делала первые шаги, наиболее актуальной частотой HFOV была 15 Гц (900 дыханий в минуту). Причина в том, что большинство пациентов, попадавших на ВЧ ИВЛ, имели очень плохо растяжимые, «жесткие» легкие. Сейчас такие критически больные новорожденные встречаются значительно реже, и легкие большинства детей обладают лучшим комплайенсом и более длинной константой времени. По этой причине чаще используется частота HFOV 6-10 Гц. Общая закономерность следующая: чем больше пациент и чем лучше комплайенс у него, тем меньшая частота ВЧ ИВЛ ему необходима.
Стратегии ВЧ ИВЛ
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
Для поддержания необходимой оксигенации используют два различных пути:
1)стратегия оптимизации легочного объема - применяется при диффузных поражениях легких, среднее давление устанавливается больше, чем при традиционной ИВЛ,
FiO2 снижают;
2)стратегия ограничения легочного объема - применяется при СУВ. Среднее давление меньше, чем при традиционной ИВЛ, FiO2 повышают.
Стратегии использования ВЧ ИВЛ эволюционировали со временем. С одной стороны, изменения происходили по мере улучшения понимания взаимодействия вентилятора и легочной патофизиологии, а с другой стороны, за последние 15-20 лет качественно изменилась и популяция пациентов. Когда-то ВЧ ИВЛ применялась для спасения новорожденных, у которых традиционная вентиляция была неэффективна. ВЧ ИВЛ рассматривалась тогда прежде всего как средство снижения давления в дыхательных путях и предотвращения легочного перерастяжения. После исследований de Lemos и
соавт. (1987, 1989) Kinsella (1991), Froese и соавт. (1993) пришло понимание, что самое большое преимущество ВЧ ИВЛ - это возможность достижения однородного легочного расправления и поддержание более высокого среднего давления в дыхательных путях без перерастяжения легких. Мысль о том, что избежание ателектазиро-вания так же важно, как и недопущение перерастяжения, привела к формированию общего подхода к ВЧ ИВЛ (как, впрочем, и к традиционной ИВЛ). Этот подход получил название стратегии легочного вовлечения. Смысл ее состоит в поддержании определенного расправляющего давления, большего, чем критическое давление коллабирования легких.
Таблица 25.9. Регуляция параметров ВЧ ИВЛ (Mummel, 2012)
Проблема |
Действие |
Неадекватная оксигенация с ателектазами/ |
Увеличить МАР на 1-2 см или временно |
низким объемом легких на рентгенограмме |
повысить МАР и снизить после |
|
улучшения |
Неадекватная оксигенация с перераздутием |
Снизить МАР на 1-2 см. Повторный |
легких на рентгенограмме ± гиперкапния |
снимок |
Гиперкапния с нормальным легочным |
Увеличить амплитуду или снизить частоту |
объемом |
|
Гипокапния |
Снизить амплитуду или повысить частоту |
Гипероксия |
Снизить FiO2 <0,3-0,4, затем МАР |
Показания к ВЧ ИВЛ. Показания к «реанимационному» применению ВЧ ИВЛ могут быть следующими:
•персистирующая утечка воздуха (например, бронхоплевральный свищ, пневмоторакс, ИЛЭ);
•сохраняющаяся дыхательная недостаточность вследствие РДС, пневмонии, ARDS, САМ, гипоплазии легких, ВДГ, водянки плода;
•трахеопищеводный свищ у больного, которого невозможно быстро прооперировать
(например, недоношенный);
• первичная легочная гипертензия, которая эффективно лечится расправлением ателектазов.
Клиническое применение ВЧ ИВЛ представлено в табл. 25.9.
Начальные параметры ВЧ ИВЛ
1. Время вдоха 33% (соотношение Твд/Твыд = 1:2).
•Контроль рН и газов артериальной крови. PaCO2 рекомендуется поддерживать на уровне 40-50 мм рт.ст. Если течение основного заболевания осложнилось ИЛЭ, другими видами СУВ либо на рентгенограммах имеются участки перераздутия или хронические изменения, значения приемлемого PaCO2 будут выше - 50-55 мм рт.ст. Приемлемый артериальный рН может быть на уровне >7,20-7,25.
•SрO2. Идеальными значениями SрO2 для большинства пациентов являются 90-94%.
•Транскутанное определение газов крови (ТcO2, ТcCO2).
•Рентгенологический контроль. Один из лучших маркеров объема легких при ВЧ ИВЛ - положение правого купола диафрагмы на рентгенограмме. Идеальным считается такое расправление, при котором правый купол располагается между VIII и IX ребрами. Допускается положение правого купола диафрагмы между IX и X ребрами. Более низкое положение оце-
нивается как перераздутие. Для пациентов с ИЛЭ или бронхоплевраль-ным свищом наиболее благоприятным положением правого купола будет считаться на одно ребро выше, чем для детей без СУВ.
•Нейросонография.
•УЗИ сердца с допплерографией.
•По возможности дыхательный объем. Sturtz и соавт. (2008) наблюдали наиболее эффективную вентиляцию при ДО = 2,5±0,68 мл/кг.
•Увлажнение дыхательных путей. Неадекватное увлажнение при ВЧ ИВЛ может приводить к реанимационным ситуациям вследствие обтурации дыхательных путей.
Заболевания, при которых применяется ВЧ ИВЛ
РДС. Исследования «спасения». ВЧ ИВЛ применяется как первичный метод респираторной поддержки недоношенным детям с РДС, так и при неэффективности традиционной ИВЛ (Bhuta T, Henderson-Smart D., 2007). Авторы метаанализа полагают, что в настоящее время недостаточно данных для применения ВЧ ИВЛ в качестве терапии «спасения» при тяжелом РДС, и ее применение должно быть ограничено включением этих больных в РКИ (рандомизированные контролируемые исследования).
РДС. Исследования раннего вмешательства. В настоящее время проведено 17
рандомизированных исследований (3652 новорожденных), в которых сравнивалась эффективность ВЧ и традиционной ИВЛ как первичного типа респираторной поддержки у недоношенных с РДС, результаты которых учитывались в метаанализе Cools и соавт. (2009). Никаких преимуществ ВЧ ИВЛ отмечено не было, кроме возможного снижения частоты ХЗЛ, но на уровне границы статистической значимости. Следует отметить, что исследования эффективности ВЧ ИВЛ в лечении РДС продолжаются с обнадеживающими результатами.
Гипоплазия легких/ВДГ. При гипоплазии легких число альвеол снижено, и возможно, что их вентиляция с большой частотой улучшит газообмен. Как минимум ВЧ ИВЛ часто позволяет стабилизировать таких больных (Mum-
mel, 2012).
«Спасение» потенциальных кандидатов на ЭКМО. Попытка перевода больного на ВЧ ИВЛ безусловно показана новорожденным с тяжелой дыхательной недостаточностью, которые являются потенциальными кандидатами на ЭКМО. Но при этом метаанализ D. Smart (2009) не показал преимуществ ВЧ ИВЛ над традиционной у доношенных детей с тяжелой ДН (2 исследования, 199 детей) в плане снижения смертности, СУВ, ХЗЛ и снижения частоты ЭКМО.
Осложнения:
• некоторые исследования ВЧ ИВЛ показали повышение частоты ВЖК 3/4
и ПВЛ;
•неблагоприятное сердечно-легочное взаимодействие; обязательно поддерживать баланс между адекватным объемом легких и венозным притоком к сердцу; нарушение этого баланса может быть причиной прогрессирующей гипотензии и гипоксемии;
•мукостаз, нечастое, но серьезное осложнение ВЧ ИВЛ.
Уход от ВЧ ИВЛ. По мере восстановления легочной функции у стабильных пациентов возникает необходимость правильно снизить параметры ВЧ ИВЛ, перевести их на другой вид респираторной поддержки или вообще экстубиро-вать. Самое главное здесь - уходить от ВЧ ИВЛ очень осторожно и грамотно, избегая получить ателектаз при снижении МАР ниже уровня критического давления закрытия легких. В первую очередь нужно добиться снижения FiO2 ниже 0,4 на фоне хорошей оксигенации. В большинстве случаев только после этого приступают к ограничению МАР. В целом, надо стараться снижать МАР или амплитуду ВЧ ИВЛ у стабильных пациентов первых двух недель жизни хотя бы каждые 6-12 ч. Чаще всего только дети с ХЗЛ не будут толерантны к этому агрессивному графику. Недоношенные новорожденные с низкой массой тела при рождении обычно могут быть экстубированы, когда МАР снижен до 6-8 см вод.ст., а FiO2 менее 0,3. Более крупные дети могут быть успешно экстубирова-ны и с более высоких параметров. В случае, когда состояние ребенка в возрасте 2-4 нед уже не улучшается, разумно предположить, что это может быть связано с повышением сопротивления дыхательных путей на этой стадии легочного заболевания.
Принимая решение о продолжении ВЧ ИВЛ, здесь нужно снижать частоту ВЧ ИВЛ в соответствии с удлиняющейся константой времени. Пока недостаточно данных о сравнительной эффективности ВЧ ИВЛ и традиционной вентиляции у пациентов с хроническими легочными заболеваниями.
Резюме. В настоящее время большинство отделений интенсивной терапии новорожденных в нашей стране для респираторной поддержки недоношенным детям рутинно применяют традиционную ИВЛ. Недостаточный клинический опыт может приводить к меньшей эффективности ВЧ ИВЛ. В отсутствие ясных преимуществ высокочастотной вентиляции имеет смысл пользоваться тем видом и режимом ИВЛ, которым вы лучше владеете. Большинство врачей пользуются разумным подходом при решении вопроса о необходимости ВЧ ИВЛ и начинают ее раннее использование, если ребенок исходно имеет высокий риск осложнений при традиционной ИВЛ или уже развившийся СУВ, даже если удается обеспечивать адекватный газообмен на традиционной ИВЛ.
25.7. ТЕРАПИЯ СУРФАКТАНТОМ
Принимая решение о продолжении ВЧ ИВЛ, здесь нужно снижать частоту ВЧ ИВЛ в соответствии с удлиняющейся константой времени. Пока недостаточно данных о сравнительной эффективности ВЧ ИВЛ и традиционной вентиляции у пациентов с хроническими легочными заболеваниями.
Резюме. В настоящее время большинство отделений интенсивной терапии новорожденных в нашей стране для респираторной поддержки недоношенным детям рутинно применяют традиционную ИВЛ. Недостаточный клинический опыт может приводить к меньшей эффективности ВЧ ИВЛ. В отсутствие ясных преимуществ высокочастотной вентиляции имеет смысл пользоваться тем видом и режимом ИВЛ, которым вы лучше владеете. Большинство врачей пользуются разумным подходом при

•снижение легочного сосудистого сопротивления;
•повышение оксигенации.
Сурфактант при РДС. Использование сурфактанта недоношенным новорожденным с РДС/риском РДС - один из наиболее хорошо изученных видов терапии в неонатологии. Более 30 рандомизированных исследований были проведены только с 1985 по 1992 год. Эти исследования показали снижение неона-тальной смертности и снижение частоты легочной баротравмы (пневмоторакс
и интерстициальная легочная эмфизема) у детей, которым вводили сурфак-тант. В основном тестировались две стратегии применения сурфактанта. Одна - применение вскоре после рождения с целью профилактики РДС и повреждения легких механической вентиляцией («профилактическое применение»). Вторая - применение в возрасте 2-24 ч жизни, после установления диагноза РДС («лечебное применение»). Метаанализ Soll и Morley (2001) показал снижение частоты синдромов утечки воздуха, БЛД, неонатальной смертности при профилактическом введении сурфактанта по сравнению с лечебным. Кроме профилактического применения, описано так называемое «раннее», до возраста менее 2 ч жизни, и анализ этих исследований тоже показал результаты лучшие, чем при отсроченном введении: уменьшение баротравмы легких, риска смерти и частоты развития ХЗЛ.
По мере расширения клинического применения раннего nСРАР опыт показал, что многие новорожденные даже очень низких сроков гестации не будут нуждаться в ИВЛ и сурфактанте. Ретроспективные клинические исследования продемонстрировали уменьшение применения сурфактанта в этой популяции без увеличения частоты БЛД, смертности или других осложнений недоношенности. Учитывая эти данные, были проведены крупные международные исследования сравнения раннего nСРАР с интубацией и «профилактическим» введением сурфактанта: COIN (Morley et al., 2008),
CURPAP (Sandri et al., 2010) и SUPPORT (Carlo et al., 2010). Анализ этих исследований показал, что рутинное раннее применение nСРАР снижает риск ХЗЛ или смерти (RojasReyes et al., 2012). Из этого можно сделать вывод, что nСРАР следует рассматривать как рутинный метод начальной респираторной поддержки у недоношенных детей.
Однако если дети массой тела менее 1500 г нуждаются в интубации сразу после рождения для проведения реанимационных мероприятий или вследствие очень тяжелой ДН - они должны получить сурфактант как можно скорее, в большой степени «профилактически».
Уребенка с РДС экзогенный и эндогенный сурфактант может ингибиро-ваться белками сыворотки крови и медиаторами воспаления, проникающими в альвеолы. Исследования, сравнивающие эффект порактанта альфа (Куро-сурф♠) в дозе 200 мг/кг со 100 мг/кг берактанта (Сюрвантa♠) или 100 мг/кг того же порактанта альфа, показали снижение смертности при введении большей дозы (Singh et al., 2011).
Удетей с тяжелым РДС проводились сравнения нескольких введений сур-фактанта с единственным введением. Было показано, что введение сурфактан-та в несколько раз снижает частоту пневмоторакса и смертность (Speer et al., 2012). Канадское педиатрическое общество рекомендует вводить второй раз сурфактант через 2 ч после первого введения, если больной находится на ИВЛ с FiO2 >30%. В клинической практике введение повторных доз должно быть индивидуальным. Если после первой дозы эффект был кратковременным, весьма высока вероятность, что у больного не РДС, а, например, врожденная пневмония.
По происхождению препараты сурфактанта подразделяют на синтетические и натуральные. Анализ 12 сравнительных исследований этих типов сурфактантов показал снижение частоты пневмоторакса и снижение смертности при введении натурального сурфактанта (Soll R., Blanco F., 2001). Синтетический препарат Лу-
