
6 курс / Неонатология / Детские болезни Баранов А.А. 2009
.pdf•Олигоартрит с поражением глаз характерен для одного из вариантов ЮРА, однако последний преимущественно развивается у девочек раннего возраста. Увеит при этом варианте ЮРА чаще носит подострый характер, развивается исподволь, без ярких клинических проявлений. Для этой формы ЮРА характерно повышение уровня антинуклеарного фактора в 40-50% случаев, отсутствует связь с HLA B27 (возможны ассоциации с HLA А2, DR5).
•Наличие асимметричного олигоартрита, выявление связи с перенесѐнной кишечной или урогенительной инфекцией, наличие маркѐров хламидийной, микоплазменной, кишечной инфекций позволяет диагностировать РеА или болезнь Райтера (при наличии артрита, уретрита, конъюнктивита). Несмотря на сходство клинической картины и схожесть патогенеза РеА и ЮАС, наличие энтезопатий и ригидности позвоночника для первого не характерно. Принципиально важный дифференциально-диагностический критерий - отсутствие рентгенологических признаков сакроилеита при РеА.
•Псориатический спондилоартрит предполагает наличие у пациента характерных кожных изменений и/или наличие в семейном анамнезе больных псориазом.
•Болезнь Крона и неспецифический язвенный колит также могут протекать со спондилоартритом. При этой патологии отмечают изменение характера стула, нарастающую дистрофию; эндоскопическое исследование кишечника позволяет поставить правильный диагноз.
•Принципиальное значение имеет дифференциальная диагностика с заболеваниями неревматической природы, обладающими схожей симптоматикой, - инфекционными артритами (туберкулѐзным, бруцеллѐзным и др.), а также патологией невоспалительного характера (дисплазии, остеохондропатии) и онкологической патологией.
Лечение
•С противовоспалительной целью для лечения ЮАС применяют НПВС. Наиболее эффективным противовоспалительным препаратом в лечении ЮАС является индометацин, который назначают перорально по 2-3 мг/кг/сут в 2-3 приѐма. Тем не менее в связи с высокой частотой побочных эффектов индометацина, лечение рекомендуют начинать с напроксена (перорально 1520 мг/кг/сут в 2 приѐма). Реже применяют диклофенак, другие НПВС при ЮАС считают неэффективными.
•Глюкокортикоиды, как наиболее мощные противовоспалительные средства, используют в период обострения суставного синдрома. Их применение ограничивается преимущественно внутрисуставным введением. При необходимости можно воспользоваться коротким курсом пульс-терапии: быстрое (30-60 мин) внутривенное введение больших доз метилпреднизолона (5-15 мг/кг) в течение 3 дней. При наличии аортита, поражения почек и торпидного к лечению увеита возможно назначение преднизолона перорально в дозах не более 0,5 мг/кг/сут. Для лечения увеита также применяют местно противовоспалительные и глюкокортикоидные препараты.
• Иммуносупрессивная терапия: в качестве базисного препарата наиболее часто применяют сульфасалазин по 30-40 мг/кг/сут, также существуют данные об использовании метотрексата по 10 мг/м2 1 раз в неделю.
Прогноз
Прогноз для жизни благоприятен. При длительном течении ЮАС у больных нарастает тугоподвижность в позвоночнике. Причиной инвалидизации может быть поражение тазобедренных суставов, анкилозирование межпозвоночных суставов. При адекватном наблюдении и лечении удаѐтся приостановить прогрессирование заболевания.
РЕАКТИВНЫЙ АРТРИТ
Реактивный артрит (РеА) - асептическое воспалительное заболевание суставов, развивающееся в ответ на внесуставную инфекцию, при котором предполагаемый первичный агент не может быть выделен из суставов на обычных искусственных питательных средах.
Термин «реактивный артрит» введѐн в литературу в 1969 г. финскими учеными К. Ахо и П. Авоненом для обозначения артритов, развившихся после перенесѐнной иерсиниозной инфекции. Подразумевалось, что при этом в полости суставов не обнаруживаются ни живой причинный агент, ни его Аг. В последующие десятилетия в суставных тканях были выявлены Аг микроорганизмов, с которыми связывают развитие артритов: иерсиний, сальмонелл, хламидий. В ряде случаев выделяют и сами микроорганизмы, способные к размножению, например на культуре клеток. В связи с этим термин РеА можно применять лишь с большой осторожностью. Тем не менее он распространѐн в ревматологической литературе и в классификации ревматических болезней всех стран.
ЭПИДЕМИОЛОГИЯ
В структуре ревматических заболеваний разных стран доля РеА составляет от 8,6 до 41,1%. Такая вариабельность показателей объясняется сложностью диагностики заболевания при слабой выраженности предшествующей инфекции, разными диагностическими подходами, а также наличием перекрѐстной клинической симптоматики с другими артритами. В последнее десятилетие в структуре ревматических заболеваний наблюдают тенденцию к нарастанию частоты РеА. В России по данным отдела медицинской статистики МЗ РФ распространѐнность РеА в 2002 г. среди детей до 18 лет составила 86,9 на 100 000, а первичная заболеваемость - 32,7 на 100 000 детского населения. В структуре ревматических заболеваний у детей до 14 лет РеА составляет 57,5%, у подростков - 41,8%. Представленные показатели доказывают, что проблема РеА в детском возрасте весьма актуальна.
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
В настоящее время к РеА относят в основном заболевания, связанные с кишечной и мочеполовой инфекциями, которые ассоциируются с Аг гистосовместимости В27 (HLA B27). Выделяют две группы артритов:
урогенитальные и постэнтероколитические. Этиологические факторы урогенитальных РеА включают Chlamydia trachomatis (серовар D, K), уреаплазму. Этиологические факторы постентероколитических РеА -
иерсинии(Yersinia |
enterocolitica, 03 |
и |
09 |
серотип; Yersinia |
|
pseudotuberculosis),сальмонеллы (Salmonella |
|
enteritidis, |
Salmonella |
||
typhimurium и |
др.), |
шигеллы(Shigella |
flexneri II-IIa), |
||
кампилобактер (Campylobacter |
jejuni). Инфекции |
респираторного тракта, |
|||
связанные с Mycoplasma pneumoniae и, особенно,Chlamydia pneumoniae также являются частыми причинами развития РеА.
Урогенитальные реактивные артриты
В настоящее время одна из наиболее частых причин развития РеА - хламидийная инфекция (до 80% случаев), что связано с пандемией хламидиоза в мире, особенностями путей передачи хламидийной инфекции, цикла развития хламидий и реакции на терапию.
Основная особенность хламидий - внутриклеточный паразитизм. Источник инфекции - люди, млекопитающие, птицы. Заражение человека Chlamydia pneumoniae и Chlamydia psittaci происходит воздушно-капельным и воздушнопылевым путѐм, Chlamydia trachomatis передаѐтся половым, вертикальным, контактно-бытовым путѐм и при прохождении плода через инфицированные родовые пути матери. В детском возрасте половой путь передачи не является приоритетным.
Перенесѐнная инфекция не обеспечивает пожизненного иммунитета, естественная резистентность отсутствует.
Хламидии имеют две клеточные формы: элементарное тельце (высокоинфекционная, не проявляющая метаболическую активность форма) и ретикулярное тельце (репродуктивная внутриклеточная форма). Жизненный цикл хламидий проходит несколько стадий. Внутриклеточный цикл развития хламидий продолжается 2-3 сут, однако он может задержаться в репродуктивной фазе на несколько дней и месяцев.
Хламидии также могут трансформироваться в L-формы. К этому предрасполагают аномальные реакции иммунной системы, а также применение неадекватных доз антибиотиков и антибиотиков, к которым хламидии не чувствительны. L-формы обладают очень слабой способностью к антигенному раздражению иммунокомпетентных клеток и могут длительно находиться внутри клеток, при делении они
передаются дочерним клеткам. Это приводит к длительной персистенции возбудителя и хроническому течению процесса.
У больных с хроническим хламидийным РеА, как правило, выявляют аномалии иммунного ответа - нарушение соотношения между Т-супрессорами и Т-хелперами (снижение количества последних), выраженное уменьшение относительного и абсолютного количества В-клеток, снижение количества NKклеток. Все указанные изменения в иммунном ответе организма больных способствуют развитию хронизации процесса. В реализации генетически
детерминированной предрасположенности индивидуума к развитию хронического РеА придают большое значение носительству HLA-B27.
Постэнтероколитические реактивные артриты
В происхождении РеА, связанных с кишечной инфекцией, основное значение также придают инфекции и генетической предрасположенности. Тем не менее истинный характер взаимоотношений микро- и макроорганизма всѐ ещѐ не ясен.
«Артритогенные» микроорганизмы проникают в слизистую оболочку кишечника и размножаются внутри полиморфноядерных лейкоцитов и макрофагов. В дальнейшем происходит транспорт бактерий и продуктов их жизнедеятельности из первичного очага в органы мишени. По данным экспериментальных исследований, наиболее длительное время микроорганизмы персистируют в клетках, экспрессирующих HLA В27. Предполагают, что наличие HLA B27 обусловливает развитие аномальной иммунной реакции на патогенную кишечную и урогенитальную микрофлору. HLA-B27 даѐт перекрѐстные серологические реакции с хламидиями и некоторыми грамотрицательными энтеробактериями, что обусловлено феноменом микробной антигенной мимикрии. В составе клеточной стенки ряда кишечных бактерий и хламидий присутствуют белки, которые содержат фрагменты, имеющие структурное сходство с отдельными участками молекулы HLA B27. Допускают, что перекрѐстно реагирующие АТ способны оказывать повреждающее действие на собственные клетки организма, которые экспрессируют достаточное для этого количество молекул HLA B27. С другой стороны, считают, что такое перекрѐстное реагирование препятствует осуществлению адекватного иммунного ответа против внутриклеточных паразитов и их эффективной элиминации, способствуя персистированию инфекции.
О значении генетических факторов в патогенезе РеА свидетельствует тесная ассоциация с HLA-B27, который выявляют при постэнтероколитических артритах в 80-90% случаев и несколько реже при урогенитальных РеА (популяционная частота этого HLA D-27 составляет 7-10%).
КЛИНИЧЕСКАЯ КАРТИНА
Синдром Райтера (уретро-окуло-синовиальный синдром) впервые был описан в 1818 г. Бенджамином Броди. Сто лет спустя Ганс Райтер опубликовал историю болезни мальчика 16 лет, у которого после перенесѐнной дизентерии развился артрит, конъюнктивит, уретрит. Позднее в диагностическую тетраду были также добавлены изменения на коже (кератодермия), которые нередко развиваются у больных синдромом Райтера.
Синдром Райтера чаще всего начинается с симптомов поражения урогенитального тракта через 2-4 нед после перенесѐнной кишечной инфекции или предполагаемого заражения хламидиозом. В последующем присоединяются симптомы поражения глаз и суставов.
•Поражение урогенитального тракта у детей характеризуется стѐртостью клинической картины. У мальчиков может развиваться баланит, инфицированные синехии, фимоз. У девочек поражение урогенитального тракта может ограничиваться вульвитом, вульвовагинитом, лейкоцит- и микрогематурией, а также циститом. Поражение урогенитального тракта может на несколько месяцев предшествовать развитию суставного синдрома.
•Поражение глаз характеризуется развитием коньюнктивита чаще катарального, невыраженного, непродолжительного, но склонного к рецидивам. При иерсиниозном РеА конъюнктивит может быть гнойным, тяжѐлым. У трети больных развивается острый иридоциклит, угрожающий слепотой. Поражение глаз также может на несколько месяцев или лет предшествовать развитию суставного синдрома.
•Поражение опорно-двигательного аппарата проявляется ограниченным асимметричным моно-, олиго-, реже полиартритом. Характерно преимущественное вовлечение в процесс суставов ног, с наиболее частым поражением коленных, голеностопных суставов, плюснефаланговых, проксимальных и дистальных межфаланговых суставов пальцев стоп. Артрит может начинаться остро, с выраженными экссудативными изменениями. У некоторых пациентов повышается температура тела, вплоть до фебрильных значений. Экссудативный артрит может протекать без боли, скованности, выраженного нарушения функции, с большим количеством синовиальной жидкости, непрерывно рецидивируя. Поражение суставов характеризуется длительным отсутствием деструктивных изменений, несмотря на рецидивирующий синовит. Типичным для РеА считают поражение первого пальца стопы, формирование «сосискообразной» деформации пальцев стоп (за счѐт выраженного отѐка и гиперемии поражѐнного пальца), развитие теносиновита и бурсита, ахиллобурсита.
У ряда больных отмечается развитие энтезита и энтезопатий (боли и болезненность при пальпации в местах прикрепления сухожилий к костям), частые боли в пятках, боли, скованность, ограничение подвижности в шейном и поясничном отделе позвоночника и илеосакральных сочленениях. Эти клинические симптомы характерны для мальчиков подросткового возраста и ассоциируются с HLA B27. В таких случаях высок риск формирования ЮАС. При затяжном (6-12 мес) или хроническом (более 12 мес) течении болезни характер суставного синдрома меняется. Увеличивается количество поражѐнных суставов, артрит становится более симметричным, чаще вовлекаются суставы верхних конечностей и позвоночник.
•Часто классические симптомы синдрома Райтера хронологически не связаны между собой, что затрудняет диагностику. Иногда даже при тщательном обследовании не удаѐтся выявить одного из симптомов (уретрита или конъюнктивита). В таких случаях заболевание расценивают как неполный синдром Райтера.
•Помимо классической триады симптомов при болезни Райтера нередко выявляют поражение кожи и слизистых оболочек. Они проявляются
кератодермией ладоней и стоп, псориазоподобными высыпаниями,
трофическими изменениями ногтей. У детей также могут развиваться эрозии слизистой оболочки полости рта по типу стоматита или глоссита, которые часто клинически не проявляются и остаются незамеченными. Из других внесуставных проявлений следует отметить лимфаденопатию, реже гепатоспленомегалию, миоперикардит, аортит.
• При лабораторном исследовании выявляют повышение СОЭ, концентрации C-реактивного белка, a2-глобулинов, фибриногена, серомукоида и других неспецифических показателей воспаления. Постэнтероколитический РеА протекает более остро, агрессивно, чем РеА, ассоциированный с хламидийной инфекцией.
Вероятный реактивный артрит. В ряде случаев РеА протекает без отчѐтливых внесуставных проявлений синдрома Райтера (конъюнктивита, уретрита, кератодермии). В таких случаях ведущим в клинической картине становится суставной синдром, который характеризуется преимущественным поражением суставов нижних конечностей асимметричного характера. В целом характер и течение артрита аналогичен таковому при синдроме Райтера. Вне зависимости от наличия внесуставных проявлений у этих детей существует риск формирования ЮАС.
В случае отсутствия полной клинической картины синдрома Райтера, даже при характерном суставном синдроме, диагноз РеА представляет значительные трудности. Наличие характерного моно-, олигоартрита, артрита с преимущественным поражением суставов ног,
выраженной экссудацией, связанного с перенесѐнной кишечной или урогенитальной инфекцией, или с наличием серологических признаков перенесѐнной инфекции позволяет отнести заболевание к «вероятному реактивному артриту».
ДИАГНОСТИКА
Диагноз синдрома Райтера или РеА основывается на информации о предшествующей инфекции, анализе особенностей клинической картины, данных лабораторных (табл. 13-8) и инструментальных методов обследования, результатах этиологической диагностики.
Таблица 13-8. Лабораторные тесты для подтверждения «артритогенной» инфекции*
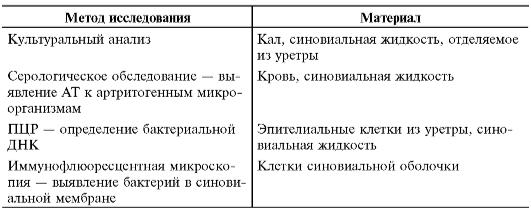
* Kingsly G., Sieper J. Third Internetional Workshop on Reactive Arthritis: an overview // Ann Rheum Dis. - 1996. - Vol. 55. - P. 564-570.
Этиологическая диагностика включает следующие тесты.
• Иммунологический метод.
-Выявление Аг хламидий в эпителиальных клетках, полученных в результате соскобов из уретры и конъюнктивы, а также в синовиальной жидкости (прямой иммунофлюоресцентный анализ и др.); выявление АТ к Аг хламидий в сыворотке крови и в синовиальной жидкости (реакция связывания комплемента, прямая и непрямая иммунофлюоресценция).
-Выявление АТ к бактериям кишечной группы в сыворотке крови
(РПГА, РСК).
•Морфологический метод: выявление морфологических структур возбудителя (окраска препаратов, иммунофлюоресцентный анализ).
•Культуральный метод: выделение хламидий (культура клеток, куриные эмбрионы, лабораторные животные).
•Молекулярно-биологические методы (ПЦР и др.): выявление ДНК возбудителя в крови и синовиальной жидкости.
•Бактериологическое исследование кала.
•Бактериологическое исследование мочи. Диагностические критерии
Диагноз РеА устанавливают на основании диагностических критериев, принятых на III Международном совещании по реактивным артритам в Берлине в 1995 г. (табл. 13-9).
Таблица 13-9. Берлинские диагностические критерии РеА*
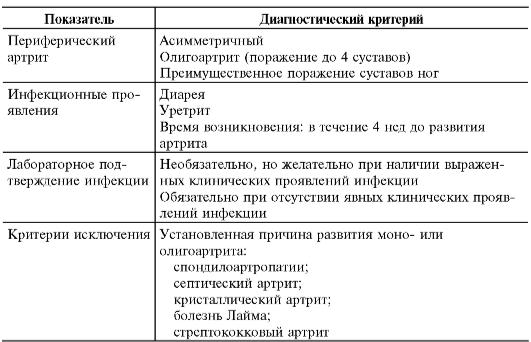
* Kingsly G., Sieper J. Third International Workshop on Reactive Arthritis: an overview // Ann Rheum Dis. - 1996. - Vol. 55. - P. 564-570.
Согласно данным критериям, диагноз «реактивный артрит» можно поставить лишь в том случае, если у больного имеет место типичный периферический артрит, протекающий по типу асимметричного олигоартрита с преимущественным поражением суставов нижних конечностей. При наличии клинических признаков инфекции (диареи или уретрита), перенесѐнной за 2-4 нед и до развития артрита, лабораторное подтверждение желательно, но не обязательно. При отсутствии клинических проявлений инфекции учитывают лабораторные данные, еѐ подтверждающие.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Проведение дифференциальной диагностики РеА от других артритов у детей часто бывает затруднено. Наиболее часто РеА приходит-
ся дифференцировать с инфекционными артритами, заболеваниями инфекционной этиологии, сопровождающимися артритами, а также ортопедической патологией и некоторыми формами ЮАС.
•Вирусные артриты: клиническая картина чаще представлена артралгиями, чем артритами. Клинические симптомы продолжаются в течение 1-2 нед и исчезают без остаточных явлений. Диагноз вирусного артрита устанавливают на основании хронологической связи с перенесѐнной вирусной инфекцией или с вакцинацией, клинической картины острого артрита.
•Постстрептококковый артрит развивается после перенесѐнной стрептококковой инфекции. Диагностические критерии постстрептококкового артрита включают: появление артрита на фоне или спустя 1-2 нед после перенесѐнной носоглоточной инфекции стрептококковой этиологии; наличие повышенных титров постстрептококковых АТ; выявление хронических очагов
инфекции в носоглотке (хронический тонзиллит, фарингит, гайморит); восстановление функции опорно-двигательного аппарата в результате лечения, включающего санацию хронических очагов инфекции.
• Болезнь Лайма проявляется поражением кожи (в виде мигрирующей эритемы), суставов, нервной системы. Развивается при инфицировании спирохетами Borrelia burgdorferi вследствие укуса клеща вида Ixodes.Диагностика болезни Лайма основана на наличии характерной клинической картины, пребывания пациента в эндемичной зоне, наличия в анамнезе факта укуса клеща. Подтверждают диагноз серологическими методами, которые выявляют АТ к Borrelia burgdorferi.
• Септический артрит: диагноз основывается на клинической картине (общие симптомы интоксикации, проявления генерализованной инфекции, преимущественно моно-, реже олигоартрит с резко выраженными симптомами воспаления), характере синовиальной жидкости, результатах посева синовиальной жидкости на флору (высевают преимущественно Staphylococcus aureus и Haemophilus influenzae) с
определением чувствительности к антибиотикам, а также рентгенологических данных (в случае развития остеомиелита).
•Туберкулѐзный артрит диагностируют на основе данных семейного анамнеза (контакт с больным туберкулѐзом); сведений о вакцинации БЦЖ, данных реакции Манту и еѐ динамики; общих симптомов туберкулѐзной инфекции (интоксикация, субфебрильная лихорадка); рентгенологической картины; анализа синовиальной жидкости; биопсии синовиальной оболочки.
•Ювенильный ревматоидный артрит: диагноз основывается на прогрессирующем течении артрита, наличии иммунологических изменений, характерных иммуногенетических маркѐров (HLA A2, DR-5,
DR-8), выявлении рентгенологических изменений в суставах, характерных для ЮРА.
•Ювенильный анкилозирующий спондилоартрит - возможный исход хронического течения РеА у предрасположенных лиц (HLA B27 носителей). Суставной синдром, как и при РеА, представлен асимметричным моно-, олигоартритом с преимущественным поражением суставов ног. Кардинальные признаки, позволяющие поставить диагноз ЮАС, - рентгенологические данные, свидетельствующие о наличии сакроилеита (одноили двустороннего), спондилоартрита.
•Ортопедические заболевания и болевые синдромы (болезни Пертеса,
Кальве, Осгуд-Шлаттера, боли роста): диагноз основывается на клиникорентгенологических особенностях, отсутствии признаков воспаления.
ЛЕЧЕНИЕ
В лечении РеА выделяют три вида терапии: этиотропную, патогенетическую и симптоматическую.
Этиотропная терапия
Реактивный артрит, ассоциированный с хламидийной инфекцией
Поскольку хламидии - внутриклеточные паразиты, выбор антибактериальных препаратов ограничивается только теми, которые способны накапливаться внутриклеточно. К таким антибиотикам относят макролиды, тетрациклины и фторхинолоны, однако последние две группы достаточно токсичны и обладают побочными эффектами, ограничивающими их применение в детской практике. В связи с этим наиболее часто для лечения хламидиоза у детей используются макролиды (азитромицин, рокситромицин). У подростков возможно использование доксициклина и фторхинолонов. Терапия антибиотиком более эффективна в острой стадии РеА. При хламидиозе следует воздержаться от назначения антибиотиков пенициллинового ряда, в связи с возможностью перехода хламидий в L-формы и развития хронической персистирующей инфекции.
Высокой антихламидийной активностью обладает азитромицин, обладающий бактерицидным действием в очаге воспаления, где создаются его высокие концентрации. Детям в первый день приѐма доза препарата составляет 10 мг/кг, в последующие 5-7 дней - 5 мг/кг в один приѐм. Лучший эффект достигается при использовании антибиотика в течение 7-10 дней.
При остром артрите, ассоциированном с хламидиями, также можно применять другие макролиды: кларитромицин (дети старше 6 мес - 15 мг/кг/сут в 2 приѐма), спирамицин (детям массой более 20 кг по 1 500 000 МЕ/10 кг массы тела в сутки в 2-3 приѐма), рокситромицин
(5-8 мг/кг/сут), джозамицин (30-50 мг/кг/сут в 3 приѐма). Курс лечения этими препаратами должен составлять 7-10 дней.
У детей подросткового возраста (старше 8-10 лет) допустимо применять антибиотик из группы тетрациклинов, высокоэффективный против хламидий, - доксициклин.
Реактивный артрит, ассоциированный с кишечной инфекцией В
отношении РеА, связанных с кишечной инфекцией, однозначных рекомендаций по антибактериальной терапии не существует. Всем детям с РеА, у которых присутствуют АТ к бактериям кишечной группы в диагностических титрах или при бактериологическом обследовании кала обнаружены бактерии кишечной группы, рекомендуют проведение антибактериальной терапии. Препараты выбора - аминогликозиды: амикацин по 15-20 мг/кг/сут в 1-2 введения внутривенно или внутримышечно в течение 7-10 сут; гентамицин по 5-7 мг/кг/сут в 2 введения внутривенно или внутримышечно в течение 7-10 сут; также применяют фторхинолоны (у детей старше 12 лет).
Патогенетическая терапия
Монотерапия антибиотиками оказывает недостаточный эффект при затяжном и хроническом течении РеА, ассоциированного с персистирующей
